Selektibitatea Uztaila 2012 A aukera G 2 8
![Selektibitatea Uztaila 2012 A aukera G 2 8. - Sodio perbromatoak [sodio tetraoxobromato(VII)a] zink Selektibitatea Uztaila 2012 A aukera G 2 8. - Sodio perbromatoak [sodio tetraoxobromato(VII)a] zink](https://slidetodoc.com/presentation_image/1765946979603a14cc126ee365334c34/image-1.jpg)
Selektibitatea Uztaila 2012 A aukera G 2 8. - Sodio perbromatoak [sodio tetraoxobromato(VII)a] zink metalarekin erreakzionatzen du ingurune azidoan (H 2 SO 4), sodio bromuroa, zink(II) sulfatoa eta ura emateko. Idatzi oxidazio-eta erredukzio- erdierreakzioak. Doitu erreakzio molekularra ioi-eketroi metodoa erabiliz Datuak: Na. Br. O 4 + Zn + H 2 SO 4 + Na. Br + Zn. SO 4 + H 2 O Ebazpena a) Idatzi oxidazio eta erredukzio- erdierreakzioak. -1 +2 +7 0 Na + + Br. O 4 - + Zn + H + +SO 42 - Na + + Br- + Zn 2+ +SO 4 -2 - + H 2 O Zn 2+ + 2 e- oxidazio erdierreakzioa Br. O 4 - + 8 H + + 8 e- Br- + 4 H 2 O erredukzio erdierreakzioa b) Doitu erreakzio molekularra ioi-eketroi metodoa erabiliz 4(Zn Zn 2+ + 2 e-) Br. O 4 - + 8 H + + 8 e- Br- + 4 H 2 O Na. Br. O 4 + 4 Zn + 4 H 2 SO 4 + Na. Br + 4 Zn. SO 4 + 4 H 2 O

Selektibitatea Uztaila 2012 B aukera G 2 9. - Erreakzio honetan: Zn + K 2 Cr 2 O 7 + HNO 3 Zn(NO 3)2 + Cr(NO 3)3 +KNO 3 + H 2 O • Izendatu erreaktibo eta produktu guztiak. • Adierazi oxidatzailea eta erreduzitzailea, eta idatzi oxidazio- eta erredukzioerreakzioerdiak • Doitu erreakzioa ioi-elektroi metodoa erabiliz. Datuak: Zn + K 2 Cr 2 O 7 + HNO 3 Zn(NO 3)2 + Cr(NO 3)3 +KNO 3 + H 2 O Ebazpena a) Izendatu erreaktibo eta produktu guztiak. Zinka + potasio dikromatoa + azido nitrikoa zink(II) nitratoa +kromo(III) nitratoa + potasio nitratoa + ura. b) Adierazi oxidatzailea eta erreduzitzailea, eta idatzi oxidazio- eta erredukzioerreakzioerdiak Zn + K+ +Cr 2 O 72 - + H+ + NO 3 - Zn 2+ + NO 3 - + Cr 3+ +K+ + H 2 O

Cr 2 O 7 2 - oxidatzailea da, elektoiak hartzen ditu eta erreduzitu egiten da Zn erreduktorea da oxidatu egiten delako elektroiak ematen Zn 2+ + 2 e- oxidazio erdierreakzioa Cr 2 O 72 - +14 H + + 6 e- 2 Cr 3+ + 7 H 2 O erredukzio erdierreakzioa c) Doitu erreakzioa ioi-elektroi metodoa erabiliz. 3(Zn Zn 2+ + 2 e-) Cr 2 O 72 - +14 H + + 6 e- 2 Cr 3+ + 7 H 2 O 3 Zn +Cr 2 O 72 - +14 H + 3 Zn 2+ + 2 Cr 3+ + 7 H 2 O 3 Zn + K 2 Cr 2 O 7 + 14 HNO 3 3 Zn(NO 3)2 + 2 Cr(NO 3)3 + 2 KNO 3 +7 H 2 O

10. -Demagun ondoko erreakzioa: HCl + K 2 Cr. O 4 Cr. Cl 3 + KCl + Cl 2 + H 2 O Kalkula ezazu 0, 25 M den potasio kromatoaren bolumena 40 g Cr. Cl 3 lortzeko, baldin etekina % 60 bada. DATUAK: Masa atomikoak. Cl= 35, 5; Cr =52 Ebazpena Erreakzioa ioi-elektroi metodoa erabiliz doituko dugu HCl + K 2 Cr. O 4 Cr. Cl 3 + KCl + Cl 2 + H 2 O H+ + Cl- +Cr. O 42 - + Cl. Cl- Cl 2 Cr. O 42 - Cr 3+ + Cl- +K+ + Cl 2 + H 2 O Erreduktorea: Cl- oxidatu egiten delako (elektroiak eman) Oxidatzailea: Cr. O 42 - erreduzitu egiten delako (elektroiak hartu) 2 Cl- Cl 2 + 2 e- Cr. O 42 - +8 H + + 3 e- Cr 3+ + 4 H 2 O
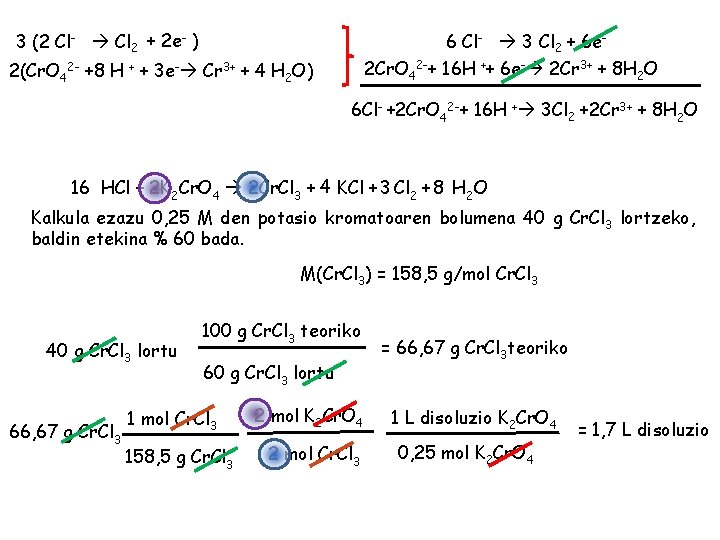
3 (2 Cl- Cl 2 + 2 e- ) 6 Cl- 3 Cl 2 + 6 e- 2 Cr. O 42 -+ 16 H ++ 6 e- 2 Cr 3+ + 8 H 2 O 2(Cr. O 42 - +8 H + + 3 e- Cr 3+ + 4 H 2 O) 6 Cl- +2 Cr. O 42 -+ 16 H + 3 Cl 2 +2 Cr 3+ + 8 H 2 O 16 HCl + 2 K 2 Cr. O 4 2 Cr. Cl 3 + 4 KCl + 3 Cl 2 + 8 H 2 O Kalkula ezazu 0, 25 M den potasio kromatoaren bolumena 40 g Cr. Cl 3 lortzeko, baldin etekina % 60 bada. M(Cr. Cl 3) = 158, 5 g/mol Cr. Cl 3 40 g Cr. Cl 3 lortu 66, 67 g Cr. Cl 3 100 g Cr. Cl 3 teoriko 60 g Cr. Cl 3 lortu 1 mol Cr. Cl 3 158, 5 g Cr. Cl 3 2 mol K 2 Cr. O 4 2 mol Cr. Cl 3 = 66, 67 g Cr. Cl 3 teoriko 1 L disoluzio K 2 Cr. O 4 0, 25 mol K 2 Cr. O 4 = 1, 7 L disoluzio
![Uztaila 2013 B auketa P 1. 11. - Potasio dikromatoak [potasio heptaoxodikromatoa(VI)] eta azido Uztaila 2013 B auketa P 1. 11. - Potasio dikromatoak [potasio heptaoxodikromatoa(VI)] eta azido](http://slidetodoc.com/presentation_image/1765946979603a14cc126ee365334c34/image-6.jpg)
Uztaila 2013 B auketa P 1. 11. - Potasio dikromatoak [potasio heptaoxodikromatoa(VI)] eta azido klorhidrikoak elkarrekin erreakzionatzen dute kromo(III) kloruroa, kloro molekularra, potasio kloruroa eta ura emanez. a) Azaldu zein diren erreakzioko oxidatzailea eta erreduktorea. (0, 5 PUNTU) b) Idatzi oxidazio- eta erredukzio-erdierreakzioak. (0, 5 PUNTU) c) Idatzi erreakzio molekular doitua. Arrazoitu. (1, 0 PUNTU) d) Zenbat m. L HCl 0, 5 M erreakzionarazi behar da gehiegizko kantitatean den K 2 Cr 2 O 7 -arekin 1 L Cl 2 (g) baldintza normaletan lortzeko? Ebazpena a) Azaldu zein diren erreakzioko oxidatzailea eta erreduktorea. HCl + K 2 Cr 2 O 7 Cr. Cl 3 + Cl 2 + KCl + H 2 O H + + Cl- +K + + Cr 2 O 72 - Cr 3+ + Cl- + Cl 2 + K + + Cl- + H 2 O Cl- Cl 2 Erreduktorea: Cl- oxidatu egiten delako (elektroiak eman) Cr 2 O 72 - Cr 3+ Oxidatzailea: Cr 2 O 72 - erreduzitu egiten delako (elektroiak hartu)

b) Idatzi oxidazio- eta erredukzio-erdierreakzioak. 2 Cl- Cl 2 + 2 e- Oxidazioa Cr 2 O 72 - + 6 e- 2 Cr 3+ Cr 2 O 7 +14 H + 2 - + 6 e- 2 Cr 3+ + 7 H 2 O Erredukzioa c) Idatzi erreakzio molekular doitua. Arrazoitu. 3 (2 Cl- Cl 2 + 2 e- ) Cr 2 O 72 - +14 H + + 6 e- 2 Cr 3+ + 7 H 2 O 6 Cl- + Cr 2 O 72 - + 14 H + 2 Cr 3+ + 3 Cl 2 + 7 H 2 O 14 HCl + K 2 Cr 2 O 7 2 Cr. Cl 3 + 3 Cl 2 + 2 KCl + 7 H 2 O d) Zenbat m. L HCl 0, 5 M erreakzionarazi behar da gehiegizko kantitatean den K 2 Cr 2 O 7 -arekin 1 L Cl 2 (g) baldintza normaletan lortzeko? 1 L Cl 2 1 mol Cl 2 14 mol HCl 1 L dis HCl 22, 4 L Cl 2 3 mol Cl 2 0, 5 mol HCl = 0, 416 L disoluzio HCl 416 m. L disoluzio HCl 0, 5 M

12. - Azido sulfurikoa duen ingurune batean, potasio tetraoxomanganato (VII)ak (potasio permanganatoak) potasio ioduroa iodo molekular bihurtzen du; horretaz gainera, manganeso (II) sulfatoa, potasio sulfatoa eta ura lortzen dira. Arrazoituz, egin itzazu jarduera hauek: a) Doitu ezazu ekuazio kimikoa ioi-elektroiaren metodoa erabiliz, eta osa ezazu dagokion ekuazio molekularra. Argi eta garbi adierazi behar dituzu oxidatzailea eta erreduktorea. (1, 5 PUNTU) b) Kalkula ezazu potasio ioduroaren disoluzioaren kontzentrazio molarra baldin eta 50 m. L disoluzio baloratzeko 25 m. L potasio permanganato 0, 5 M —ingurune azidoaren soberakina dagoela— behar badira. (1 PUNTU) Ebazpena Datuak: H 2 SO 4 +KMn. O 4 + KI ---> I 2 + Mn. SO 4 + K 2 SO 4 + H 2 O a)Doitu ezazu ekuazio kimikoa ioi-elektroiaren metodoa erabiliz, eta osa ezazu dagokion ekuazio molekularra. Argi eta garbi adierazi behar dituzu oxidatzailea eta erreduktorea. H + + SO 42 - +K + +Mn. O 4 - +K + + I- I 2 + Mn 2+ +SO 42 - + K + + SO 42 - + H 2 O Mn. O 4 - + Mn 2+ erredukziozko erdierreakzioa I - I 2 oxidaziozko erdierreakzioa

Masa-balantzea eta karga-balantzea (8 H + + Mn. O 4 - + 5 e - Mn 2+ + 4 H 2 O) (2 I - I 2 + 2 e -) x 5 KMn. O 4 oxidatzialea da, berak elektoiak askatzeagatik iodoa oxidatuko da Koruro anioak erredaktoreak dira, elektroiak hartuz eragiten dute KMn. O 4 K-ren erredukzioa 16 H + + 2 Mn. O 4 - + 10 e - 2 Mn 2+ + 8 H 2 O 10 I - 5 I 2 + 10 e - 16 H + + 2 Mn. O 4 - + 10 I - 5 I 2 + 2 Mn 2+ + 8 H 2 O 8 H 2 SO 4 + 2 KMn. O 4 + 10 KI ---> 5 I 2 + 2 Mn. SO 4 + 6 K 2 SO 4 + 8 H 2 O
- Slides: 9