SELAMAT DATANG DI PENERBANGAN KIMIALINES KAMI Kelompok 1

SELAMAT DATANG DI PENERBANGAN KIMIALINES KAMI !! Kelompok : 1. Farizal Cahya Saputra 2. Iqbal Razif 3. Maslukha 4. Muhammad Adiansyah 5. Rahmad Wicaksono 6. Vina Rachmaya
Kimia Unsur : >> Unsur-unsur Periode Ketiga >> Unsur-unsur Transisi Periode Keempat

Unsur-unsur Periode Ketiga Cex it out!!!

@ Unsur-unsur Periode Ketiga di Alam Unsur Rumus Nama Sehari-hari Na ~ Na. NO 3 ~ Na. Cl ~ Senyawa chilli ~ Dalam air laut Mg ~ Mg. CO 3 ~ Mg. SO 4. 7 H 2 O ~ KCl. Mg. Cl 2. 6 H 2 O ~ Mg. CO 3. Ca. CO 3 ~Mg. Cl 2 ~ Magnesit ~ Garam inggris ~ Karnalit ~ Dolomit ~ Dalam air laut Al ~ Al 2 O 3. n. H 2 O ~ Na 3 Al. F 6 ~ Kaolin ~ Bauksit ~ Kriolit Si ~ Si. O 2 ~ Pasir ~ Al 2 O 3. 2 Si. O 2. 2 H 2 O ~ Tanah liat P ~ Ca 3(PO 4)2 ~ Fosfit (dalam tulang) S Bebas di alam ~ Fe. S 2 ~ Ca. SO 4. 2 H 2 O ~ Pirit ~ Gips ~ Na. Cl ~ Dalam air laut Cl
![@ Sifat-sifat Periode Ketiga Unsur Elektron Valensi Natrium (Na) [Ne] 3 S 1 Magnesium @ Sifat-sifat Periode Ketiga Unsur Elektron Valensi Natrium (Na) [Ne] 3 S 1 Magnesium](http://slidetodoc.com/presentation_image_h/841f17f6222149d625ec1946e8b733a8/image-5.jpg)
@ Sifat-sifat Periode Ketiga Unsur Elektron Valensi Natrium (Na) [Ne] 3 S 1 Magnesium (Mg) [Ne] 3 s 2 Aluminium (Al) [Ne] 3 s 2 3 p 1 Silikon (Si) [Ne] 3 S 2 3 p 2 Fosfor (P) [Ne] 3 S 2 3 p 3 Belerang (S) [Ne] 3 S 2 3 p 4 Klor (Cl) [Ne] 3 S 2 3 p 5 Nana Mangan Almini, Si Paijo Sarapan Color (alternatif untuk menghafal) Elektron valensi merupakan elektron pada kulit terluar. Susunan Elektron valensi sangat menentukan sifat-sifat kimia suatu atom dan berperan penting dalam membentuk ikatan dengan atom lain.
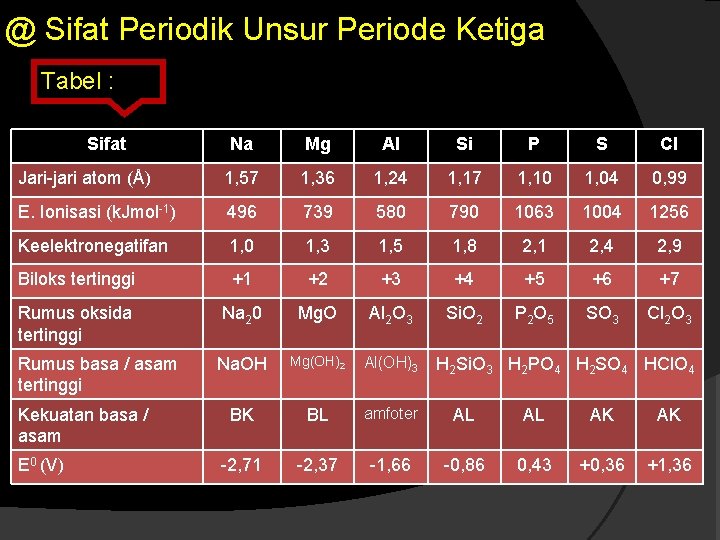
@ Sifat Periodik Unsur Periode Ketiga Tabel : Sifat Na Mg Al Si P S Cl Jari-jari atom (Å) 1, 57 1, 36 1, 24 1, 17 1, 10 1, 04 0, 99 E. Ionisasi (k. Jmol-1) 496 739 580 790 1063 1004 1256 Keelektronegatifan 1, 0 1, 3 1, 5 1, 8 2, 1 2, 4 2, 9 Biloks tertinggi +1 +2 +3 +4 +5 +6 +7 Rumus oksida tertinggi Na 20 Mg. O Al 2 O 3 Si. O 2 P 2 O 5 SO 3 Cl 2 O 3 Rumus basa / asam tertinggi Na. OH Mg(OH)2 Al(OH)3 BK BL amfoter AL AL AK AK -2, 71 -2, 37 -1, 66 -0, 86 0, 43 +0, 36 +1, 36 Kekuatan basa / asam E 0 (V) H 2 Si. O 3 H 2 PO 4 H 2 SO 4 HCl. O 4

@ Uraian @ jari-jari atom merupakan jarak dari inti atom sampai kulit terluar. Dan dalam satu golongan jari-jari atom bertambah besar dari atas kebawah. Dan dalam satu periode, jari-jari ataom makin kecil dari kiri ke kanan. @ energi ionisasi merupakan energi yg diperlukan untuk melepaskan elektron terluar suatu atom. Pada golongan yg sama, energi ionisasi makin kebawah semakin kecil. Sedangkan unsur-unsur seperiode, gaya tarik inti makin kekanan makin kuat. @ Keelektronegatifan merupakan kemampuan atau kecenderungan suatu atom untuk melepas atau menangkap elektron dari atom lain. Unsur segolongan keelektronegatifan makin kebawah makin kecil sebab gaya tarik inti makin lemah. Unsur yg seperiode, makin kekanan semakin besar. @ sifat reduktor dan oksidator makin kuat Na Cl reduktor makin kuat
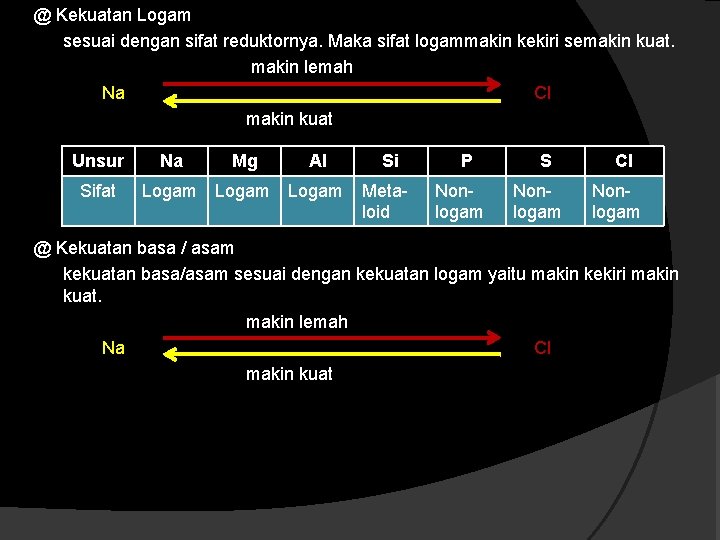
@ Kekuatan Logam sesuai dengan sifat reduktornya. Maka sifat logammakin kekiri semakin kuat. makin lemah Na Cl makin kuat Unsur Na Mg Al Sifat Logam Si Metaloid P Nonlogam S Nonlogam Cl Nonlogam @ Kekuatan basa / asam kekuatan basa/asam sesuai dengan kekuatan logam yaitu makin kekiri makin kuat. makin lemah Na Cl makin kuat

Unsur-unsur Transisi Periode Keempat Cex it out!!!

@ Unsur-unsur transisi periode keempat di alam Logam Nama mineral Rumus Ti ~ Rutile ~ Ti. O 2 Cr ~ Kromit ~ Cr 2 O 3. Fe. O Mn ~ Pirolusit ~ Manganit ~ Mn. O 2 ~ Mn 2 O 3. H 2 O Fe ~ Hematit ~ Magnetit ~ Pirit ~ Fe 2 O 3 ~ Fe 3 O 4 ~Fe. S 2 Co ~ Kobaltit ~ Co. As. S Ni ~ Pentlandit ~ Fe. Ni. S Cu ~ Kalkopirit ~ Kalkosite ~ Cu. Fe. S 2 ~ Cu 2 S Zn ~ Seng blende ~ Smith Sonite ~ Zn. S ~ Zn. CO 3 Di alam unsur periode keempat terdapat dalam senyawa / mineral berupa oksida, sulfida atau karbonat

@ Sifat umum unsur transisi P 4 Unsur-unsuar transisi memiliki sifat khas yang membedakannya dengan unsur golongan utama, antara lain : 1. Sifat logam, semua unsur transisi tergolong logam yang titik cair dan titik didihnya relatif tinggi. 2. Bersifat paramagnetik (sedikit tertarik kedalam medan magnet). 3. Membentuk senyawa-senyawa yang berwarna. 4. Mempunyai beberapa tingkat oksidasi. 5. Membentuk berbagai macan ion kompleks. 6. Berdaya katalitik, unsur serta senyawanya banyak yang berfungsi sebagai katalis, baik dalam proses industri maupun dalam metabolisme.
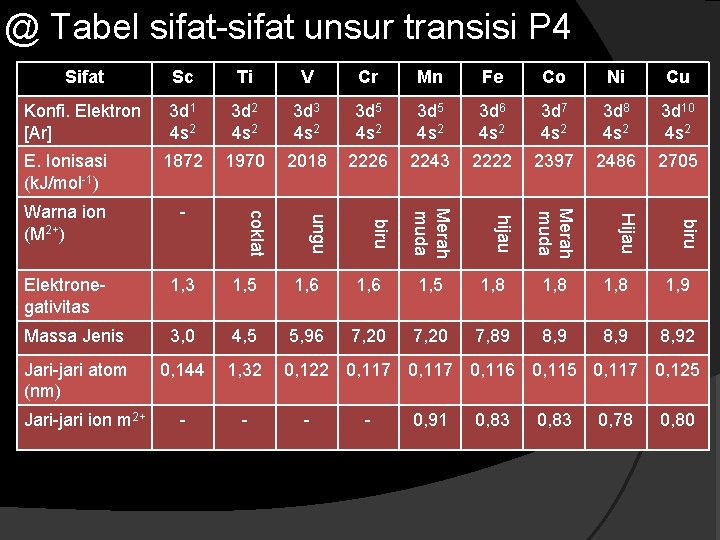
@ Tabel sifat-sifat unsur transisi P 4 Cr Mn Fe Co Ni Cu Konfi. Elektron [Ar] 3 d 1 4 s 2 3 d 2 4 s 2 3 d 3 4 s 2 3 d 5 4 s 2 3 d 6 4 s 2 3 d 7 4 s 2 3 d 8 4 s 2 3 d 10 4 s 2 E. Ionisasi (k. J/mol-1) 1872 1970 2018 2226 2243 2222 2397 2486 2705 Warna ion (M 2+) - biru Merah muda hijau Merah muda Elektronegativitas 1, 3 1, 5 1, 6 1, 5 1, 8 1, 9 Massa Jenis 3, 0 4, 5 5, 96 7, 20 7, 89 8, 92 Jari-jari atom (nm) 0, 144 1, 32 0, 122 0, 117 0, 116 0, 115 0, 117 0, 125 - - Jari-jari ion m 2+ - - 0, 91 0, 83 0, 78 biru V Hijau Ti ungu Sc coklat Sifat 0, 80
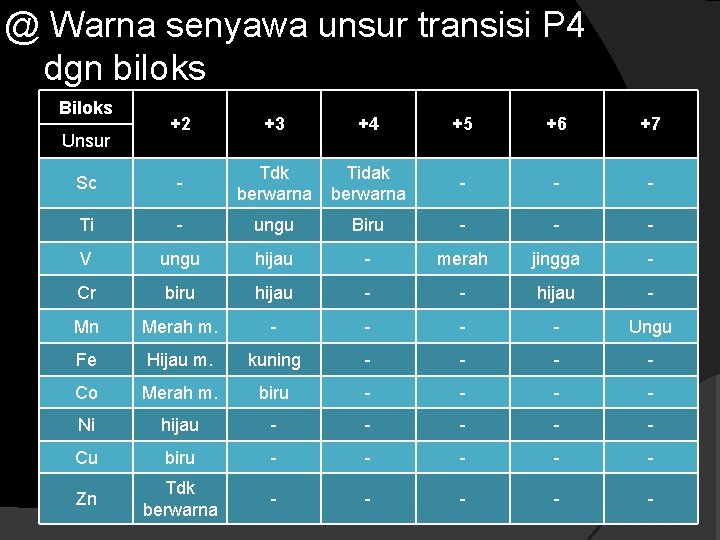
@ Warna senyawa unsur transisi P 4 dgn biloks Biloks +2 +3 +4 +5 +6 +7 Sc - Tdk berwarna Tidak berwarna - - - Ti - ungu Biru - - - V ungu hijau - merah jingga - Cr biru hijau - - hijau - Mn Merah m. - - Ungu Fe Hijau m. kuning - - Co Merah m. biru - - Ni hijau - - - Cu biru - - - Zn Tdk berwarna - - - Unsur
![Senyawa/ ion kompleks Rumus umum -> [A(x)m] ⁿ⁺ Keterangan: * A : atom pusat Senyawa/ ion kompleks Rumus umum -> [A(x)m] ⁿ⁺ Keterangan: * A : atom pusat](http://slidetodoc.com/presentation_image_h/841f17f6222149d625ec1946e8b733a8/image-14.jpg)
Senyawa/ ion kompleks Rumus umum -> [A(x)m] ⁿ⁺ Keterangan: * A : atom pusat => pada ion-ion transisi * X : ligan => senyawa yang diikat oleh atom pusat * m : bilangan koordinasi => jumlah ligan * n⁺ : muatan ion kompleks

Macam-macam Ligan NH₃ H₂O OH¯ F¯ Br¯ I¯ Cl¯ NO₂¯ = asam amino = aquo = hidrokso = fluoro = bromo = iodo = kloro = nitrito
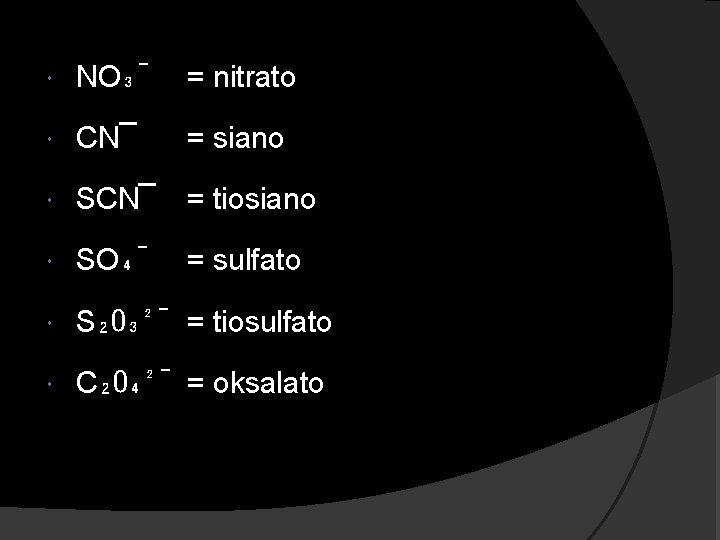
NO₃¯ = nitrato CN¯ = siano SCN¯ = tiosiano SO₄¯ = sulfato S₂O₃²¯ = tiosulfato C₂O₄²¯ = oksalato

Pemberian Nama Senyawa Kompleks Menyebutkan jumlah ligan diikuti nama ligan, kemudian ion pusat. Jika ion kompleks bermuatan (+), nama ion pusat menjadi: 1. latin 2. indonesis Jika ion kompleks bermuatan (-), nama ion pusat menggunakan nama latin dan diberi akhiran “at”

![[CO (NH₃)₄ Cl₂]⁺ X + 4(0) + 2(-1) = +1 X + 0 [CO (NH₃)₄ Cl₂]⁺ X + 4(0) + 2(-1) = +1 X + 0](http://slidetodoc.com/presentation_image_h/841f17f6222149d625ec1946e8b733a8/image-19.jpg)
[CO (NH₃)₄ Cl₂]⁺ X + 4(0) + 2(-1) = +1 X + 0 + (-2) = +1 X– 2 = +1 X = +3 Maka namanya: [CO (NH₃)₄ Cl₂]⁺ Ion tetra amino dikloro kobalt (III)

Matur nuwun atas perhatinipun Wassalamualaikum Wr. Wb.
- Slides: 20