Selamat Datang Dalam Kuliah Terbuka Ini 1 Kuliah

Selamat Datang Dalam Kuliah Terbuka Ini 1

Kuliah terbuka kali ini berjudul “Mengenal Sifat Material I” 2

Disajikan oleh Sudaryatno Sudirham melalui www. darpublic. com 3

Sesi 5 Konfigurasi Elektron dalam Atom 4

Bilangan Kuantum Ada tiga bilangan kuantum yang sudah kita kenal, yaitu: (1) bilangan kuantum utama, n, yang menentukan tingkat energi; (2) bilangan kuantum momentum sudut, atau bilangan kuantum azimuthal, l; (3) bilangan kuantum magnetik, ml. bilangan kuantum utama n: 1 2 3 4 5 3 s, 3 p, 3 d 1, 5 0 1 energi 3, 4 2 s, 2 p total [ e. V ] 13, 6 1 s Bohr (4) Spin Elektron: lebih cermat ½ dikemukakan oleh Uhlenbeck 5
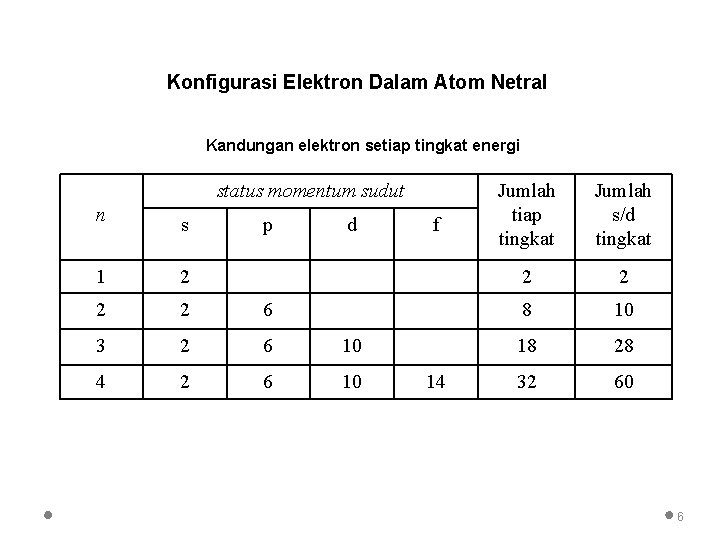
Konfigurasi Elektron Dalam Atom Netral Kandungan elektron setiap tingkat energi status momentum sudut n s 1 2 2 2 6 3 2 6 10 4 2 6 10 p d f 14 Jumlah tiap tingkat Jumlah s/d tingkat 2 2 8 10 18 28 32 60 6
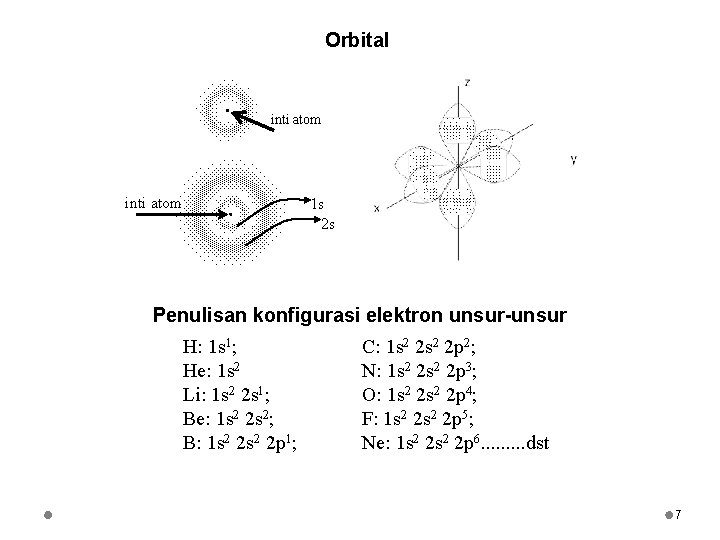
Orbital inti atom 1 s 2 s Penulisan konfigurasi elektron unsur-unsur H: 1 s 1; He: 1 s 2 Li: 1 s 2 2 s 1; Be: 1 s 2 2 s 2; B: 1 s 2 2 p 1; C: 1 s 2 2 p 2; N: 1 s 2 2 p 3; O: 1 s 2 2 p 4; F: 1 s 2 2 p 5; Ne: 1 s 2 2 p 6. . dst 7
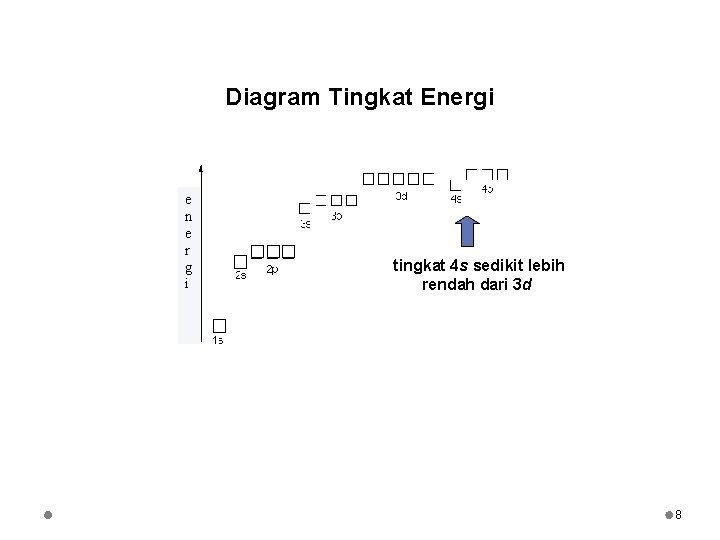
Diagram Tingkat Energi e n e r g i tingkat 4 s sedikit lebih rendah dari 3 d 8
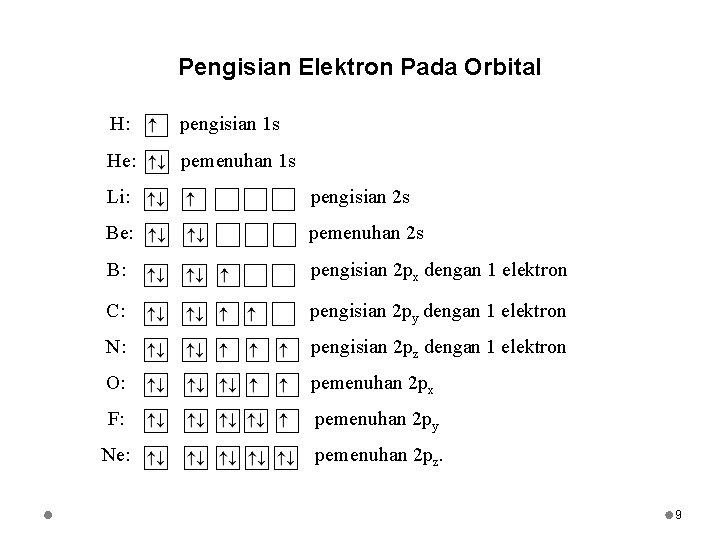
Pengisian Elektron Pada Orbital H: pengisian 1 s He: pemenuhan 1 s Li: pengisian 2 s Be: pemenuhan 2 s B: pengisian 2 px dengan 1 elektron C: pengisian 2 py dengan 1 elektron N: pengisian 2 pz dengan 1 elektron O: pemenuhan 2 px F: pemenuhan 2 py Ne: pemenuhan 2 pz. 9

Tingkat energi 4 s lebih rendah dari 3 d. Hal ini terlihat pada perubahan konfigurasi dari Ar (argon) ke K (kalium). Ar: 1 s 2 2 p 6 3 s 2 3 p 6 K: 1 s 2 2 p 6 3 s 2 3 p 6 4 s 1 (bukan 3 d 1) Ca: 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 (bukan 3 d 2) Sc: 1 s 2 2 p 6 3 s 2 3 p 6 3 d 1 4 s 2 (orbital 3 d baru mulai terisi setelah 4 s penuh) Y: 1 s 2 2 p 6 3 s 2 3 p 6 3 d 2 4 s 2 (dan unsur selanjutnya pengisian 3 d sampai penuh) 10
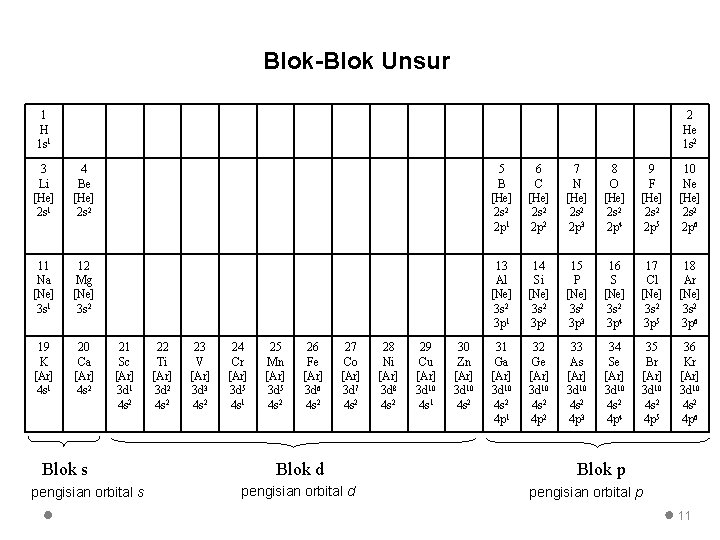
Blok-Blok Unsur 1 H 1 s 1 2 He 1 s 2 3 Li [He] 2 s 1 4 Be [He] 2 s 2 5 B [He] 2 s 2 2 p 1 6 C [He] 2 s 2 2 p 2 7 N [He] 2 s 2 2 p 3 8 O [He] 2 s 2 2 p 4 9 F [He] 2 s 2 2 p 5 10 Ne [He] 2 s 2 2 p 6 11 Na [Ne] 3 s 1 12 Mg [Ne] 3 s 2 13 Al [Ne] 3 s 2 3 p 1 14 Si [Ne] 3 s 2 3 p 2 15 P [Ne] 3 s 2 3 p 3 16 S [Ne] 3 s 2 3 p 4 17 Cl [Ne] 3 s 2 3 p 5 18 Ar [Ne] 3 s 2 3 p 6 19 K [Ar] 4 s 1 20 Ca [Ar] 4 s 2 31 Ga [Ar] 3 d 10 4 s 2 4 p 1 32 Ge [Ar] 3 d 10 4 s 2 4 p 2 33 As [Ar] 3 d 10 4 s 2 4 p 3 34 Se [Ar] 3 d 10 4 s 2 4 p 4 35 Br [Ar] 3 d 10 4 s 2 4 p 5 36 Kr [Ar] 3 d 10 4 s 2 4 p 6 21 Sc [Ar] 3 d 1 4 s 2 Blok s pengisian orbital s 22 Ti [Ar] 3 d 2 4 s 2 23 V [Ar] 3 d 3 4 s 2 24 Cr [Ar] 3 d 5 4 s 1 25 Mn [Ar] 3 d 5 4 s 2 26 Fe [Ar] 3 d 6 4 s 2 27 Co [Ar] 3 d 7 4 s 2 Blok d pengisian orbital d 28 Ni [Ar] 3 d 8 4 s 2 29 Cu [Ar] 3 d 10 4 s 1 30 Zn [Ar] 3 d 10 4 s 2 Blok p pengisian orbital p 11

Ionisasi dan Energi Ionisasi: Energi ionisasi adalah jumlah energi yang diperlukan untuk melepaskan elektron terluar suatu unsur guna membentuk ion positif bermuatan +1. Energi ionisasi dalam satuan e. V disebut juga potensial ionisasi. Potensial ionisasi didefinisikan sebagai energi yang diperlukan untuk melepaskan elektron yang paling lemah terikat pada atom. Pada atom dengan banyak elektron, pengertian ini sering disebut sebagai potensial ionisasi yang pertama, karena sesudah ionisasi yang pertama ini bisa terjadi ionisasi lebih lanjut dengan terlepasnya elektron yang lebih dekat ke inti atom. Energi Ionisasi [e. V] 1 H 13, 6 2 He 24, 5 3 Li 5, 39 4 Be 9, 32 5 B 8, 29 6 C 11, 2 7 N 14, 6 8 O 13, 6 9 F 17, 4 10 Ne 21, 6 11 Na 5, 14 12 Mg 7, 64 13 Al 5, 98 14 Si 8, 15 15 P 10, 4 16 S 10, 4 17 Cl 13, 0 18 Ar 15, 8 19 K 4, 34 20 Ca 6, 11 31 Ga 6, 00 32 Ge 7, 88 33 As 9, 81 34 Se 9, 75 35 Br 11, 8 36 Kr 14 21 Sc 6, 54 22 Ti 6, 83 23 V 6, 74 24 Cr 6, 76 25 Mn 7, 43 26 Fe 7, 87 27 Co 7, 86 28 Ni 7, 63 29 Cu 7, 72 30 Zn 9, 39 12
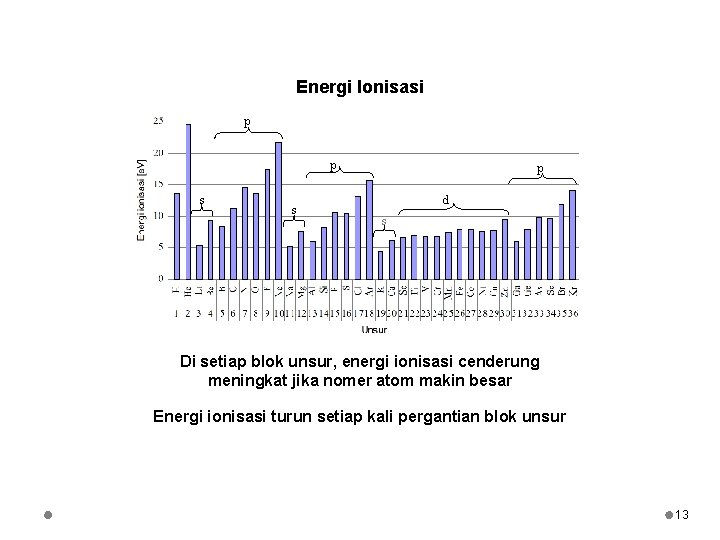
Energi Ionisasi p p s s p d s Di setiap blok unsur, energi ionisasi cenderung meningkat jika nomer atom makin besar Energi ionisasi turun setiap kali pergantian blok unsur 13

Afinitas Elektron Afinitas elektron adalah energi yang dilepaskan jika atom netral menerima satu elektron membentuk ion negatif bermuatan 1. Afinitas elektron dinyatakan dengan bilangan negatif, yang berarti pelepasan energi. Afinitas elektron merupakan ukuran kemampuan suatu unsur untuk menarik elektron, bergabung dengan unsur untuk membentuk ion negatif. Makin kuat gaya tarik ini, berarti makin besar energi yang dilepaskan. Gaya tarik ini dipengaruhi oleh jumlah muatan inti atom, jarak orbital ke inti, dan screening (tabir elektron). 14
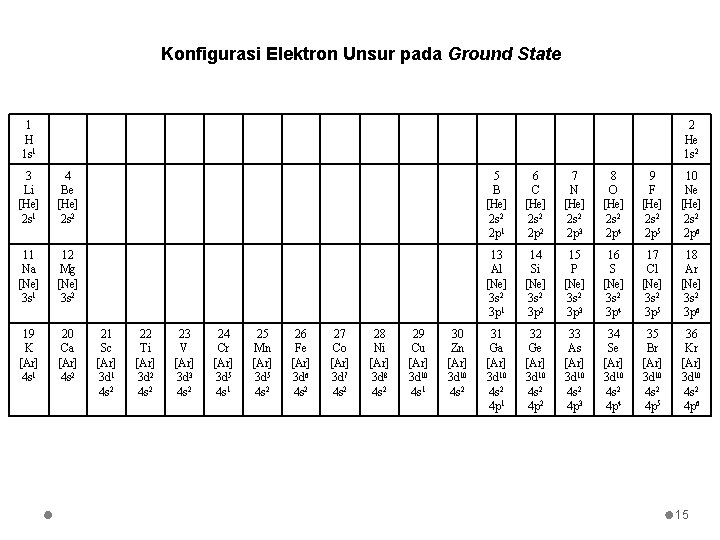
Konfigurasi Elektron Unsur pada Ground State 1 H 1 s 1 2 He 1 s 2 3 Li [He] 2 s 1 4 Be [He] 2 s 2 5 B [He] 2 s 2 2 p 1 6 C [He] 2 s 2 2 p 2 7 N [He] 2 s 2 2 p 3 8 O [He] 2 s 2 2 p 4 9 F [He] 2 s 2 2 p 5 10 Ne [He] 2 s 2 2 p 6 11 Na [Ne] 3 s 1 12 Mg [Ne] 3 s 2 13 Al [Ne] 3 s 2 3 p 1 14 Si [Ne] 3 s 2 3 p 2 15 P [Ne] 3 s 2 3 p 3 16 S [Ne] 3 s 2 3 p 4 17 Cl [Ne] 3 s 2 3 p 5 18 Ar [Ne] 3 s 2 3 p 6 19 K [Ar] 4 s 1 20 Ca [Ar] 4 s 2 31 Ga [Ar] 3 d 10 4 s 2 4 p 1 32 Ge [Ar] 3 d 10 4 s 2 4 p 2 33 As [Ar] 3 d 10 4 s 2 4 p 3 34 Se [Ar] 3 d 10 4 s 2 4 p 4 35 Br [Ar] 3 d 10 4 s 2 4 p 5 36 Kr [Ar] 3 d 10 4 s 2 4 p 6 21 Sc [Ar] 3 d 1 4 s 2 22 Ti [Ar] 3 d 2 4 s 2 23 V [Ar] 3 d 3 4 s 2 24 Cr [Ar] 3 d 5 4 s 1 25 Mn [Ar] 3 d 5 4 s 2 26 Fe [Ar] 3 d 6 4 s 2 27 Co [Ar] 3 d 7 4 s 2 28 Ni [Ar] 3 d 8 4 s 2 29 Cu [Ar] 3 d 10 4 s 1 30 Zn [Ar] 3 d 10 4 s 2 15
![Konfigurasi Elektron Unsur pada Ground State 37 Rb [Kr] 5 s 1 38 Sr Konfigurasi Elektron Unsur pada Ground State 37 Rb [Kr] 5 s 1 38 Sr](http://slidetodoc.com/presentation_image_h2/73864b730051f4423b016efe4ffe739d/image-16.jpg)
Konfigurasi Elektron Unsur pada Ground State 37 Rb [Kr] 5 s 1 38 Sr [Kr] 5 s 2 39 Y [Kr] 4 d 1 5 s 2 40 Zr [Kr] 4 d 2 5 s 2 41 Nb [Kr] 4 d 4 5 s 1 42 Mo [Kr] 4 d 5 5 s 1 43 Tc [Kr] 4 d 6 5 s 1 44 Ru [Kr] 4 d 7 5 s 1 45 Rh [Kr] 4 d 8 5 s 1 46 Pd [Kr] 4 d 10 47 Ag [Kr] 4 d 10 5 s 1 48 Cd [Kr] 4 d 10 5 s 2 49 In [Kr] 4 d 10 5 s 2 5 p 1 50 Sn [Kr] 4 d 10 5 s 2 5 p 2 51 Sb [Kr] 4 d 10 5 s 2 5 p 3 52 Te [Kr] 4 d 10 5 s 2 5 p 4 53 I [Kr] 4 d 10 5 s 2 5 p 5 55 Cs [Xe] 6 s 1 56 Ba [Xe] 6 s 2 57 La [Xe] 5 d 1 6 s 2 58 Ce [Xe] 4 f 1 5 d 1 6 s 2 59 Pr [Xe] 4 f 3 6 s 2 60 Nd [Xe] 4 f 4 6 s 2 61 Pm [Xe] 4 f 5 6 s 2 62 Sm [Xe] 4 f 6 6 s 2 63 Eu [Xe] 4 f 7 6 s 2 64 Gd [Xe] 4 f 7 5 d 1 6 s 2 65 Tb [Xe] 4 f 9 6 s 2 66 Dy [Xe] 4 f 10 6 s 2 67 Ho [Xe] 4 f 11 6 s 2 68 Er [Xe] 4 f 12 6 s 2 69 Tm [Xe] 4 f 13 6 s 2 70 Yb [Xe] 4 f 14 6 s 2 71 Lu [Xe] 4 f 14 5 d 1 6 s 2 72 Hf [Xe] 4 f 14 5 d 2 6 s 2 73 Ta [Xe] 4 f 14 5 d 3 6 s 2 74 W [Xe] 4 f 14 5 d 4 6 s 2 75 Re [Xe] 4 f 14 5 d 5 6 s 2 76 Os [Xe] 4 f 14 5 d 6 6 s 2 77 Ir [Xe] 4 f 14 5 d 7 6 s 2 78 Pt [Xe] 4 f 14 5 d 9 6 s 1 79 Au [Xe] 4 f 14 5 d 10 6 s 1 80 Hg [Xe] 4 f 14 5 d 10 6 s 2 81 Tl [Xe] 4 f 14 5 d 10 6 s 2 6 p 1 82 Pb [Xe] 4 f 14 5 d 10 6 s 2 6 p 2 83 Bi [Xe] 4 f 14 5 d 10 6 s 2 6 p 3 84 Po [Xe] 4 f 14 5 d 10 6 s 2 6 p 4 85 At [Xe] 4 f 14 5 d 10 6 s 2 6 p 5 90 Th [Rn] 6 d 2 7 s 2 91 Pa [Rn] 5 f 2 6 d 1 7 s 2 92 U [Rn] 5 f 3 6 d 1 7 s 2 93 Np [Rn] 5 f 4 6 d 1 7 s 2 94 Pu [Rn] 5 f 6 7 s 2 95 Am [Rn] 5 f 7 7 s 2 96 Cm [Rn] 5 f 7 6 d 1 7 s 2 97 Bk [Rn] 98 Cf [Rn] 99 Es [Rn] 100 Fm [Rn] 101 Md [Rn] 102 No [Rn] 103 Lw [Rn] 87 Fr [Rn] 7 s 1 88 Ra [Rn] 7 s 2 89 Ac [Rn] 6 d 1 7 s 2 54 Xe [Kr] 4 d 10 5 s 2 5 p 6 86 Rn [Xe] 4 f 14 5 d 10 6 s 2 6 p 6 16

Kuliah Terbuka Mengenal Sifat Material I Sesi-5 Sudaryatno Sudirham 17
- Slides: 17