Selamat Datang Dalam Kuliah Terbuka Ini 1 Kuliah

Selamat Datang Dalam Kuliah Terbuka Ini 1

Kuliah terbuka kali ini berjudul “Mengenal Sifat Material II” 2

Disajikan oleh Sudaryatno Sudirham melalui www. darpublic. com 3

Sesi 1 Ikatan Atom dan Ikatan Molekul 4

Ikatan Atom Gaya Ikat : gaya yang menyebabkan dua atom menjadi terikat; gaya ini terbentuk jika terjadi penurunan energi total ketika dua atom saling mendekat Ikatan Primer : Kuat Ikatan Kovalen : terbentuk karena orbital yang setengah terisi dari dua atom saling overlap. Ikatan Metal : terbentuk oleh terjadinya peningkatan perluasan spasial dari fungsi gelombang elektron valensi, ketika sejumlah atom metal saling berdekatan. Ikatan Sekunder : Lemah Ikatan Hidrogen : terbentuk karena gaya tarik antar dipole di mana hidrogen menjadi ujung positif dari dipole. Ikatan van der Waals : terbentuk karena dipole yang fluktuatif dari atom. Ikatan Ion : terbentuk oleh gaya tarik elektrostatik antara dua ion yang berlawanan tanda. Inti Ion : atom yang kehilangan elektron valensi 5

Ikatan terarah: kovalen dipole permanen Ikatan tak terarah: metal ion van der Waals terutama terjadi pada ikatan kovalen antara unsur non metal: Nitrogen; Oksigen; Carbon; Fluor; Chlor terutama pada Ikatan metal yang terjadi antara sejumlah besar atom dengan ikatan terarah akan terkumpul sedemikian rupa sehingga terpenuhi sudut ikatan atom dengan ikatan tak terarah pada umumnya terkumpul secara rapat (kompak) dan mengikuti aturan geometris yang ditentukan oleh perbedaan ukuran atom walaupun kita bedakan ikatan atom berarah dan ikatan tak berarah, namum dalam kenyataan material bisa terbentuk dari campuran dua macam ikatan tersebut 6
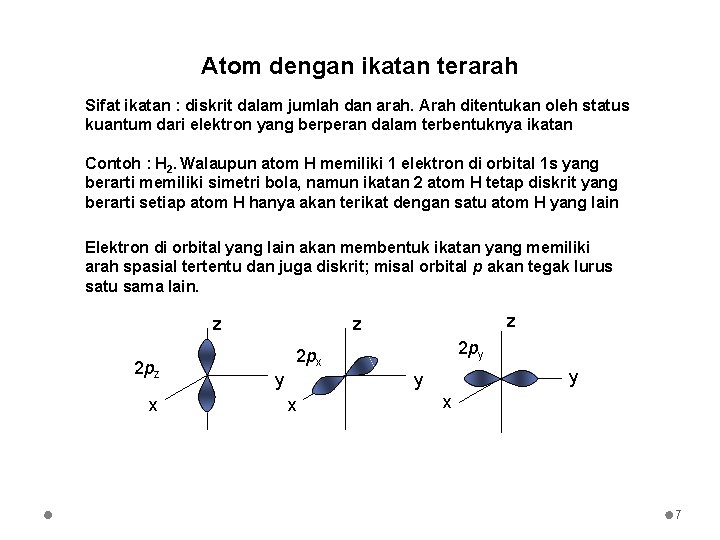
Atom dengan ikatan terarah Sifat ikatan : diskrit dalam jumlah dan arah. Arah ditentukan oleh status kuantum dari elektron yang berperan dalam terbentuknya ikatan Contoh : H 2. Walaupun atom H memiliki 1 elektron di orbital 1 s yang berarti memiliki simetri bola, namun ikatan 2 atom H tetap diskrit yang berarti setiap atom H hanya akan terikat dengan satu atom H yang lain Elektron di orbital yang lain akan membentuk ikatan yang memiliki arah spasial tertentu dan juga diskrit; misal orbital p akan tegak lurus satu sama lain. z 2 pz x z z 2 py 2 px y y y x x 7
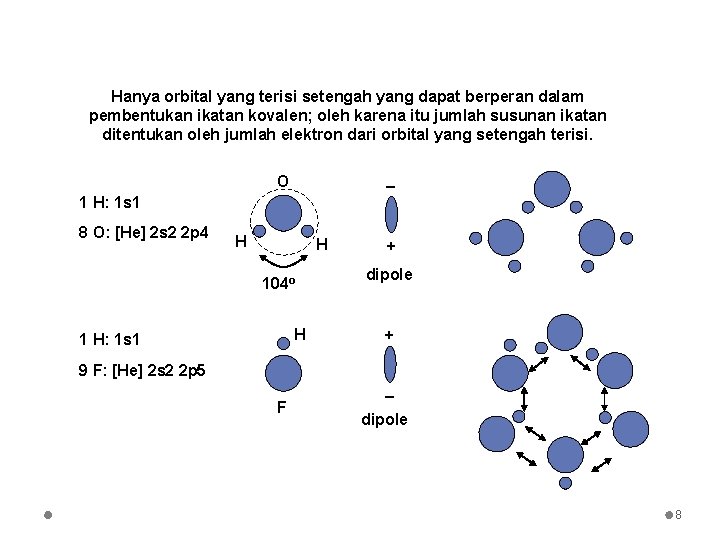
Hanya orbital yang terisi setengah yang dapat berperan dalam pembentukan ikatan kovalen; oleh karena itu jumlah susunan ikatan ditentukan oleh jumlah elektron dari orbital yang setengah terisi. O 1 H: 1 s 1 8 O: [He] 2 s 2 2 p 4 H H 104 o H 1 H: 1 s 1 + dipole + 9 F: [He] 2 s 2 2 p 5 F dipole 8
![Hibrida dari fungsi gelombang s dan p bisa terjadi 6 C: [He] 2 s Hibrida dari fungsi gelombang s dan p bisa terjadi 6 C: [He] 2 s](http://slidetodoc.com/presentation_image_h/1773e5bb9a6f97d1472fb25b0e83300e/image-9.jpg)
Hibrida dari fungsi gelombang s dan p bisa terjadi 6 C: [He] 2 s 2 2 p 2 Hibrida dari fungsi gelombang s dan p pada karbon membuat karbon memiliki 4 ikatan yang kuat mengarah ke susut-sudut tetrahedron Intan dan methane (CH 4) terbentuk dari ikatan hibrida ini. 14 Si [Ne] 3 s 2 3 p 2 32 Ge [Ar] 3 d 10 4 s 2 4 p 2 50 Sn [Kr] 4 d 10 5 s 2 5 p 2 juga membentuk orbital tetrahedral seperti karbon karena hibrida 3 s-sp, 4 s 4 p, dan 5 s-5 p, sama dengan 2 s-2 p. Karena ikatan kovalen adalah diskrit dalam jumlah maupun arah, maka terdapat banyak kemungkinan struktur ikatan, tergantung dari ikatan mana yang digunakan oleh setiap atom. 9
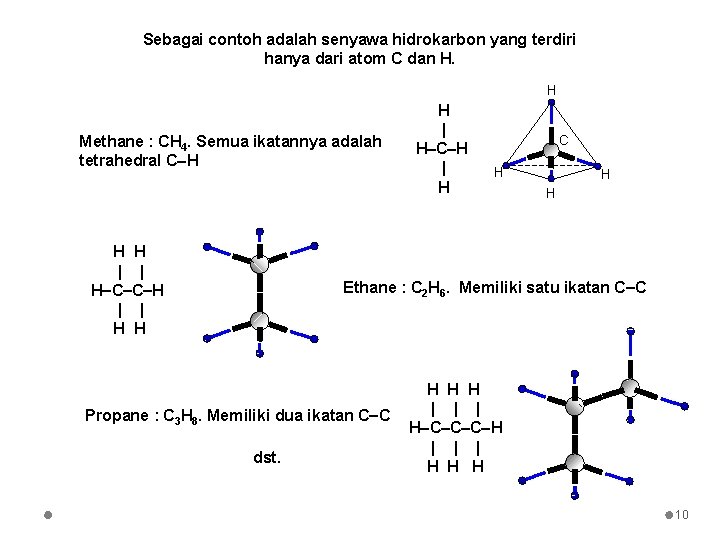
Sebagai contoh adalah senyawa hidrokarbon yang terdiri hanya dari atom C dan H. H Methane : CH 4. Semua ikatannya adalah tetrahedral C H H H | | H C C H | | H H H | H C H H H Ethane : C 2 H 6. Memiliki satu ikatan C C Propane : C 3 H 8. Memiliki dua ikatan C C dst. H H H | | | H C C C H | | | H H H 10
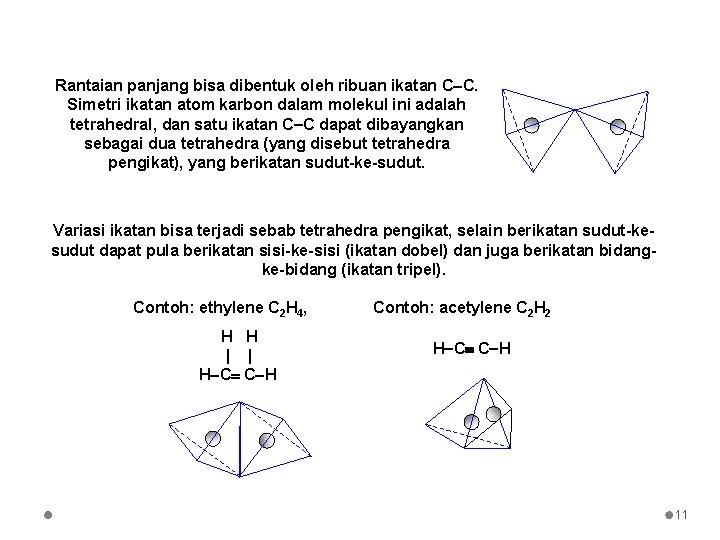
Rantaian panjang bisa dibentuk oleh ribuan ikatan C C. Simetri ikatan atom karbon dalam molekul ini adalah tetrahedral, dan satu ikatan C C dapat dibayangkan sebagai dua tetrahedra (yang disebut tetrahedra pengikat), yang berikatan sudut-ke-sudut. Variasi ikatan bisa terjadi sebab tetrahedra pengikat, selain berikatan sudut-kesudut dapat pula berikatan sisi-ke-sisi (ikatan dobel) dan juga berikatan bidangke-bidang (ikatan tripel). Contoh: ethylene C 2 H 4, H H | | H C C H Contoh: acetylene C 2 H 2 H C C H 11

Peningkatan kekuatan ikatan sebagai hasil dari terjadinya ikatan multiple disertai penurunan jarak antar atom karbon: 1, 54 Ä pada ikatan tunggal 1, 33 Ä pada ikatan dobel 1, 20 Ä pada ikatan tripel Ikatan C C juga bisa digabung dari ikatan tunggal dan ikatan dobel, seperti yang terjadi pada benzena 12

Atom dengan Ikatan Tak Terarah Atom berukuran sama Pada ikatan tak terarah kita dapat mengharapkan bahwa atom-atom material dalam keadaan padat akan terkumpul secara ringkas / kompak menempati ruang sekecil mungkin. Dengan cara ini jumlah ikatan per satuan volume menjadi maksimum yang berarti energi ikatan per satuan volume menjadi minimum. Sebagai pendekatan pertama kita memandang atom sebagai kelereng keras. Secara geometris, ada 12 kelereng yang dapat berposisi mengelilingi 1 kelereng (terletak di pusat) dan mereka saling menyentuh satu sama lain. Ada 2 macam susunan kompak yang teramati dalam banyak struktur metal dan elemen mulia, yaitu hexagonal close-packed (HCP) dan face-centered cubic (FCC). 13
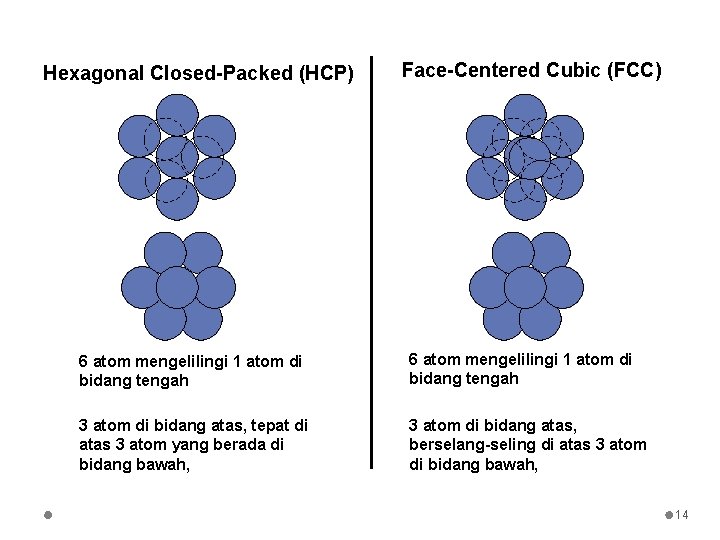
Hexagonal Closed-Packed (HCP) Face-Centered Cubic (FCC) 6 atom mengelilingi 1 atom di bidang tengah 3 atom di bidang atas, tepat di atas 3 atom yang berada di bidang bawah, 3 atom di bidang atas, berselang-seling di atas 3 atom di bidang bawah, 14

Semua elemen mulia membentuk struktur kompak jika membeku pada temperatur sangat rendah, dan sekitar 2/3 dari jenis metal membentuk struktur HCP atau FCC pada temperatur kamar. 1/3 dari jenis metal yang tidak membentuk struktur kompak pada temperatur kamar adalah metal alkali (Na, K, dll) dan metal transisi (Fe, Cr, W, dsb). Mereka cenderung membentuk struktur body-centered cubic (BCC). Walaupun kurang kompak, susunan ini memiliki energi total relatif rendah. Kebanyakan metal alkali berubah dari BCC ke FCC atau HCP pada temperatur yang sangat rendah. Hal ini menunjukkan bahwa susunan kurang kompak yang terjadi pada temperatur kamar adalah akibat dari pengaruh energi thermal Susunan BCC pada metal transisi diduga sebagai akibat dari ikatan metal ini yang sebagian berupa ikatan kovalen (yang merupakan ikatan berarah). 15

Atom dengan Ikatan Tak Terarah Atom berukuran tak sama Ikatan ion membentuk struktur yang terdiri dari atom-atom yang berbeda ukuran karena anion dan kation pada umumnya sangat berbeda ukuran. Perbedaan ini terjadi karena transfer elektron dari atom yang elektro-positif ke atom yang elektronegatif membuat anion berukuran lebih besar dari kation. Anion : ion negatif sebagai hasil dari atom elektronegatif yang memperoleh tambahan elektron. Kation : ion positif sebagai hasil dari atom elektropositif yang kehilangan satu atau lebih elektron. Ikatan ini tak terarah dan juga tidak diskrit, namun pada skala besar kenetralan harus tetap terjaga. 16

Bilangan Koordinasi Bilangan yang menunjukkan perbandingan jumlah ion elemen A yang mengelilingi ion elemen K yang lebih kecil disebut bilangan koordinasi (Ligancy). Bilangan Koordinasi tergantung dari perbedaan radius antara ion K dan A : makin besar perbedaannya, ligancy akan semakin kecil. Bilangan Koordinasi Rasio Radius K/A 2 0 – 0, 155 3 Polyhedron Koordinasi Packing garis linier 0, 155 – 0, 225 segitiga triangular 4 0, 225 – 0, 414 tetrahedron Tetrahedral 6 0, 414 – 0, 732 oktahedron Octahedral 8 0, 732 – 1, 0 kubus cubic 12 1, 0 HCP 12 1, 0 FCC 17
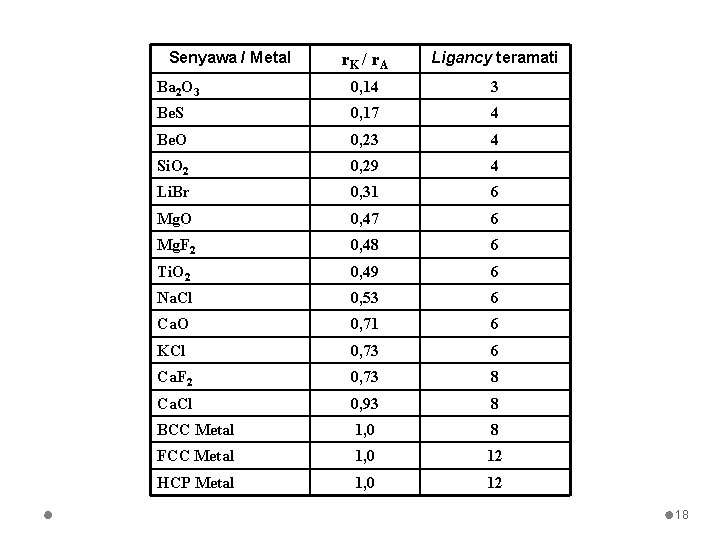
Senyawa / Metal r. K / r A Ligancy teramati Ba 2 O 3 0, 14 3 Be. S 0, 17 4 Be. O 0, 23 4 Si. O 2 0, 29 4 Li. Br 0, 31 6 Mg. O 0, 47 6 Mg. F 2 0, 48 6 Ti. O 2 0, 49 6 Na. Cl 0, 53 6 Ca. O 0, 71 6 KCl 0, 73 6 Ca. F 2 0, 73 8 Ca. Cl 0, 93 8 BCC Metal 1, 0 8 FCC Metal 1, 0 12 HCP Metal 1, 0 12 18
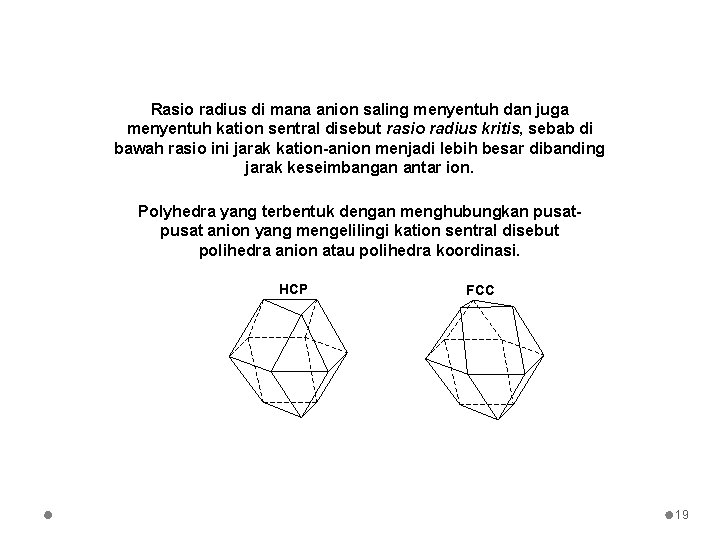
Rasio radius di mana anion saling menyentuh dan juga menyentuh kation sentral disebut rasio radius kritis, sebab di bawah rasio ini jarak kation-anion menjadi lebih besar dibanding jarak keseimbangan antar ion. Polyhedra yang terbentuk dengan menghubungkan pusat anion yang mengelilingi kation sentral disebut polihedra anion atau polihedra koordinasi. HCP FCC 19
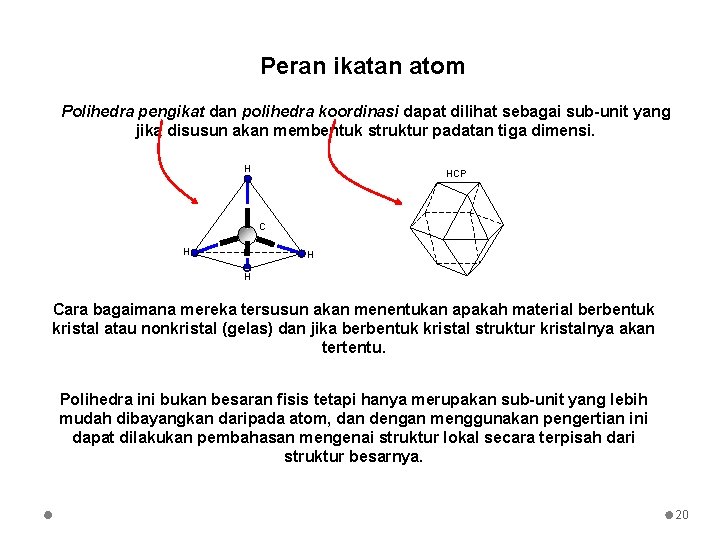
Peran ikatan atom Polihedra pengikat dan polihedra koordinasi dapat dilihat sebagai sub-unit yang jika disusun akan membentuk struktur padatan tiga dimensi. H HCP C H H H Cara bagaimana mereka tersusun akan menentukan apakah material berbentuk kristal atau nonkristal (gelas) dan jika berbentuk kristal struktur kristalnya akan tertentu. Polihedra ini bukan besaran fisis tetapi hanya merupakan sub-unit yang lebih mudah dibayangkan daripada atom, dan dengan menggunakan pengertian ini dapat dilakukan pembahasan mengenai struktur lokal secara terpisah dari struktur besarnya. 20

Polihedra koordinasi berperilaku sebagai suatu unit yang erat terikat jika valensi atom sentral lebih dari setengah dari total valensi atom yang terikat dengannya. Jika valensi atom sentral sama dengan valensi total atom yang mengelilinginya maka sub-unit itu adalah molekul. Titik leleh suatu material bergantung dari kekuatan ikatan atom. Ia makin rendah jika polihedra sub-unit terbangun dari kelompok atom yang diskrit, yang terikat satu sama lain dengqan ikatan sekunder dibandingkan dengan bila ikatannya primer. Contoh: methane, CH 4, memiliki titik leleh 184 o. C; ethane, C 2 H 6, titik leleh 172 o. C; polyethylene, titik leleh 125 o. C; polyethylene saling terikat dengan ikatan C-C dapat stabil sampai 300 o. C. 21

Kuliah Terbuka Mengenal Sifat Material II Sesi-1 Sudaryatno Sudirham 22
- Slides: 22