Sejtmag II Dr habil Khidai Lszl SE Genetikai

Sejtmag II. Dr. habil. Kőhidai László SE, Genetikai, Sejt- és Immunbiológiai Intézet 2008.
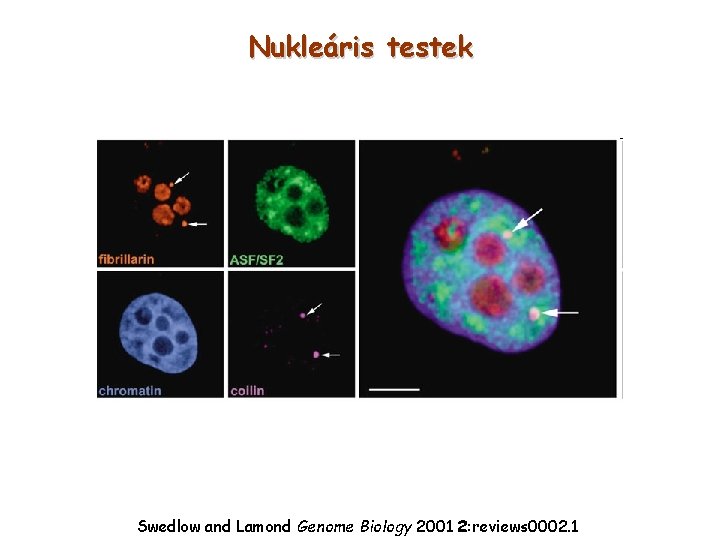
Nukleáris testek Swedlow and Lamond Genome Biology 2001 2: reviews 0002. 1
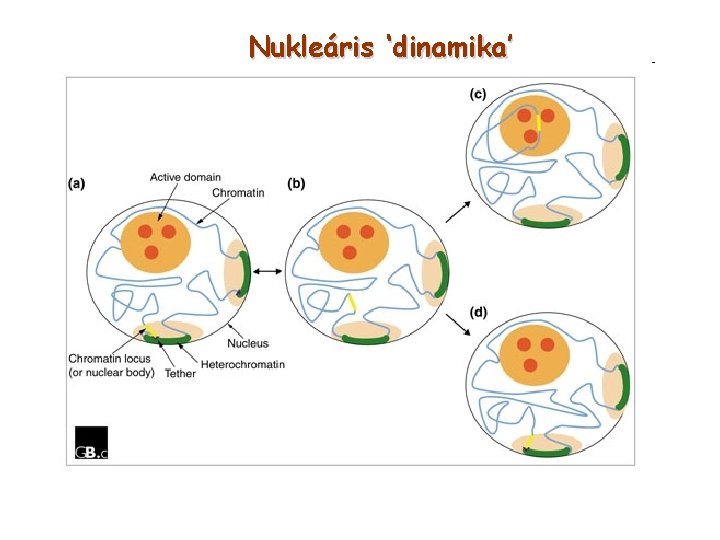
Nukleáris ‘dinamika’

Adatok a humán genomról 3, 000, 000 bázispár ~ 500, 000 kodon Ha 1 kodon = 1 szó és 1 oldal 850 szó AKKOR A humán genom 590, 000 oldalnak felel meg Ha a fenti könyvet 3 bázis/perc sebességgel olvasnánk AKKOR 47. 6 évig tartana az elolvasása
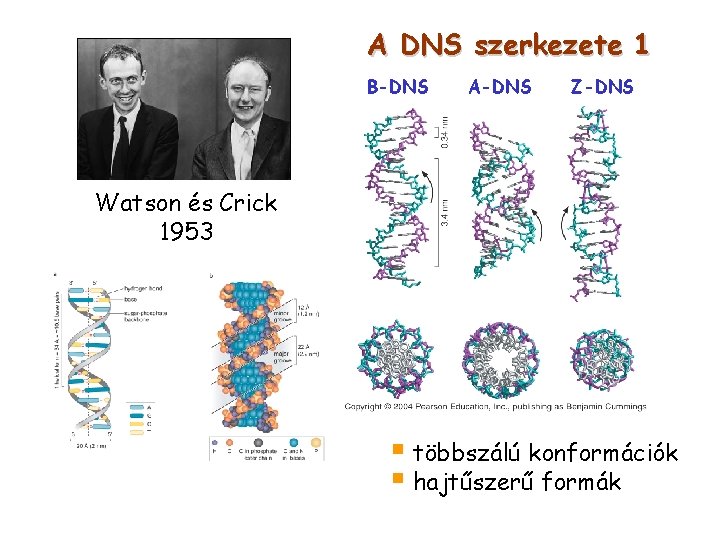
A DNS szerkezete 1 B-DNS A-DNS Z-DNS Watson és Crick 1953 § többszálú konformációk § hajtűszerű formák
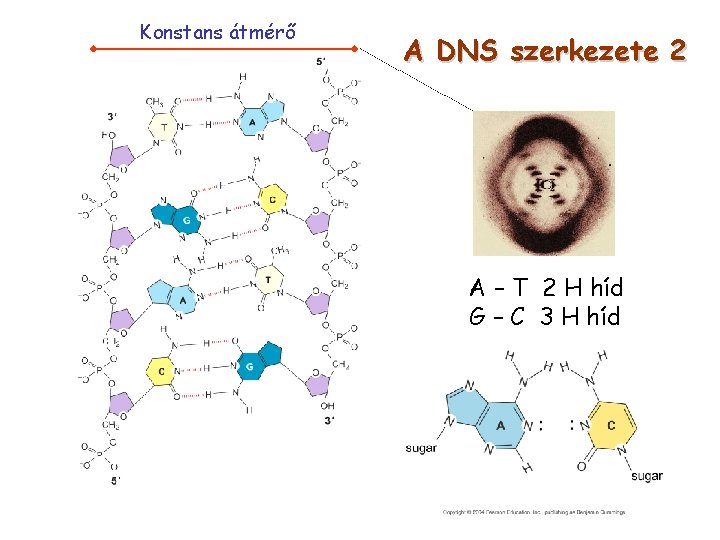
Konstans átmérő A DNS szerkezete 2 A – T 2 H híd G – C 3 H híd
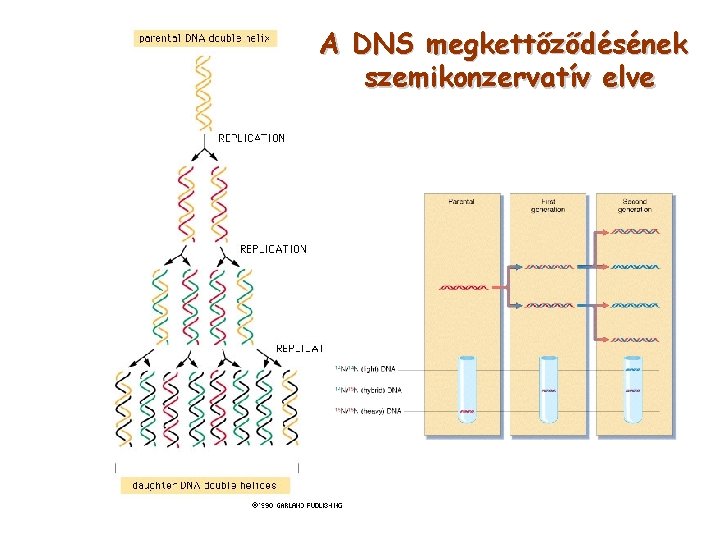
A DNS megkettőződésének szemikonzervatív elve

Néhány fontosabb enzim Kornberg, Arthur 1959 DNS replikáció enzimeinek szerepe § Helikáz – DNS széttekerése § Topoizomeráz – „supercoil”-ok letekerése § Primáz – RNS-primer készítése § DNS polimeráz III – új DNS szál szintézise § DNS polimeráz I – az RNS primer 1. bázisának leválasztása § DNS ligáz – DNS fragmentumok összeillesztése
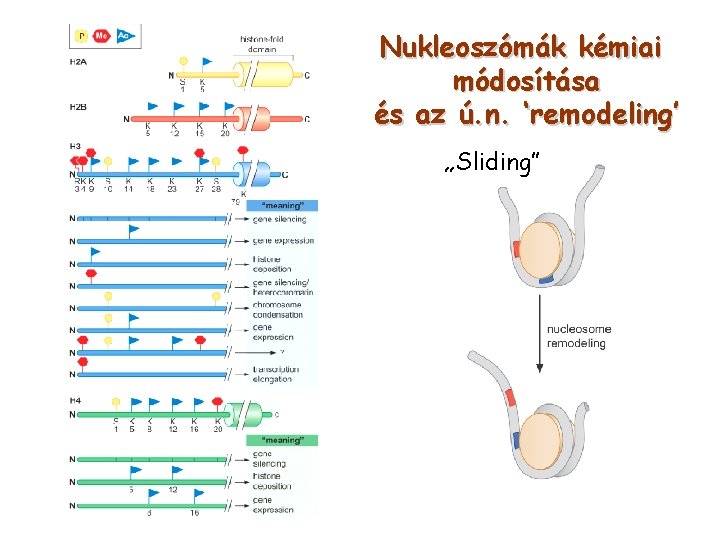
Nukleoszómák kémiai módosítása és az ú. n. ‘remodeling’ „Sliding”
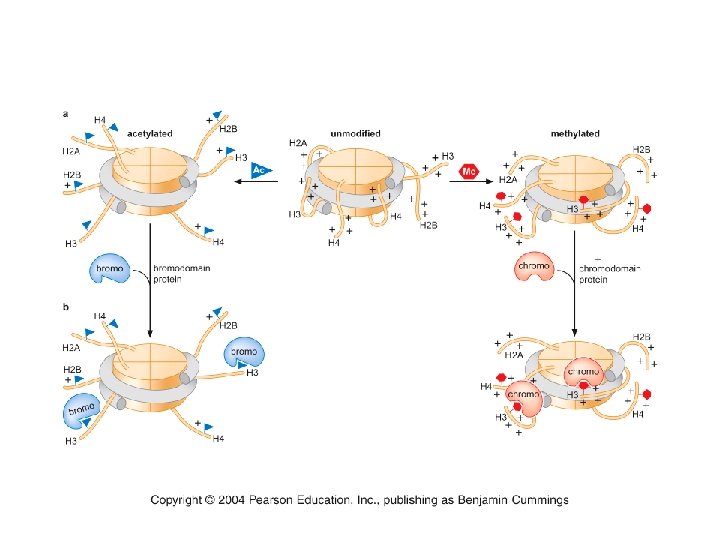
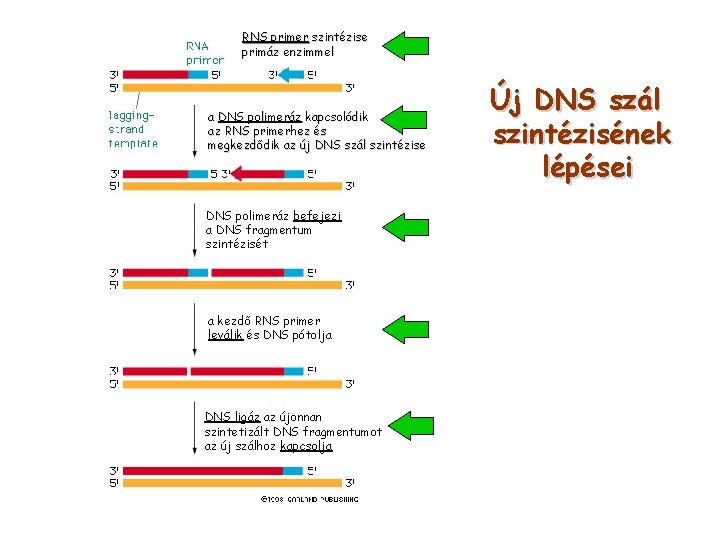
RNS primer szintézise primáz enzimmel a DNS polimeráz kapcsolódik az RNS primerhez és megkezdődik az új DNS szál szintézise DNS polimeráz befejezi a DNS fragmentum szintézisét a kezdő RNS primer leválik és DNS pótolja DNS ligáz az újonnan szintetizált DNS fragmentumot az új szálhoz kapcsolja Új DNS szál szintézisének lépései
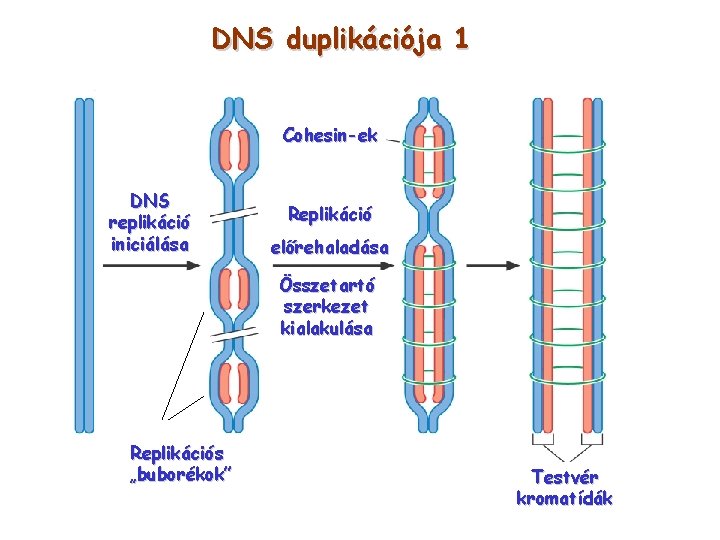
DNS duplikációja 1 Cohesin-ek DNS replikáció iniciálása Replikáció előrehaladása Összetartó szerkezet kialakulása Replikációs „buborékok” Testvér kromatídák
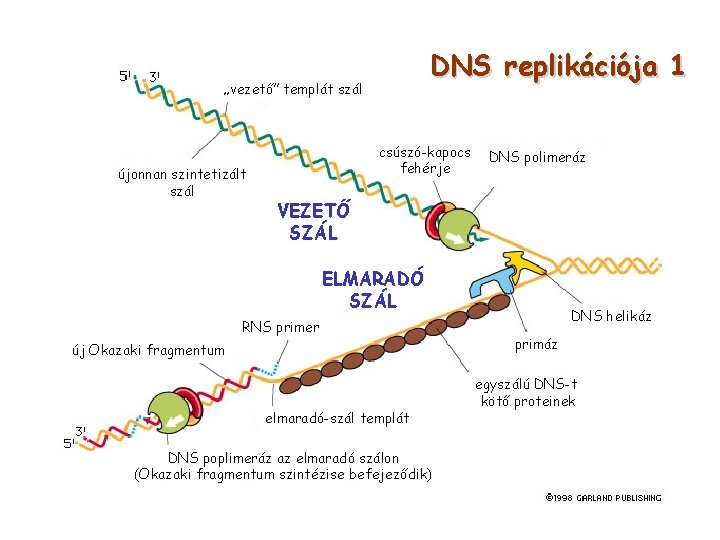
DNS replikációja 1 „vezető” templát szál újonnan szintetizált szál csúszó-kapocs fehérje DNS polimeráz VEZETŐ SZÁL ELMARADÓ SZÁL RNS primer új Okazaki fragmentum elmaradó-szál templát DNS poplimeráz az elmaradó szálon (Okazaki fragmentum szintézise befejeződik) DNS helikáz primáz egyszálú DNS-t kötő proteinek
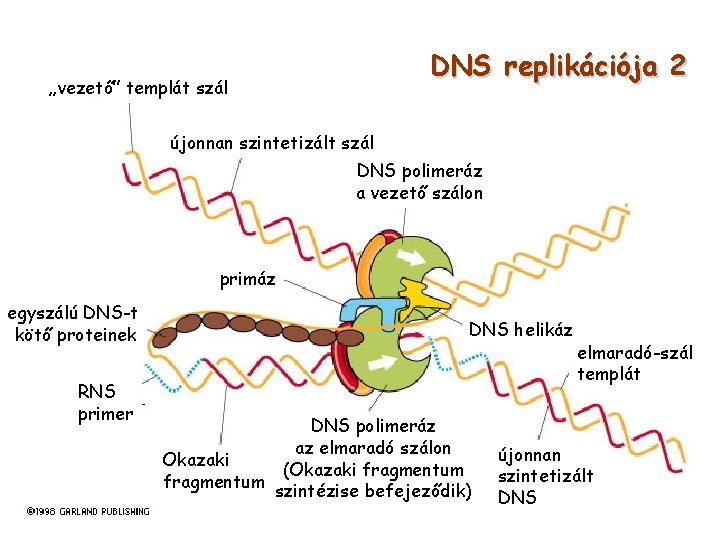
DNS replikációja 2 „vezető” templát szál újonnan szintetizált szál DNS polimeráz a vezető szálon primáz egyszálú DNS-t kötő proteinek RNS primer DNS helikáz DNS polimeráz az elmaradó szálon Okazaki (Okazaki fragmentum szintézise befejeződik) elmaradó-szál templát újonnan szintetizált DNS
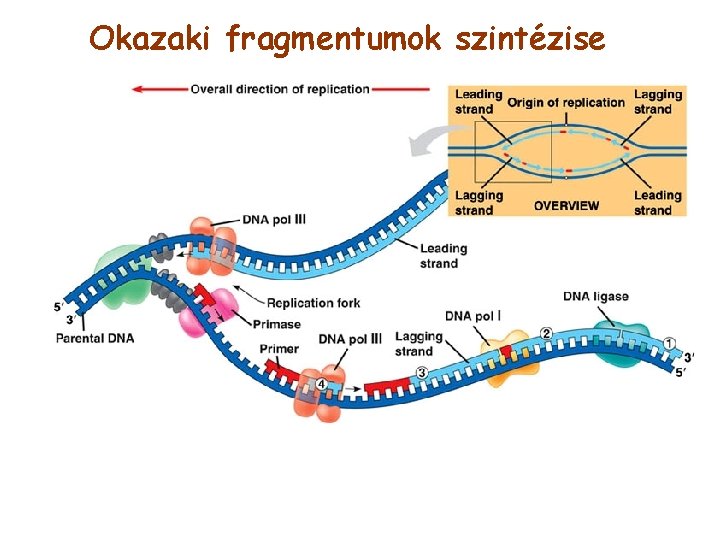
Okazaki fragmentumok szintézise
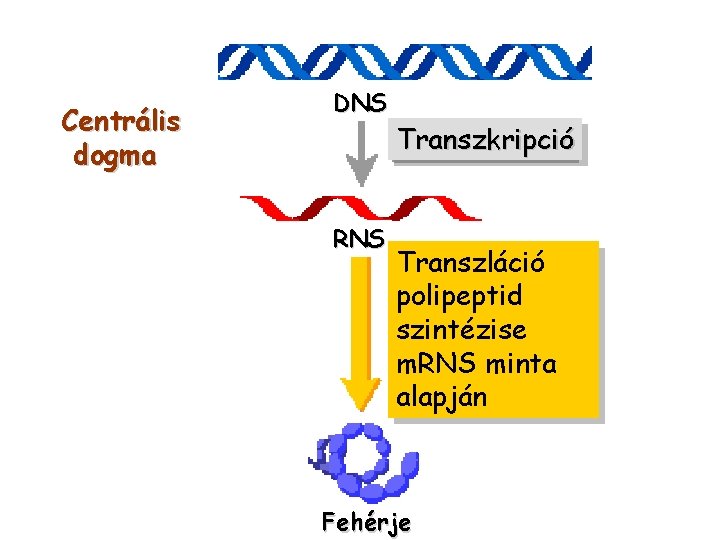
Centrális dogma DNS RNS Transzkripció Transzláció polipeptid szintézise m. RNS minta alapján Fehérje

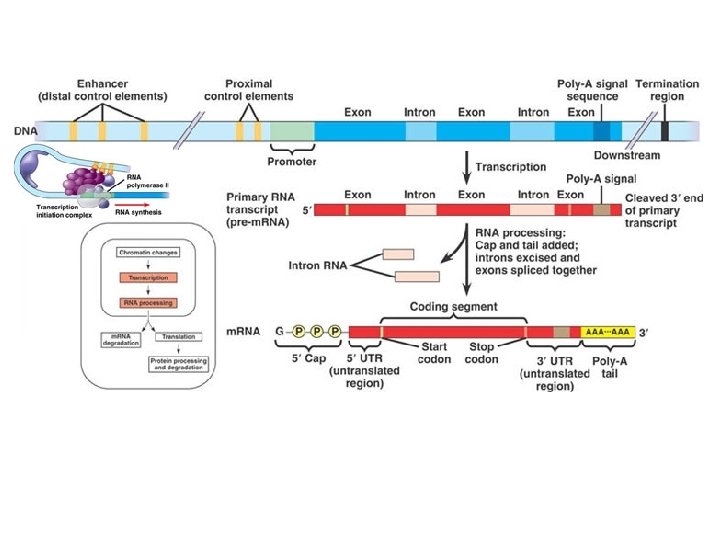
m. RNS érés és „szerkesztés” hn. RNS - (heterogeneous nuclear RNA) – elsődlegesen átíródó RNS - eukaryotákban 5’ sapka – 7 -methylguanosine az m. RNS 5’ végén 3’ jellegűvé teszi a molekulát védi az m. RNS-t a lebomlástól Poli-adenin farok – 20 -200 adenin tartalmú szekvencia a poli-A-polimeráz helyezi fel növeli az m. RNS életidejét pre-m. RNS - 100 -400 nukleotidos RNS
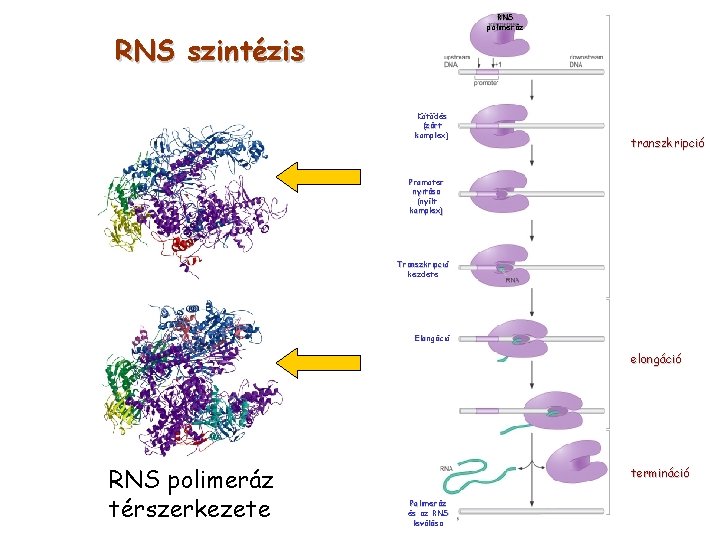
RNS polimeráz RNS szintézis Kötődés (zárt komplex) transzkripció Promoter nyitása (nyílt komplex) Transzkripció kezdete Elongáció elongáció RNS polimeráz térszerkezete termináció Polimeráz és az RNS leválása
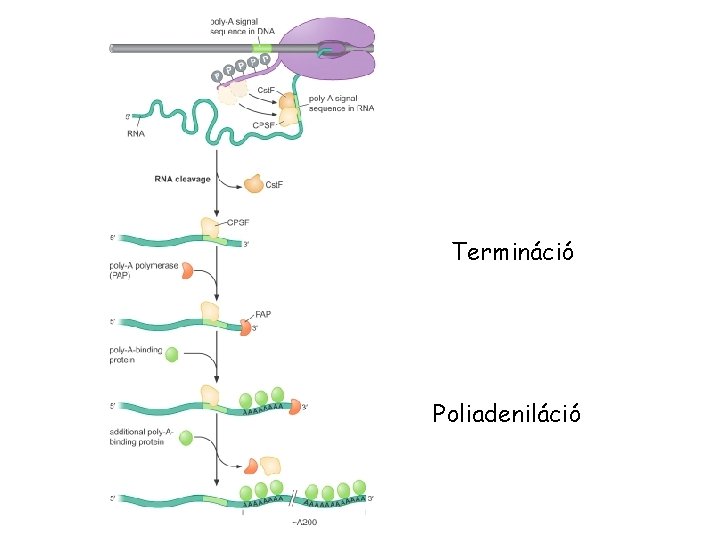
Termináció Poliadeniláció
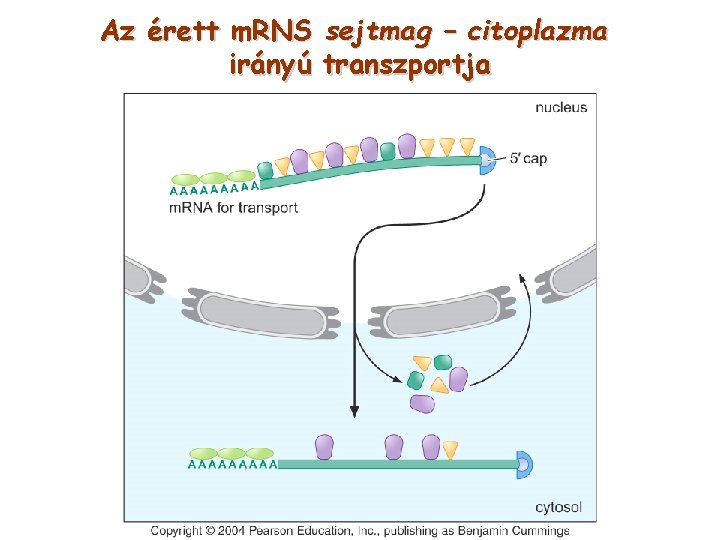
Az érett m. RNS sejtmag – citoplazma irányú transzportja
Roberts, Richard J. 1993 Sharp, Phillip A.
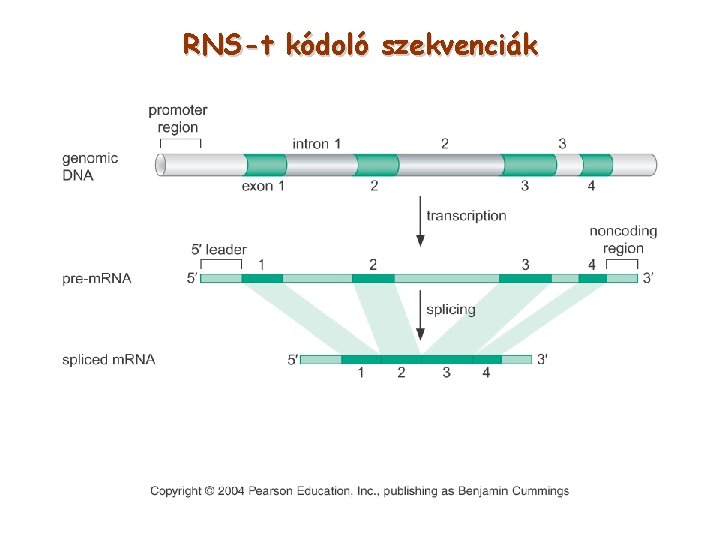
RNS-t kódoló szekvenciák
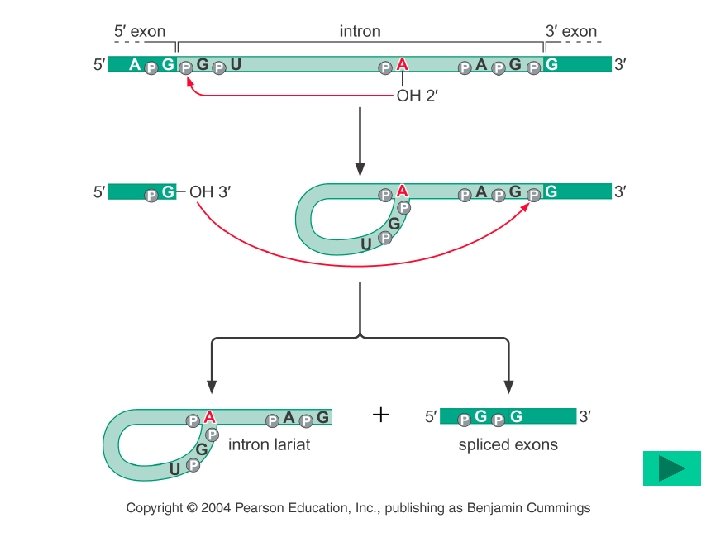
Splicing
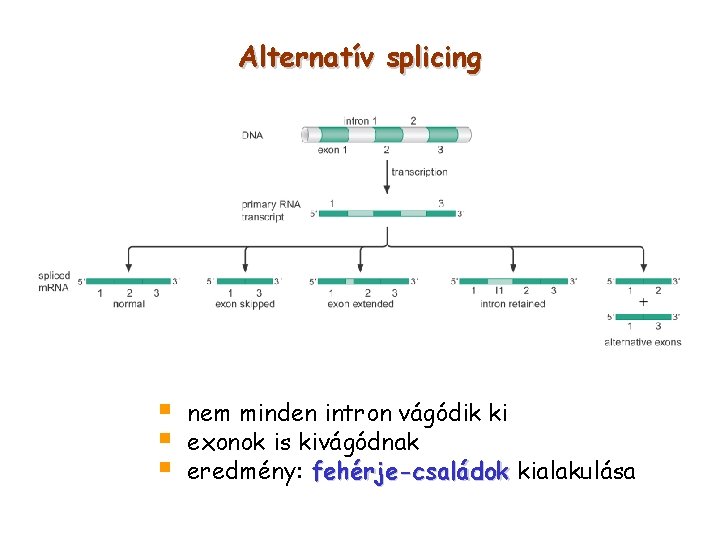
Alternatív splicing § § § nem minden intron vágódik ki exonok is kivágódnak eredmény: fehérje-családok kialakulása
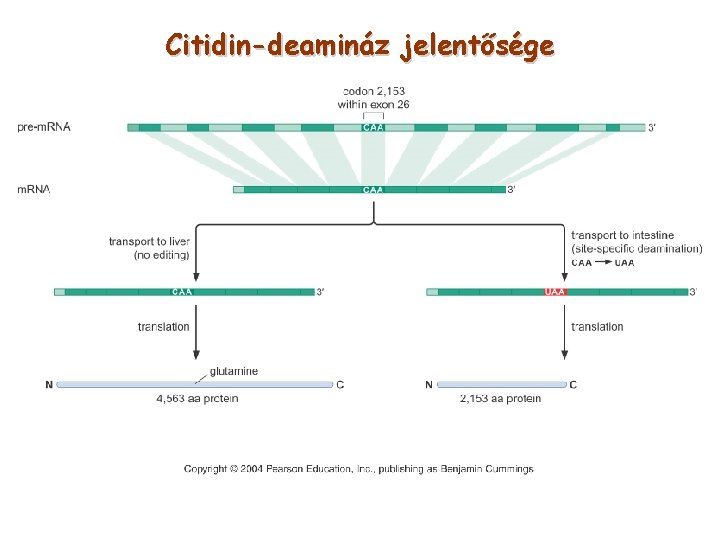
Citidin-deamináz jelentősége
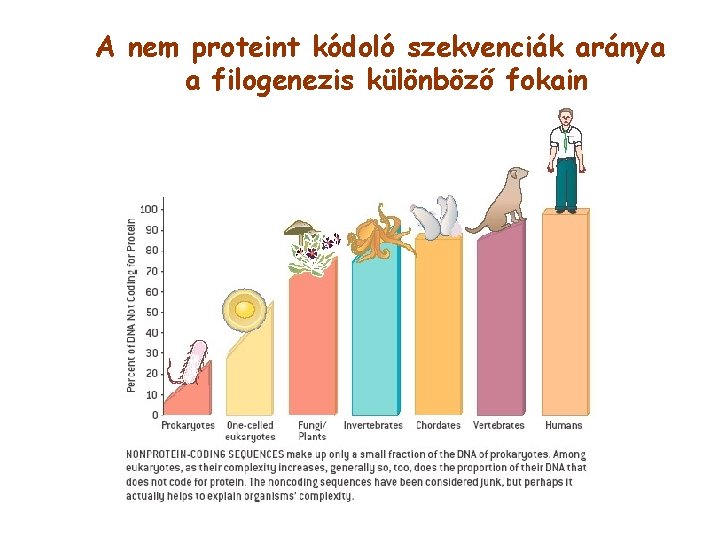
A nem proteint kódoló szekvenciák aránya a filogenezis különböző fokain
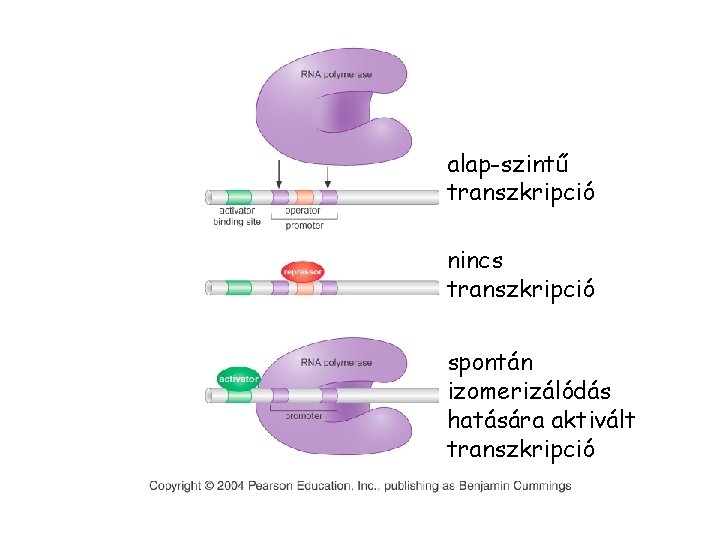
alap-szintű transzkripció nincs transzkripció spontán izomerizálódás hatására aktivált transzkripció
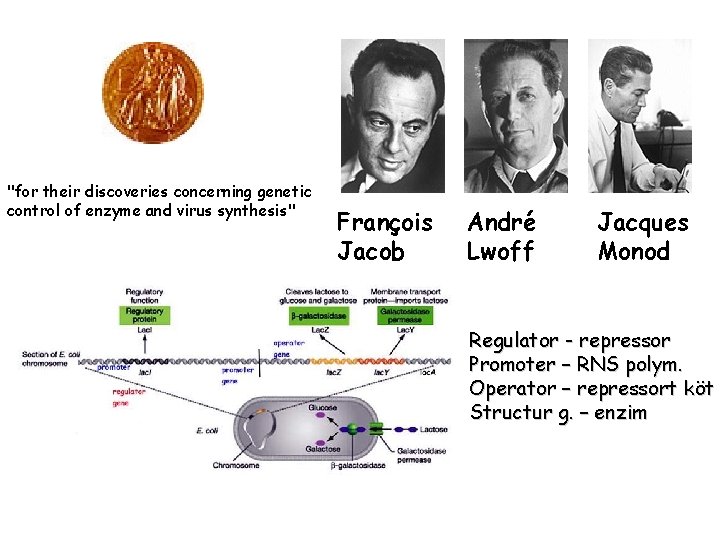
"for their discoveries concerning genetic control of enzyme and virus synthesis" François Jacob André Lwoff Jacques Monod Regulator - repressor Promoter – RNS polym. Operator – repressort köt Structur g. – enzim
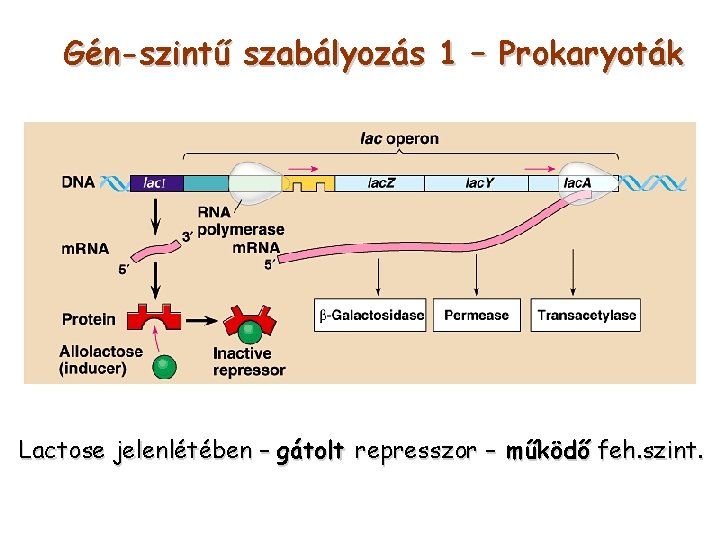
Gén-szintű szabályozás 1 – Prokaryoták Lactose jelenlétében – gátolt represszor – működő feh. szint.
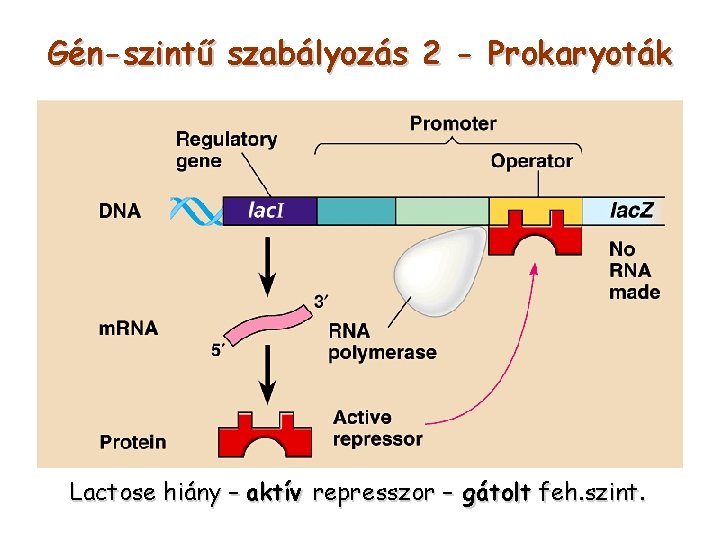
Gén-szintű szabályozás 2 - Prokaryoták Lactose hiány – aktív represszor – gátolt feh. szint.

Gén-szintű szabályozás 3 - Prokaryoták Trp hiány – gátolt represszor – működő feh. szint. Trp jelenlétében – aktív represszor – gátolt feh. szint.
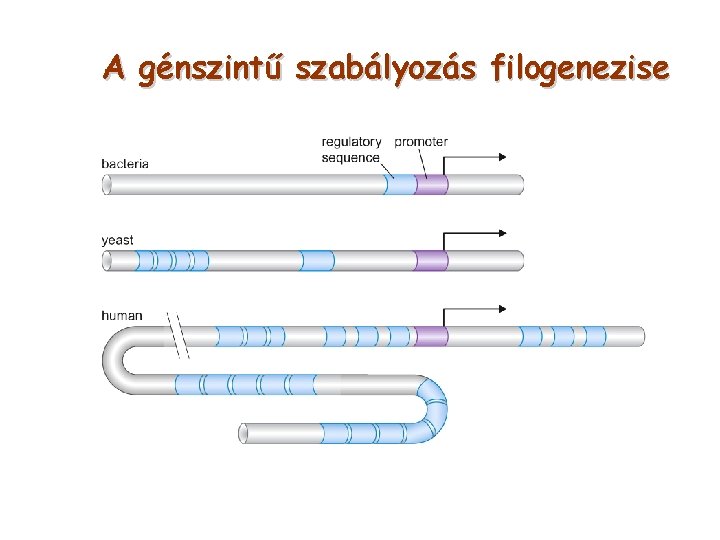
A génszintű szabályozás filogenezise
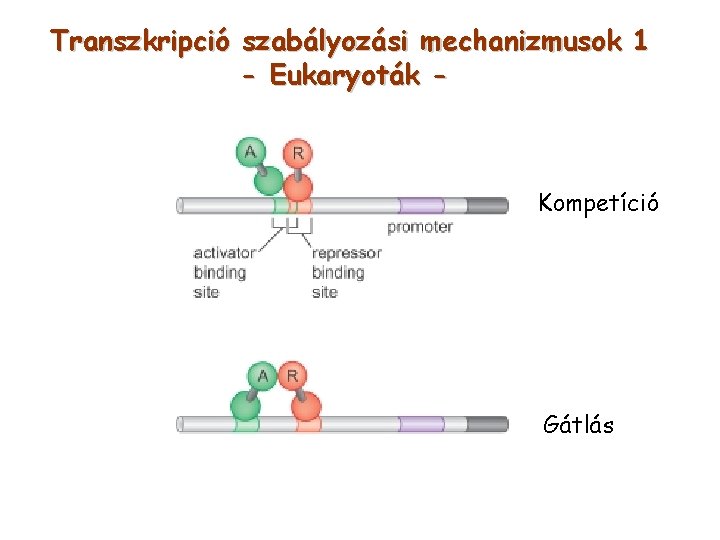
Transzkripció szabályozási mechanizmusok 1 - Eukaryoták - Kompetíció Gátlás
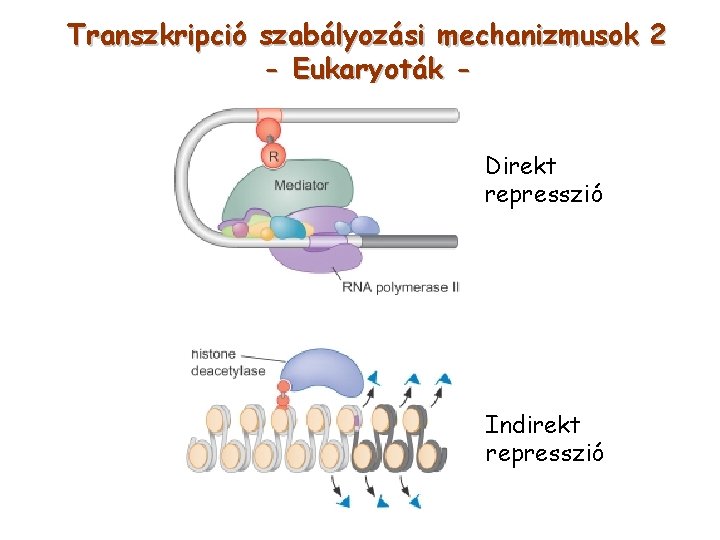
Transzkripció szabályozási mechanizmusok 2 - Eukaryoták Direkt represszió Indirekt represszió
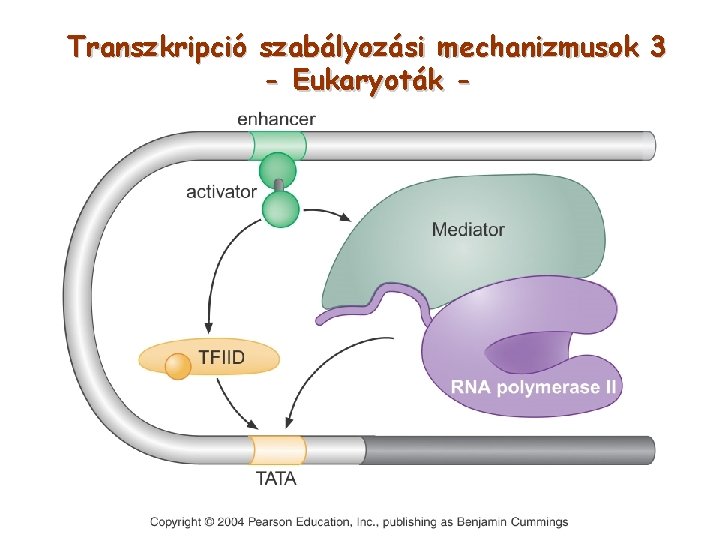
Transzkripció szabályozási mechanizmusok 3 - Eukaryoták -
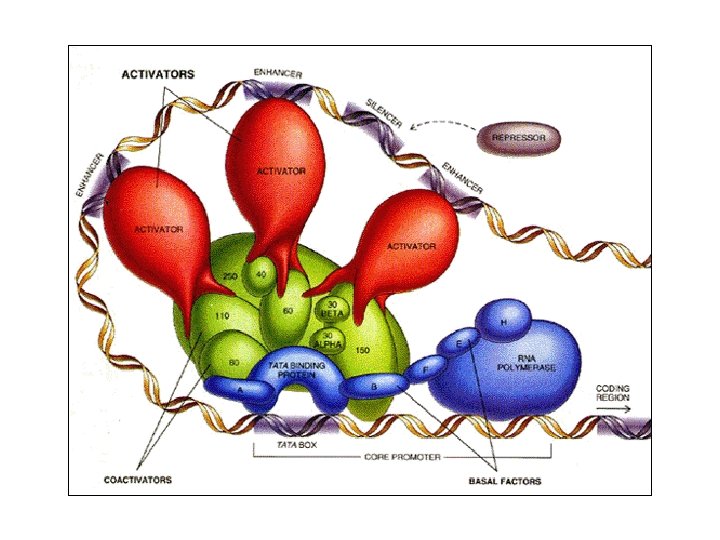
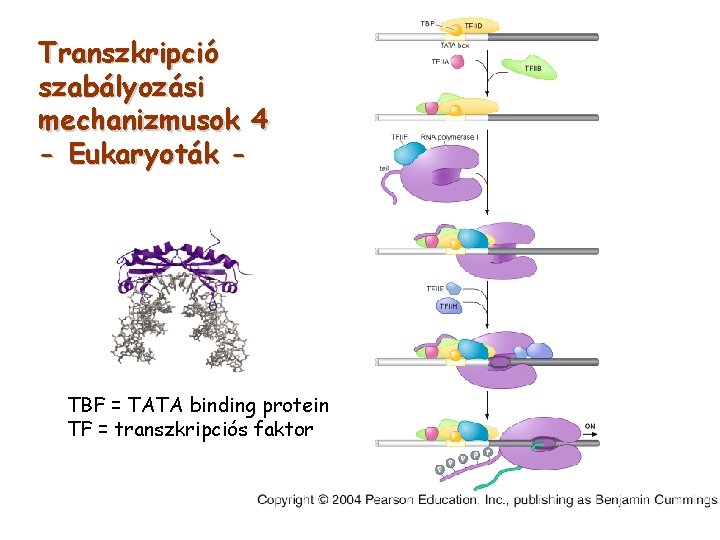
Transzkripció szabályozási mechanizmusok 4 - Eukaryoták - TBF = TATA binding protein TF = transzkripciós faktor
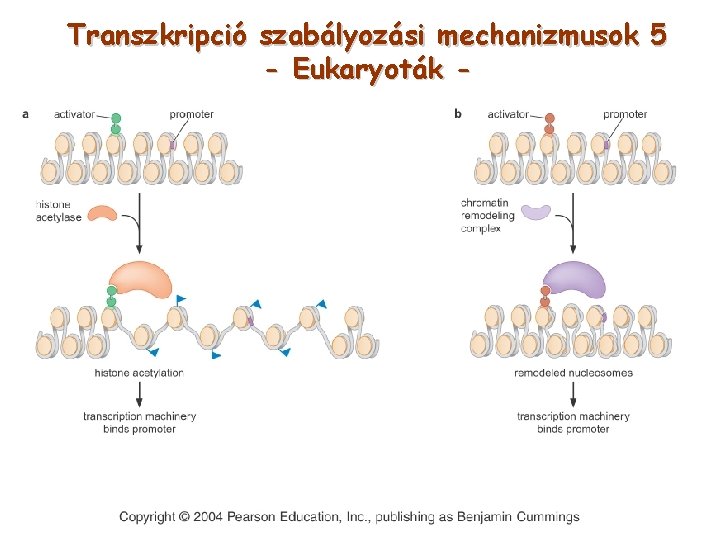
Transzkripció szabályozási mechanizmusok 5 - Eukaryoták -
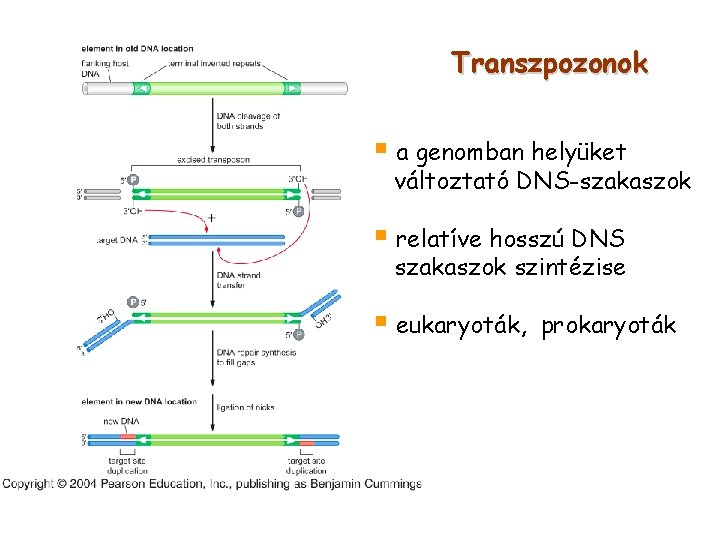
Transzpozonok § a genomban helyüket változtató DNS-szakaszok § relatíve hosszú DNS szakaszok szintézise § eukaryoták, prokaryoták
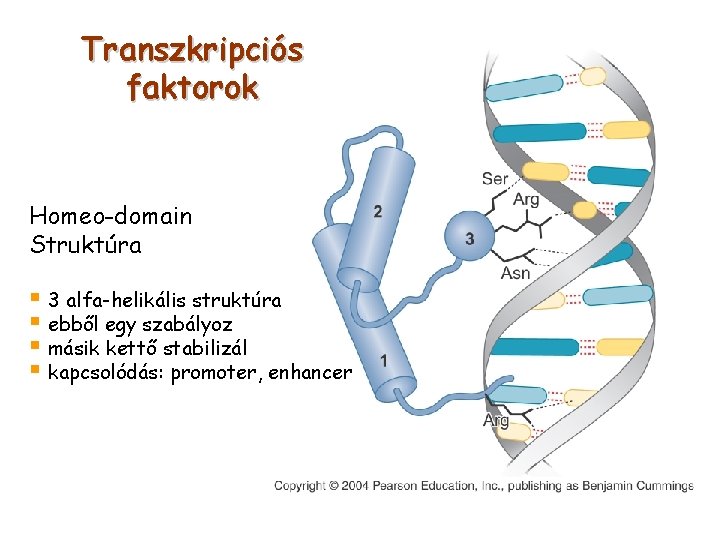
Transzkripciós faktorok Homeo-domain Struktúra § 3 alfa-helikális struktúra § ebből egy szabályoz § másik kettő stabilizál § kapcsolódás: promoter, enhancer
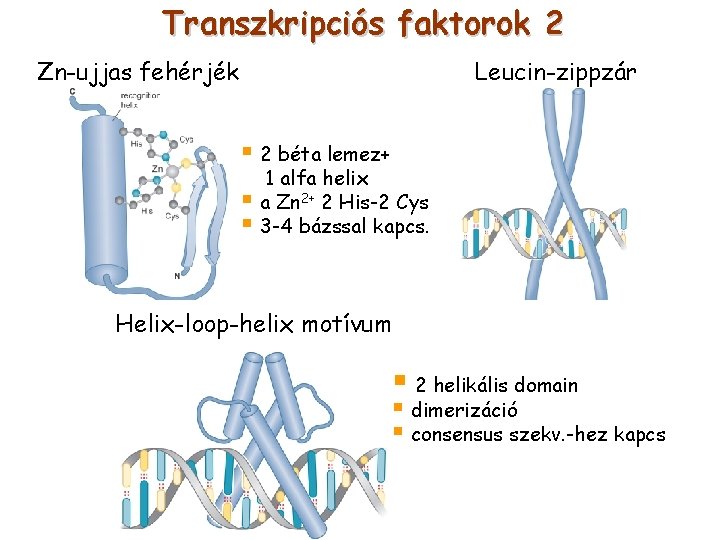
Transzkripciós faktorok 2 Zn-ujjas fehérjék Leucin-zippzár § 2 béta lemez+ 1 alfa helix § a Zn 2+ 2 His-2 Cys § 3 -4 bázssal kapcs. Helix-loop-helix motívum § 2 helikális domain § dimerizáció § consensus szekv. -hez kapcs
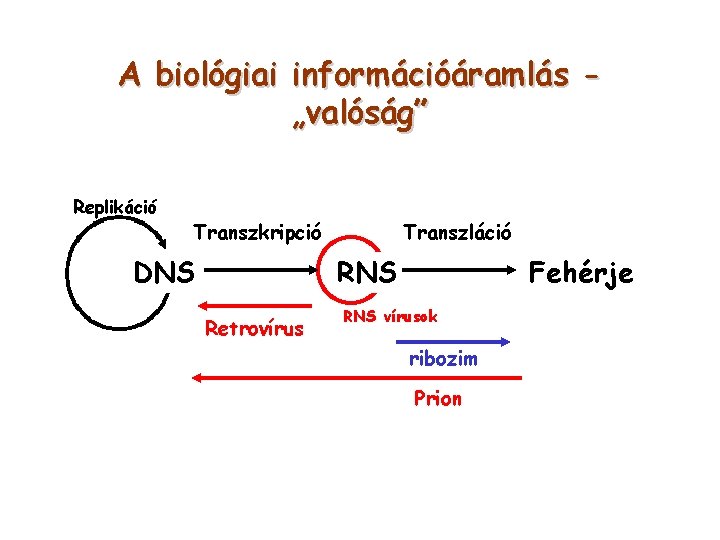
A biológiai információáramlás „valóság” Replikáció Transzkripció DNS Transzláció RNS Retrovírus Fehérje RNS vírusok ribozim Prion
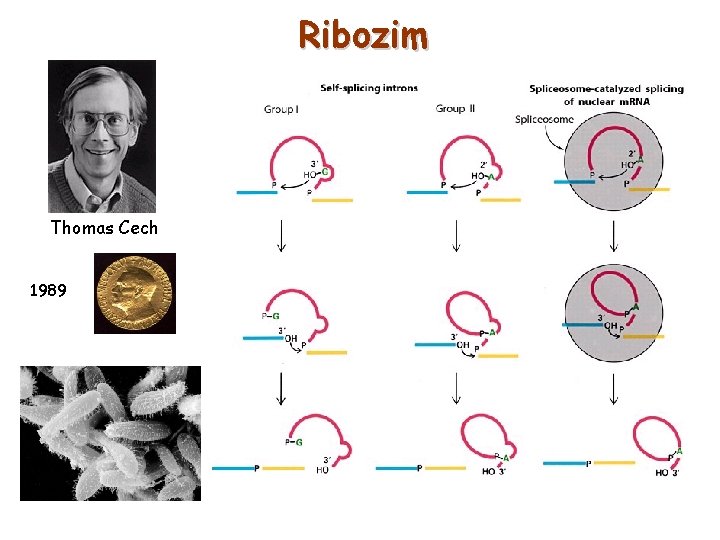
Ribozim Thomas Cech 1989
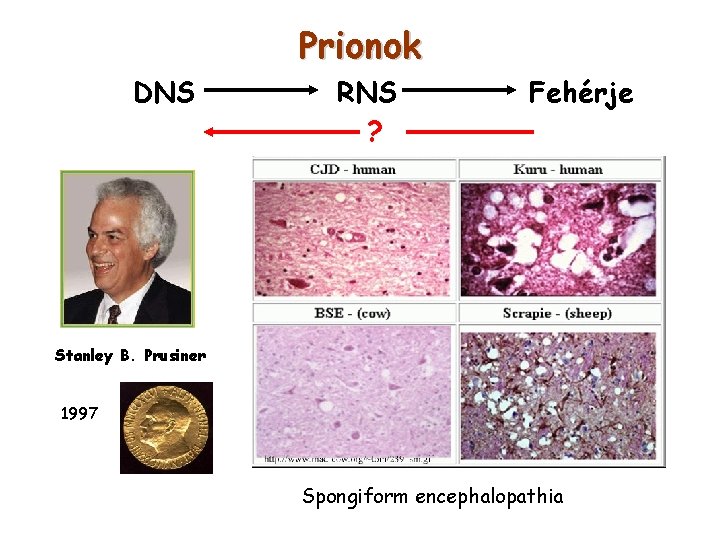
Prionok DNS RNS ? Fehérje Stanley B. Prusiner 1997 Spongiform encephalopathia
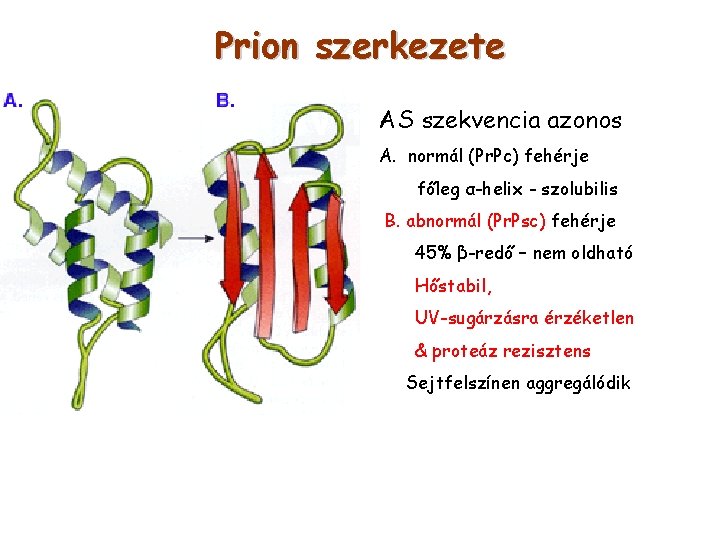
Prion szerkezete AS szekvencia azonos A. normál (Pr. Pc) fehérje főleg α-helix - szolubilis B. abnormál (Pr. Psc) fehérje 45% β-redő – nem oldható Hőstabil, UV-sugárzásra érzéketlen & proteáz rezisztens Sejtfelszínen aggregálódik
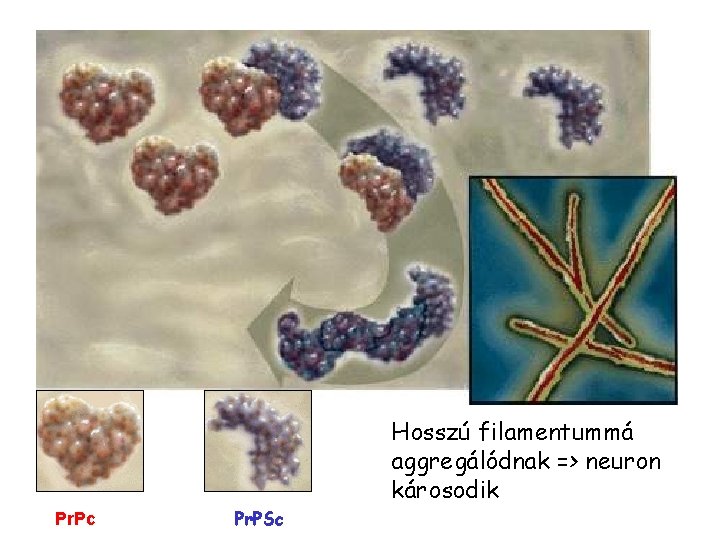
Hosszú filamentummá aggregálódnak => neuron károsodik Pr. Pc Pr. PSc
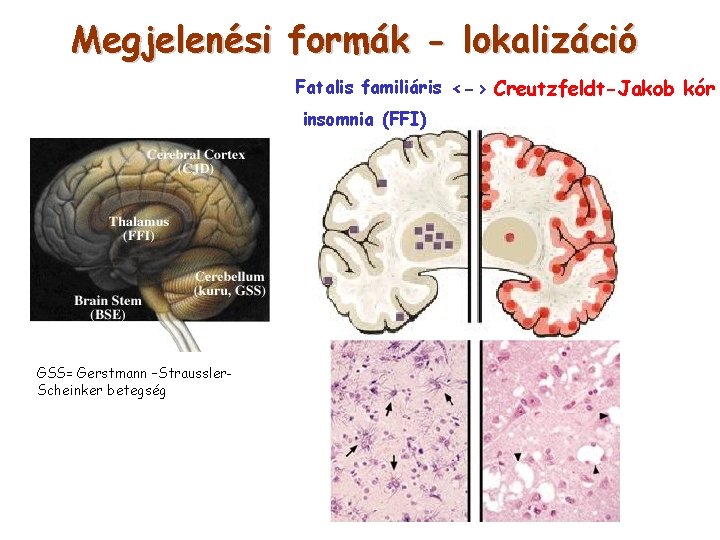
Megjelenési formák - lokalizáció Fatalis familiáris <-> Creutzfeldt-Jakob kór insomnia (FFI) GSS= Gerstmann –Straussler. Scheinker betegség

Egyéb ellentmondások § Metilációs mintázat öröklődése => Epigenetika § Strukturális öröklődés § Szenz – antiszenz szál?
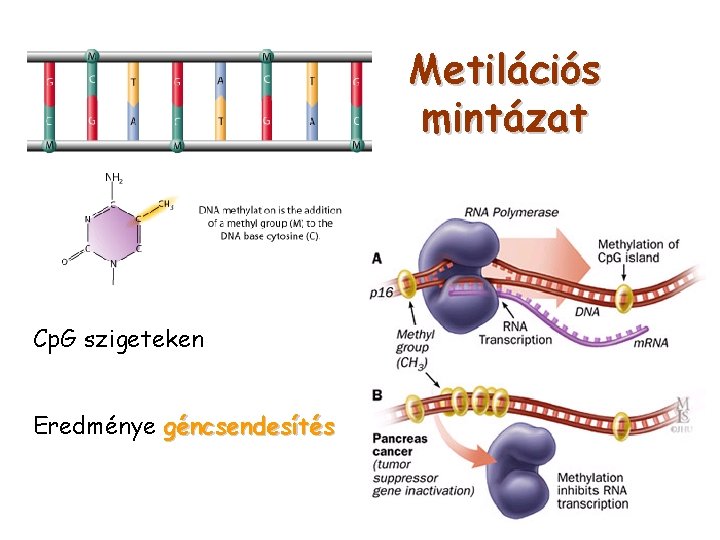
Metilációs mintázat Cp. G szigeteken Eredménye géncsendesítés
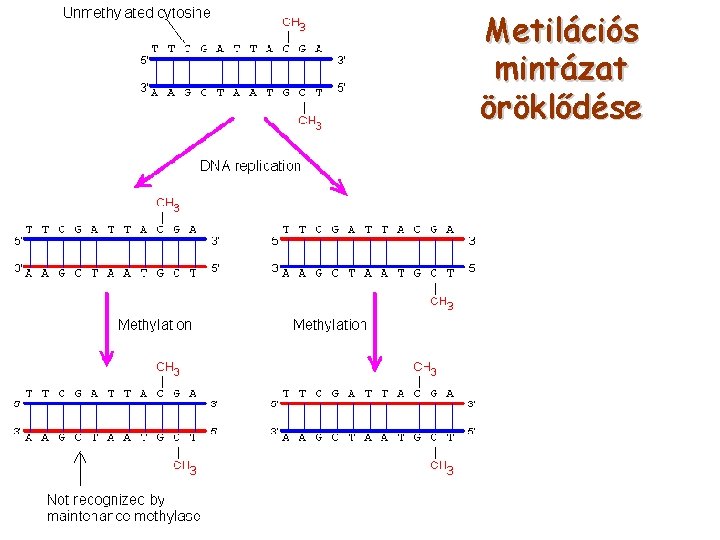
Metilációs mintázat öröklődése
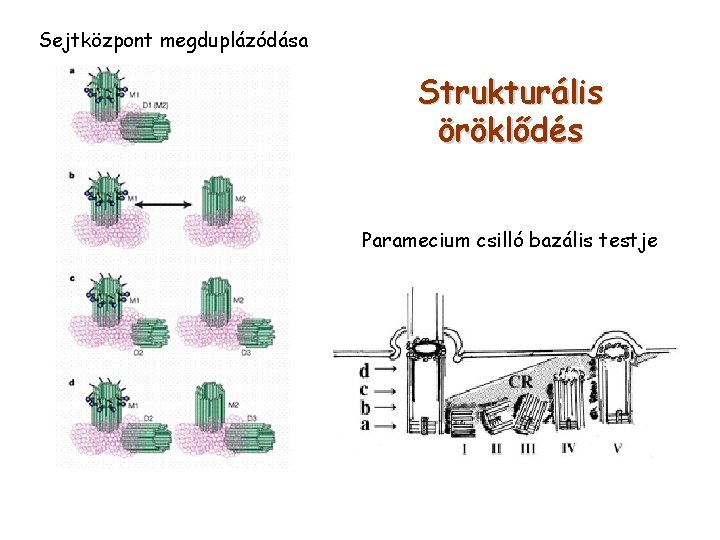
Sejtközpont megduplázódása Strukturális öröklődés Paramecium csilló bazális testje

„Szenz” az antiszenz szálban? Szenz – m. RNS-sel megegyező szekvencia- erről íródik a fehérje Antiszenz - m. RNS erről íródik Receptor ‘ 5 ‘ 3 ‘ 5 Ligand
- Slides: 53