SEGUNDAS NEOPLASIAS LARGOS SUPERVIVIENTES 28 de octubre de

SEGUNDAS NEOPLASIAS LARGOS SUPERVIVIENTES 28 de octubre de 2010 Dr. Javier Espinosa Arranz Jefe de Oncología Médica Hospital General Universitario de

SEGUNDAS NEOPLASIAS n n n Aproximadamente el 66% de los pacientes con cáncer sobreviven 5 ó más años (3. 3%4% de la población) Más del 75% (92% en algunas series) de los pacientes pediátricos se consideran “curados”. Aproximadamente 22 millones de largos supervivientes en el mundo SEER Cancer statistics review, NCI 2006 Solimna H. Cancer Control 2008; 15: 55 -62. Cardous-Ubbink MC et al. Eur J Cancer 2007; 43: 351 -362.

SEGUNDAS NEOPLASIAS 1 de cada 6 pacientes padecerán más de una neoplasia. n Son el 13% de las neoplasias. n Los supervivientes pediátricos tienen de 3 a 11 veces más probabilidad de tener una segunda neoplasia. n Los pacientes adultos, doble probabilidad. n

SEGUNDAS NEOPLASIAS n Definición: n Aparición de un nuevo cáncer que es biológicamente independiente del primero. n American Cancer Society, Atlanta, GA, 2004.

SEGUNDAS NEOPLASIAS n ADEMÁS… n El 62% de los supervivientes ha tenido al menos un problema de salud crónico, el 28% una condición severa y el 24% 3 ó más problemas crónicos de salud.

SEGUNDAS NEOPLASIAS n En esta charla hablaremos de… Las causas de las SN n SN en niños, adolescentes y adultos n Prevención primaria y Dx precoz de las SN (actuaciones concretas) n Acciones futuras sobre las infraestructuras y los pacientes n Investigación futura. n

SEGUNDAS NEOPLASIAS n Posibles causas : n n n n Secuelas tardías de los tratamientos. Estilos de vida que favorecen el desarrollo de neoplasias. Exposición ambiental. Factores del huésped. Interacciones genes-ambiente y genes-genes. Predisposición genética. Combinaciones. El azar. Travis L. The epidemiology of second primary cancer. Cancer Epidemiol Biomarkers Prev 2006; 15: 2020 -2026.

SEGUNDAS NEOPLASIAS n Factores etiológicos de las SN: n Predisposición genética: n n n 10% de los pacientes con cáncer tienen predisposición genética. La exposición a carcinogénicos produce la pérdida del segundo alelo (segundo evento). Ejemplos: mutaciones del BRCA 1 y BRCA 2. Otras: VHL, NFM 1 y 2, S. de Cowden, PAF, S. Lynch I y II, Muir-Torre, Peutz-Jegher, Xeroderma P, Ataxiatelangiectasia, S. de Bloom, S. de Li-Fraumeni, MEN I y II. Atención a: múltiples familiares, tumores bilaterales, edad temprana. Referir a la consulta de consejo genético.

SEGUNDAS NEOPLASIAS n Exposición a carcinógenos ambientales: Son más frecuentes las neoplasias metacrónicas (separadas en el tiempo). n Ejemplos: n n exposición a Rx UV (segundo melanoma), n exposición al tabaco (segundos tumores en pulmón, cabeza y cuello o en la vejiga o el cervix). n El abandono del tabaco con el primer tumor reduce el riesgo de una segunda neoplasia. Do KA. Cancer Causes Control 2003; 14: 131 -138.

SEGUNDAS NEOPLASIAS n SEGUNDAS NEOPLASIAS INDUCIDAS POR QUIMIOTERAPIA: POR ALQUILANTES. n POR PLATINOS. n POR INHIBIDORES DE TOPOISOMERASA II. n

SEGUNDAS NEOPLASIAS n n Tumores sólidos asociados al tratamiento: Quimioterapia: n Se ha demostrado la carcinogénesis en modelos animales. Alquilantes sobre todo. n Mecloretamina y procarbazina. Relación dosis respuesta. n Ciclofosfamida cáncer de vejiga (>50 Gy, 15 veces más riesgo). Travis LB. JNCI 2002; 94: 182 -192. Hawlins MM. JNCI 1996; 88: 270 -278. Travis LB. JNCI 1995; 87: 524 -530.

SEGUNDAS NEOPLASIAS n LAM INDUCIDAS POR ALQUILANTES: Su riesgo se inicia a 1 -2 años y alcanza su pico a los 5 -10 años. n Muchas veces precede un S. mielodisplásico. n Traslocaciones o deleciones de los cromosomas 5 y/o 7. n El riesgo aumenta con la dosis acumulada y la duración. n Refractarias. Mal pronóstico. n

SEGUNDAS NEOPLASIAS n LAM INDUCIDAS POR PLATINOS: Los platinos inducen enlaces covalentes con el DNA (funcionan como los alquilantes). n A mayor dosis acumulada y tiempo (7 veces más riesgo si > 12 m), o si se asocia RT, mayor riesgo. n
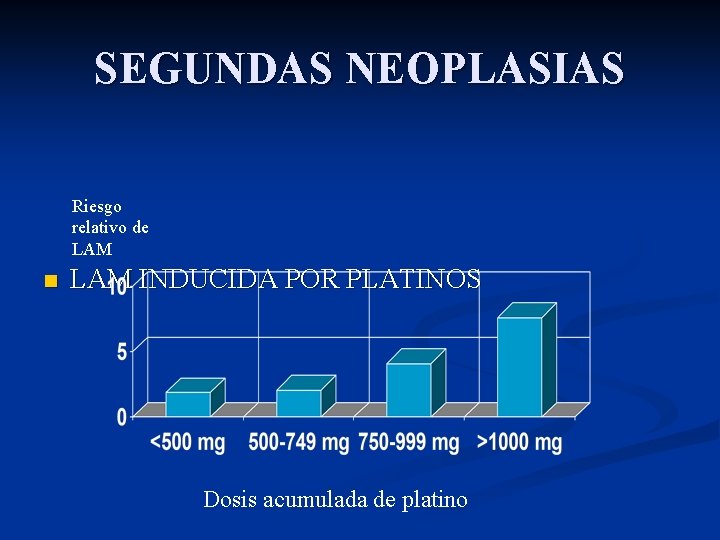
SEGUNDAS NEOPLASIAS Riesgo relativo de LAM n LAM INDUCIDA POR PLATINOS Dosis acumulada de platino

SEGUNDAS NEOPLASIAS n LAM INDUCIDA POR INHIBIDORES DE TOPOISOMERASA II: Etopósido, tenipósido, antraciclinas. n Latencia mediana de 2 -3 años. n Traslocaciones balanceadas: t(9; 11), t(11; 19), t(6; 11). n Monoblásticas o mielomonocíticas. n Puede haber LAL: t(4; 11)(q 21; q 23). n n Suele responder al tratamiento.
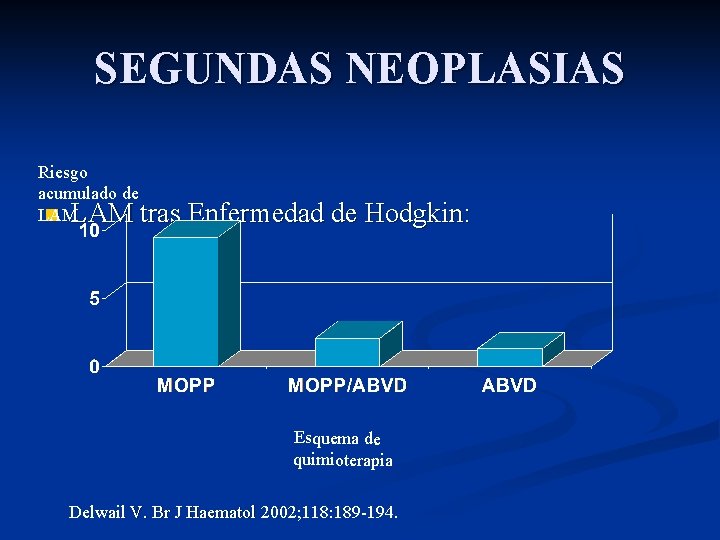
SEGUNDAS NEOPLASIAS Riesgo acumulado de LAM n LAM tras Enfermedad de Hodgkin: Esquema de quimioterapia Delwail V. Br J Haematol 2002; 118: 189 -194.

SEGUNDAS NEOPLASIAS Tumores sólidos asociados al tratamiento: n Quimioterapia: n Cuestiones sin resolver: n ¿Órganos más susceptibles? n ¿Papel de la edad de exposición? n ¿Relación entre la primera y la segunda neoplasia? n ¿Susceptibilidad individual? . n

SEGUNDAS NEOPLASIAS n SEGUNDAS NEOPLASIAS ASOCIADAS A RADIOTERAPIA: n Leucemias n Tumores sólidos

SEGUNDAS NEOPLASIAS n LAM tras Radioterapia: El riesgo aumenta unas 2 veces. n Máximo a los 5 -9 años tras la exposición. n En función de la cantidad de médula ósea radiada. n También la irradiación corporal total a dosis bajas aumenta el riesgo. n Relacionada con LAM, LMC y la LAL. n Travis LB. J Clin Oncol 1996; 14: 565 -571. Travis LB. Cancer Epidemiol Biomarkers Prev 2006; 15: 2020 -2026.

SEGUNDAS NEOPLASIAS n n Tumores sólidos asociados al tratamiento: Radioterapia: n n Frecuentes: n Cáncer de mama (RR= 1. 1 -3. 4) n Cáncer de tiroides (RR= 1. 3 -3. 5) Ocasionales: n T. del SNC (5. 1) Cáncer de ovario (2. 3) n Cáncer n n de pulmón (2. 0) Cáncer de vejiga (1. 8) Cáncer de esófago (1. 8) Cáncer de estómago (1. 5) Cáncer de colon (1. 7) Hepatocarcinoma(1. 5)

SEGUNDAS NEOPLASIAS Tumores sólidos asociados al tratamiento: n Radioterapia: n Período de latencia 10 ó más años. n Máximo riesgo de cáncer de mama en mujeres tratadas de Enfermedad de Hodgkin antes de los 30 años. n El riesgo persiste incluso durante más de 25 años después de la exposición. n

SEGUNDAS NEOPLASIAS Tumores sólidos asociados al tratamiento: n Radioterapia: n Si se asocian alquilantes, el riesgo se incrementa 1. 4 veces. n El riesgo disminuye si: n n se irradiaron los ovarios (50% de reducción) si la menopausia llegó antes de los 40 años. ¿Se espera que disminuya el riesgo al reducir las dosis y los campos? Travis LB. JAMA 2003; 290: 465 -475.
SEGUNDAS NEOPLASIAS n Tumores sólidos asociados al tratamiento: Riesgo de ca. de mama n Radioterapia: Dosis de radiación por E. de Hodgkin
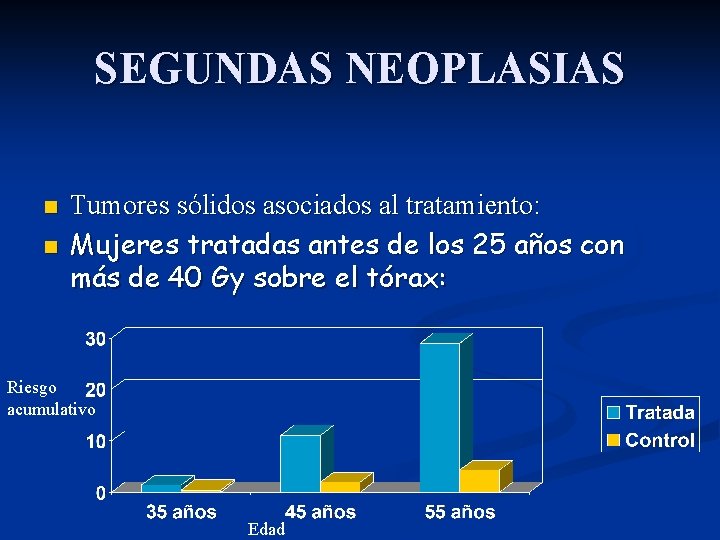
SEGUNDAS NEOPLASIAS n n Tumores sólidos asociados al tratamiento: Mujeres tratadas antes de los 25 años con más de 40 Gy sobre el tórax: Riesgo acumulativo Edad

SEGUNDAS NEOPLASIAS Tumores sólidos asociados al tratamiento: n Radioterapia n n n Supervivencia mediana de la segunda neoplasia: 4. 3 años (T. gastrointestinales: 1. 9 años, ca. pulmón: 1 año). Vivos a 5 años global: 42%. (T. gastrointestinales: 12. 4%, ca. de mama: 76%). Ng AK, et al. Blood 2002; 100: 1989 -1996.
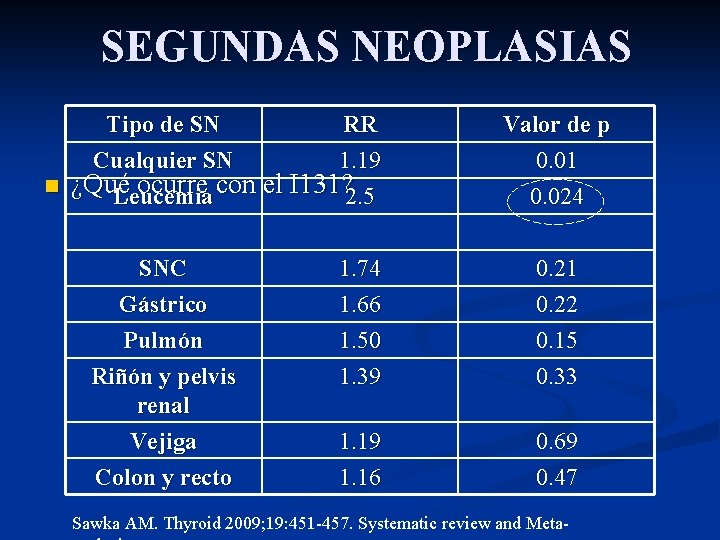
SEGUNDAS NEOPLASIAS Tipo de SN RR Cualquier SN 1. 19 n ¿Qué ocurre con el I 131? Leucemia 2. 5 Valor de p 0. 01 0. 024 SNC Gástrico Pulmón 1. 74 1. 66 1. 50 0. 21 0. 22 0. 15 Riñón y pelvis renal Vejiga Colon y recto 1. 39 0. 33 1. 19 1. 16 0. 69 0. 47 Sawka AM. Thyroid 2009; 19: 451 -457. Systematic review and Meta-

SEGUNDAS NEOPLASIAS Tumores sólidos asociados al tratamiento: n Radioterapia: n Cuestiones sin resolver: n n ¿Qué ocurre con las personas tratadas con las nuevas técnica radioterápicas: radioterapia conformacional en 3 D, IMRT, anticuerpos monoclonales radio-marcados, radiocirugía estereotáctica?

SEGUNDAS NEOPLASIAS n ¿Qué ocurre con la RT-3 D y la IMRT? Reducen el volumen irradiado y por tanto de las zonas sanas que reciben altas dosis de radiación. n Con esta técnica se esperaría reducir los sarcomas y quizá los carcinomas radioinducidos. n Hall EJ, Wuu CS. Int J Radiat Oncol Biol Phys 2003; 56: 83 -88. Kry SF et al. Int J Radiat Oncol Biol Phys 2005; 62: 1195 -1203.

SEGUNDAS NEOPLASIAS n n En la transición RT-3 D a IMRT sin embargo se afectan más campos, se exponen a dosis menores, más zonas sanas y aumenta la irradiación corporal total La IMRT podría aumentar la incidencia de segundas neoplasias de 1% a 1. 75%, casi el doble, en pacientes que sobreviven 10 o más años. Otros autores sitúan esta cifra en 5. 1%. Hall EJ, Wuu CS. Int J Radiat Oncol Biol Phys 2003; 56: 83 -88. Kry SF et al. Int J Radiat Oncol Biol Phys 2005; 62: 1195 -1203.

SEGUNDAS NEOPLASIAS Tumores sólidos asociados al tratamiento: n Quimioterapia y radioterapia: n Otras cuestiones sin resolver: n ¿Interacción QT- RT? n ¿Papel de otros factores de riesgo: tabaco, alcohol? n ¿Interacción con los estilos de vida (tabaco por ejemplo) y la susceptibilidad genética? . n

SEGUNDAS NEOPLASIAS NIÑOS SUPERVIVIENTES

SEGUNDAS NEOPLASIAS Neoplasia primaria Segunda neoplasia Enfermedad de Hodgkin n Segundas neoplasias en Cáncer de mama supervivientes: Ca. Tiroides sarcomas T. Gastrointestinales Ca. Piel, neoplasias hematológicas niños Leucemias SNC, Ca. Tiroides Ca. mama Ca. Piel Neoplasias hematológicas Sarcomas Ca. Hueso, mama y tiroides SNC, tiroides, sarcoma

SEGUNDAS NEOPLASIAS n Segundas neoplasias en niños supervivientes: La incidencia acumulada a 30 años es del 9. 3%. n Supervivientes de LLA: 5. 2% a 25 años. n LAM: 1. 7% a 20 años. n LNH: 4% a 30 años (12% si incluimos meningioma y S. mielodisplásicos). n

SEGUNDAS NEOPLASIAS El 33% de los niños que tienen una SN tuvieron una E. de Hodgkin. n De los pacientes que tienen un ca. de mama como SN, el 60% tuvieron una E. de Hodgkin. n La SN más frecuente en este grupo es el cáncer de mama. También tuvieron más riesgo de un segundo sarcoma. n CA. MAMA

SEGUNDAS NEOPLASIAS n Factores de riesgo en niños: n Radioterapia: n Ca. Tiroides (10% de las SN): OR = 9. 8 para dosis de hasta 29 Gy. A partir de esta dosis el riesgo disminuye (“cell-killing effect”). n n n T. Más efecto en niños menores de 10 años. La QT no se asoció a un aumento de ca. de tiroides. del SNC (8% de las SN) (OR = 6. 8 para glioma y OR = 9. 9 para meningioma). n Máximo riesgo menores de 5 años. n Tumores óseos (27% de las SN).

SEGUNDAS NEOPLASIAS n Predisposición genética: n. Puede haber predisposición a segundas neoplasias: polimorfismos en el gen de la glutatión-S-transferasa M 1. Doi K. Ped Perinatal Epiemiol 2009; 23: 370 -379.

SEGUNDAS NEOPLASIAS n Impacto de tener una segunda neoplasia en la infancia: n Los supervivientes tienen 3. 3 veces más riesgo de tener una entidad crónica y 8. 2 veces más riesgo de tener una enfermedad que amenaza la vida. Meadows AT. J Clin Oncol 2009; 27: 2356 -2362. Findings from the Childhood Cancer Survivor Study Cohort.

SEGUNDAS NEOPLASIAS n Impacto de tener una SN en la infancia: n El 13% de los niños que sobreviven 5 años mueren: n Principal causa: la recidiva en el 67% de los casos. n La segunda neoplasia: 18. 6% de los casos. n A los 20 años, la SN es la primera causa de muerte, siendo la RT el principal factor predisponente. Meadows AT. J Clin Oncol 2009; 27: 2356 -2362. Findings from the Childhood Cancer Survivor Study Cohort.

SEGUNDAS NEOPLASIAS Los cambios en los protocolos de QT y RT pueden hacer descender el riesgo en los próximos años. n El seguimiento de estas cohortes es por tanto obligatorio. n Meadows AT. J Clin Oncol 2007; 27: 2356 -2362.

SEGUNDAS NEOPLASIAS ADOLESCENTES Y ADULTOS JÓVENES

SEGUNDAS NEOPLASIAS n Adolescentes y adultos jóvenes (15 -29 años) Pronóstico no tan favorable n El cáncer es 2. 5 veces más frecuente que antes de los 15 años. n En el 80% de los casos la segunda neoplasia ocurre en otro órgano. n El riesgo es doble si se asociaron QT y RT. n Soliman H. Cancer Control 2008; 15: 55 -62.

SEGUNDAS NEOPLASIAS n Posibles causas: n n La mayoría de las veces espontáneos, es decir, no relacionados con el ambiente. En ocasiones: n n n luz UV: melanoma virus del papiloma humano: ca. de cervix virus del SIDA: S. de Kaposi V. Epstein-Barr: Linfomas. Herencia (5%). secuelas de los tratamientos en infancia. Bleyer A. The Oncologist 2006; 11: 590 -601.
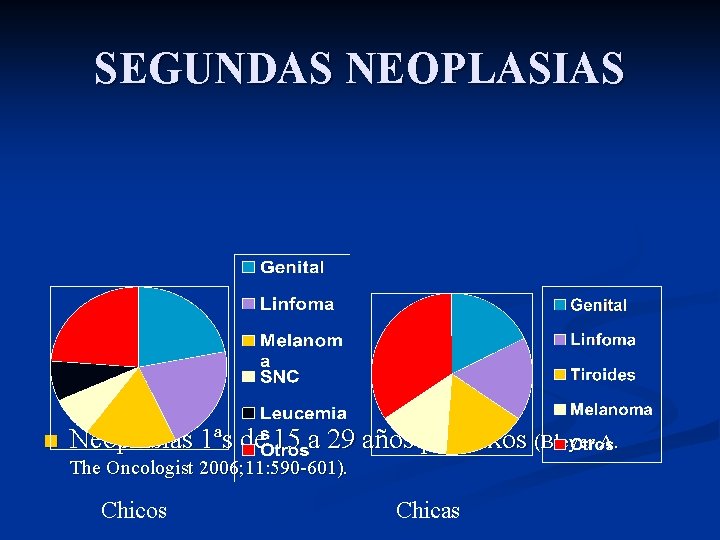
SEGUNDAS NEOPLASIAS n Neoplasias 1ªs de 15 a 29 años por sexos (Bleyer A. The Oncologist 2006; 11: 590 -601). Chicos Chicas

SEGUNDAS NEOPLASIAS n SEGUNDOS TUMORES EN ADOLESCENTES Y ADULTOS JÓVENES: Leucemias (tratados con antraciclinas e inhibidores de topoisomerasa II) n Linfomas no Hodgkin y Enfermedad de Hodgkin. n Sarcomas. n Cáncer de tiroides. n Otros: cáncer de mama y pulmón. n Leone G. Haematologica 1999; 84: 937 -945

SEGUNDAS NEOPLASIAS n Las SN son sólo uno más de sus problemas…: n Segundas neoplasias n Cardiotoxicidad. n Neuropatía y ototoxicidad. n Infertilidad. n Amputaciones.

SEGUNDAS NEOPLASIAS n Otros problemas: Insuficiencia renal n Parestesias n Linfedema. n Problemas psicosociales derivados del diagnóstico y/o el tratamiento. n n Efectos psiquiátricos y psicológicos. n Reinserción educacional y social. n Reinserción laboral.

SEGUNDAS NEOPLASIAS EDAD ADULTA

SEGUNDAS NEOPLASIAS n SEGUNDAS NEOPLASIAS EN LA EDAD ADULTA: Los largos supervivientes adultos tienen doble riesgo de desarrollar segundos tumores. n Causas: factores genéticos, ambientales, inmunosupresión, secuelas tardías de los tratamientos… n Fossa SD. J Cancer Surv 2008; 2: 3 -11

SEGUNDAS NEOPLASIAS n Segundas neoplasias en la edad adulta: n Leucemias (RT previa o QT –alquilantes-) n Cáncer de mama n Cáncer de tiroides n Cáncer de pulmón (neoplasias hematológicas) n Otros Samanta DR. J Cancer Res Ther 2009; 5: 302 -304 Wilkins KL. Oncology Nursing Forum 2008; 35: E 12 -22 Amadori D. Semin Respir Crit Care Med 2005; 26: 520 -526

SEGUNDAS NEOPLASIAS n ¿Qué ocurre con los pacientes con ca. de próstata tratados con RT? Posible aumento del cáncer de vejiga (R. A. de 1. 3 a 5 -8 años, 1. 5 después de 8 años). Ca. Pobremente diferenciados y localmente avanzados. RT externa. n Posible aumento del riesgo de cáncer de recto (OR = 1. 60) con la RT externa o combinada con braquiterapia. n Bostrom PJ, Soloway MS. Eur Urol 2007; 52: 973 -982.

SEGUNDAS NEOPLASIAS RT y cáncer de próstata: n Relación con otros tumores fuera del campo de la RT: sarcomas, cáncer de pulmón, ciego, colon transverso, cerebro, estómago y melanoma. n La IMRT aumenta el riesgo de segunda neoplasia 3 veces. Bostrom PJ, Soloway MS. Eur Urol 2007; 52: 973 -982.

SEGUNDAS NEOPLASIAS n Segundas neoplasias por agentes hormonales: Tamoxifeno: utilizado en mujeres premenopáusicas con cáncer de mama hormonosensible. n Incremento de ca. de endometrio. n Se puede asociar a otros factores de riesgo. n

SEGUNDAS NEOPLASIAS n Problemas de los largos supervivientes en la edad adulta (I): Mayor morbilidad (5 -10 veces) debido al cáncer, los tratamientos y factores de riesgo subyacentes n Menor sensación de bienestar (mama, aparato reproductor femenino, colon, otros) n Más días de baja laboral n Mayor riesgo de problemas mentales (mama) n Reducción de la agilidad mental : “ chemo brain”. n Osteoporosis. n Eakin EG. Cancer Epidemiol Biomark Prev 2006; 15: 1969 -1976 Diller L. J Clin Oncol 2007; 27: 2339 -2353.

SEGUNDAS NEOPLASIAS n Problemas de los largos supervivientes en la edad adulta (II): Precisan atención incrementada del Sistema de Salud. n Quizá se deberían tratar como “entidades crónicas” y crearse ayudas para su incorporación a la vida social y laboral normal. n Cada uno de los problemas debe ser atendido por un profesional para su prevención, detección y abordaje precoz. n Demark-Wahnefried W. J Clin Oncol 2005; 23: 5814 -5830.

SEGUNDAS NEOPLASIAS DIAGNÓSTICO PRECOZ Y PREVENCIÓN DE LAS SEGUNDAS NEOPLASIAS

SEGUNDAS NEOPLASIAS n Identificación de subgrupos de riesgo de padecer una segunda neoplasia por: n Susceptibilidad genética. n Factores de riesgo asociados y estilos de vida. n Secuelas tardías de los tratamientos.

SEGUNDAS NEOPLASIAS n OBJETIVOS: n Modificar los protocolos de seguimiento de estos pacientes y su manejo con el fin de detectarlos y tratarlos más precozmente. n Campañas de prevención: primaria y secundaria.

SEGUNDAS NEOPLASIAS Prevención terciaria: n Incluye el seguimiento y la detección precoz de segundas neoplasias y otras n complicaciones relacionadas con el tratamiento en los supervivientes. Mahon SM. Semin Oncol Nursing 2005; 21: 260 -270.

SEGUNDAS NEOPLASIAS n Prevención primaria en largos supervivientes: n Abandono del hábito tabáquico. n Moderación en la exposición a Rad. UV. n Consideraciones dietéticas.

SEGUNDAS NEOPLASIAS n Prevención secundaria: seguimiento tras la primera neoplasia: n Tema no resuelto. n El 60% de los supervivientes no tienen un seguimiento regular según la literatura. n De los pacientes en seguimiento, menos de la mitad lo hacen con el oncólogo. Wilkins K. Oncol Nursing Forum 2008; 35: 12 -20

SEGUNDAS NEOPLASIAS n n Prevención secundaria: Más aceptada por mujeres, casadas, con alto nivel educativo, de ingresos y laboral Las consultas bajan después de los 30 años: el 40% visitarán a un especialista y sólo un 10% al oncólogo. A los 40 años, sólo el 12% se revisa. Aparicio-Ting F. J Cancer Education 2003; 18: 230 -236. Shaw AK. Cancer 2006; 106: 1829 -1837.

SEGUNDAS NEOPLASIAS n La enfermedad padecida también influye: n n Se revisan más: Los supervivientes de leucemias y linfomas Se revisan menos: los que sobreviven a tumores del SNC, retinoblastoma o tumores germinales. Citología: 18% de supervivientes de ca. de colon, 77% de las que sobreviven a un cáncer de cervix y 60 -86% de las que sobreviven a un cáncer de mama. Mamografía: 54% de las que tuvieron cáncer de colon, 80% cáncer de cervix y 70%-92% de las que se curaron de un cáncer de mama. Wilkins KL. Oncol Nursing Forum 2008; 35: 12 -22.

SEGUNDAS NEOPLASIAS Método por el que se detectó su neoplasia: si el cáncer de mama se detectó por mamografía, se harán mamografías con más facilidad. n Tiempo transcurrido: a mayor tiempo desde el diagnóstico, más visitas al médico de cabecera y menos al oncólogo. n Actitud del médico: más vigilancia si le visita un oncólogo y más test de screening, y si se le anima a hacerlo. n

SEGUNDAS NEOPLASIAS n Otros factores que influyen en el seguimiento: Miedo: a que le encuentren algo, a que no descubran lo que pueda haber, a conocer riesgos futuros. n Motivación: si el paciente piensa que ello redunda en prevenir un segundo tumor. n Si perciben que tienen mayor riesgo de segundo tumor, se adhieren mejor a las revisiones. n El conocimiento también mejora la participación Wilkins KL. Oncol Nursing Forum 2008; 35: 12 -22. n

SEGUNDAS NEOPLASIAS n Se ha visto que las personas que participan en las campañas de screening de segundos tumores adquieren comportamientos y hábitos de salud Eiser C. Psico-Oncol 2000; 9: 214 -220.

SEGUNDAS NEOPLASIAS n Problemas para las campañas: Faltan estudios de intervención que muestren su utilidad. n Falta determinar los componentes que mejor predicen cambios en el comportamiento futuro. n Faltan estudios aleatorizados para evaluar las intervenciones para prevenir segundos tumores y el coste. n Falta interés en la promoción de la salud. n Tercyak KP. J Pediat Psychol 2006; 31: 252 -261.

SEGUNDAS NEOPLASIAS n Consideraciones psicológicas: n El miedo y la ansiedad son trastornos comunes. n No se conoce con exactitud cuántos largos supervivientes son conscientes del riesgo y el miedo que esto genera. n Debemos informarles del riesgo de manera que no parezca una amenaza. n El pronóstico es excelente si se descubren precozmente. n Llevar a cabo las recomendaciones supone la detección más precoz, mejor supervivencia y mejor calidad de vida. n Considerar remitir al psico-oncólogo.

SEGUNDAS NEOPLASIAS n Segundas neoplasias asociadas al cáncer de mama: n Cáncer de mama n n n Cáncer de endometrio. n n Riesgo de 1. 2 a 2. 4. A veces causa genética (BRCA 1/2 24% a 54% a los 70 años o HNPCC -15%-20%). Cáncer colorrectal. n n 1. 72 más riesgo. Posible causa hormonal o del tratamiento (Tamoxifeno). HNPCC (30% riesgo) Cáncer de ovario. n n 15% riesgo de ca. en la mama contralateral. 65% riesgo acumulado si BRCA 1/2 2 -3 veces más riesgo. Factores dietéticos y genéticos. Otros cánceres.

SEGUNDAS NEOPLASIAS n Screening para cáncer de mama: n n Niñas curadas de E. de Hodgkin y que recibieron RT mediastínica: autoexploración mensual comenzando en la pubertad, exploración clínica anual empezando en la pubertad hasta los 25 años, y después exploración clínica cada 6 meses con mamografía anual y RNM empezando 8 años tras la RT o a los 25 años, lo que ocurra más tarde. La autoexploración sola no está recomendada Rosolowich V. J Obstet Gynecol 2006; 28: 728 -730.

SEGUNDAS NEOPLASIAS n Actuaciones para mujeres que han tenido ca. de mama: n Informarlas del riesgo de posible segunda neoplasia. n Mamografía anual, exploración física cada 6 meses, autoexamen regular, atención a cambios. Análisis: ojo a citopenias. n BRCA 1/2: plantear consulta de CG ¿cirugía profiláctica? n Exploración ginecológica anual. Educación sanitaria. n No claro el beneficio del CA 125, la ecografía pélvica o la exploración pélvica (explicárselo). n Atenta a cambios en el hábito intestinal, o al sangrado rectal. Colonoscopia a partir de los 50 años.

SEGUNDAS NEOPLASIAS n Segundas neoplasias asociadas al cáncer de ovario: n Cáncer de ovario. n n Cáncer de mama. n n Riesgo de un 20% de tener un 2º cáncer de ovario. El riesgo relativo es 4. 0. Comparten factores de riesgo comunes: nuliparidad, menarquia precoz, menopausia tardía. Mutaciones BRCA ½ (riesgo del 90% de padecer un cáncer de mama) Cáncer colorrectal. n Susceptibilidad genética (HNPCC),

SEGUNDAS NEOPLASIAS n Actuaciones: Educación sanitaria de la paciente. n Mamografía anual hacia los 40 años. n Exploración física por un médico cada 6 meses. n Autoexploración, limitada. n BRCA 1/2: RNM mamaria o mastectomía profiláctica. n Colonoscopias: recomendable. n HNPCC: colonoscopia anual. Considerar colectomía profiláctica. n

SEGUNDAS NEOPLASIAS n Segundas neoplasias asociadas al cáncer de endometrio: n Cáncer de mama. n Riesgo relativo: 1. 3 -4. 0. n Factores de riesgo compartidos. n Factores genéticos comunes, incluido el HNPCC. n Cáncer colorrectal. n Riesgo relativo: 1. 19 -5. 92. n Factores genéticos comunes. n Ojo mujeres con historia familiar de cáncer de colon y endometrio.

SEGUNDAS NEOPLASIAS n Actuaciones: Mamografía anual. n Exploración física anual. n Considerar colonoscopia, sobre todo por encima de los 50 años y n Ritmo de colonoscopias dependiendo del resultado de la primera colonoscopia. n

SEGUNDAS NEOPLASIAS n Segundas neoplasias asociadas al cáncer colorrectal: n Cáncer colorrectal. n n Cáncer de mama. n n n Riesgo relativo: 3. 0 (riesgo bi-direccional). Factores hormonales. Hª familiar de cáncer de colon y ovario: testar HNPCC. Cáncer de endometrio. n n Riesgo relativo: 1. 26. Factores hormonales. Cáncer de ovario. n n Riesgo 3. 3. Predisposición genética, pólipos, factores ambientales. Riesgo: 1. 6 -2. 0. Factores hormonales. Otros cánceres. n Riñón, vejiga (RR = 1. 5 -2. 0) y próstata (RR = 1. 3)

SEGUNDAS NEOPLASIAS n Actuaciones para pacientes que han tenido ca. de colon-recto: Colonoscopia: anual si existe una mutación conocida o considerar colectomía profiláctica. n Mamografía y exploración física mamaria anual. n Educación sanitaria: mama, sangrados genitales. n Exploración ginecológica regular. n Si mutación HNPCC: cirugía profiláctica. n Educación: sangrados urinarios. PSA y tacto rectal anuales a partir de los 40 años. n

SEGUNDAS NEOPLASIAS n Segundas neoplasias asociadas al cáncer de piel: n Melanoma maligno. n 5% desarrollan un segundo melanoma. n Predisposición genética. 75% de probabilidad si existe el S. de melanoma asociado a nevus displásico. n Seguimiento dermatológico. n Cánceres de piel no melanoma. n 20%-40% desarrollan un segundo ca. de piel. n Exposición ambiental o supresión inmune.

SEGUNDAS NEOPLASIAS n Actuaciones: Uso de cremas protectoras. n Prendas de vestir, sombrero. n Reducir la exposición UV. n Si Hª familiar, referir a la consulta de C. G. n Instruir en signos y síntomas. n Examen regular por el dermatólogo. n Seguimiento fotográfico para pacientes con múltiples nevi. n

SEGUNDAS NEOPLASIAS n Segundas neoplasias asociadas al linfoma: riesgo de segunda neoplasia: 2. 6 -2. 9. n Leucemias agudas. n n n Cáncer de tiroides. n n En relación con el campo de la RT. Cáncer de pulmón. n n Tras Tto de E. de Hodgkin: riesgo 20% a 40%. El riesgo se reduce 15 años después. Riesgo: 2. 7. Relacionado con la RT. Cáncer de mama. n Riesgo relativo: 4. 7. Máximo riesgo si recibieron RT torácica de niñas o adolescentes.

SEGUNDAS NEOPLASIAS n Actuaciones: Monitorizar valores sanguíneos, ojo citopenias. n Palpación regular de la glándula tiroides. n Vigilar parámetros de función tiroidea. n Abandono del hábito tabáquico. n Autoexploración mamaria, exploración médica cada 6 meses empezando 5 años tras la exposición a la RT. n Mamografías: comenzar a los 25 años. Contemplar ecografía o RNM (mamas densas). n

SEGUNDAS NEOPLASIAS Screening para segundas neoplasias: n Cáncer de cervix: n n La citología es una práctica muy extendida tanto en la población general como en las pacientes supervivientes, algo más en estas últimas.

SEGUNDAS NEOPLASIAS Screening para segundas neoplasias: n Cáncer de próstata: n En la población general, del 57% al 85% tienen un test de PSA. n ¿Deberían tener un seguimiento especial si fueron tratados con RT? No consenso, quizá en pacientes con otros factores de riesgo: Hª de cáncer de vejiga, tabaquismo, exposición ocupacional… n Mayer DK. J Cancer Survivorship 2007; 1: 17 -26.

SEGUNDAS NEOPLASIAS Screening para segundas neoplasias: n Cáncer de testículo: n La autoexploración no está recomendada, pero permite conocer los posibles cambios. n En algunas series de niños supervivientes alcanzan el 27% de autoexploraciones una vez al mes n Hudson MM. Med Pediat Oncol 2002; 39: 2 -11.

SEGUNDAS NEOPLASIAS n Pacientes que recibieron RT en abdomen, pelvis o columna (30 Gy o más): riesgo de cáncer colorrectal, colonoscopia cada 5 años comenzando a los 35 años o 10 años tras la RT, lo que ocurra más tarde. Wendy L. , Smita B. The Oncologist 2008; 13: 1181– 1192

SEGUNDAS NEOPLASIAS n Futuro: infraestructura Definir tiempos y métodos más efectivos para intervenir en el comportamiento de salud. n Estudios coste-efectivos en vigilancia y prevención de segundas neoplasias. n Campañas en familiares y amigos para animar a los supervivientes a adherirse a los estudios y futuras campañas. n Implicación de la Enfermería en las campañas de screening y prevención. n

SEGUNDAS NEOPLASIAS n Futuro (Travis LB, JNCI 2006; 98: 15 -25): infraestructura Desarrollar una infraestructura nacional de vigilancia en largos supervivientes. n Crear un sistema coordinado para conservar especímenes. n Creación de nueva tecnología, bioinformática y biomarcadores. n Diseño de nuevos métodos epidemiológicos. n Desarrollo de guías de práctica clínica basadas en la evidencia. n

SEGUNDAS NEOPLASIAS n Futuro (Fossa SD, Vassilopoulo-Sellin R. J Cancer Surviv 2008; 2: 3 -11): Pacientes Hacer comprender a los pacientes tratados con nuevas terapias que se desconocen las secuelas a largo plazo. n Si el paciente pasa al médico de familia, se debería trazar, por parte del oncólogo, un plan individualizado para cada paciente. n

SEGUNDAS NEOPLASIAS n Futuro: pacientes n n n Esforzarnos porque los pacientes curados de cáncer participen activamente en su seguimiento. Enseñarles estilos de vida saludables. Enseñarles la importancia del screening y la detección precoz. Transmitir dicha información a la familia. Identificar y monitorizar individuos de alto riesgo de manera consistente y rigurosa. Realizar protocolos de recomendaciones con materiales educativos, escritos, visuales, diagramas, videos, material informático, etc.

SEGUNDAS NEOPLASIAS n Investigación futura en largos supervivientes: n n n Comunicación médico-paciente sobre consecuencia a largo plazo. Se deberían planear ensayos aleatorizados sobre cuándo, cómo, por quién, a quién, qué efecto. Identificación de toxicidades a largo plazo y su relación con estilos de vida. Conservar material biológico (sangre, biopsias, orina). Elaborar guías para prevención, detección precoz y Tto de efectos adversos físicos y psicosociales a largo plazo. Estudios aleatorizados que investiguen la factibilidad y eficacia de tales medidas. Investigación diferente para largos supervivientes curados y no curados. Fossa SD. J Cancer Surviv 2008; 2: 3 -11
- Slides: 89