Schema tipo di purificazione Lisi cellulare non necessaria















- Slides: 21

Schema tipo di purificazione • Lisi cellulare (non necessaria in caso di esoenzimi) • Passaggi di chiarificazione • Passaggi di arricchimento e purificazione preliminare a bassa efficienza • Passaggi di purificazione ad alta efficienza

Cromatografia • Tecnica elettiva per la separazione enzimatica – Buona purezza del campione – Selettività – efficienza • Tecnica di separazione di una miscela di composti che sfrutta la differente distribuzione dei composti stessi tra due fasi immiscibili – Fase stazionaria – Fase mobile

• Il processo cromatografico può essere definito come il risultato di una serie di equilibramenti, durante il movimento dei componenti della miscela attraverso il letto della fase stazionaria • La separazione conseguente è proporzionale alla differenza dei coefficienti di ripartizione o di distribuzione (rapporto tra la concentrazione del componente nella fase stazionaria/concentrazione dello stesso componente nella fase mobile) dei vari componenti del campione tra le due fasi mobile e stazionaria

Coefficienti di ripartizione differenti significa di fatto tempi di permanenza all’interno della fase stazionaria differenti • Tempo di ritensione assoluto: il tempo che intercorre tra l’applicazione del campione alla fase stazionaria e il suo rilevamento in uscita della stessa fase stazionaria (assoluto) • Tempo di ritensione relativo: quando il tempo in uscita è riferito non al tempo di applicazione ma al tempo di uscita di un altro componente (componente di riferimento, solvente)

• Sistemi di rivelazione: strumento analitico in grado di rivelare, registrare (sotto forma di picchi di eluizione) ed eventualmente quantificare il rilascio delle molecole dalla fase stazionaria • Efficienza: numero di equilibramenti di ripartizione (numero di piatti teorici) del soluto tra le due fasi (maggiore il numero di equilibramenti maggiore l’efficienza) • Risoluzione: distanza tra due picchi di eluizione, matematicamente ottenuto come rapporto tra la differenza dei due tempi di ritenzione e la media dell’ampiezza dei picchi


Cromatografia su colonna


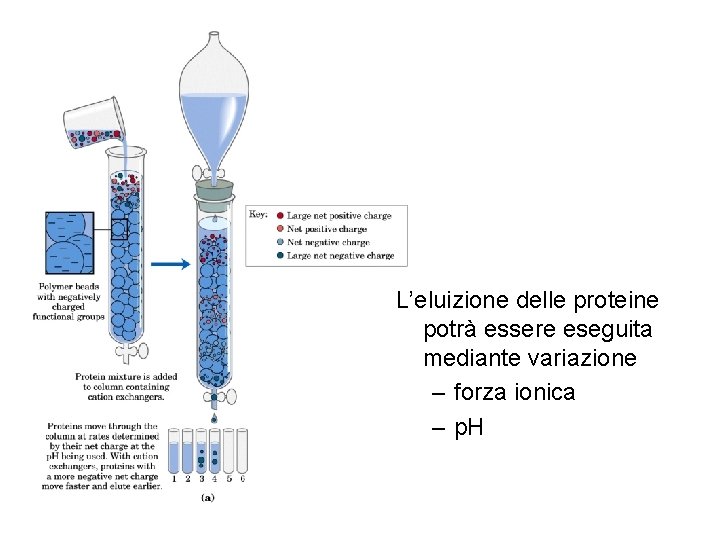
Cromatografia a scambio ionico • Si basa sull’adsorbimento reversibile di molecole cariche su gruppi ionici con carica opposta alla propria. Poiché il legame è reversibile, le molecole potranno essere facilmente recuperate con un eluente che scambierà i gruppi adsorbiti. Molecole che hanno cariche differenti reagiranno con i gruppi della fase stazionaria in maniera differente e verranno quindi eluiti a tempi diversi

L’eluizione delle proteine potrà essere eseguita mediante variazione – forza ionica – p. H

Vantaggi della cromatografia a scambio ionico • Processo relativamente semplice, vi sono parecchi tipi di scambiatori con matrici di varia natura • Gli scambiatori ionici hanno buone capacità ed è possibile caricare grandi quantità di proteine • Si possono utilizzare velocità di flusso elevate • Può essere applicata nei primi passaggi di purificazione • Il passaggio di scala non comporta problemi

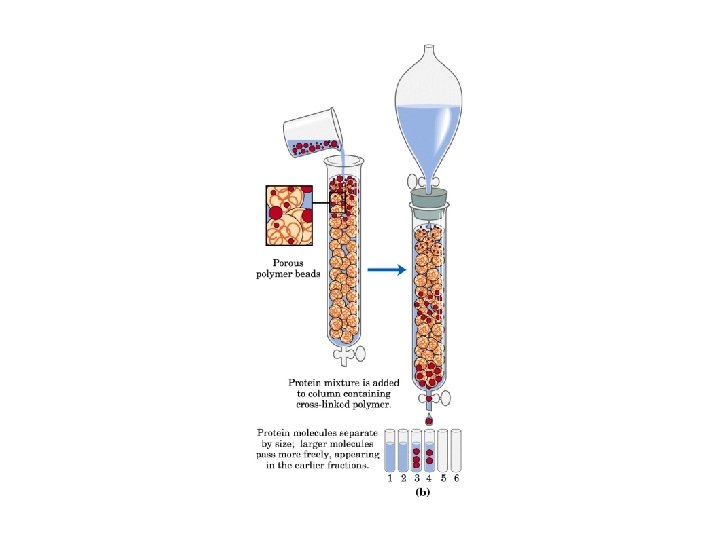
Gel filtrazione o cromatografia di esclusione molecolare • La tecnica separa le molecole di soluto della fase mobile in base alle loro dimensioni, attraversando il letto di resina della fase stazionaria che funge da setaccio molecolare


Vantaggi e svantaggi della gel filtrazione • Tecnica applicabile nei passaggi finali di purificazione, con soluzioni limpide e volumi ridotti • Eluizione molto semplice, senza gradienti o cambi di eluenti ma a velocità di flusso piuttosto basse

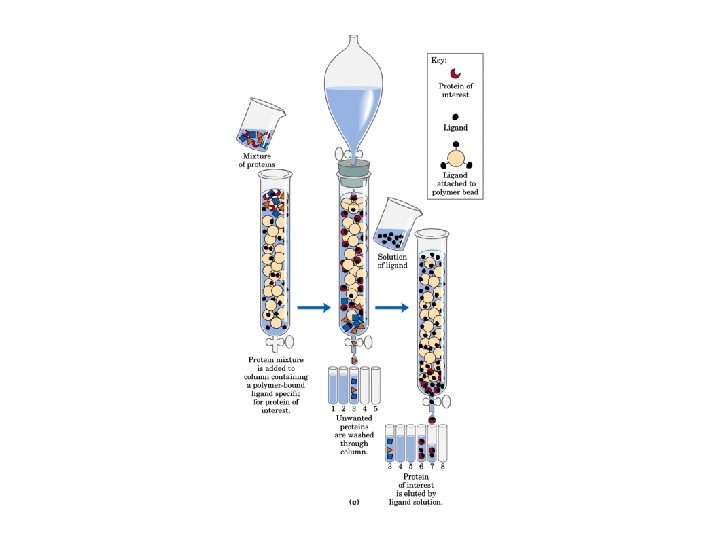
Cromatografia di affinità E’ la tecnica più specifica e selettiva in quanto il principio di base non è relativo a caratteristiche fisico-chimiche generiche, ma ad interazioni altamente specifiche e reversibili delle biomolecole: – – – Anticorpo – antigene Enzima – substrato Enzima – inibitore Ormone – recettore Acido nucleico – frammento di acido nucleico complementare


Vantaggi e svantaggi della cromatografia di affinità • Interazioni altamente selettive e specifiche utilizzabili anche nei primi passaggi di purificazione con alti indici di purificazione • Nel caso degli enzimi, se il ligando si lega al sito attivo, la tecnica consente di selezionare le molecole proteiche cataliticamente attive • Matrici costose, speso preparate appositamente per la separazione

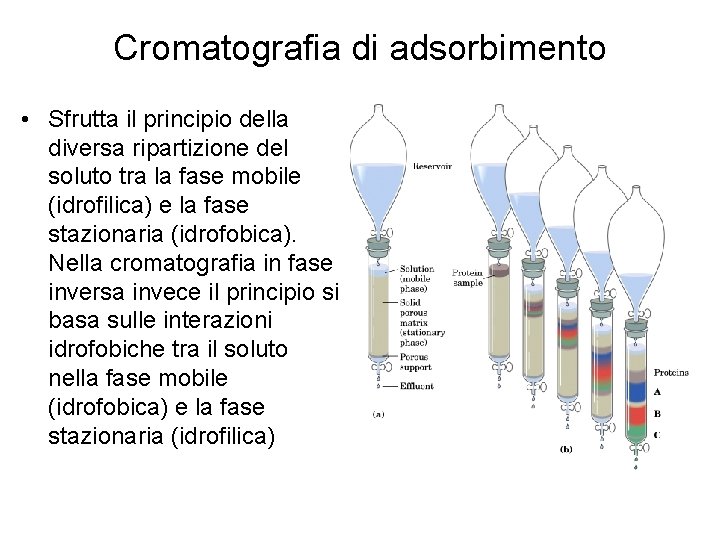
Cromatografia di adsorbimento • Sfrutta il principio della diversa ripartizione del soluto tra la fase mobile (idrofilica) e la fase stazionaria (idrofobica). Nella cromatografia in fase inversa invece il principio si basa sulle interazioni idrofobiche tra il soluto nella fase mobile (idrofobica) e la fase stazionaria (idrofilica)

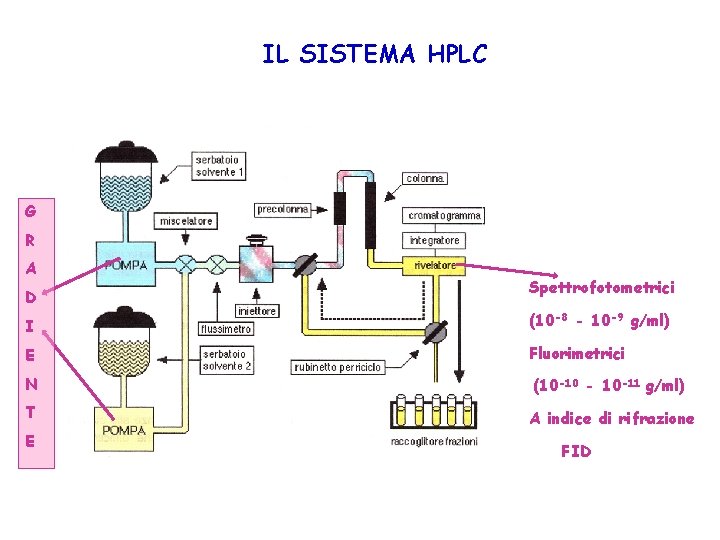
IL SISTEMA HPLC G R A D Spettrofotometrici I (10 -8 - 10 -9 g/ml) E Fluorimetrici N (10 -10 - 10 -11 g/ml) T A indice di rifrazione E FID

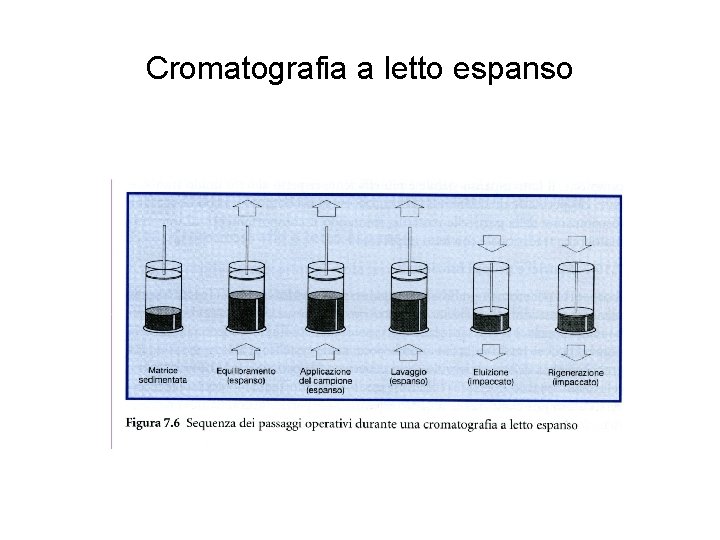
Cromatografia a letto espanso

Vantaggi e svantaggi • Il letto espanso può sopportare campioni molto grezzi, non chiarificati, con pochi passaggi operativi • I costi su scala industriale possono essere rilevanti