Scheikunde Hoofdstuk 2 Moleculaire Stoffen 2 2 Elektrisch



























- Slides: 32

Scheikunde Hoofdstuk 2 Moleculaire Stoffen

2. 2 Elektrisch geleidingsvermogen en naamgeving • Stoffen kunnen worden ingedeeld in groepen door te kijken naar het elektrisch geleidend vermogen.

Wat is elektrische stroom? • Letterlijk: transport van geladen deeltjes Er zijn twee mogelijkheden: 1) Elektronen die door een draad bewegen (natuurkunde) 2) Ionen (alleen in vloeibare fase of in oplossingen)

Moleculaire stoffen • • Bestaan alleen uit niet-metaal atomen Bevatten atoombindingen Geleiden geen stroom Voorbeelden: Aardgas CH 4 Zuurstof O 2 Glucose C 6 H 12 O 6

Moleculaire stoffen geleiden geen stroom • Zuiver water is een moleculaire stof en kan geen stroom geleiden. Als je keukenzout in water doet geleid water wel stroom zie onderstaande afbeelding • Dat komt omdat keukenzout GEEN moleculaire stof is • Keukenzout heeft als formule Na. Cl: Na is een metaal dus is keukenzout niet moleculair! » Hieronder een oplossing van keukenzout in water

Voorbeelden • Kaarsvet bestaat uit stearinezuur en heeft de volgende formule: C 17 H 35 COOH Kan gesmolten kaarsvet stroom geleiden? • • Oplossing Kijk naar de formule van kaarsvet: Kijk met behulp van Binas tabel 99 of de atomen in kaarsvet niet-metalen zijn Ja C = niet metaal H= niet metaal O = niet metaal Kaarsvet is moleculair kan dus geen stroom geleiden

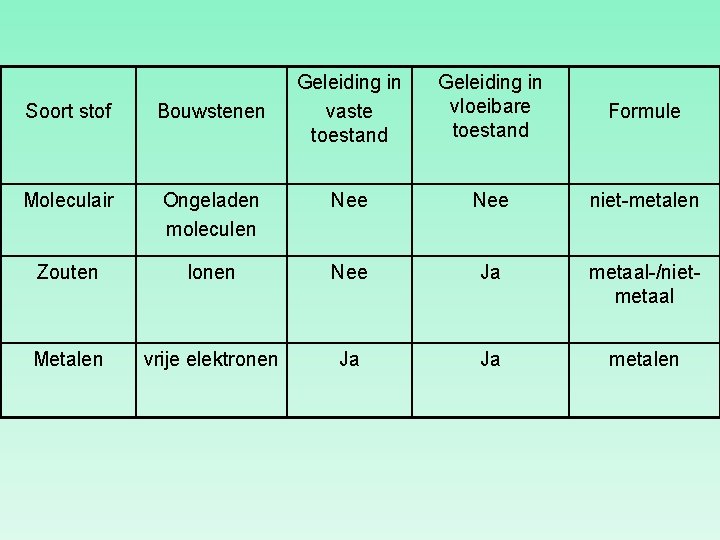
Geleiding in vaste toestand Geleiding in vloeibare toestand Formule Soort stof Bouwstenen Moleculair Ongeladen moleculen Nee niet-metalen Zouten Ionen Nee Ja metaal-/nietmetaal Metalen vrije elektronen Ja Ja metalen

Element • Als de atomen allemaal hetzelfde zijn Bijvoorbeeld: N 2 stikstof

Verbinding • Als de atomen verschillend zijn Bijvoorbeeld: NO 2 Stikstofdioxide http: //vimeo. com/4433312

Molecuulformule • Aan een molecuulformule kun je zien hoeveel en welke atomen aan elkaar zijn gebonden. Bijvoorbeeld : coëfficent Water: notatie : 3 H 2 O index 3 moleculen water die elk bestaan uit 2 waterstof en 1 zuurstofatoom

Systematische naamgeving • De index in de molecuulformule geven we aan met een voorvoegsel (BINAS 66 C) INDEX voorvoegsel 1 mono 2 di 3 tri 4 tetra 5 penta 6 hexa

Tweede symbool achtervoegsel ide Tweede symbool O S N Naam oxide sulfide nitride P Se fosfide selenide Voorbeeld 1: CS 2 monokoolstofdisulfide

Voorbeeld 2 • Systematische naam H 2 O 2 • Index H-atoom: 2 di • Index O-atoom: 2 di • De naam wordt dan diwaterstofdioxide

Voorbeeld 3 • Systematische naam P 2 O 5 • Index P-atoom: 2 di • Index O-atoom: 5 penta • De naam wordt dan difosforpentaoxide telwoord- atoomsoort- telwoord-atoomsoort-ide

Voorbeeld 4 • As 2 O 3 • • • As = niet-metaal O = niet-metaal Index As = 2 di Index O = 3 tri Naam: diarseentrioxide

Triviale namen Naam formule Glucose C 6 H 12 O 6 Methaan CH 4 Water H 2 O Waterstofperoxide H 2 O 2

2. 3 Atoombindingen

Structuurformule • Kun je zien hoe de atomen in een molecuul zijn gebonden • Atoombindingen worden aangegeven met streepjes. • Een atoombinding wordt ook wel covalente binding genoemd.

Covalentie • Getal dat aangeeft hoeveel atoombindingen een atoomsoort kan vormen. Elementen Covalentie H , F, I, Cl , Br 1 O N C 2 3 4

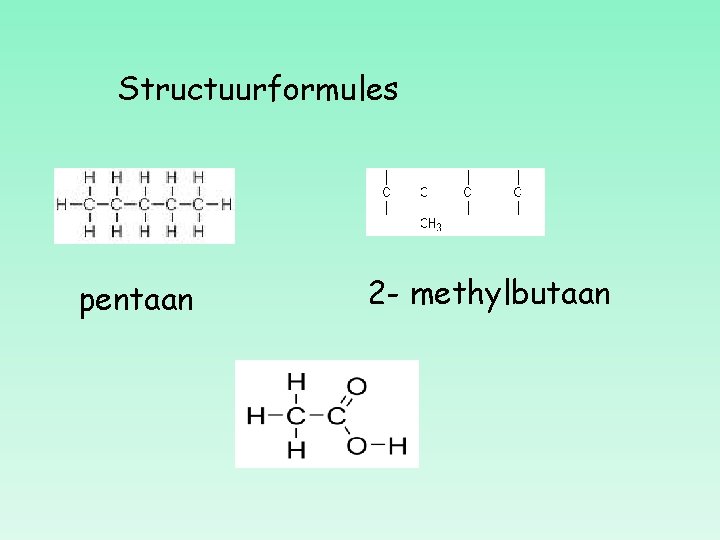
Structuurformules pentaan 2 - methylbutaan

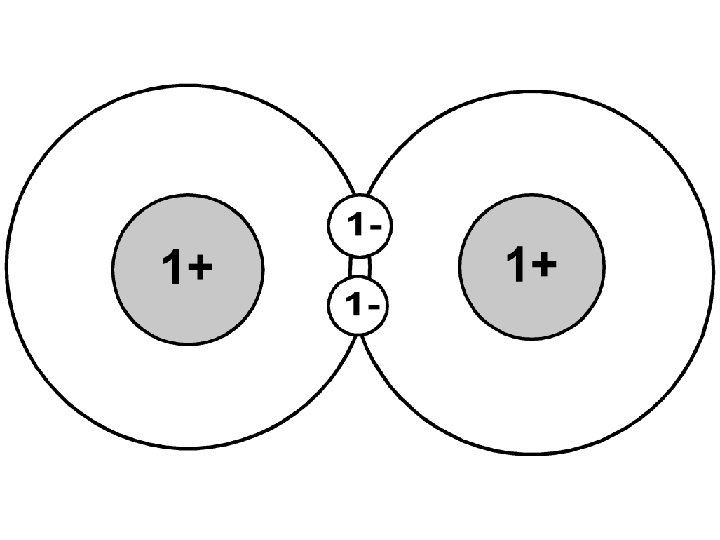
Atoom(covalente)binding • Worden gevormd door overlap van e-wolken. • Elk atoom levert per atoombinding 1 e-. De 2 e- samen noemt men het bindings- of gemeenschappelijk e- - paar. Als moleculen kapot gaan worden er atoombindingen verbroken.


Waterstof heeft maar 1 edus kan ook nooit meer dan 1 binding vormen. Alleen de e- in de buitenste schil spelen een rol, deze enoemt de valentie-e-.

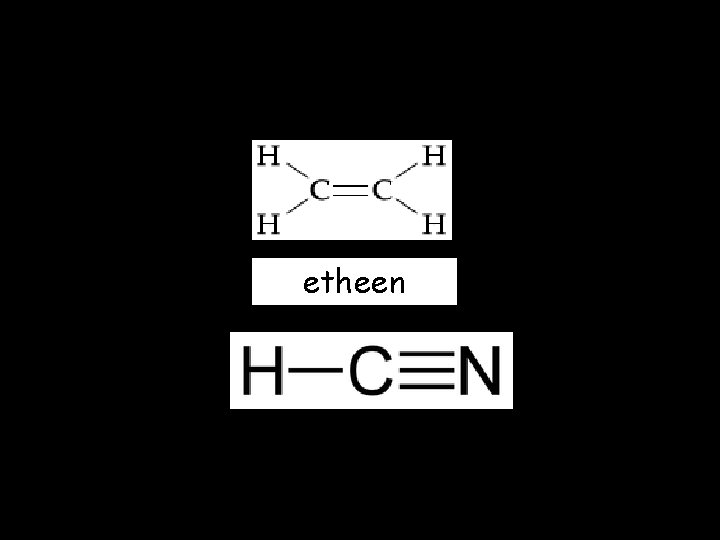
Meervoudige bindingen • Een koolstofatoom heeft covalentie 4. Er moeten dus altijd vier bindingen om heen getekend worden , dit heeft soms tot gevolg dat er een meervoudige binding ontstaat. Ethyn (C 2 H 2) HCN

etheen

2. 4 Vanderwaalsbindingen

Vander. Waalsbindingen • Aantrekkende krachten tussen moleculen: cohesie. • Er geldt in het algemeen: Hoe groter de molecuulmassa, hoe sterker de Vander. Waalsbindingen, hoe hoger het smelt, - kookpunt.

Vast H 2 O(s)= ijs • De moleculen zitten vast in een rooster (gestapeld), trillen beetje • Tussen de moleculen heb je Vander. Waalsbindingen • Kleine intermoleculaire ruimten

Vloeibaar H 2 O (l)= water • Moleculen bewegen door elkaar, sommige laten elkaar los • Vander. Waalsbinding kleiner

GAS H 2 O(g) = waterdamp • Moleculen bewegen los en ver van elkaar • De moleculen trekken elkaar niet aan • De intermoleculaire ruimte is zeer groot • Er zijn geen Vander. Waalsbindingen meer aanwezig

Fase-overgangen • Bij een fase-overgang spelen alleen de Fvdw een rol Bijvoorbeeld: verdampen Als een stof verdampt worden de Fvdw verbroken. De atoombindingen blijven heel.

2. 4 Waterstofbruggen Powerpoint grt