Samenvatting Hfdst 8 en 9 Zuren en basen

Samenvatting Hfdst. 8 en 9 Zuren en basen

Kennis: Een zuur is een deeltje dat een H+ kan afstaan. . . + Een zure oplossing bevat H. . . . ionen 3 O Een base is een deeltje dat een H+ kan opnemen. . . . OH⁻ ionen Een basische oplossing bevat. . . .

Als je aan neutraal water HCl toevoegt, ontstaat een zure oplossing. Een zure oplossing bevat H 3 O+ ionen. HCl moet dus een. . H+ aan H 2 O hebben gegeven
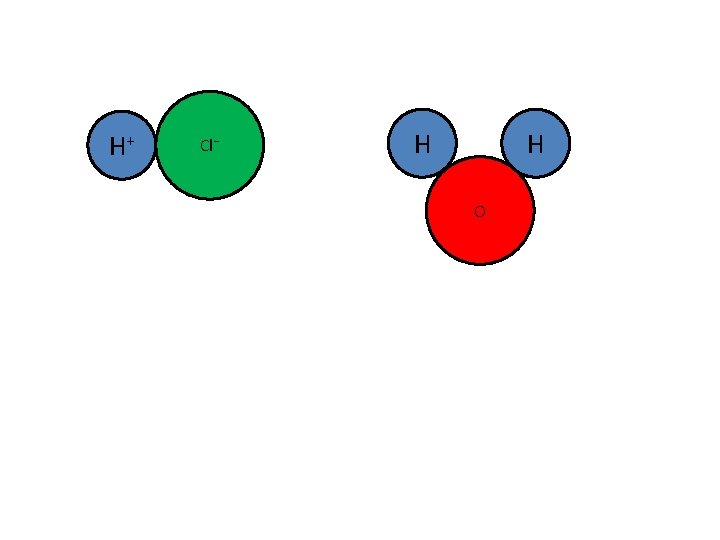
H+ Cl⁻ H H O
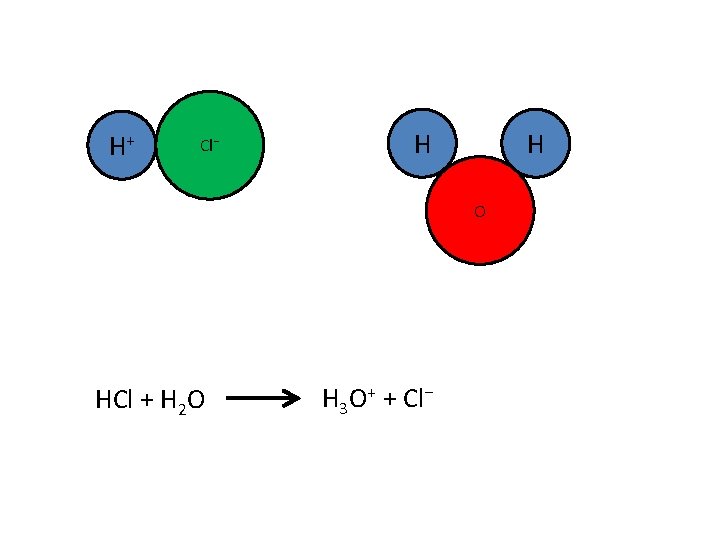
H+ Cl⁻ H H O HCl + H 2 O H 3 O+ + Cl⁻

Als je H 2 SO 4 in water oplost, krijg je ook een zure oplossing
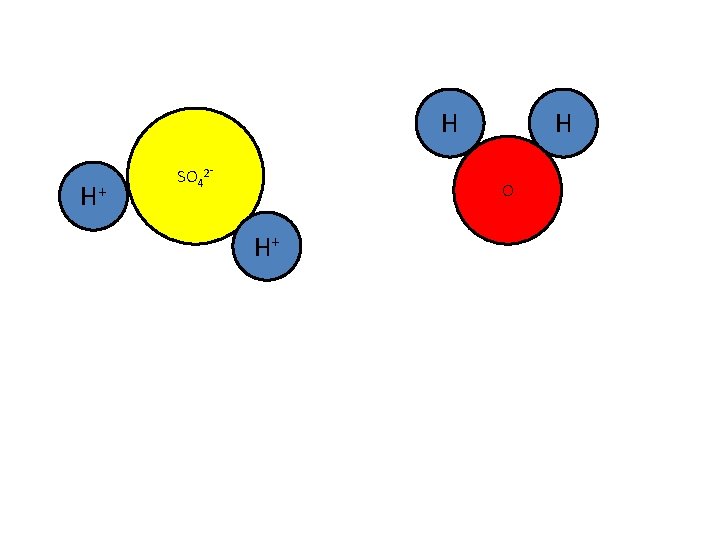
H H+ SO 42⁻ H O H+
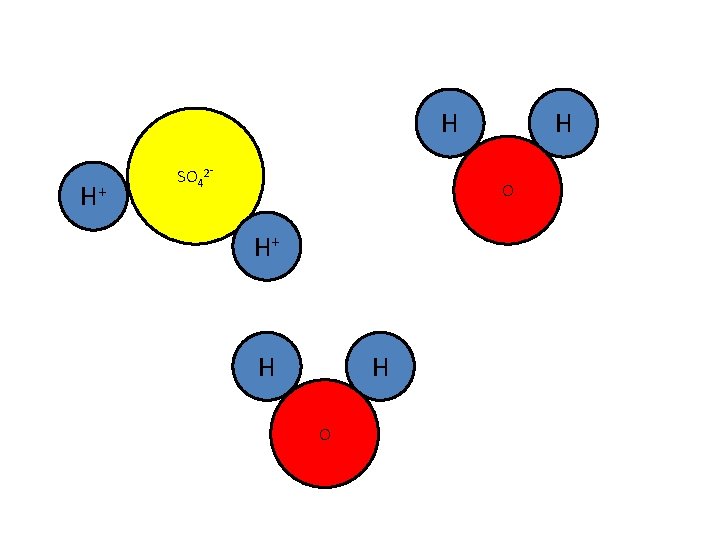
H H+ SO 42⁻ H O H+ H H O
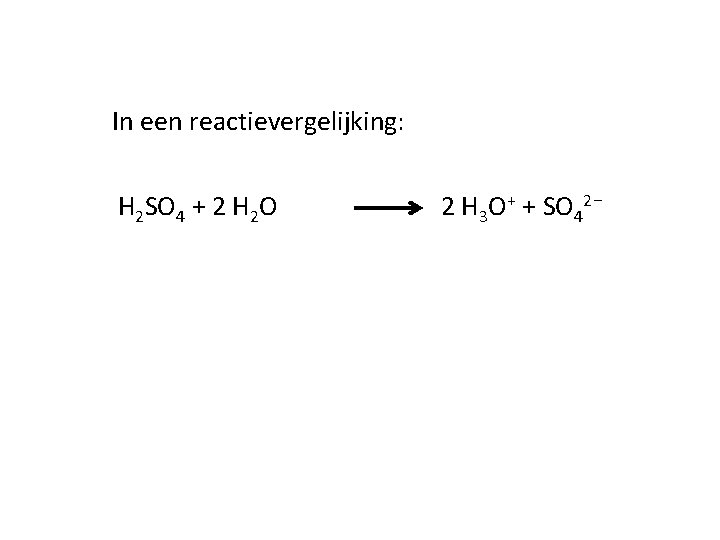
In een reactievergelijking: H 2 SO 4 + 2 H 2 O 2 H 3 O+ + SO 42⁻
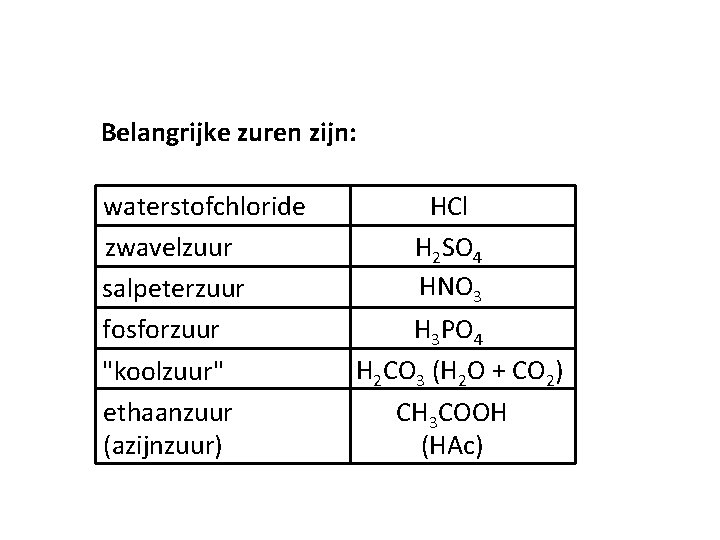
Belangrijke zuren zijn: waterstofchloride zwavelzuur salpeterzuur fosforzuur "koolzuur" ethaanzuur (azijnzuur) HCl H 2 SO 4 HNO 3 H 3 PO 4 H 2 CO 3 (H 2 O + CO 2) CH 3 COOH (HAc)

Sterke zuren zijn zuren die in water geheel. . . . . in ionen splitsen De sterke zuren zijn: HCl HNO 3 H 2 SO 4 Deze staan in tabel 49 . . . boven H 3 O+ Een oplossing van een sterk zuur (een verdund sterk zuur) schrijf je in. . . IONEN

Pas op: oplossing van HCl in water Zoutzuur is een. . . . Zoutzuur is dus altijd: . . . H 3 O+ + Clˉ

Een zwak zuur geeft met water een. . . . reactie: evenwichts. . . CH 3 COOH + H 2 O H 3 O+ + CH 3 COO‾. . . Deze evenwichten liggen sterk . . LINKS

Zwakke zuren zijn zuren die in water voor een klein deel. . . . in ionen splitsen De zwakke zuren staan in tabel 49. . . ONDER H 3 O+ Een oplossing van een zwak zuur (een verdund zwak zuur) schrijf je in MOLECULEN. . . . .
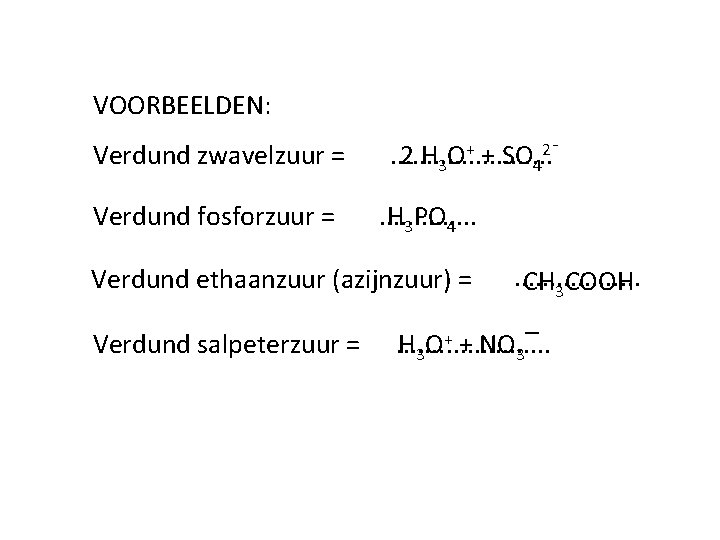
VOORBEELDEN: Verdund zwavelzuur = Verdund fosforzuur = . . . 2 H 3 O+ + SO 42⁻. . . H 3 PO 4 Verdund ethaanzuur (azijnzuur) = Verdund salpeterzuur = . . . . CH 3 COOH . . H 3 O+ + NO 3‾

Belangrijke base zijn: Hydroxide-ion: OH⁻ Oxide-ion: O 2⁻ Carbonaation: CO 32⁻ Waterstofcarbonaation: HCO 3⁻ Ammoniakmolecuul: NH 3

Een zwakke base geeft met water een. . . . evenwichts reactie: CH 3 COO⁻ + H 2 O CO 32⁻ + H 2 O CH. . . 3 COOH + OH‾. . . . . HCO 3‾ + OH‾ Deze evenwichten liggen sterk. . . LINKS De zwakke basen staan in tabel 49: BOVEN. . . de base OH‾

Calciumoxide in water: r Binas, tabel 45: . . . Calciumoxide reageert dus met water Maar hoe ? ? ?

Ca. O bestaat uit: . . . . Ca 2+ en O 2⁻ ionen In water splitst het in ionen: Ca. O(s). . . . Ca 2+(aq) + O 2⁻(aq) De O 2⁻ ionen reageren met water:
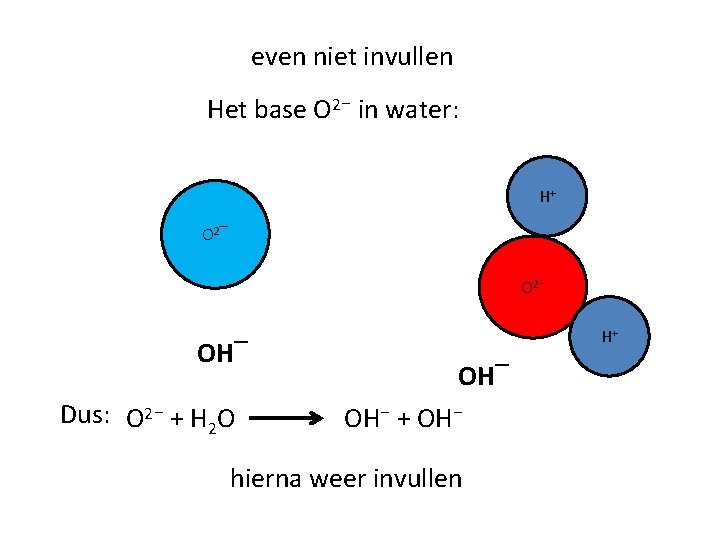
even niet invullen Het base O 2⁻ in water: H+ O 2‾ O 2⁻ OH‾ Dus: O 2⁻ + H 2 O H+ OH‾ OH⁻ + OH⁻ hierna weer invullen
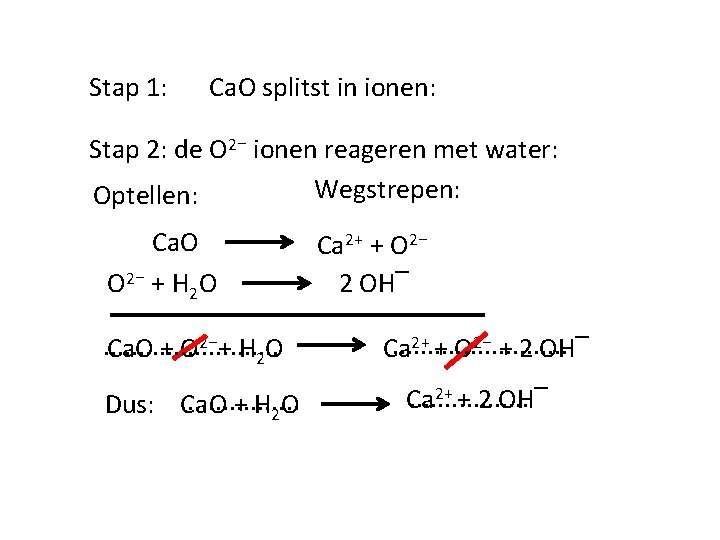
Stap 1: Ca. O splitst in ionen: Stap 2: de O 2⁻ ionen reageren met water: Wegstrepen: Optellen: Ca. O O 2 ⁻ + H 2 O. . . Ca. O + O 2⁻+ H 2 O Ca. O + H 2 O Dus: . . . . Ca 2+ + O 2⁻ 2 OH‾ 2+ + O 2⁻ + 2 OH‾. . . Ca 2+ + 2 OH‾. . . . Ca

Zuur-base reacties Verloopt elke zuur-basereactie ?

Wanneer reageert een zuur met een base ? ? ? . . staat Als het zuur in tabel 49 hoger dan het base waar hij mee kan reageren
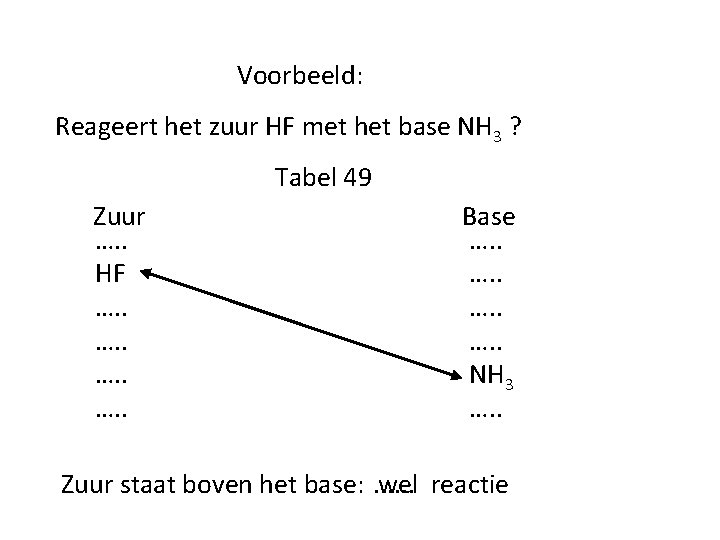
Voorbeeld: Reageert het zuur HF met het base NH 3 ? Tabel 49 Zuur …. . HF …. . Base …. . NH 3 …. . Zuur staat boven het base: . . . wel reactie
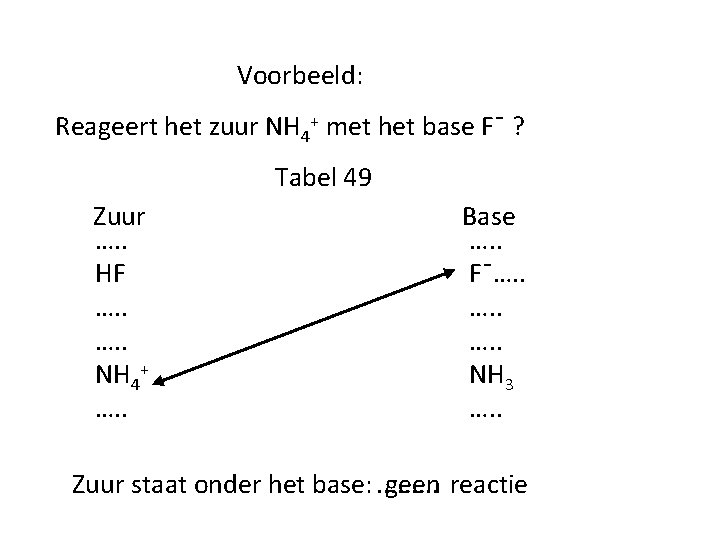
Voorbeeld: Reageert het zuur NH 4+ met het base Fˉ ? Tabel 49 Zuur …. . HF …. . NH 4+ …. . Base …. . Fˉ…. . NH 3 …. . Zuur staat onder het base: . . geen reactie

Handig als je weet dat: + het sterkste zuur is dat H. . . . O 3 in water kan voorkomen . . . . OHˉ het sterkste base is dat in water kan voorkomen. . . . Clˉ , NO 3ˉ en SO 42ˉ in water geen H+ opnemen

Hoe stel je een zuur-basereactie op? 1. Geef de juiste notatie van het zuur en van de base 2. Ga met behulp van tabel 49 na of het zuur met de base kan reageren Als er een reactie optreedt: 3. 4. Ga na of er nóg een H+ overgedragen kan worden Stel de vergelijking op

Voorbeelden: Azijnzuur opl. + natriumsulfide-opl. 1. (CH 3 COOH) HAc. . . . 2. HAc staat boven S 2ˉ HAc + S 2ˉ. . . . 3. . . . S 2ˉ dus: HSˉ + Acˉ. . . . dus: HAc staat boven HSˉ. . . H 2 S + Acˉ HAc + HSˉ. . . 4. Totaal: 2. . . . HAc + S 2ˉ H. . . . 2 S + 2 Acˉ

Voorbeelden: HCN opl. + natriumcarbonaat-opl. 1. HCN. . . . 2. HCN staat boven CO 32ˉ 2ˉ CO. . . . 3 . . . . HCN + CO 32ˉ 3. HCO. . . . 3ˉ + CNˉ HCN staat onder HCO 3ˉ HCN reageert niet met HCO 3ˉ 4. Totaal: . . . . HCN + CO 32ˉ dus: HCO. . . . . 3ˉ + CNˉ
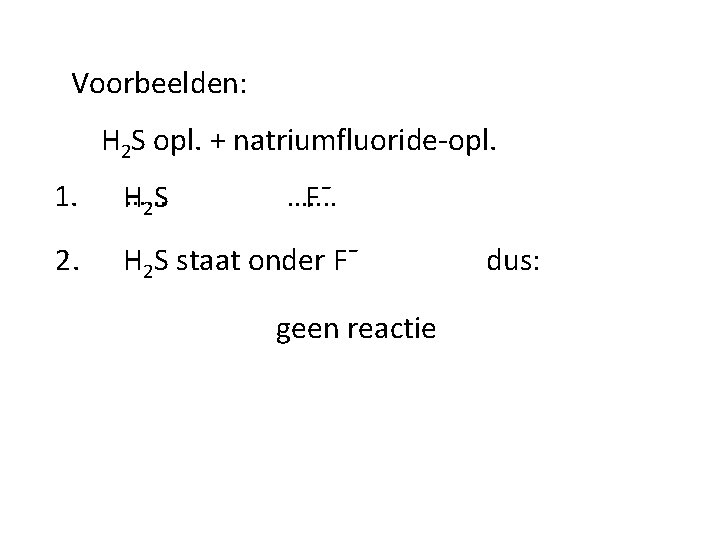
Voorbeelden: H 2 S opl. + natriumfluoride-opl. 1. . . . H 2 S 2. H 2 S staat onder Fˉ . . . . Fˉ geen reactie dus:

En nu zelf: 1. Verdund fosforzuur + overmaat ammonia 2. Citroenzuur oplossing (H 3 Cz) + overmaat benzeenamine opl. (C 6 H 5 NH 2) 3. Een oplossing van benzenol met natronloog Gebruik structuurformules voor de organische deeltjes 4. Vast calciumcarbonaat + verdund zoutzuur 5. 0, 1 mol H 3 PO 4 opl. + 0, 1 mol Na. OH opl. 6. 0, 1 mol H 3 PO 4 opl. + 0, 2 mol Na. OH opl. 7. 0, 1 mol H 3 PO 4 opl. + 0, 3 mol Na. OH opl.
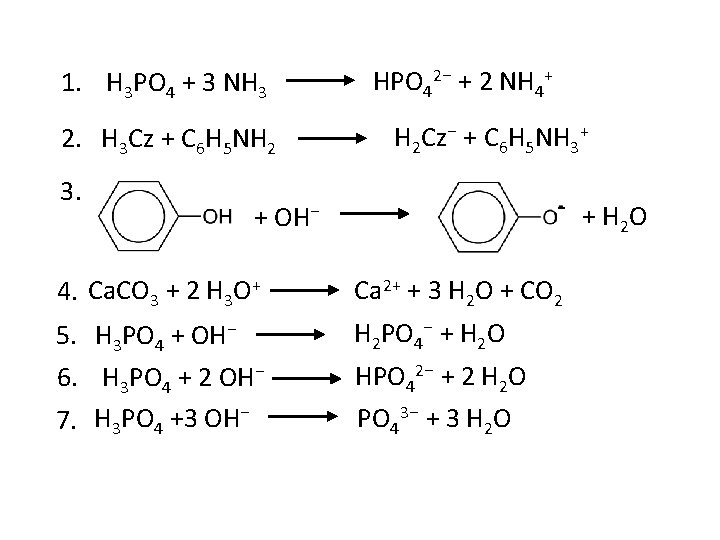
1. H 3 PO 4 + 3 NH 3 2. H 3 Cz + C 6 H 5 NH 2 3. HPO 42⁻ + 2 NH 4+ H 2 Cz⁻ + C 6 H 5 NH 3+ - +H O 2 + OH⁻ 4. Ca. CO 3 + 2 H 3 O+ Ca 2+ + 3 H 2 O + CO 2 5. H 3 PO 4 + OH⁻ 6. H 3 PO 4 + 2 OH⁻ 7. H 3 PO 4 +3 OH⁻ H 2 PO 4⁻ + H 2 O HPO 42⁻ + 2 H 2 O PO 43⁻ + 3 H 2 O
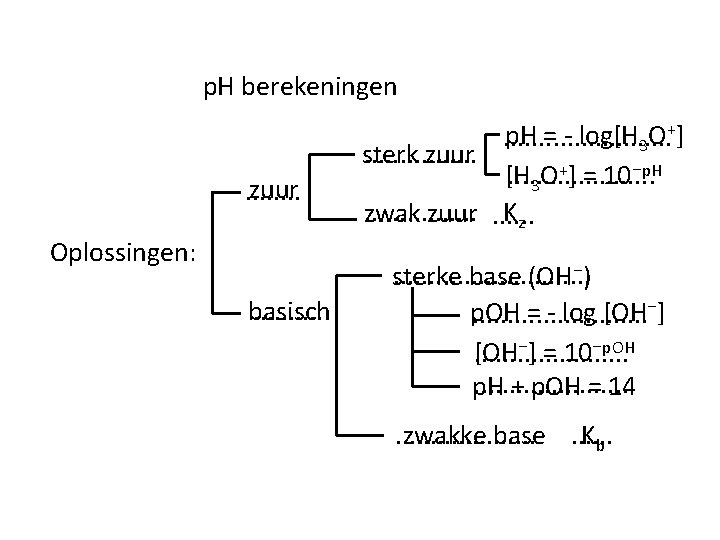
p. H berekeningen zuur. . . . Oplossingen: basisch. . p. H = - log[H 3 O+]. . . . . sterk zuur +] = 10⁻p. H [H O. . . . . 3. . . . Kz zwak zuur. . . . sterke base (OH⁻) p. OH = - log [OH⁻]. . . [OH⁻] = 10⁻p. OH. . . p. H + p. OH = 14. . . . . Kb zwakke base. . .

H 2 O is zowel een zuur als een base: een. . . amfolyt Het waterevenwicht: + + OH⁻ H 2 O + H 2 O H. . . . O 3 +]. [OH⁻] O De waterconstante KW = [H. . . . . 3 Bij 25 ⁰C (298 K) geldt: KW = 1, 0. . . . 10⁻ 14 14 Dus: [H 3 O+]. [OH⁻] = 1, 0. 10⁻. . . Hieruit is af te leiden dat: p. H + p. OH = 14. . .

Je lost 1, 96 g zwavelzuur op in 5, 00 liter water. Bereken de p. H Antwoord: p. H = 2, 10 Molaire massa H 2 SO 4 =. . . 98, 079 g mol⁻ 1 1, 96 g H 2 SO 4 = =. . 0, 0200 mol 98, 079 + + SO 2⁻ H. . . . . SO + 2 H O. . . . . 2 H O 2 4 2 3 4 0, 020 mol H 2 SO 4. . . 0, 040 mol H 3 O+ 0, 040 [H 3 = =. . . 0, 0080 mol L⁻ 1 5 p. H =. . . . -log 0, 0080 = 2, 10. . . . O +]

Aan 100 m. L zwavelzuur met p. H = 2, 63 wordt 400 m. L water toegevoegd. Bereken de nieuwe p. H. Dit kan je op twee manieren berekenen. 1. Met de verdunningsfactor 2. Met een berekening Eerst: p. H = 2, 63 2, 234. 10⁻ 3 dus: [H 3 O+] =. . . .

Aan 100 m. L zoutzuur met p. H = 2, 63 wordt 400 m. L water toegevoegd. Bereken de nieuwe p. H. 1. Met de verdunningsfactor 3 mol L⁻ 1 [H 3 O+] was vóór verdunning: 2, 34. 10⁻. . . . . Het volume was eerst: 100 m. L Het volume wordt: . . 500 m. L 5 x verdund Het zoutzuur is dus. . . . [H 3 O+] wordt dan 5 x kleiner 3 2, 34. 10⁻ [H 3 O+] wordt dus = 4, 698. 10⁻. . . . 4 5. . . . log 4, 69. 10⁻ 4 = 3, 33 p. H = -. . . . .

Aan 100 m. L zoutzuur met p. H = 2, 63 wordt 400 m. L water toegevoegd. Bereken de nieuwe p. H. 2. Met een berekening [H 3 O+] = 2, 34. 10⁻ 3 2, 34. 10⁻ 4 mol H 3 O+ In 100 m. L zit. . . . m. L Het nieuwe volume wordt 500 2, 34. 10⁻ 4 mol H 3 O+ in 500 m. L [H 3 O+] =. . . 4, 69. 10⁻ 4. . . . log 4, 6. 10⁻ 4 = 3, 33 p. H = -. . . . .

Hoe bereken je nu de p. H van een zwak zuur in water? Een zwak zuur is niet. . . volledig in ionen gesplitst:

De zuurconstante Een zwak zuur in water: + HZ(aq) + H 2 O(l). . . H 3 O (aq) + Zˉ(aq) De evenwichtsvoorwaarde is: [H 3 O+]. [Zˉ] Dus: Kz= [HZ] Deze K is de …………. …. . ……. . Zuurconstante: . . . Kz zwakker Hoe kleiner de waarde van Kz is, des te. . . het zuur is Zie Binas, tabel 49 !!!

Bereken de p. H van 0, 10 M azijnzuur oplossing Azijnzuur =. . . . . CH 3 - COOH HAc Afgekort: . . . Binas, tabel 49: Kz (CH 3 COOH) =. . . 1, 7. 10ˉ5
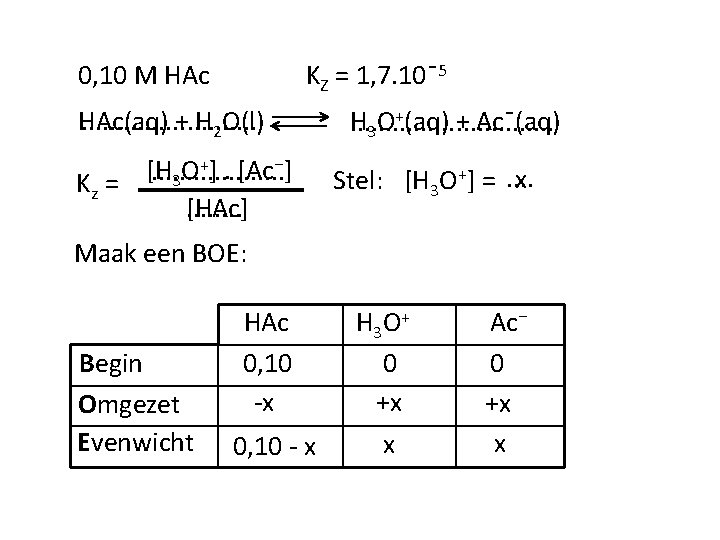
0, 10 M HAc KZ = 1, 7. 10ˉ5 HAc(aq). . . + H 2 O(l) +]. [Ac⁻] [H O. . . . . 3 Kz = [HAc]. . . . H 3 O+(aq) + Acˉ(aq). . . . x Stel: [H 3 O+] =. . Maak een BOE: Begin Omgezet Evenwicht HAc 0, 10 -x 0, 10 - x H 3 O + 0 +x x Ac⁻ 0 +x x
![0, 10 M HAc KZ = 1, 7. 10ˉ5 [HAc] = 0, 1 -x 0, 10 M HAc KZ = 1, 7. 10ˉ5 [HAc] = 0, 1 -x](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-43.jpg)
0, 10 M HAc KZ = 1, 7. 10ˉ5 [HAc] = 0, 1 -x [H 3 O+] = [Acˉ] = x KZ = [H 3 O+]. [Acˉ] [HAc] Dus: x 2 = 1, 7. 10ˉ5 x. x = 0, 10 - x Dit kan je op twee manieren oplossen: 1. Met de abc-formule 2. Met een verwaarlozing

Met de abc-formule
![0, 10 M HAc [HAc] = 0, 10 -x We hebben: KZ = 1, 0, 10 M HAc [HAc] = 0, 10 -x We hebben: KZ = 1,](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-45.jpg)
0, 10 M HAc [HAc] = 0, 10 -x We hebben: KZ = 1, 7. 10ˉ5 [H 3 O+] = [Acˉ] = x x 2 0, 10 - x = 1, 7. 10ˉ5 1. Met de abc-formule x 2 = 1, 7. 10ˉ5. (0, 10 -x) x 2 = 1, 7. 10ˉ6 - 1, 7. 10ˉ5. x x 2 + 1, 7. 10ˉ5. x - 1, 7. 10ˉ6 = 0 a=1 b = +1, 7. 10ˉ5 c = - 1, 7. 10ˉ6

1. Met de abc-formule x 2 + 1, 7. 10ˉ5. x – 1, 7. 10ˉ6 = 0 a = 1 b = +1, 7. 10ˉ5 c = - 1, 7. 10ˉ6 Dus: x = 1, 30. 10ˉ3 of x = -2, 55. 10ˉ3 p. H =. . . . . - log(1, 30. 10ˉ3) = 2, 89

Met een verwaarlozing
![0, 10 M HAc KZ = 1, 7. 10ˉ5 [HAc] = 0, 10 -x 0, 10 M HAc KZ = 1, 7. 10ˉ5 [HAc] = 0, 10 -x](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-48.jpg)
0, 10 M HAc KZ = 1, 7. 10ˉ5 [HAc] = 0, 10 -x [H 3 O+] = [Acˉ] = x 2. Met een verwaarlozing x 2 Kz = = 1, 7. 10ˉ5 0, 10 -x x 2 = 1, 7. 10ˉ6 x = 1, 30. 10ˉ3 p. H = -. . . . log(1, 30. 10ˉ3) = 2, 88

Dus: De p. H van een 0, 10 M HAc oplossing is: met de abc formule: p. H = 2, 89 met een verwaarlozing: p. H = 2, 88

H 3 PO 4 in water: H 3 PO 4 + H 2 O H 2 PO 4⁻ + H 2 O HPO 42⁻ + H 2 O + + H PO ⁻ K = 6, 9. 10⁻ 3 H. . . . . O z 3 2 4 H 3 O+ + HPO 42⁻ Kz = 7, 4. 10⁻ 8. . . . . + + PO 3⁻ H O. . . . . 3 4 Kz = 4, 8. 10⁻ 13 Bij de p. H berekening van H 3 PO 4. . . . . verwaarlozen we de tweede en derde stap Dus: Ook een meerwaardig zwak zuur in water kunnen we schrijven als: + + Z⁻. . . H. . . O HZ + H 2 O 3

En nu zelf

1. Bereken de p. H van 0, 20 M H 2 S oplossing Binas, tabel 49: KZ = 8, 9. 10ˉ8 Pas de verwaarlozing toe 2. Bereken de p. H van 0, 10 M H 3 PO 4 oplossing Binas, tabel 49: KZ = 6, 9. 10ˉ3 Pas de verwaarlozing toe Antwoorden: 1. p. H = 3, 87 2. p. H = 1, 58
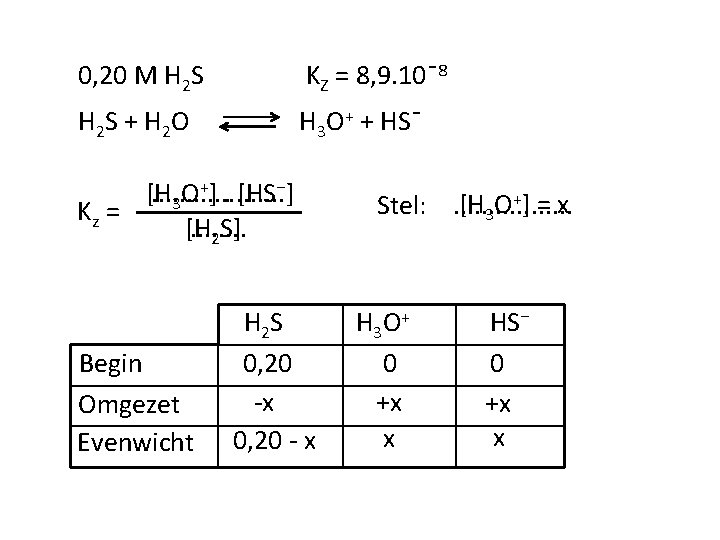
0, 20 M H 2 S KZ = 8, 9. 10ˉ8 H 2 S + H 2 O H 3 O+ + HSˉ +]. [HS⁻] [H. . . . . O 3 Kz = [H. . . . 2 S] Begin Omgezet Evenwicht H 2 S 0, 20 -x 0, 20 - x [H 3 O+] = x Stel: . . . . H 3 O + 0 +x x HS⁻ 0 +x x
![0, 20 M H 2 S KZ = 8, 9. 10ˉ8 [H 2 S] 0, 20 M H 2 S KZ = 8, 9. 10ˉ8 [H 2 S]](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-54.jpg)
0, 20 M H 2 S KZ = 8, 9. 10ˉ8 [H 2 S] = 0, 20 -x [H 3 O+] = [HSˉ] = x KZ = [H 3 O+]. [HSˉ] Dus: [H 2 S] x 2 0, 20 -x = 8, 9. 10ˉ8 x. x = 0, 20 - x = 8, 9. 10ˉ8 Verwaarloos x in 0, 20 -x:
![0, 20 M H 2 S KZ = 8, 9. 10ˉ8 [H 2 S] 0, 20 M H 2 S KZ = 8, 9. 10ˉ8 [H 2 S]](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-55.jpg)
0, 20 M H 2 S KZ = 8, 9. 10ˉ8 [H 2 S] = 0, 1 -x [H 3 O+] = [HSˉ] = x x 2 We hebben: x 2 0, 20 -x = 8, 9. 10ˉ8 x 2 = 1, 78. 10ˉ8 x = 1, 33. 10ˉ4 p. H = - log(1, 33. 10ˉ4) = 3, 87

Dus: De p. H van een 0, 20 M H 2 S oplossing is: Berekend met de verwaarlozing: p. H = 3, 87 Berekend met de abc formule: p. H = 3, 87
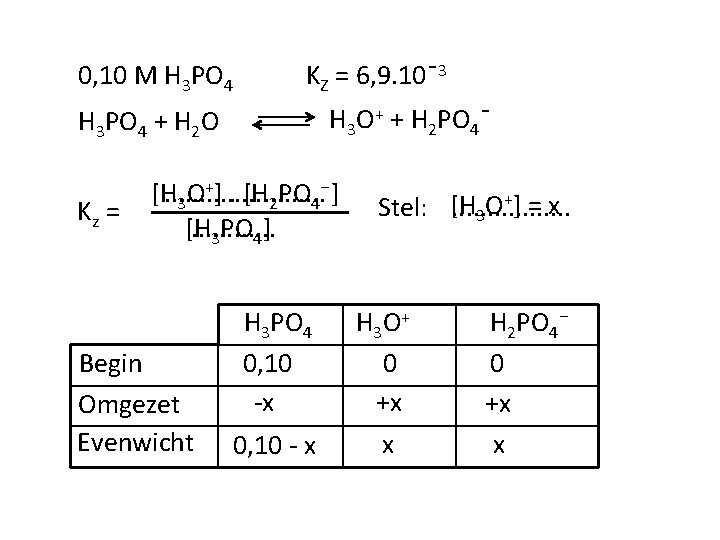
0, 10 M H 3 PO 4 KZ = 6, 9. 10ˉ3 H 3 O+ + H 2 PO 4ˉ H 3 PO 4 + H 2 O Kz = +]. [H PO ⁻] [H. . . O 3 2 4. . . [H 3 PO 4] Begin Omgezet Evenwicht H 3 PO 4 0, 10 -x 0, 10 - x +] = x O Stel: [H. . . . 3 H 3 O + 0 +x x H 2 PO 4⁻ 0 +x x
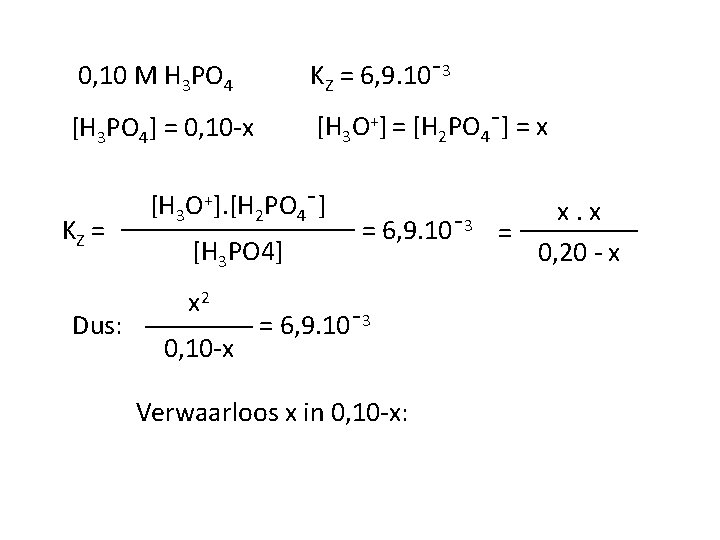
0, 10 M H 3 PO 4 KZ = 6, 9. 10ˉ3 [H 3 PO 4] = 0, 10 -x [H 3 O+] = [H 2 PO 4ˉ] = x KZ = Dus: [H 3 O+]. [H 2 PO 4ˉ] [H 3 PO 4] x 2 0, 10 -x = 6, 9. 10ˉ3 Verwaarloos x in 0, 10 -x: x. x = 0, 20 - x
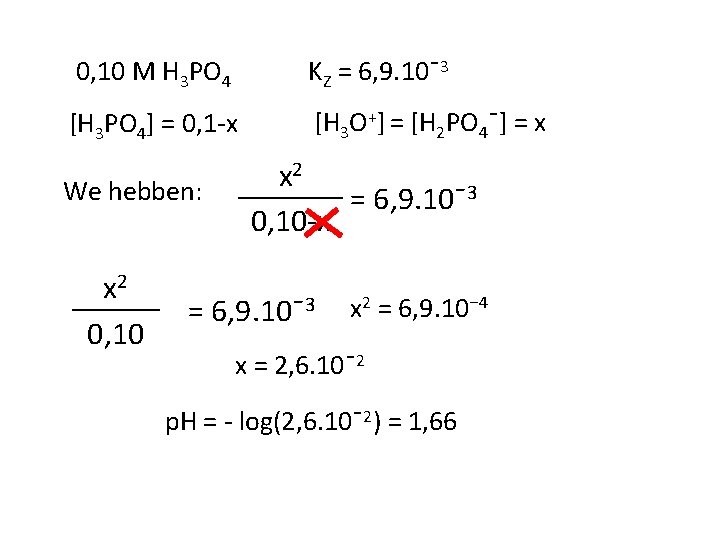
0, 10 M H 3 PO 4 KZ = 6, 9. 10ˉ3 [H 3 PO 4] = 0, 1 -x [H 3 O+] = [H 2 PO 4ˉ] = x We hebben: x 2 0, 10 x 2 = 6, 9. 10ˉ3 0, 10 -x = 6, 9. 10ˉ3 x 2 = 6, 9. 10⁻ 4 x = 2, 6. 10ˉ2 p. H = - log(2, 6. 10ˉ2) = 1, 66

Dus: De p. H van een 0, 10 M H 3 PO 4 oplossing is: Berekend met de verwaarlozing: p. H = 1, 58 Berekend met de abc formule: p. H = 1, 66

Nu nog een drietal puzzeltjes

1. Een 0, 10 M oplossing van het zwakke zuur HZ heeft p. H = 2, 15 Bereken hoeveel% van de HZ moleculen is geïoniseerd 2. Een oplossing van het zwakke zuur HF heeft p. H = 3, 30 Bereken de molariteit van deze oplossing 3. Een 0, 010 M oplossing van het zwakke zuur HZ heeft p. H = 2, 20 Bereken de waarde van Kz Antwoorden: 1. 7, 1% 2. 9, 0. 10⁻ 4 3. Kz = 1, 1. 10⁻ 2
![1. p. H = 2, 15 dus: [H 3 O+] = 7, 08. 10⁻ 1. p. H = 2, 15 dus: [H 3 O+] = 7, 08. 10⁻](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-63.jpg)
1. p. H = 2, 15 dus: [H 3 O+] = 7, 08. 10⁻ 3 H 3 O+(aq) + F⁻(aq) HF(aq) + H 2 O(l) Van de oorspronkelijke 0, 10 mol HF heeft 7, 08. 10⁻ 3 mol gereageerd 7, 08. 10⁻ 3 x 100% = 7, 1% 0, 10
![2. p. H = 3, 30 dus: [H 3 O+] = 5, 0. 10⁻ 2. p. H = 3, 30 dus: [H 3 O+] = 5, 0. 10⁻](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-64.jpg)
2. p. H = 3, 30 dus: [H 3 O+] = 5, 0. 10⁻ 4 HF(aq) + H 2 O(l) H 3 O+(aq) + F⁻(aq) 5, 0. 10⁻ 4 4 )2 [H 3 O+]. [F⁻] (5, 0. 10⁻ = 6, 3. 10⁻ 4 = Kz = [HF] Dus : [HF] = 4, 0. 10⁻ 4 Begin Omgezet Evenwicht HF H 3 O + 9, 0. 10⁻ ? 4 0 -5, 0. 10⁻ 4 +5, 0. 10⁻ 4 4, 0. 10⁻ 4 5, 0. 10⁻ 4 De molariteit is 9, 0. 10⁻ 4 F⁻ 0 +5, 0. 10⁻ 4
![3. p. H = 2, 20 dus: [H 3 O+] = 6, 31. 10⁻ 3. p. H = 2, 20 dus: [H 3 O+] = 6, 31. 10⁻](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-65.jpg)
3. p. H = 2, 20 dus: [H 3 O+] = 6, 31. 10⁻ 3 HA(aq) + H 2 O(l) Begin Omgezet Evenwicht H 3 O+(aq) + A⁻(aq) 6, 31. 10⁻ 3 HA H 3 O+ A⁻ 0 0, 010 0 -6, 31. 10⁻ 3 +6, 31. 10⁻ 3 3, 70. 10⁻ 3 6, 31. 10⁻ 3 [H 3 O+]. [A⁻] (6, 31. 10⁻ 3)2 2 1, 1. 10⁻ Kz = = = [HA] 3, 70. 10⁻ 3
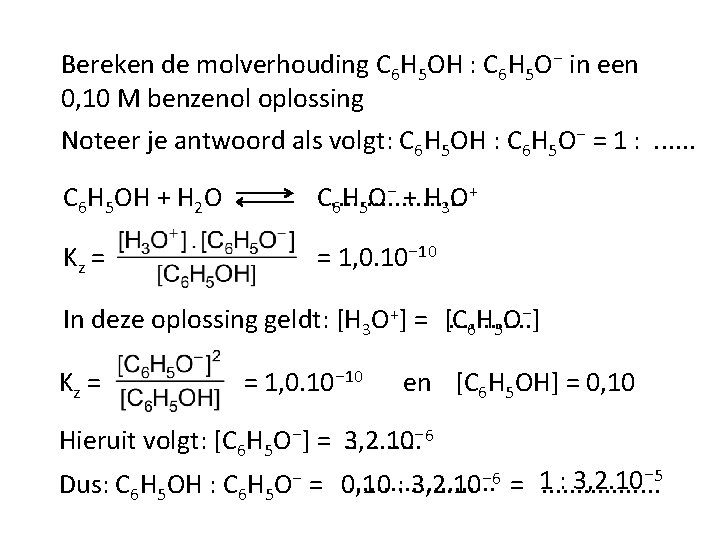
Bereken de molverhouding C 6 H 5 OH : C 6 H 5 O⁻ in een 0, 10 M benzenol oplossing Noteer je antwoord als volgt: C 6 H 5 OH : C 6 H 5 O⁻ = 1 : . . . C 6 H 5 OH + H 2 O + C. . . . . H O⁻ + H O 6 5 3 Kz = = 1, 0. 10⁻ 10 In deze oplossing geldt: [H 3 O+] = [C. . . 6 H 5 O⁻] Kz = = 1, 0. 10⁻ 10 en [C 6 H 5 OH] = 0, 10 . . . 6 Hieruit volgt: [C 6 H 5 O⁻] = 3, 2. 10⁻ : 3, 2. 10⁻ 5. . . . . Dus: C 6 H 5 OH : C 6 H 5 O⁻ = 0, 10 : 3, 2. 10⁻ 6 = 1. . . .

In 35 m. L oplossing is 0, 13 mmol Ba(OH)2 opgelost Bereken de p. H Antwoord: p. H = 11, 87

In 35 m. L oplossing is 0, 13 mmol Ba(OH)2 opgelost Bereken de p. H 1. Ba(OH)2(s) 0, 13 mmol 2. mmol OH⁻ Ba 2+(aq) + 2 OH⁻(aq) 0, 26 mmol 0, 26 35 m. L x 1 m. L volume 0, 26 = 7, 4. 10⁻ 3 x= 35 3. [OH⁻] = 7, 4. 10⁻ 3 mol L⁻ 1 p. OH = - log 7, 4. 10⁻ 3 = 2, 13 4. p. H = 14 – 2, 13 = 11, 87

Aan 50 m. L natronloog met p. H = 12, 30 wordt 450 m. L water gevoegd. Bereken de nieuwe p. H. Voordat je aan de slag gaat, eerst: Dit is een basische oplossing, dus: p. OH = 14 – 12, 3 = 1, 7 Dus [OH⁻] = 10⁻ 1, 70 = 2, 0. 10⁻ 2 mol L⁻ 1 1. Met de verdunningsfactor 2. Met een berekening

Aan 50 m. L natronloog met p. H = 12, 30 wordt 450 m. L water gevoegd. Bereken de nieuwe p. H. 1. Met de verdunningsfactor [OH⁻] = 2, 0. 10⁻ 2. . Het volume was eerst: 50 m. L Het volume wordt: . . 500 m. L 10 x verdund Het natronloog is dus. . . . [OH⁻] wordt dan 10 x kleiner 2, 0. 10⁻ 2 [OH⁻] wordt dus = 2, 0. 10⁻ 3 10 p. OH =- log 2, 0. 10⁻ 3 = 2, 7 p. H = 11, 30

Aan 50 m. L natronloog met p. H = 12, 30 wordt 450 m. L water gevoegd. Bereken de nieuwe p. H. 2. Met een berekening: [OH⁻] = 2, 0. 10⁻ 2 In 50 m. L zit: 1, 0. 10⁻. . 3 mol OH⁻ Het volume wordt: . . 500 m. L 1, 0. 10⁻ 3 mol OH⁻ in 500 m. L. . . 3 [OH⁻] = 2, 0. 10⁻ p. OH = - log 2, 0. 10⁻ 3 = 2, 7 p. H = 11, 30

De baseconstante Een zwakke base in water: Z⁻(aq) + H 2 O(l) HZ(aq) + OHˉ(aq). . . De evenwichtsvoorwaarde is: [HZ]. [OHˉ] Dus: Kb= [Z⁻] Baseconstante: K. . Deze K is de …………. …. . ……. . b Hoe kleiner de waarde van Kb is, des te. . . zwakker het base is
![De p-waarde p. H = -. . . . log[H 3 O+] - log[OH⁻] De p-waarde p. H = -. . . . log[H 3 O+] - log[OH⁻]](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-73.jpg)
De p-waarde p. H = -. . . . log[H 3 O+] - log[OH⁻] p. OH =. . . . p. Kz = -. . log Kz p. Kb = -. . log Kb Bewezen kan worden dat: 14 (bij 25 ⁰C) Kz x Kb = Kw = 1, 0. 10ˉ. . . Dus: . . . (bij 25 ⁰C) p. Kz + p. Kb = p. Kw = 14
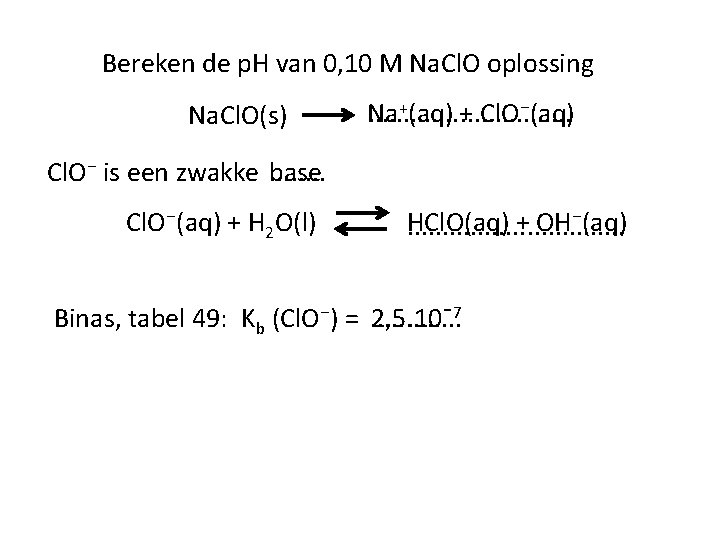
Bereken de p. H van 0, 10 M Na. Cl. O oplossing Na. Cl. O(s) +(aq) + Cl. O⁻(aq) Na. . . . Cl. O⁻ is een zwakke base. . . . Cl. O⁻(aq) + H 2 O(l) HCl. O(aq) + OH⁻(aq). . . . Binas, tabel 49: Kb (Cl. O⁻) =. . . 2, 5. 10ˉ7
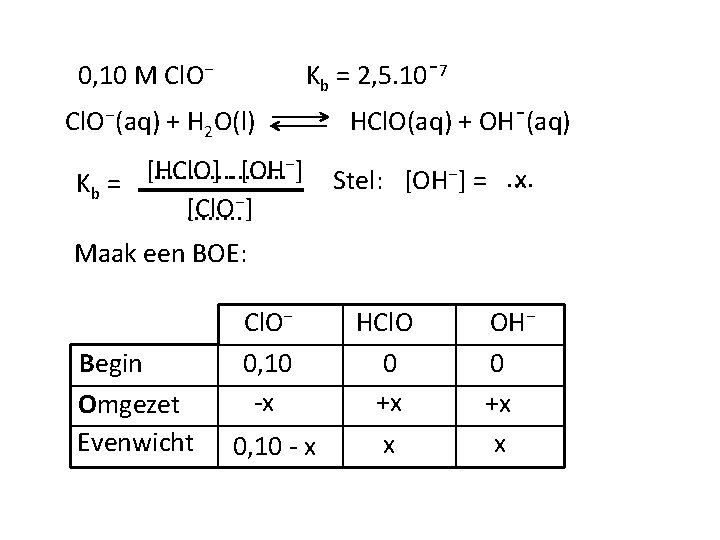
0, 10 M Cl. O⁻ Kb = 2, 5. 10ˉ7 Cl. O⁻(aq) + H 2 O(l). . . . . [OH⁻] Kb = [HCl. O] [Cl. O⁻]. . . . HCl. O(aq) + OHˉ(aq) x Stel: [OH⁻] =. . Maak een BOE: Begin Omgezet Evenwicht Cl. O⁻ 0, 10 -x 0, 10 - x HCl. O 0 +x x OH⁻ 0 +x x
![0, 10 M Cl. O⁻ Kb = 2, 5. 10ˉ7 [Cl. O⁻] = 0, 0, 10 M Cl. O⁻ Kb = 2, 5. 10ˉ7 [Cl. O⁻] = 0,](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-76.jpg)
0, 10 M Cl. O⁻ Kb = 2, 5. 10ˉ7 [Cl. O⁻] = 0, 1 -x [HCl. O] = [OHˉ] = x Kb = [HCl. O]. [OHˉ] [Cl. O⁻] Dus: x 2 = 2, 5. 10ˉ7 x. x = 0, 10 - x Dit kan je op twee manieren oplossen: 1. Met de abc-formule 2. Met een verwaarlozing

Met de abc-formule
![0, 10 M Cl. O⁻ [Cl. O⁻] = 0, 10 -x We hebben: Kb 0, 10 M Cl. O⁻ [Cl. O⁻] = 0, 10 -x We hebben: Kb](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-78.jpg)
0, 10 M Cl. O⁻ [Cl. O⁻] = 0, 10 -x We hebben: Kb = 2, 5. 10ˉ7 [HCl. O] = [OHˉ] = x x 2 0, 10 - x = 2, 5. 10ˉ7 1. Met de abc-formule x 2 = 2, 5. 10ˉ7. (0, 10 -x) x 2 = 2, 5. 10ˉ8 – 2, 5. 10ˉ7. x x 2 + 2, 5. 10ˉ7. x - 2, 5. 10ˉ8 = 0 a=1 b = +2, 5. 10ˉ7 c = - 2, 5. 10ˉ8

1. Met de abc-formule x 2 + 2, 5. 10ˉ7. x – 2, 5. 10ˉ8 = 0 a = 1 b = +2, 5. 10ˉ7 c = - 2, 5. 10ˉ8 Dus: x = 1, 58. 10ˉ4 of x = -1, 58. 10ˉ4 log(1, 58. 10ˉ4) = 3, 80 p. OH = -. . . . p. H = 14. . . – 3, 80 = 10, 20

Met een verwaarlozing
![0, 10 M Cl. O⁻ Kb = 2, 5. 10ˉ7 [Cl. O⁻] = 0, 0, 10 M Cl. O⁻ Kb = 2, 5. 10ˉ7 [Cl. O⁻] = 0,](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-81.jpg)
0, 10 M Cl. O⁻ Kb = 2, 5. 10ˉ7 [Cl. O⁻] = 0, 10 -x [HCl. O] = [OHˉ] = x 2. Met een verwaarlozing x 2 Kb = = 2, 5. 10ˉ7 0, 10 -x x 2 = 2, 5. 10ˉ8 x = 1, 58. 10ˉ4 p. OH =. . . . - log(1, 58. 10ˉ4) = 3, 80. . . p. H = 14 – 3, 80 = 10, 20

Dus: De p. H van een 0, 10 M Na. Cl. O oplossing is: met de abc formule: p. H = 10, 20 met een verwaarlozing: p. H = 10, 20

En nu zelf

1. Bereken de p. H van 0, 20 M natriumcarbonaat oplossing Binas, tabel 49: Kb = 2, 1. 10ˉ4 Pas de verwaarlozing toe 2. Bereken de p. H van 0, 10 M natriumacetaat oplossing Binas, tabel 49: Kb = 5, 8. 10ˉ10 Pas de verwaarlozing toe Antwoorden: 1. p. H = 11, 81 2. p. H = 8, 88
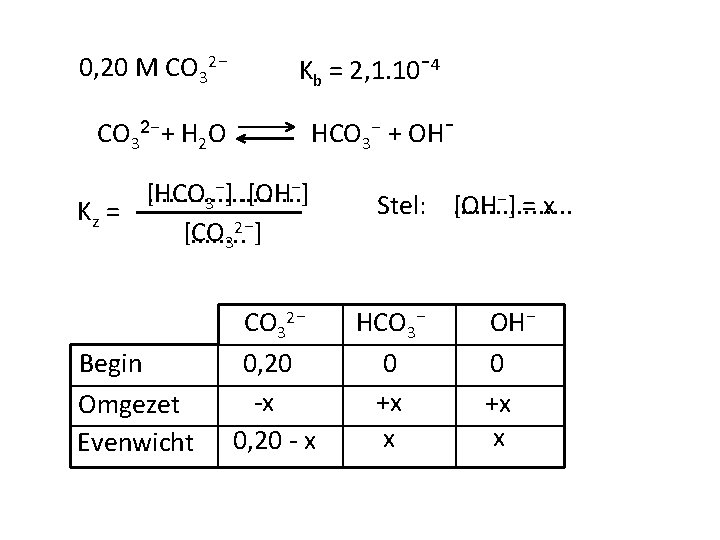
0, 20 M CO 32⁻ Kb = 2, 1. 10ˉ4 CO 32⁻+ H 2 O HCO 3⁻ + OHˉ [HCO. . . . . 3⁻]. [OH⁻] Kz = 2⁻] [CO. . . . 3 Begin Omgezet Evenwicht CO 32⁻ 0, 20 -x 0, 20 - x [OH⁻] = x Stel: . . . . HCO 3⁻ 0 +x x OH⁻ 0 +x x
![0, 20 M CO 32⁻ Kb = 2, 1. 10ˉ4 [HCO 3⁻] = [OHˉ] 0, 20 M CO 32⁻ Kb = 2, 1. 10ˉ4 [HCO 3⁻] = [OHˉ]](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-86.jpg)
0, 20 M CO 32⁻ Kb = 2, 1. 10ˉ4 [HCO 3⁻] = [OHˉ] = x [CO 32⁻] = 0, 20 -x KZ = [HCO 3⁻]. [OHˉ] Dus: [CO 3 2⁻] x 2 0, 20 -x = 2, 1. 10ˉ4 Verwaarloos x in 0, 20 -x: x. x = 0, 20 - x
![0, 20 M CO 32⁻ Kb = 2, 1. 10ˉ4 [HCO 3⁻] = [OHˉ] 0, 20 M CO 32⁻ Kb = 2, 1. 10ˉ4 [HCO 3⁻] = [OHˉ]](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-87.jpg)
0, 20 M CO 32⁻ Kb = 2, 1. 10ˉ4 [HCO 3⁻] = [OHˉ] = x [CO 32⁻] = 0, 20 -x x 2 We hebben: x 2 0, 20 -x = 2, 1. 10ˉ4 x 2 = 4, 2. 10ˉ5 x = 6, 5. 10ˉ3 p. OH = - log(6, 5. 10ˉ3) = 2, 19 p. H = 14 – 2, 19 = 11, 81
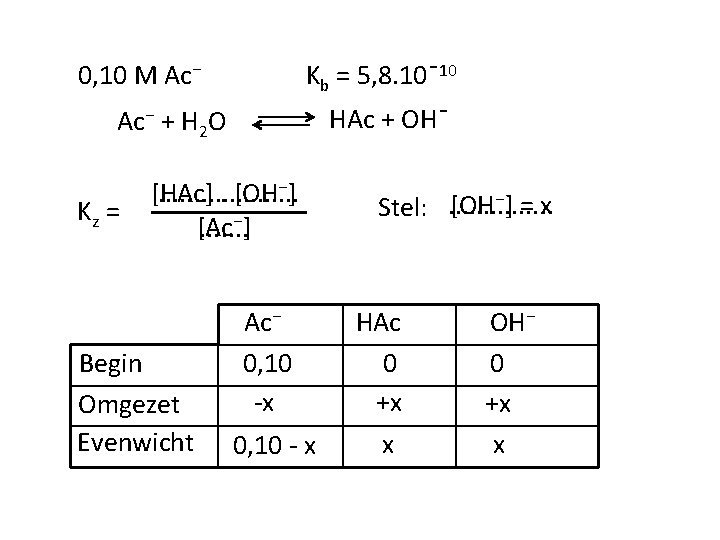
0, 10 M Ac⁻ Kb = 5, 8. 10ˉ10 HAc + OHˉ Ac⁻ + H 2 O Kz = [HAc]. . . . . [OH⁻] [Ac⁻]. . . . Begin Omgezet Evenwicht Ac⁻ 0, 10 -x 0, 10 - x [OH⁻] = x Stel: . . . . HAc 0 +x x OH⁻ 0 +x x
![0, 10 M Ac⁻ Kb = 5, 8. 10ˉ10 [HAc] = [OHˉ] = x 0, 10 M Ac⁻ Kb = 5, 8. 10ˉ10 [HAc] = [OHˉ] = x](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-89.jpg)
0, 10 M Ac⁻ Kb = 5, 8. 10ˉ10 [HAc] = [OHˉ] = x [Ac⁻] = 0, 10 -x KZ = Dus: [HAc]. [OHˉ] [Ac⁻] x 2 0, 10 -x x. x = 6, 9. 10ˉ3 = 0, 10 - x = 5, 8. 10ˉ10 Verwaarloos x in 0, 10 -x:
![0, 10 M Ac⁻ [Ac⁻] = 0, 10 -x We hebben: x 2 0, 0, 10 M Ac⁻ [Ac⁻] = 0, 10 -x We hebben: x 2 0,](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-90.jpg)
0, 10 M Ac⁻ [Ac⁻] = 0, 10 -x We hebben: x 2 0, 10 Kb = 5, 8. 10ˉ10 [HAc] = [OHˉ] = x x 2 = 5, 8. 10ˉ10 0, 10 -x = 5, 8. 10ˉ10 x 2 = 5, 8. 10⁻ 11 x = 7, 6. 10ˉ6 p. OH = - log(7, 6. 10ˉ6) = 5, 12 p. H = 14 – 5, 12 = 8, 88

Nu nog een viertal puzzeltjes

1. Een 0, 10 M oplossing van het zwakke base Z⁻ heeft p. H = 11, 85 Bereken hoeveel % van het Z⁻ omgezet is 2. Een oplossing van het zwakke base NH 3 heeft p. H = 11, 04 Bereken de molariteit van deze oplossing 3. Een 0, 010 M oplossing van het zwakke base Z⁻ heeft p. H = 11, 80 Bereken de waarde van Kz van HZ 4. Leg uit of een oplossing van H 2 PO 4ˉ zuur, basisch of neutraal is Antwoorden: 1. 7, 1% 2. 6, 8. 10⁻ 2 3. Kz = 9, 1. 10⁻ 13 4. (zwak) zuur
![1. p. H = 11, 85 dus: p. OH = 2, 15 en [OH⁻] 1. p. H = 11, 85 dus: p. OH = 2, 15 en [OH⁻]](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-93.jpg)
1. p. H = 11, 85 dus: p. OH = 2, 15 en [OH⁻] = 7, 08. 10⁻ 3 HZ(aq) + OH⁻(aq) Z⁻(aq) + H 2 O(l) Van de oorspronkelijke 0, 10 mol Z⁻ heeft 7, 08. 10⁻ 3 mol gereageerd 7, 08. 10⁻ 3 x 100% = 7, 1% 0, 10
![2. p. H = 11, 04 dus: p. OH = 2, 96 en [OH⁻] 2. p. H = 11, 04 dus: p. OH = 2, 96 en [OH⁻]](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-94.jpg)
2. p. H = 11, 04 dus: p. OH = 2, 96 en [OH⁻] = 1, 1. 10⁻ 3 NH 4+ + OH⁻ NH 3 + H 2 O 1, 1. 10⁻ 3 3 )2 [NH 4+]. [OH⁻] (1, 1. 10⁻ = 1, 9. 10⁻ 5 = Kb = [NH 3] Dus : [NH 3] = 6, 7. 10⁻ 2 Begin Omgezet Evenwicht NH 3 NH 4+ ? 2 0 6, 8. 10⁻ -1, 1. 10⁻ 3 +1, 1. 10⁻ 3 6, 7. 10⁻ 2 1, 1. 10⁻ 3 De molariteit is 6, 8. 10⁻ 2 OH⁻ 0 +1, 1. 10⁻ 3
![3. p. H =11, 80 dus: p. OH = 2, 20 en [OH⁻] = 3. p. H =11, 80 dus: p. OH = 2, 20 en [OH⁻] =](http://slidetodoc.com/presentation_image_h2/6ab24e00d1a0589ef7e73b283714c24a/image-95.jpg)
3. p. H =11, 80 dus: p. OH = 2, 20 en [OH⁻] = 6, 3. 10⁻ 3 HZ + OH⁻ 6, 3. 10⁻ 3 Z⁻ + H 2 O Begin Omgezet Evenwicht Z⁻ 0, 010 -6, 3. 10⁻ 3 3, 7. 10⁻ 3 HZ 0 +6, 3. 10⁻ 3 OH⁻ 0 +6, 3. 10⁻ 3 [HZ]. [OH⁻] (6, 3. 10⁻ 3)2 2 1, 1. 10⁻ Kb = = = [Z⁻] 3, 7. 10⁻ 3 Kz. K b = 1, 0. 10⁻ 14 13 = 9, 1. 10⁻ Kz = 1, 1. 10⁻ 2
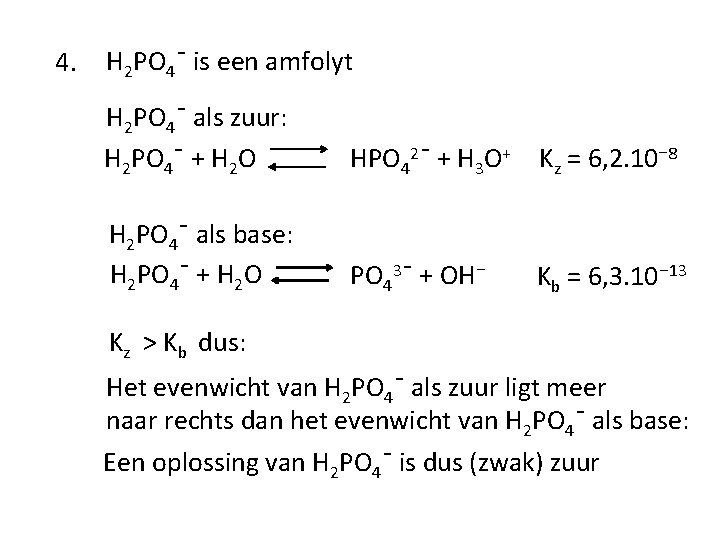
4. H 2 PO 4ˉ is een amfolyt H 2 PO 4ˉ als zuur: H 2 PO 4ˉ + H 2 O HPO 42ˉ + H 3 O+ Kz = 6, 2. 10⁻ 8 H 2 PO 4ˉ als base: H 2 PO 4ˉ + H 2 O PO 43ˉ + OH⁻ Kb = 6, 3. 10⁻ 13 Kz > Kb dus: Het evenwicht van H 2 PO 4ˉ als zuur ligt meer naar rechts dan het evenwicht van H 2 PO 4ˉ als base: Een oplossing van H 2 PO 4ˉ is dus (zwak) zuur
- Slides: 96