Salze Eigenschaften Salze sind chemische Verbindungen die aus
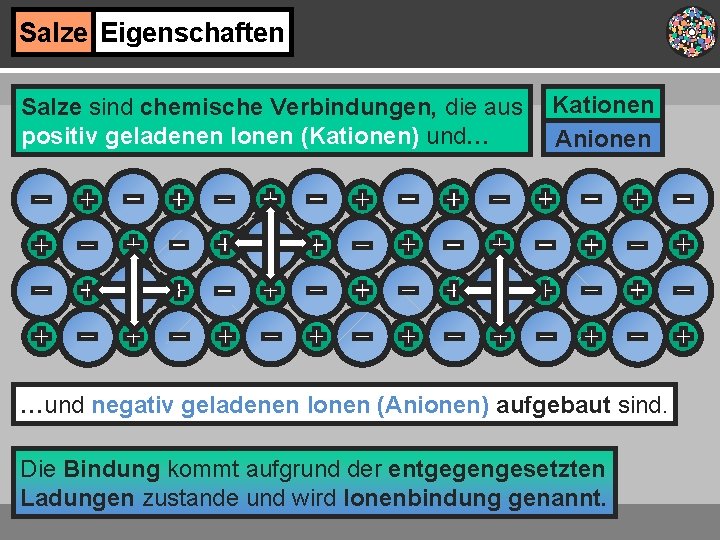
Salze Eigenschaften Salze sind chemische Verbindungen, die aus positiv geladenen Ionen (Kationen) und… Kationen Anionen …und negativ geladenen Ionen (Anionen) aufgebaut sind. Die Bindung kommt aufgrund der entgegengesetzten Ladungen zustande und wird Ionenbindung genannt.
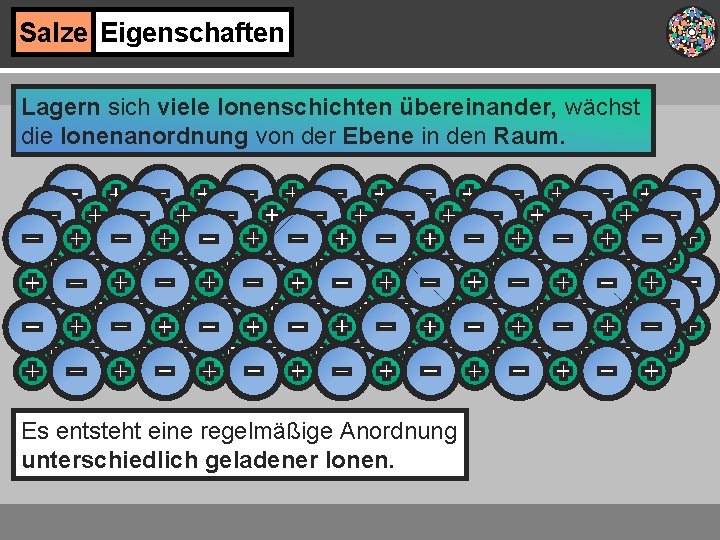
Salze Eigenschaften Lagern sich viele Ionenschichten übereinander, wächst die Ionenanordnung von der Ebene in den Raum. Es entsteht eine regelmäßige Anordnung unterschiedlich geladener Ionen.
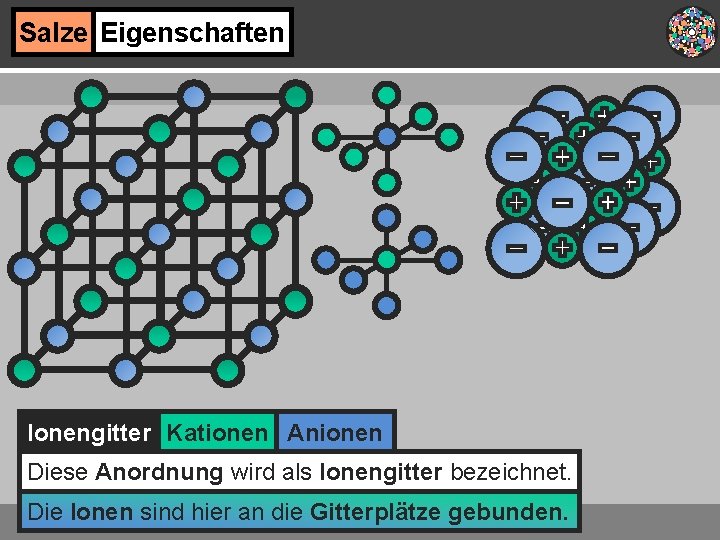
Salze Eigenschaften Ionengitter Kationen Anionen Diese Anordnung wird als Ionengitter bezeichnet. Die Ionen sind hier an die Gitterplätze gebunden.
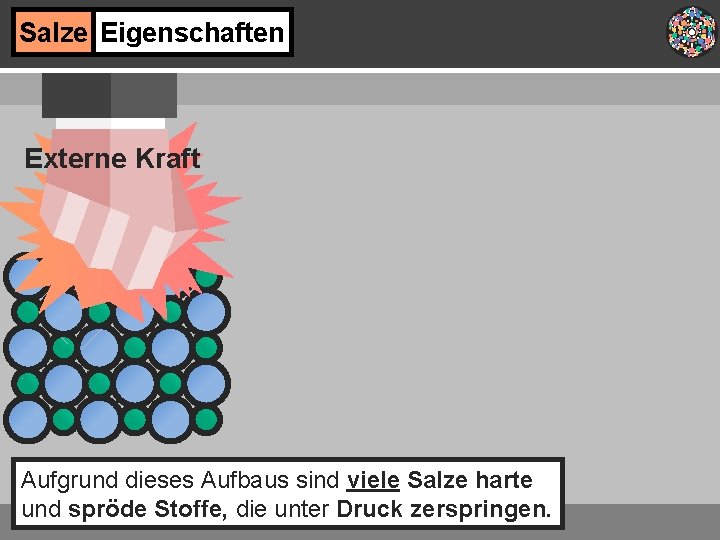
Salze Eigenschaften Externe Kraft Aufgrund dieses Aufbaus sind viele Salze harte und spröde Stoffe, die unter Druck zerspringen.
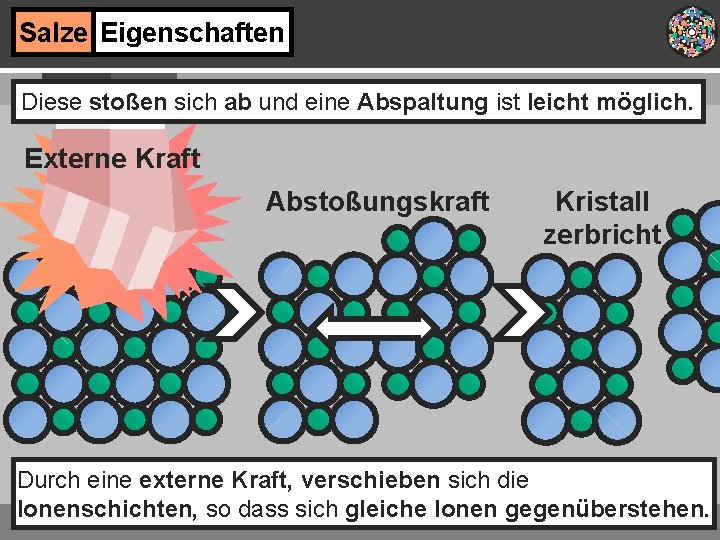
Salze Eigenschaften Diese stoßen sich ab und eine Abspaltung ist leicht möglich. Externe Kraft Abstoßungskraft Kristall zerbricht Durch eine externe Kraft, verschieben sich die Ionenschichten, so dass sich gleiche Ionen gegenüberstehen.
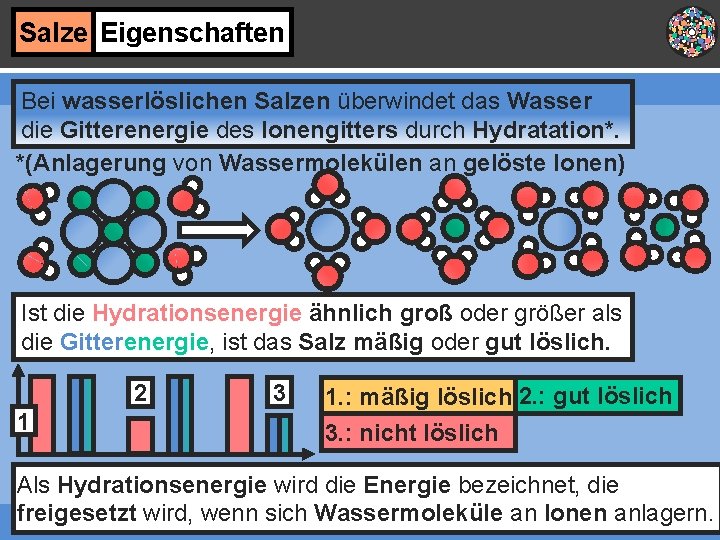
Salze Eigenschaften Bei wasserlöslichen Salzen überwindet das Wasser die Gitterenergie des Ionengitters durch Hydratation*. *(Anlagerung von Wassermolekülen an gelöste Ionen) Ist die Hydrationsenergie ähnlich groß oder größer als die Gitterenergie, ist das Salz mäßig oder gut löslich. 2 1 3 1. : mäßig löslich 2. : gut löslich 3. : nicht löslich Als Hydrationsenergie wird die Energie bezeichnet, die freigesetzt wird, wenn sich Wassermoleküle an Ionen anlagern.
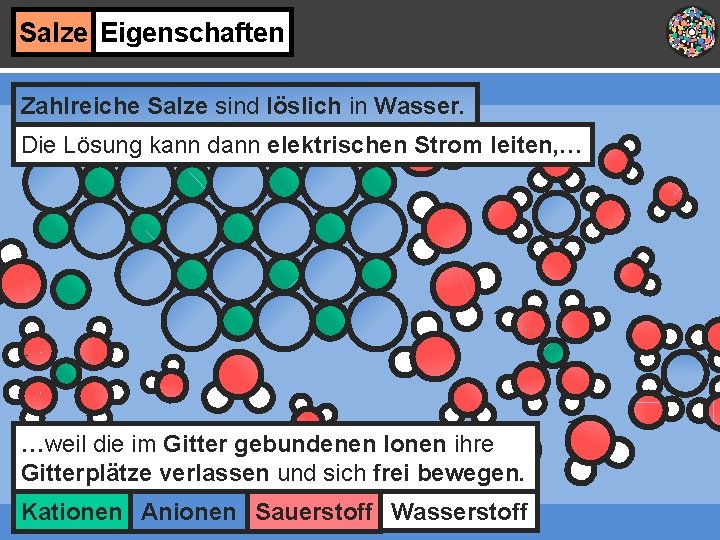
Salze Eigenschaften Zahlreiche Salze sind löslich in Wasser. Die Lösung kann dann elektrischen Strom leiten, … …weil die im Gitter gebundenen Ionen ihre Gitterplätze verlassen und sich frei bewegen. Kationen Anionen Sauerstoff Wasserstoff
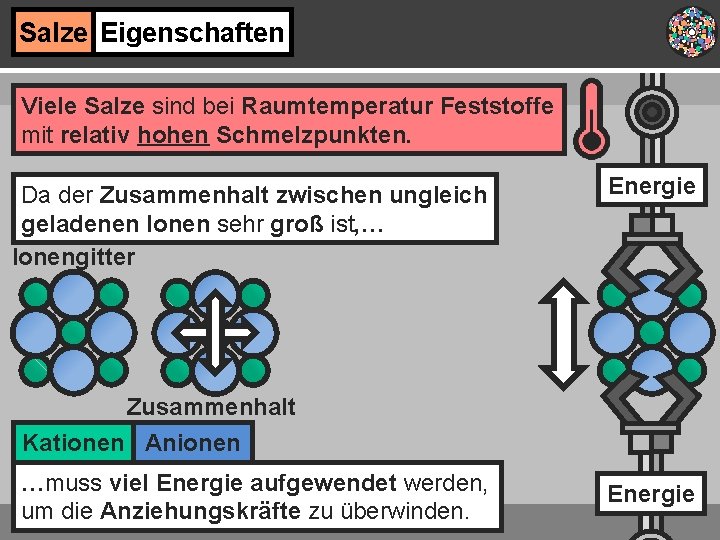
Salze Eigenschaften Viele Salze sind bei Raumtemperatur Feststoffe mit relativ hohen Schmelzpunkten. Da der Zusammenhalt zwischen ungleich geladenen Ionen sehr groß ist, … Ionengitter Energie Zusammenhalt Kationen Anionen …muss viel Energie aufgewendet werden, um die Anziehungskräfte zu überwinden. Energie
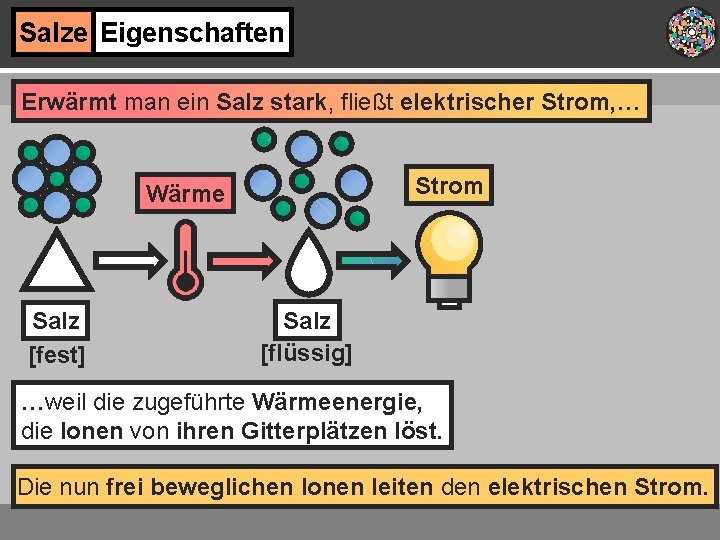
Salze Eigenschaften Erwärmt man ein Salz stark, fließt elektrischer Strom, … Strom Wärme Salz [fest] Salz [flüssig] …weil die zugeführte Wärmeenergie, die Ionen von ihren Gitterplätzen löst. Die nun frei beweglichen Ionen leiten den elektrischen Strom.
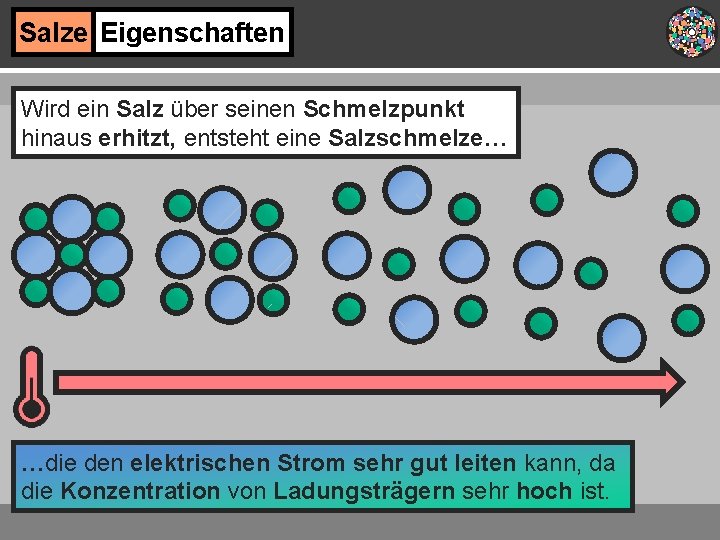
Salze Eigenschaften Wird ein Salz über seinen Schmelzpunkt hinaus erhitzt, entsteht eine Salzschmelze… …die den elektrischen Strom sehr gut leiten kann, da die Konzentration von Ladungsträgern sehr hoch ist.
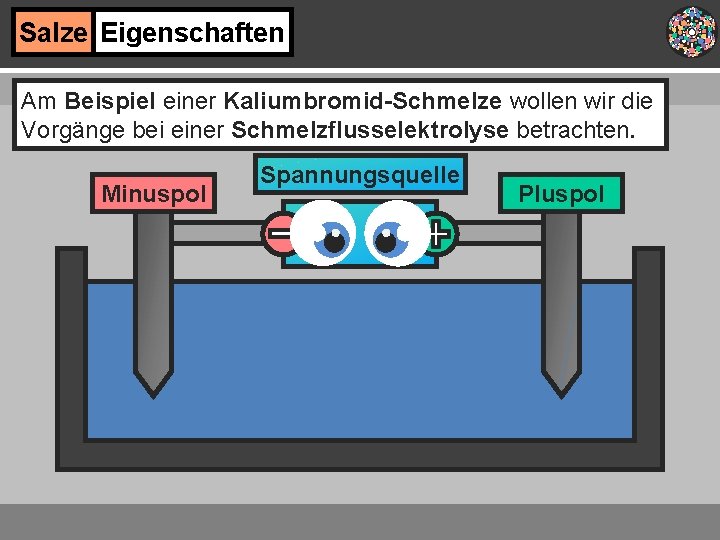
Salze Eigenschaften Am Beispiel einer Kaliumbromid-Schmelze wollen wir die Vorgänge bei einer Schmelzflusselektrolyse betrachten. Minuspol Spannungsquelle Pluspol
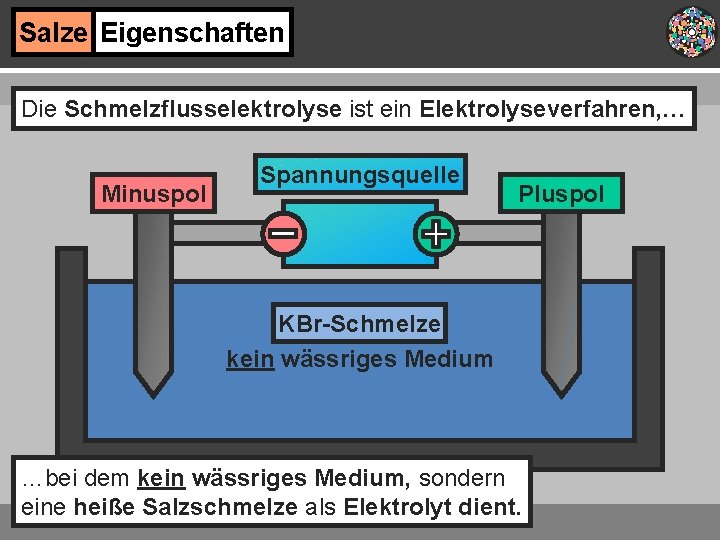
Salze Eigenschaften Die Schmelzflusselektrolyse ist ein Elektrolyseverfahren, … Minuspol Spannungsquelle Pluspol KBr-Schmelze kein wässriges Medium …bei dem kein wässriges Medium, sondern eine heiße Salzschmelze als Elektrolyt dient.
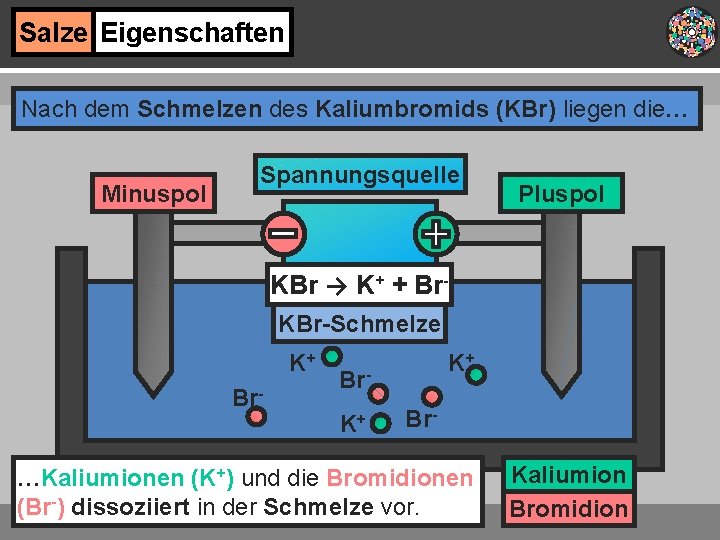
Salze Eigenschaften Nach dem Schmelzen des Kaliumbromids (KBr) liegen die… Minuspol Spannungsquelle Pluspol KBr → K+ + Br. KBr-Schmelze K+ Br- …Kaliumionen (K+) und die Bromidionen (Br-) dissoziiert in der Schmelze vor. Kaliumion Bromidion
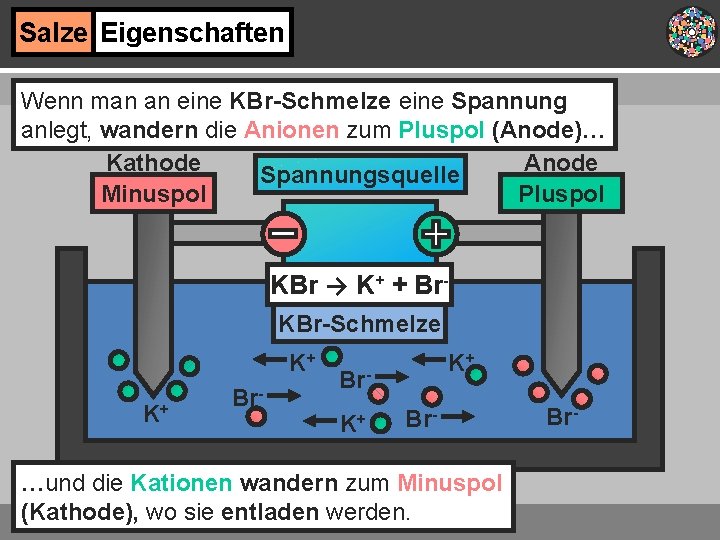
Salze Eigenschaften Wenn man an eine KBr-Schmelze eine Spannung anlegt, wandern die Anionen zum Pluspol (Anode)… Kathode Anode Spannungsquelle Minuspol Pluspol KBr → K+ + Br. KBr-Schmelze K+ K+ Br- …und die Kationen wandern zum Minuspol (Kathode), wo sie entladen werden. Br-
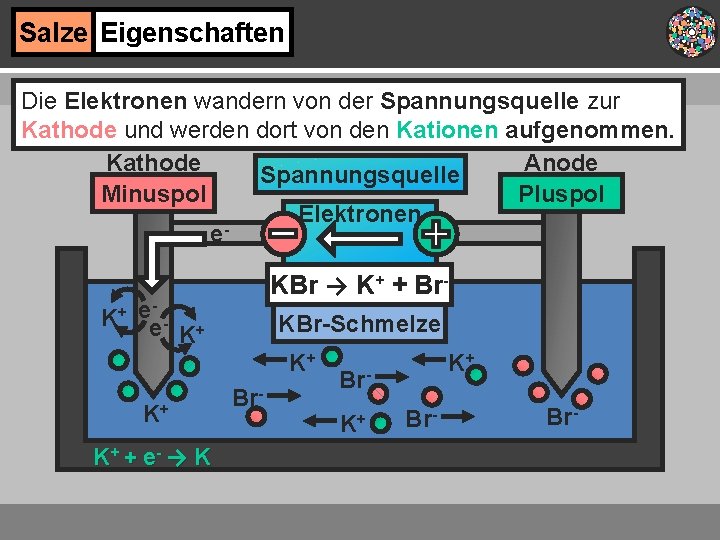
Salze Eigenschaften Die Elektronen wandern von der Spannungsquelle zur Kathode und werden dort von den Kationen aufgenommen. Kathode Anode Spannungsquelle Minuspol Pluspol Elektronen e K+ KBr → K+ + Br- e- e K+ KBr-Schmelze K+ K+ K+ + e- → K Br- K+ Br-
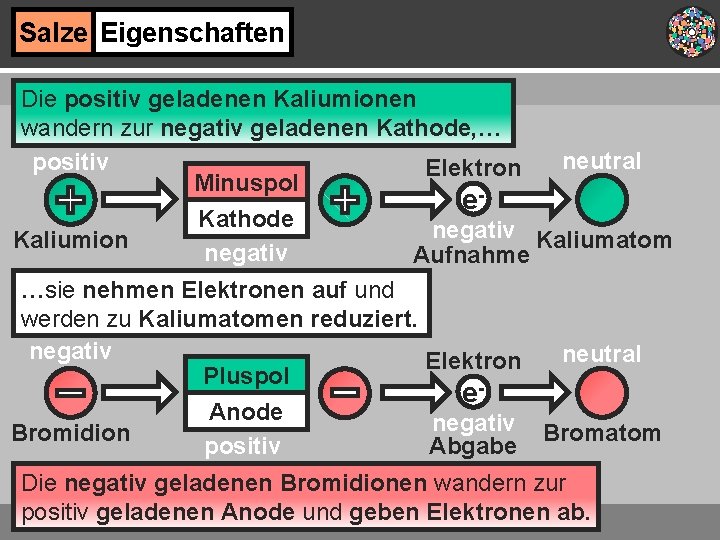
Salze Eigenschaften Die positiv geladenen Kaliumionen wandern zur negativ geladenen Kathode, … positiv Elektron Minuspol Kaliumion Kathode negativ Kaliumatom Aufnahme …sie nehmen Elektronen auf und werden zu Kaliumatomen reduziert. negativ Elektron Pluspol Bromidion Anode positiv neutral e negativ Abgabe Bromatom Die negativ geladenen Bromidionen wandern zur positiv geladenen Anode und geben Elektronen ab.
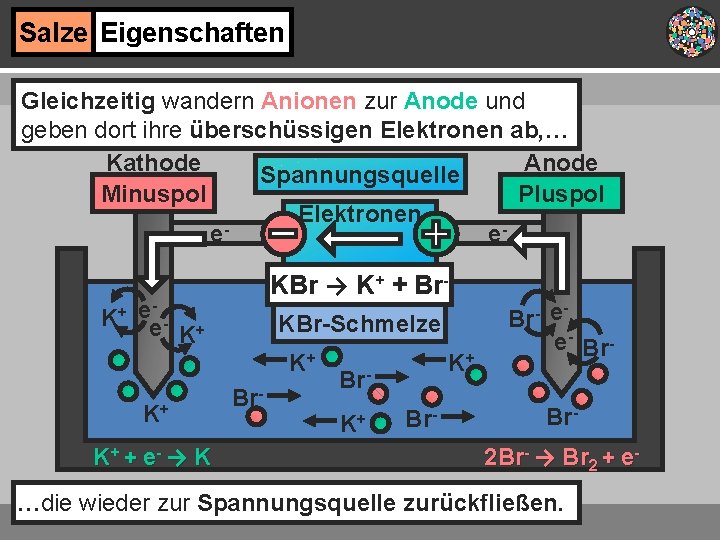
Salze Eigenschaften Gleichzeitig wandern Anionen zur Anode und geben dort ihre überschüssigen Elektronen ab, … Kathode Anode Spannungsquelle Minuspol Pluspol Elektronen e e. K+ KBr → K+ + Br- e- e K+ KBr-Schmelze K+ K+ K+ + e- → K Br- K+ Br- e e- Br 2 Br- → Br 2 + e- …die wieder zur Spannungsquelle zurückfließen.
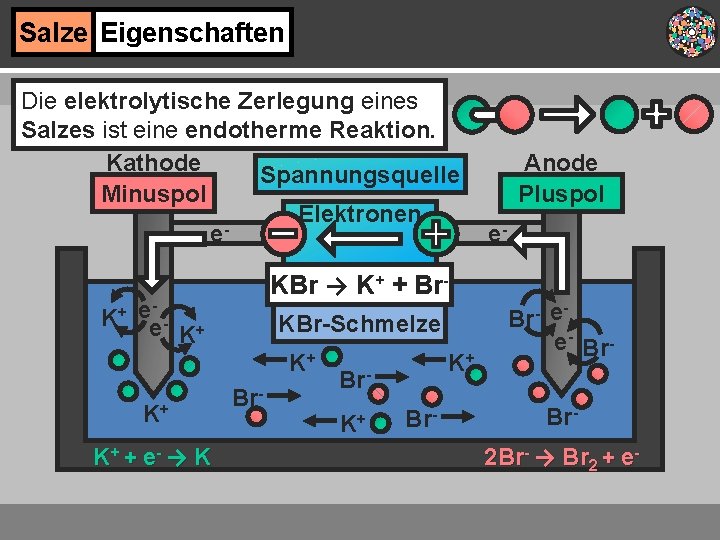
Salze Eigenschaften Die elektrolytische Zerlegung eines Salzes ist eine endotherme Reaktion. Kathode Spannungsquelle Minuspol Elektronen e K+ KBr → K+ + Br- e- e K+ KBr-Schmelze K+ K+ K+ + e- → K Br- K+ Br- Anode Pluspol e. Br- e e- Br 2 Br- → Br 2 + e-
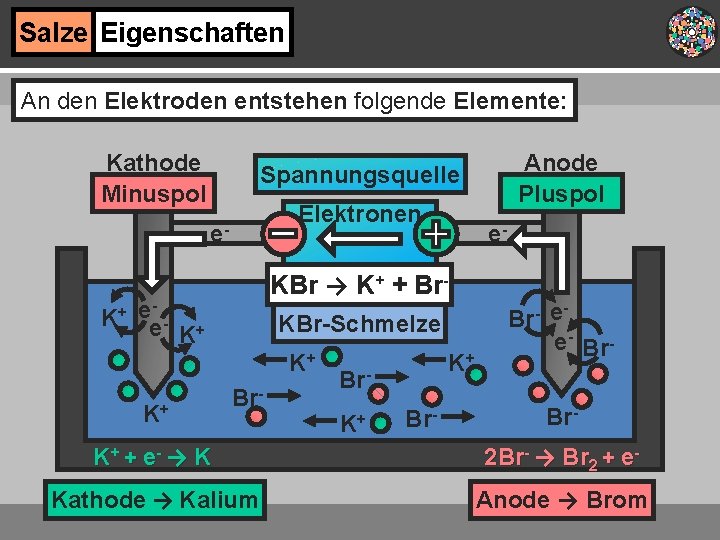
Salze Eigenschaften An den Elektroden entstehen folgende Elemente: Kathode Minuspol Elektronen e. K+ Anode Pluspol Spannungsquelle KBr → K+ + Br- e- e K+ KBr-Schmelze K+ K+ e- Br- K+ Br- e e- Br- K+ + e- → K 2 Br- → Br 2 + e- Kathode → Kalium Anode → Brom
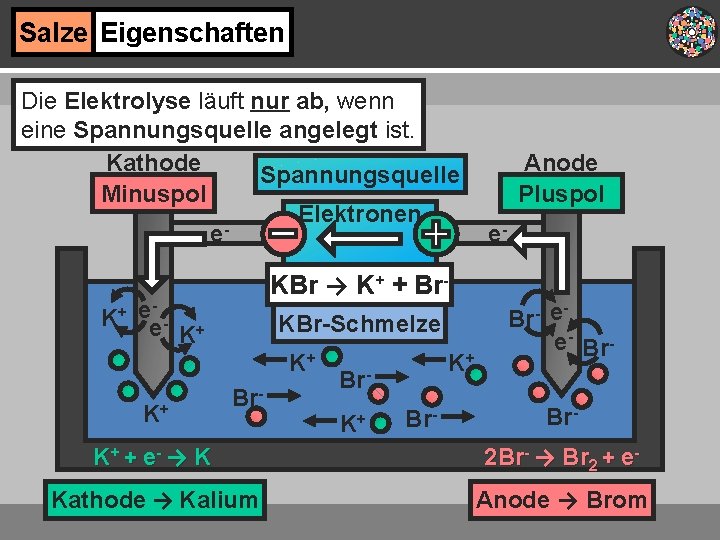
Salze Eigenschaften Die Elektrolyse läuft nur ab, wenn eine Spannungsquelle angelegt ist. Kathode Spannungsquelle Minuspol Elektronen e K+ KBr → K+ + Br- e- e K+ KBr-Schmelze K+ K+ Br- Anode Pluspol e. Br- e e- Br- K+ + e- → K 2 Br- → Br 2 + e- Kathode → Kalium Anode → Brom

Salze Eigenschaften Zusammenfassung: Salze haben den gleichen molekularen Aufbau. Salze sind bei Zimmertemperatur in der Regel fest. Zahlreiche Salze sind in Wasser löslich. In organischen Flüssigkeiten sind sie fast immer unlöslich. Salze haben hohe Schmelzpunkte. Salzschmelzen leiten den elektrischen Strom.
- Slides: 21