Sais e xidos Sais Os sais so compostos








- Slides: 11

Sais e Óxidos


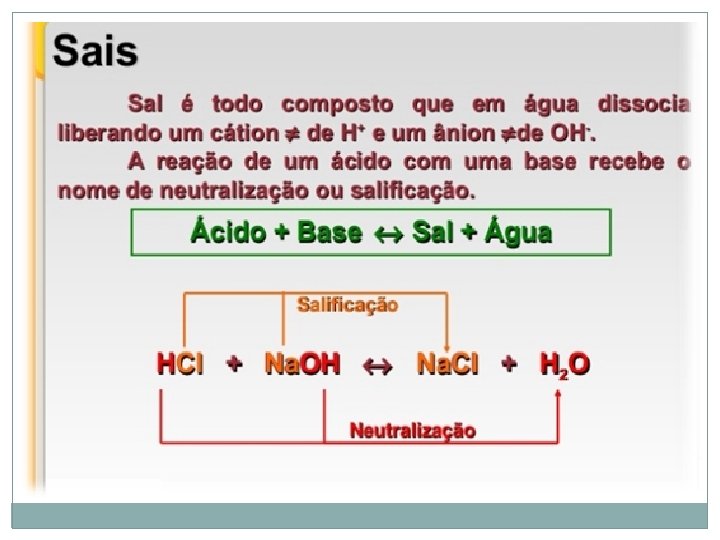
Sais Os sais são compostos iônicos. Sólidos. Características dos sais: 1 - Conduzem corrente elétrica quando estão em solução. 2 - Apresentam sabor salgado. 3 - Reagem com ácidos, com hidróxidos (bases), com outros sais e com metais.

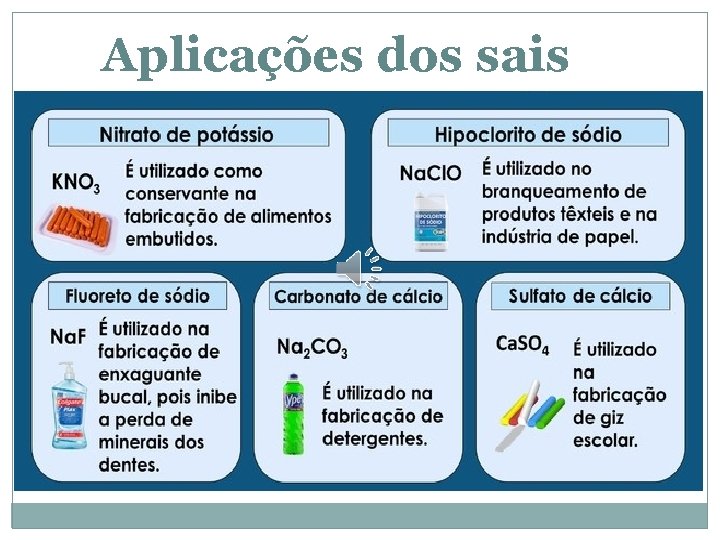
Aplicações dos sais


Óxidos São substâncias inorgânicas binárias (formada por dois elementos químicos diferentes) em que um dos elementos é o oxigênio (sigla O), e apresenta NOX igual a -2. Fórmula geral de um óxido YO Ca. O – Óxido de cálcio Ba. O – Óxido de Bário

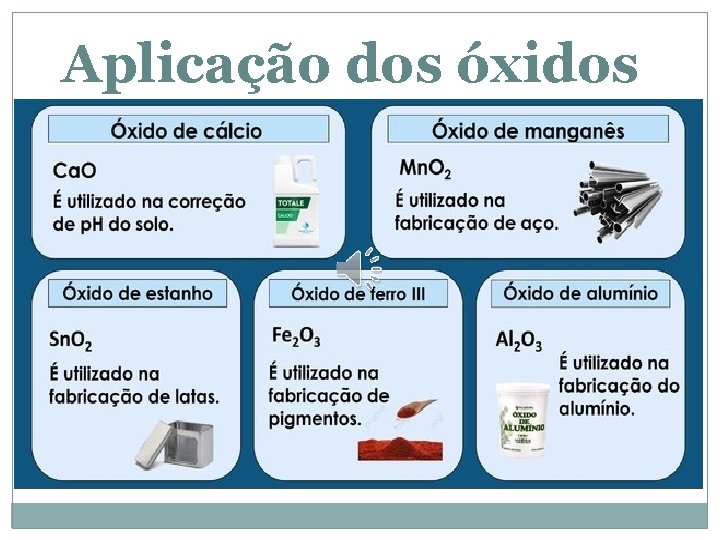
Aplicação dos óxidos


Exercícios sobre Sais e Óxidos 1. O salitre do Chile, Na. NO 3, utilizado como fertilizante, pertence à função: a) sal. b) base. c) ácido. d) óxido ácido. 2. O gás CO 2 (dióxido de carbono) se faz presente na atmosfera e é um dos responsáveis pela poluição. A cada ano pesquisas revelam um aumento na emissão desse poluente. Marque as opções que apresentam os possíveis responsáveis por essa emissão: a) Sprays aerossóis. b) Usinas nucleares. c) Hidrelétricas. d) Os veículos movidos a combustíveis fósseis (petróleo), que realizam a queima incompleta.

3. Quando o oxigênio se combina com um elemento para formar um composto binário(formada por dois elementos), onde o Oxigênio é mais eletronegativo deles(maior atração pelos elétrons da ligação) a espécie resultante é chamada de: a) ácido. b) sal. c) oxigênio molecular. d) óxido. 4. A equação abaixo representa a reação química de obtenção industrial do sulfato de sódio, utilizado na produção do papel reciclado. 2 Na. OH + H 2 SO 4 → Na 2 SO 4 + 2 H 2 O, Nessa reação: a) o H 2 SO 4 é um óxido ácido. b) o Na. OH é um hidrácido. c) o óxido de sódio é um dos reagentes. d) ocorre a formação de um sal. 5. A cal viva é um material muito usado por pedreiros, pintores e agricultores, representada pela fórmula Ca. O. Verifique essa função representada corretamente: a) Sal. b) Hidreto metálico. c) Óxido. d) Ácido.

Resposta: 1) A 2) D 3) D 4) D 5) C