Sacharidy Biochemick stav LF MU E T 2013

Sacharidy Biochemický ústav LF MU (E. T. ) 2013 1

Sacharidy (glycidy) polyhydroxykarbonylové sloučeniny (řecky ζάχαρη -sachari) = cukr uhlovodany, uhlohydráty, karbohydráty nepoužívá se!! 2

Význam: • všeobecně rozšířené látky, obsaženy ve všech buňkách • hlavní živina heterotrofů (60 % potravy člověka) - zdroj energie • zdroj uhlíku pro syntézu buněčných složek • zásoba energie v organismu (glykogen) • strukturní složka (proteoglykany pojiva, glykoproteiny membrán) • součásti signálních molekul (glykoproteiny jako receptory, antigeny) • součásti nízkomolekulárních složek buňky (nukleosidy, nukleotidy, kofaktory) • ribosa a deoxyribosa součásti nukleových kyselin 3
Glykomika, glykobiologie 4

Dělení sacharidů Monosacharidy Oligosacharidy (2 -10 mono-) Polysacharidy > 10 mono- cukr - souborné označení pro monosacharidy a oligosacharidy 5
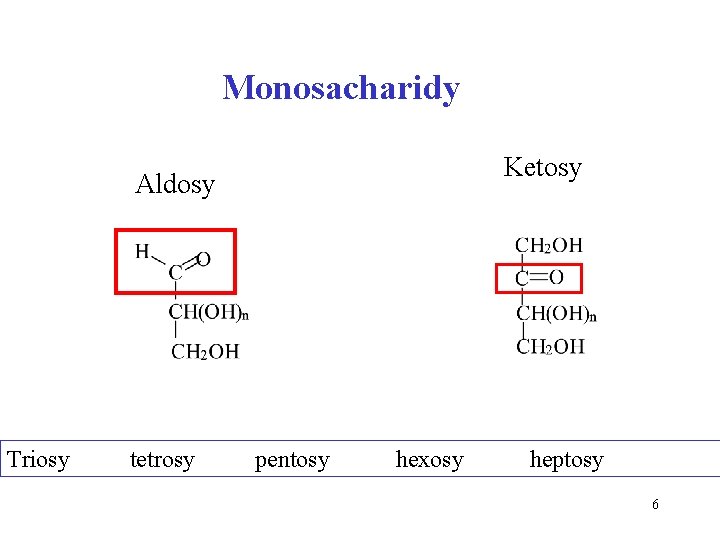
Monosacharidy Ketosy Aldosy Triosy tetrosy pentosy hexosy heptosy 6
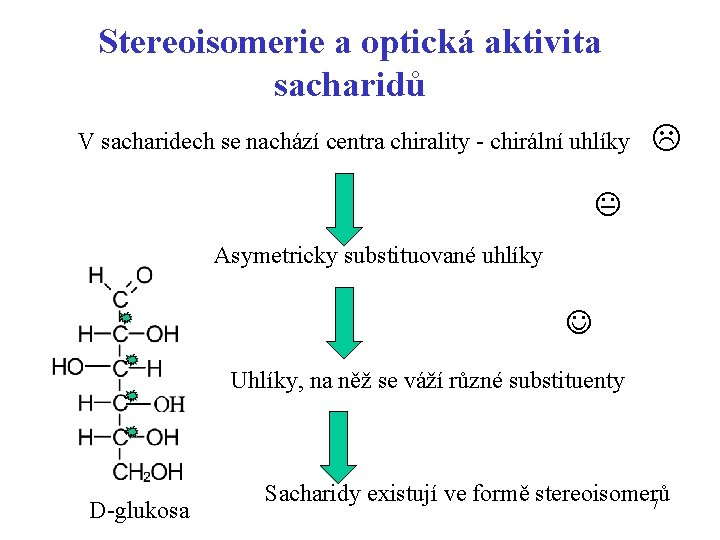
Stereoisomerie a optická aktivita sacharidů V sacharidech se nachází centra chirality - chirální uhlíky Asymetricky substituované uhlíky Uhlíky, na něž se váží různé substituenty D-glukosa Sacharidy existují ve formě stereoisomerů 7

Stereoisomery Sloučeniny, které mají stejný strukturní vzorec (konstituci), ale liší se prostorovým uspořádáním konfigurací 8

Konstituce X konfigurace nezaměňujte Konstituce popisuje druh a pořadí atomů i vazeb v molekule bez ohledu na jejich prostorové uspořádání. Konfigurace vyjadřuje prostorové uspořádání atomů bez ohledu na rotaci kolem jednoduchých vazeb. 9
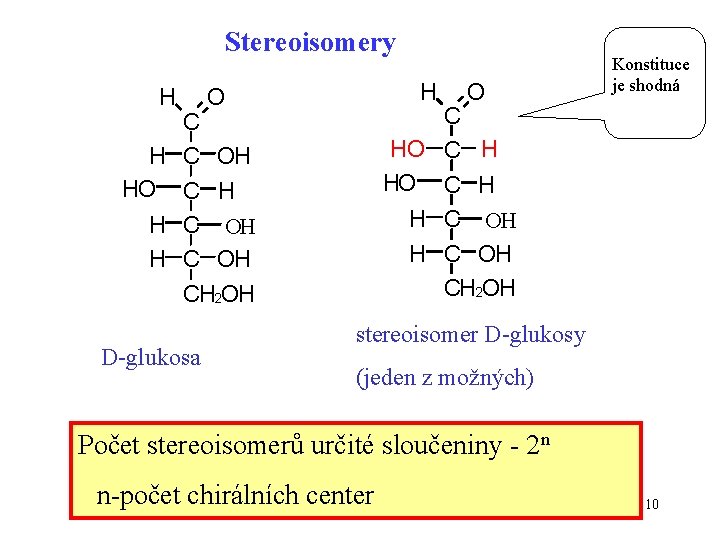
Stereoisomery H H O C H HO C H H C OH CH 2 OH C OH HO C H H C OH CH 2 OH D-glukosa O Konstituce je shodná stereoisomer D-glukosy (jeden z možných) Počet stereoisomerů určité sloučeniny - 2 n n-počet chirálních center 10

Kolik možných stereoisomerů lze odvodit od D-glukosy ? 11
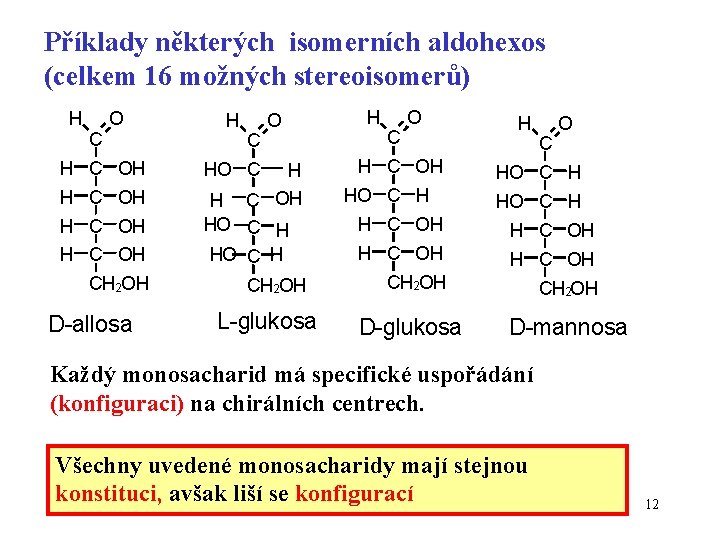
Příklady některých isomerních aldohexos (celkem 16 možných stereoisomerů) H C OH H C O HO C H C OH HO C H CH 2 OH H C OH D-allosa L-glukosa H C OH HO C H H C OH H C OH CH 2 OH D-glukosa D-mannosa Každý monosacharid má specifické uspořádání (konfiguraci) na chirálních centrech. Všechny uvedené monosacharidy mají stejnou konstituci, avšak liší se konfigurací 12
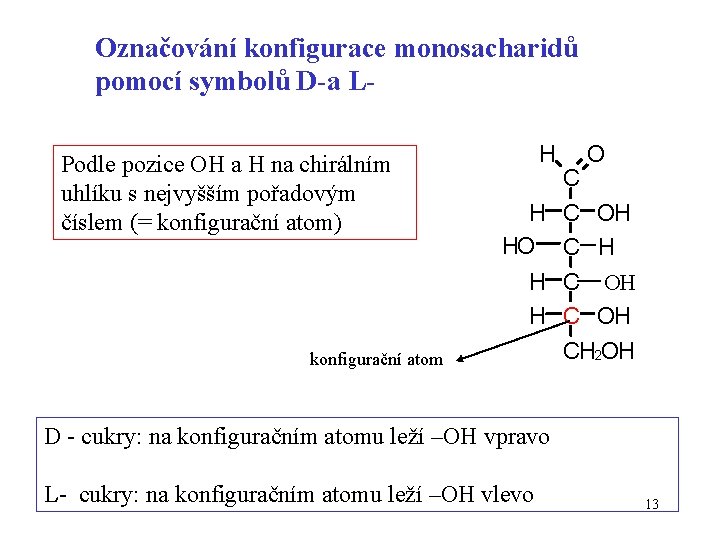
Označování konfigurace monosacharidů pomocí symbolů D-a LPodle pozice OH a H na chirálním uhlíku s nejvyšším pořadovým číslem (= konfigurační atom) konfigurační atom H O C H C OH HO C H H C OH CH 2 OH D - cukry: na konfiguračním atomu leží –OH vpravo L- cukry: na konfiguračním atomu leží –OH vlevo 13
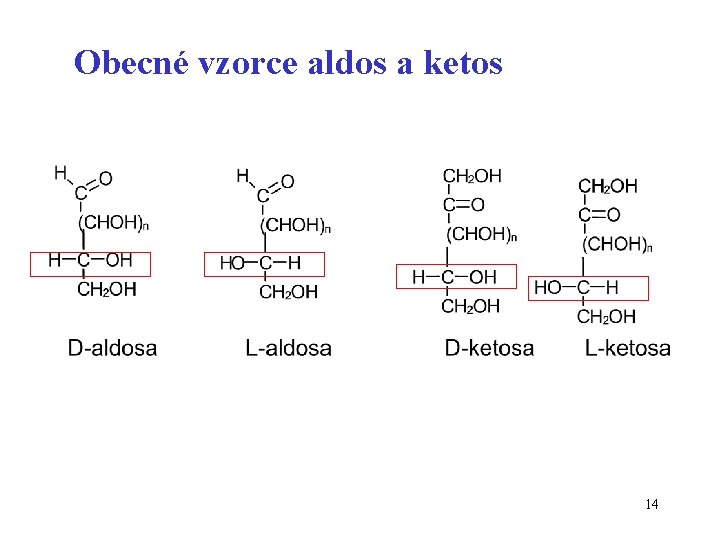
Obecné vzorce aldos a ketos 14
z označení D-, L- nelze vyvodit konfiguraci na ostatních chirálních centrech (tu si musíme pro významnější monosacharidy pamatovat) 15

Přítomnost chirálních uhlíků způsobuje optickou aktivitu sacharidů • roztoky mono- a oligosacharidů stáčejí rovinu polarisovaného světla • směr optické otáčivosti nesouvisí se symboly D- a L- , sloučenina může být D(-), D(+), L(-) nebo L(+) 16
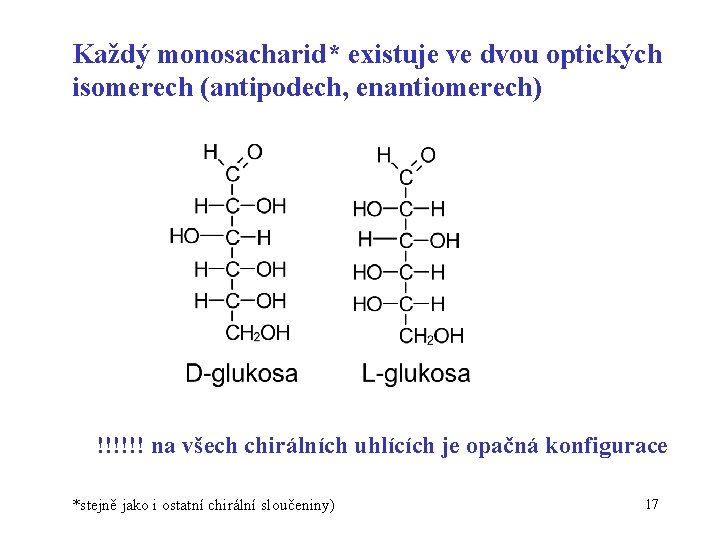
Každý monosacharid* existuje ve dvou optických isomerech (antipodech, enantiomerech) !!!!!! na všech chirálních uhlících je opačná konfigurace *stejně jako i ostatní chirální sloučeniny) 17

Optické antipody (enantiomery) specifická dvojice stereoisomerů s opačnou konfigurací na všech chirálních centrech vztah jako předmět a jeho obraz v zrcadle 18

Enantiomery • mají shodné chemické vlastnosti • liší se znaménkem optické otáčivosti • liší se biologickou a farmakologickou aktivitou Většina monosacharidů vyskytujících se u vyšších organismů má konfiguraci D. Enzymy zodpovědné za jejich metabolismus jsou specificky zaměřeny na tuto konfiguraci 19

D- a L-glukosa D-glukosa • nejběžnější monosacharid u vyšších organismů • sladká chuť • je metabolizován L-glukosa • u vyšších organismů nevzniká • vyrábí se synteticky • u vyšších organismů se neresorbuje ani nemetabolizuje • sladká chuť • byla navržena jako efektivní nízkokalorické sladidlo, avšak výrobní cena příliš vysoká 20
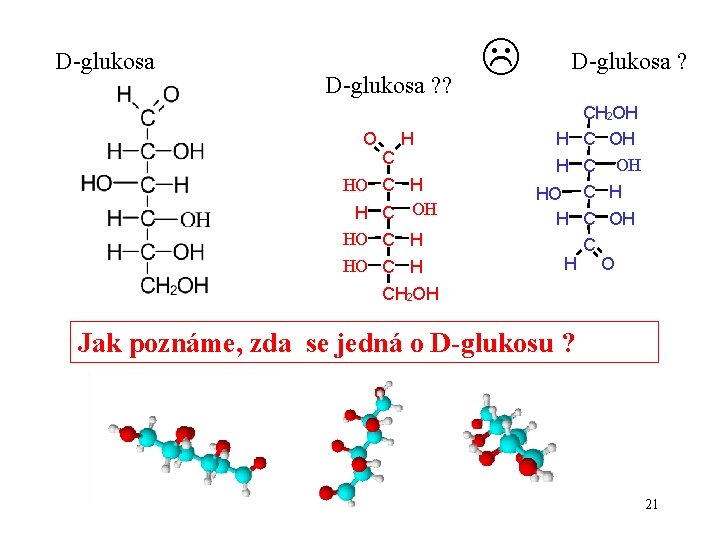
D-glukosa ? ? O C H H C OH HO C H D-glukosa ? CH 2 OH H C OH HO C H H C OH C H O CH 2 OH Jak poznáme, zda se jedná o D-glukosu ? 21

Strukturu monosacharidu musíme pozorovat a zakreslovat podle určitých dohodnutých pravidel 22
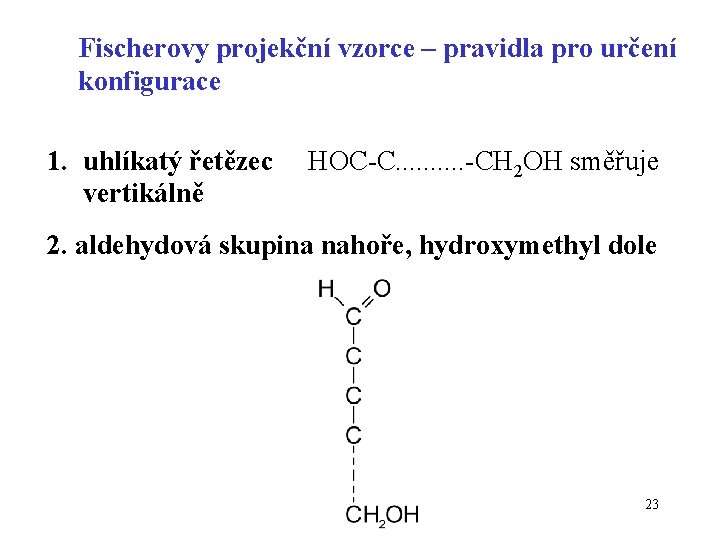
Fischerovy projekční vzorce – pravidla pro určení konfigurace 1. uhlíkatý řetězec vertikálně HOC-C. . -CH 2 OH směřuje 2. aldehydová skupina nahoře, hydroxymethyl dole 23
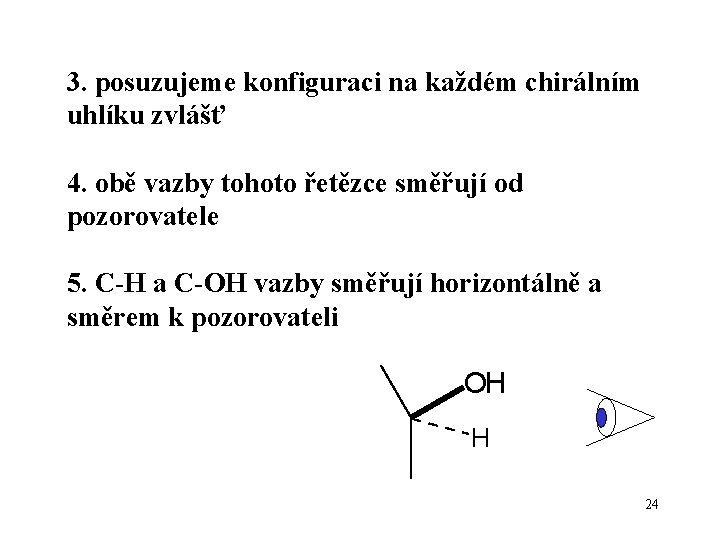
3. posuzujeme konfiguraci na každém chirálním uhlíku zvlášť 4. obě vazby tohoto řetězce směřují od pozorovatele 5. C-H a C-OH vazby směřují horizontálně a směrem k pozorovateli OH H 24
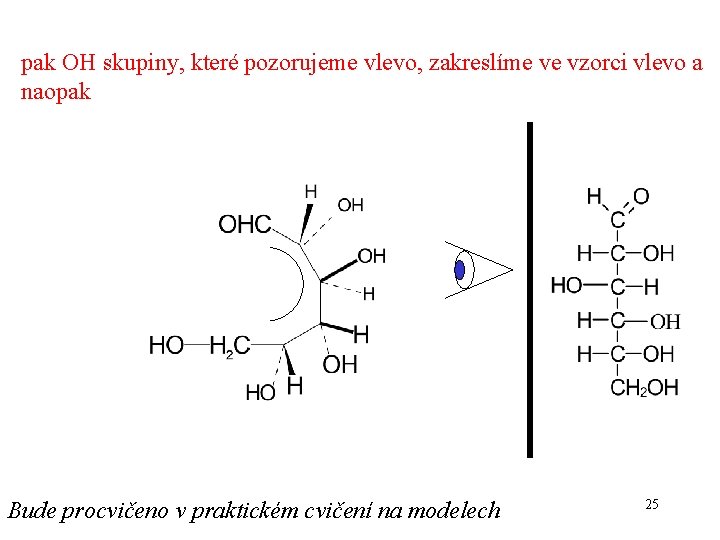
pak OH skupiny, které pozorujeme vlevo, zakreslíme ve vzorci vlevo a naopak Bude procvičeno v praktickém cvičení na modelech 25
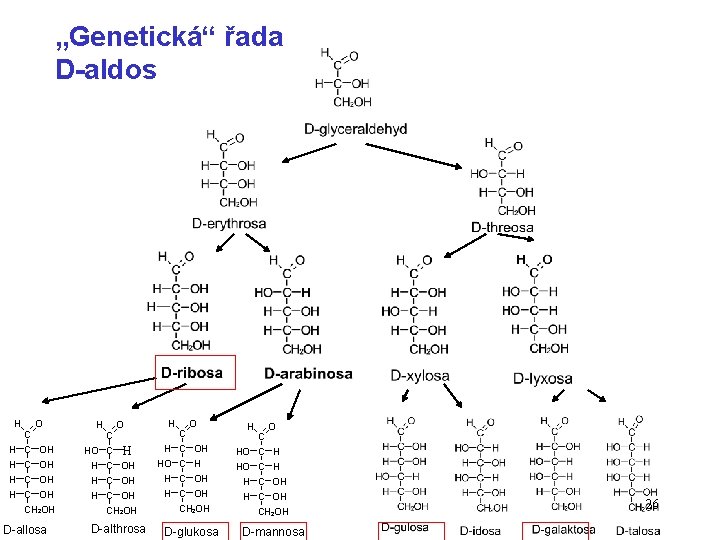
„Genetická“ řada D-aldos H O C H C OH CH 2 OH D-allosa H O C H H C OH CH 2 OH D-althrosa H H HO H H C C C O OH H OH OH CH 2 OH D-glukosa H O C H HO C H H C OH CH 2 OH D-mannosa 26
Názvosloví Triviální D-glukosa D-fruktosa Odvozeny z řečtiny nebo z latiny, odkazují na původ nebo vlastnost Systematické (složité, nepoužívá se) Glukosa 6 -(hydroxymethyl)oxan 2, 3, 4, 5 -tetrol Arabinosa – vyskytuje se v arabské gumě Glukosa – řecky glykos, glykeros = sladký Gulosa – obměna názvu glukosa Mannosa – manna (biblický pokrm židů na poušti) 27
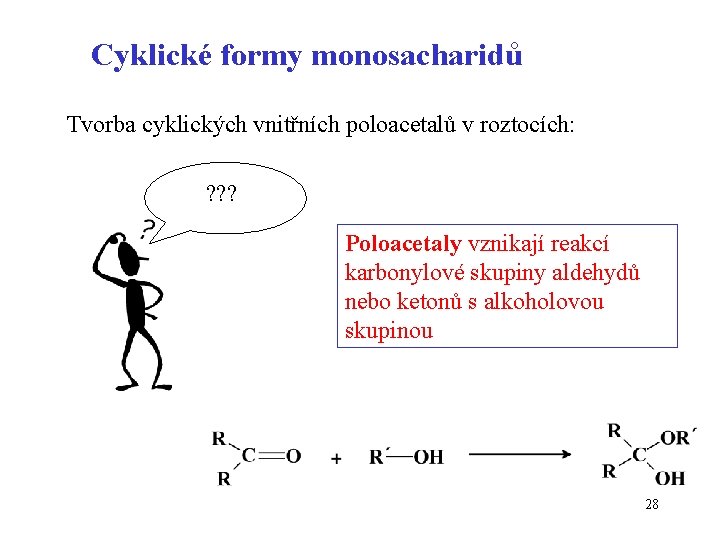
Cyklické formy monosacharidů Tvorba cyklických vnitřních poloacetalů v roztocích: ? ? ? Poloacetaly vznikají reakcí karbonylové skupiny aldehydů nebo ketonů s alkoholovou skupinou 28
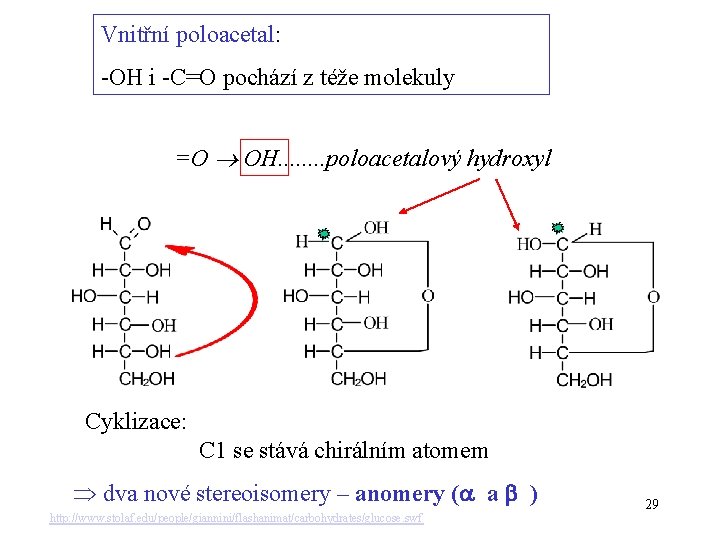
Vnitřní poloacetal: -OH i -C=O pochází z téže molekuly =O OH. . . . poloacetalový hydroxyl Cyklizace: C 1 se stává chirálním atomem dva nové stereoisomery – anomery ( a ) http: //www. stolaf. edu/people/giannini/flashanimat/carbohydrates/glucose. swf 29
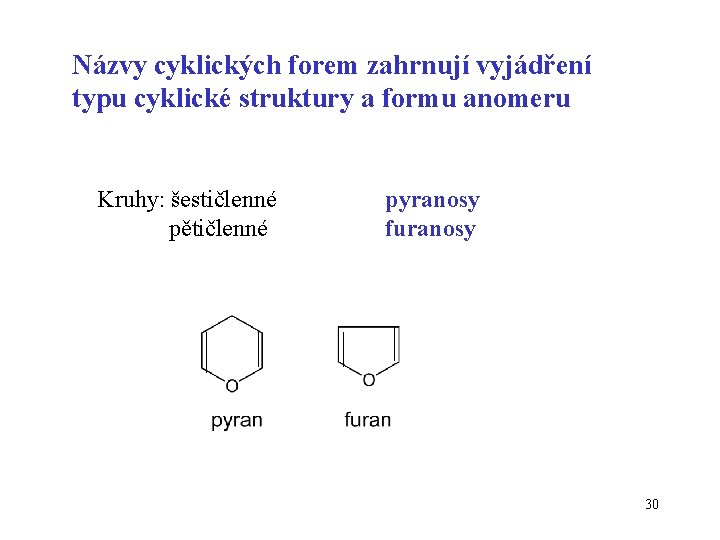
Názvy cyklických forem zahrnují vyjádření typu cyklické struktury a formu anomeru Kruhy: šestičlenné pětičlenné pyranosy furanosy 30
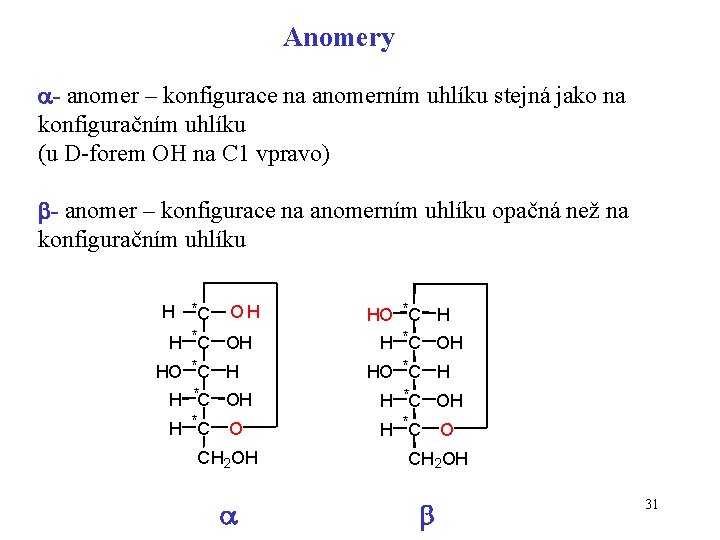
Anomery - anomer – konfigurace na anomerním uhlíku stejná jako na konfiguračním uhlíku (u D-forem OH na C 1 vpravo) - anomer – konfigurace na anomerním uhlíku opačná než na konfiguračním uhlíku H *C O H H *C OH HO *C H H *C OH H *C O CH 2 OH 31
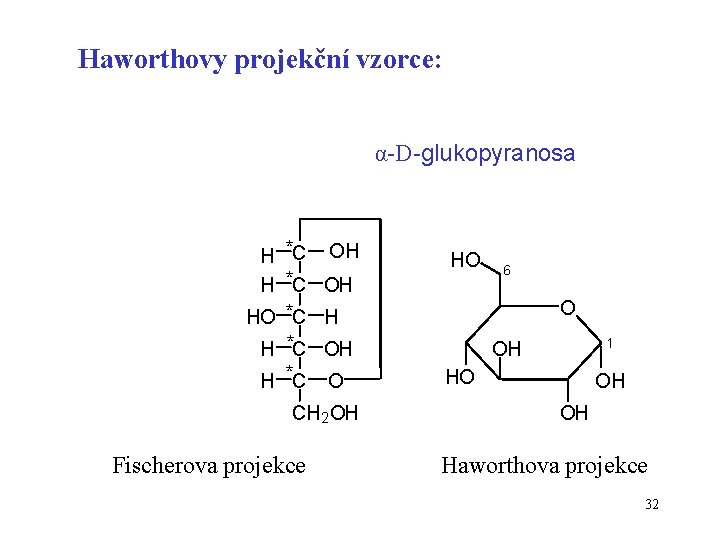
Haworthovy projekční vzorce: α-D-glukopyranosa *C OH HO *C H H *C OH H *C O CH 2 OH Fischerova projekce HO 6 O 1 OH HO OH OH Haworthova projekce 32
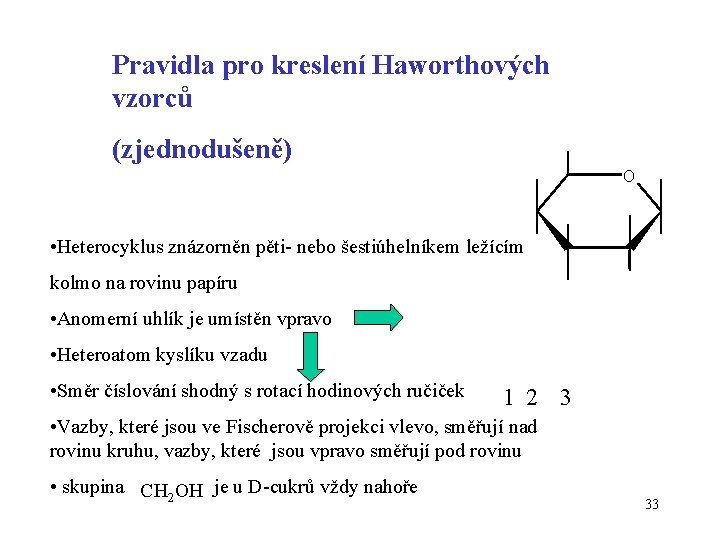
Pravidla pro kreslení Haworthových vzorců (zjednodušeně) O • Heterocyklus znázorněn pěti- nebo šestiúhelníkem ležícím kolmo na rovinu papíru • Anomerní uhlík je umístěn vpravo • Heteroatom kyslíku vzadu • Směr číslování shodný s rotací hodinových ručiček 1 2 3 • Vazby, které jsou ve Fischerově projekci vlevo, směřují nad rovinu kruhu, vazby, které jsou vpravo směřují pod rovinu • skupina CH 2 OH je u D-cukrů vždy nahoře 33
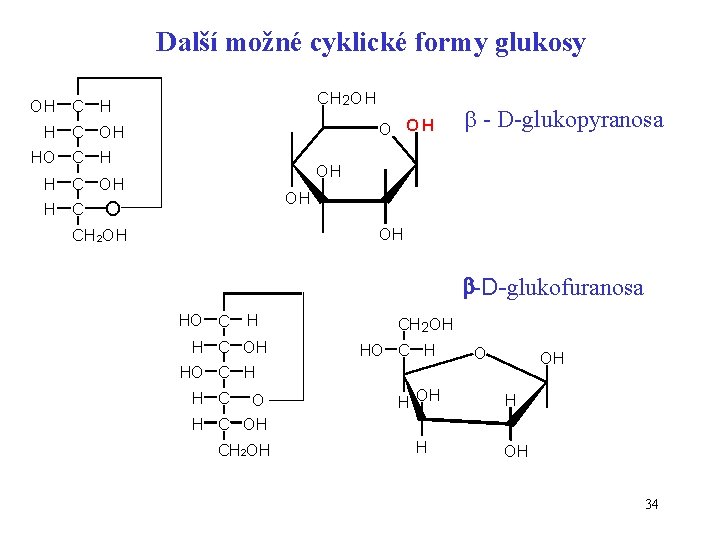
Další možné cyklické formy glukosy CH 2 OH OH C H O OH H C OH HO C H OH H C - D-glukopyranosa OH O OH CH 2 OH -D-glukofuranosa HO C H H C OH CH 2 OH HO C H O OH HO C H H C OH CH 2 OH H H OH 34

Vodný roztok D-glukosy za rovnováhy 36 % - D-glukopyranosy 62 % - D-glukopyranosy převažují cyklické formy < 0, 5 % - D-glukofuranosy < 0, 02 % aldehydové formy Krystalizace z methanolu : z octové kyseliny z vody - D-glukopyranosa monohydrát D-glukosy 35
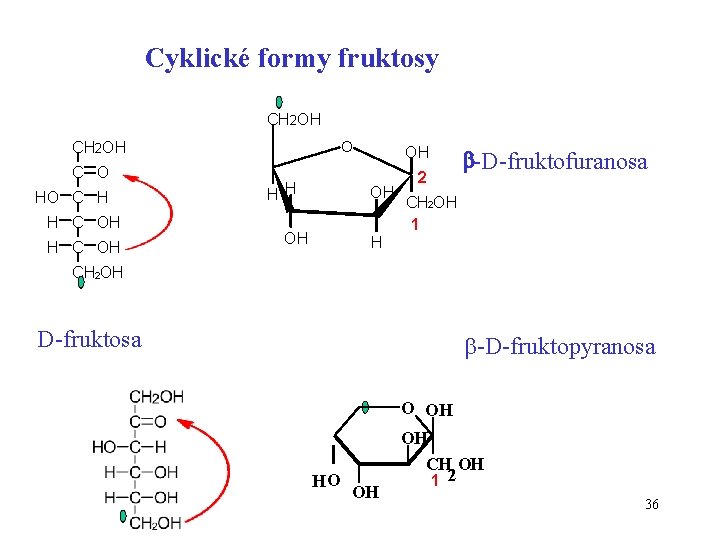
Cyklické formy fruktosy CH 2 OH C O HO C H H C OH CH 2 OH O HH OH OH -D-fruktofuranosa 2 OH CH 2 OH 1 H D-fruktosa -D-fruktopyranosa O OH HO OH OH CH OH 1 2 36

!!!!!! - a - formy (anomery) = diastereomery (ne enantiomery ! ) (odlišné fyzikální vlastnosti) 37
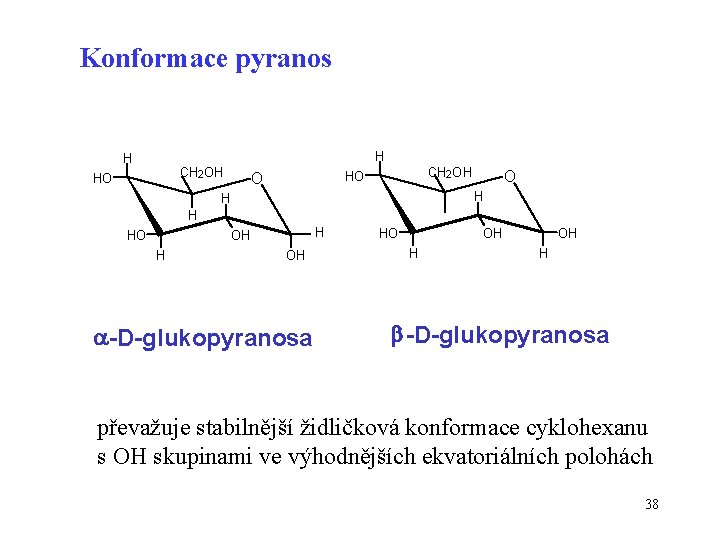
Konformace pyranos H H CH 2 OH HO O O H HO H OH -D-glukopyranosa HO OH H -D-glukopyranosa převažuje stabilnější židličková konformace cyklohexanu s OH skupinami ve výhodnějších ekvatoriálních polohách 38

Rozlišujte!!!! Optické antipody (enantiomery): D- a L-forma téhož monosacharidu, liší se konfigurací na všech centrech Diastereomery – stereoisomery, které nejsou ve vztahu optických antipodů Epimery – diastereomery lišící se konfigurací na jediném chirálním C Anomery - cyklické formy určitého monosacharidu lišící se pouze konfigurací na anomerním uhlíku, jsou diastereomery 39
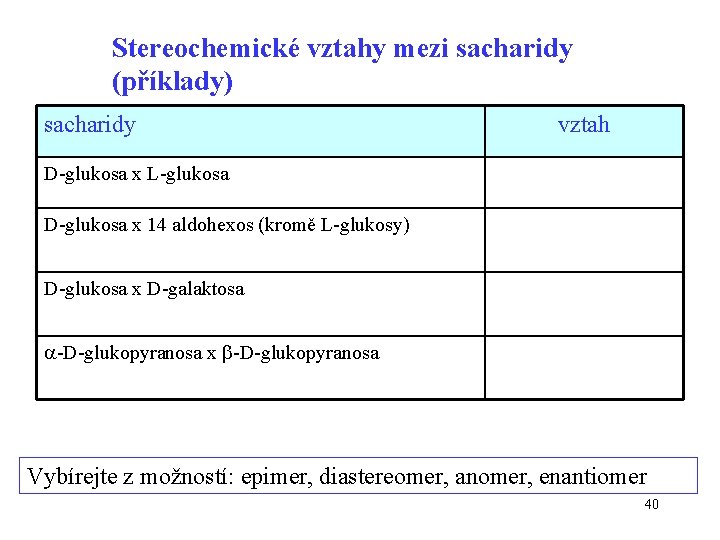
Stereochemické vztahy mezi sacharidy (příklady) sacharidy vztah D-glukosa x L-glukosa D-glukosa x 14 aldohexos (kromě L-glukosy) D-glukosa x D-galaktosa -D-glukopyranosa x -D-glukopyranosa Vybírejte z možností: epimer, diastereomer, anomer, enantiomer 40

Typické vlastnosti monosacharidů • polární • dobře rozpustné ve vodě • neelektrolyty • sladké Proč jsou monosacharidy rozpustné ve vodě? Proč jsou neelektrolyty? 41
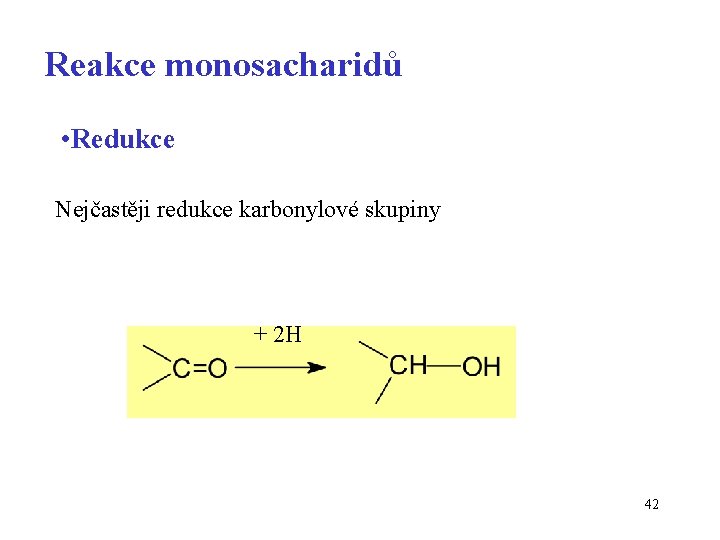
Reakce monosacharidů • Redukce Nejčastěji redukce karbonylové skupiny + 2 H 42
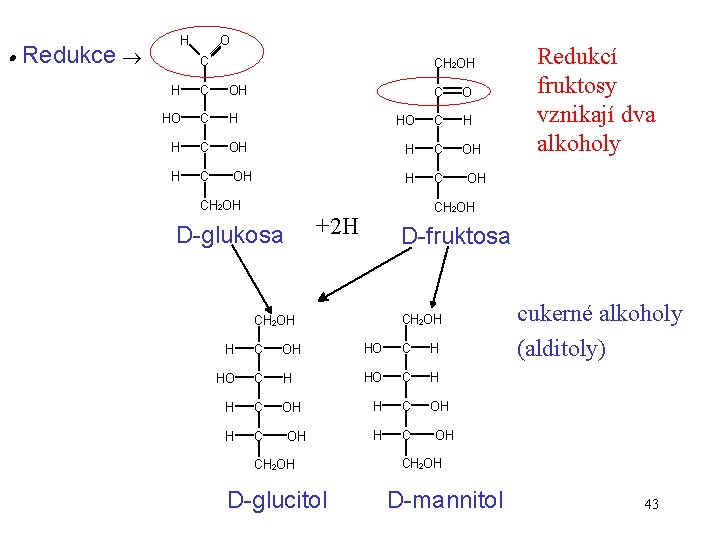
Redukce H O C CH 2 OH H C OH HO C H H C OH C O HO C H H C OH H C CH 2 OH D-fruktosa CH 2 OH H C OH HO C H H C OH CH 2 OH D-glucitol OH CH 2 OH +2 H D-glukosa Redukcí fruktosy vznikají dva alkoholy cukerné alkoholy (alditoly) OH CH 2 OH D-mannitol 43

Glucitol (sorbitol), xylitol, mannitol, galaktitol • umělá sladidla Sladká chuť – specifická reakce s chuťovými receptory (3 receptory pro sladké sloučeniny) • mají nižší energetickou hodnotu než sacharosa, ale stejný objem (tzv. „objemná sladidla“) Jiná sladidla • acesulfam K. , aspartam, cyklamáty, sacharin, thaumatin, neohesperidin DC Jsou to tzv. „intenzivní sladidla“ (vysoká sladivost, nulová energetická hodnota, používají se v nepatrných množstvích ) 44
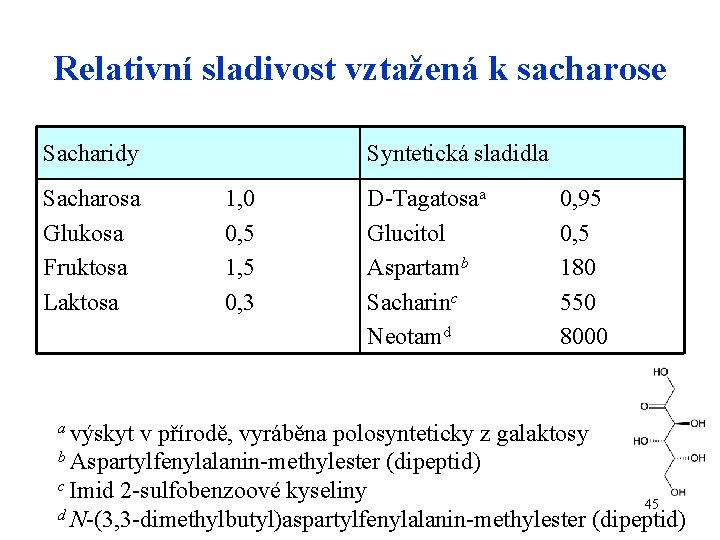
Relativní sladivost vztažená k sacharose Sacharidy Sacharosa Glukosa Fruktosa Laktosa a výskyt Syntetická sladidla 1, 0 0, 5 1, 5 0, 3 D-Tagatosaa Glucitol Aspartamb Sacharinc Neotamd 0, 95 0, 5 180 550 8000 v přírodě, vyráběna polosynteticky z galaktosy b Aspartylfenylalanin-methylester (dipeptid) c Imid 2 -sulfobenzoové kyseliny 45 d N-(3, 3 -dimethylbutyl)aspartylfenylalanin-methylester (dipeptid)

Polyolová metabolická dráha - přeměna glukosy na glucitol v některých buňkách NADPH + D-glukosa H+ NADP+ D-glucitol aldosareduktasa Při vysoké hladině glukosy v krvi proniká do některých buněk více glukosy a vzniká i větší množství D-glucitolu. Ten nemůže přecházet zpět a hromadí se (retina, čočka, nervová b. ) Zvýšený osmotický tlak vyvolává poruchy buněk (diabetická katarakta, retinopatie, neuropatie) 46
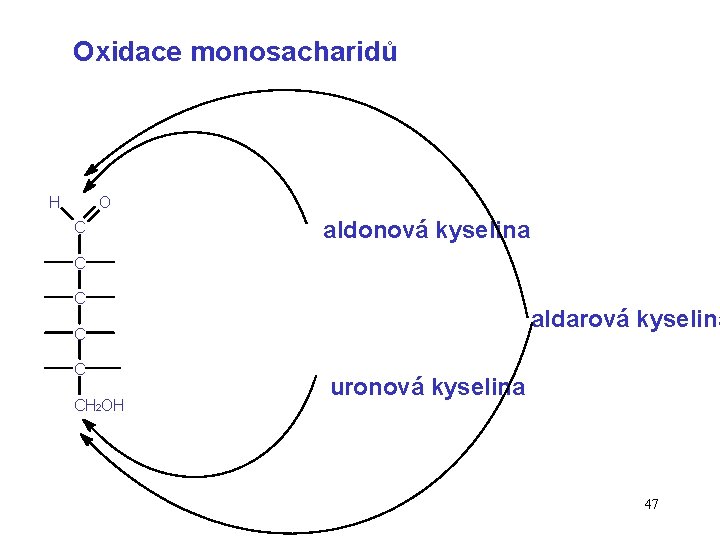
Oxidace monosacharidů H O C aldonová kyselina C C aldarová kyselina C C CH 2 OH uronová kyselina 47
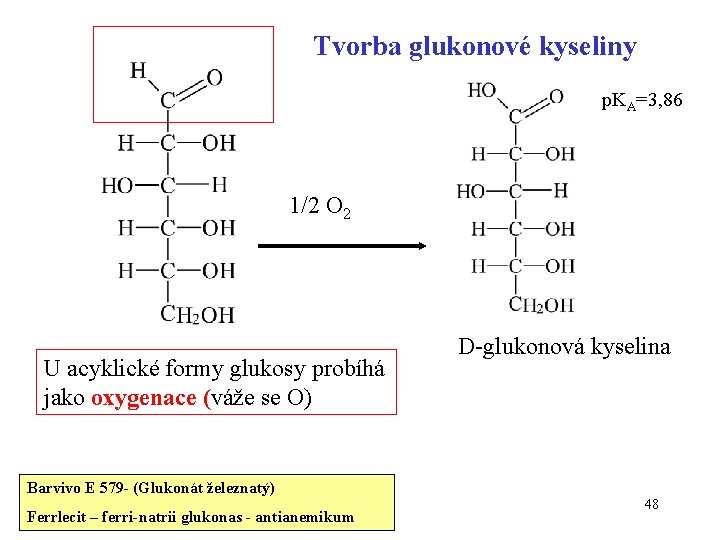
Tvorba glukonové kyseliny p. KA=3, 86 1/2 O 2 U acyklické formy glukosy probíhá jako oxygenace (váže se O) D-glukonová kyselina Barvivo E 579 - (Glukonát železnatý) Ferrlecit – ferri-natrii glukonas - antianemikum 48
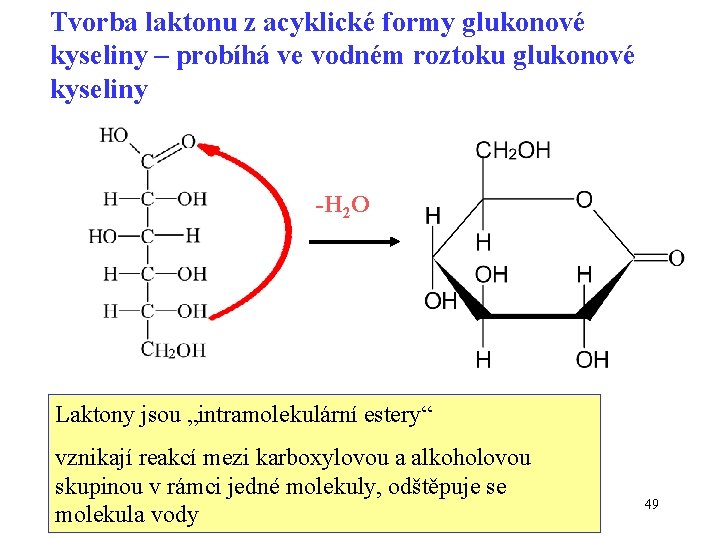
Tvorba laktonu z acyklické formy glukonové kyseliny – probíhá ve vodném roztoku glukonové kyseliny -H 2 O Laktony jsou „intramolekulární estery“ vznikají reakcí mezi karboxylovou a alkoholovou skupinou v rámci jedné molekuly, odštěpuje se molekula vody 49

Lakton x poloacetal Srovnejte : - tvorba poloacetalu: adice, voda se neodštěpuje - tvorba laktonu: kondenzace, odštěpuje se voda 50
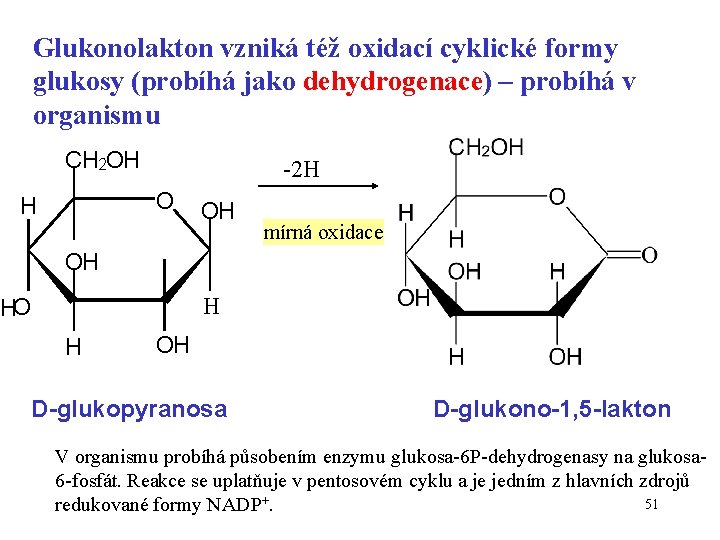
Glukonolakton vzniká též oxidací cyklické formy glukosy (probíhá jako dehydrogenace) – probíhá v organismu CH 2 OH -2 H O H OH mírná oxidace OH H HO H OH D-glukopyranosa D-glukono-1, 5 -lakton V organismu probíhá působením enzymu glukosa-6 P-dehydrogenasy na glukosa 6 -fosfát. Reakce se uplatňuje v pentosovém cyklu a je jedním z hlavních zdrojů 51 redukované formy NADP+.
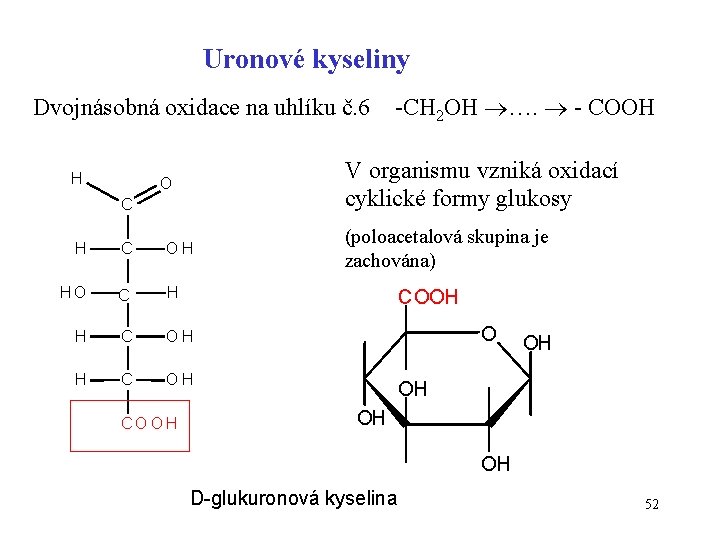
Uronové kyseliny Dvojnásobná oxidace na uhlíku č. 6 H V organismu vzniká oxidací cyklické formy glukosy O C H C OH HO C H H C OH COOH -CH 2 OH …. - COOH (poloacetalová skupina je zachována) COOH OH D-glukuronová kyselina 52

„Redukující cukry“ snadná oxidace aldehydové nebo poloacetalové skupiny pozitivní reakce s Fehlingovým nebo Benediktovým činidlem /redukce Cu 2+(modrá) na Cu 2 O (oranžová)/ využívá se k důkazům cukrů + všechny monosacharidy a disacharidy s volnou poloacetalovou skupinou Benediktovo činidlo se připravuje smícháním roztoků síranu měďnatého (skalice modrá), citronanu sodného a uhličitanu sodného. Citronan sodný má za úkol zabránit po smíchání vzniku sraženiny uhličitanu měďnatého. Měďnaté kationty se v alkalickém prostředí redukují na měďné. 53
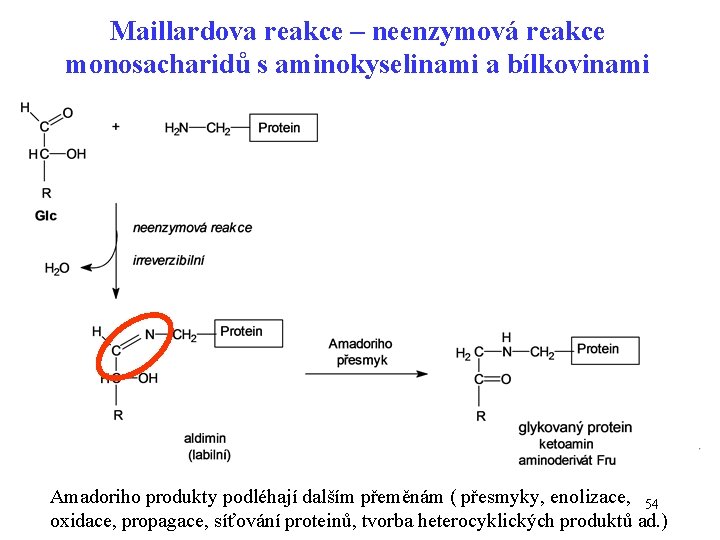
Maillardova reakce – neenzymová reakce monosacharidů s aminokyselinami a bílkovinami Amadoriho produkty podléhají dalším přeměnám ( přesmyky, enolizace, 54 oxidace, propagace, síťování proteinů, tvorba heterocyklických produktů ad. )

Význam Maillardovy reakce • Poprvé popsána Maillardem (1912) – hnědnutí bílkovin při zahřívání s cukry • Probíhá v živých organismech – reakce glukosy s bílkovinami. Zvýšená tvorba produktů glykace nastává při diabetu. Vede k poškození bílkovin (advanced glycation endproducts AGE) • V potravinách – vyvolává zhnědnutí při pečení a smažení (reakce neenzymového zhnědnutí). Vyvolá žádoucí změny v chuti, barvě a vůni, ale i nežádoucí snížení nutriční hodnoty a tvorbu toxických a mutagenních látek • Stanovení glykovaného hemoglobinu u diabetiků - slouží k zjištění glykemického profilu během cca 2 měsíců 55
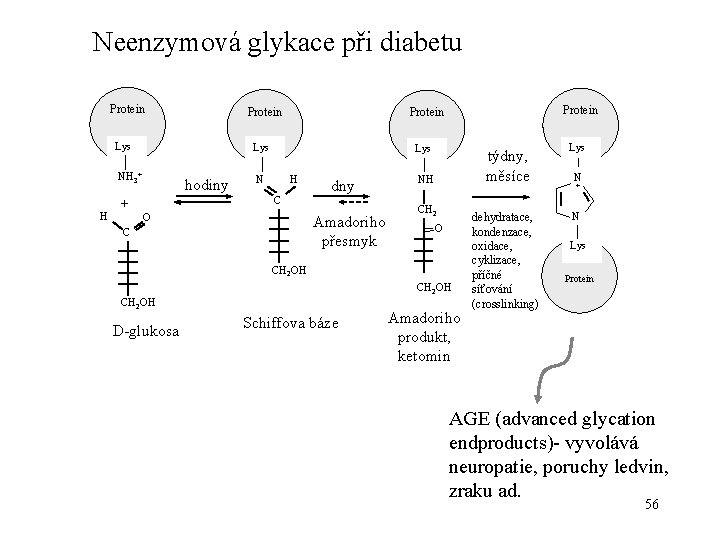
Neenzymová glykace při diabetu Protein Lys NH 3+ hodiny H Lys N H C + Protein O dny Amadoriho přesmyk C týdny, měsíce NH CH 2 O CH 2 OH D-glukosa Schiffova báze Amadoriho produkt, ketomin dehydratace, kondenzace, oxidace, cyklizace, příčné síťování (crosslinking) Lys N + N Lys Protein AGE (advanced glycation endproducts)- vyvolává neuropatie, poruchy ledvin, zraku ad. 56
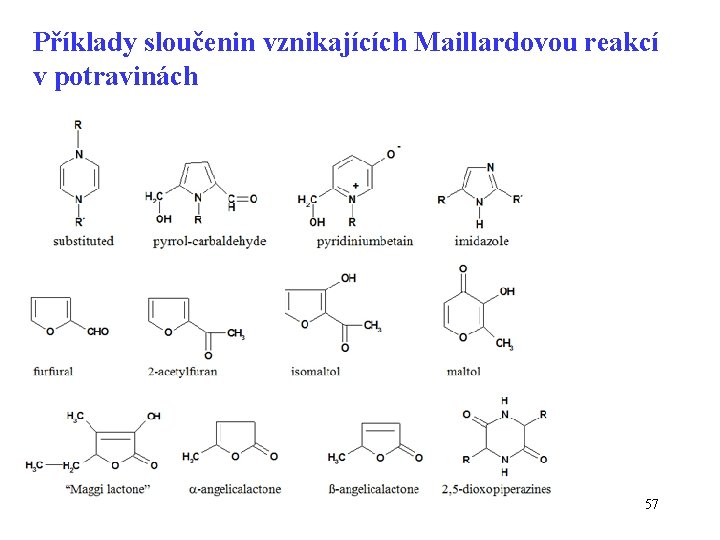
Příklady sloučenin vznikajících Maillardovou reakcí v potravinách 57
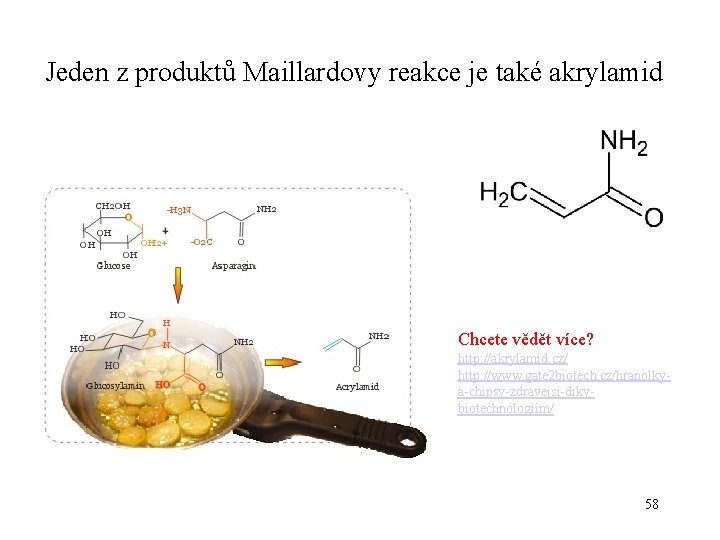
Jeden z produktů Maillardovy reakce je také akrylamid Chcete vědět více? http: //akrylamid. cz/ http: //www. gate 2 biotech. cz/hranolkya-chipsy-zdravejsi-dikybiotechnologiim/ 58

Významné monosacharidy 59

D – Glukosa • nejrozšířenější v přírodě „hroznový cukr“ stavební jednotka škrobu, glykogenu, celulosy • koncentrace v krvi 3, 3 -5, 5 mmol/l je velmi striktně regulována CH 2 OH OH 60
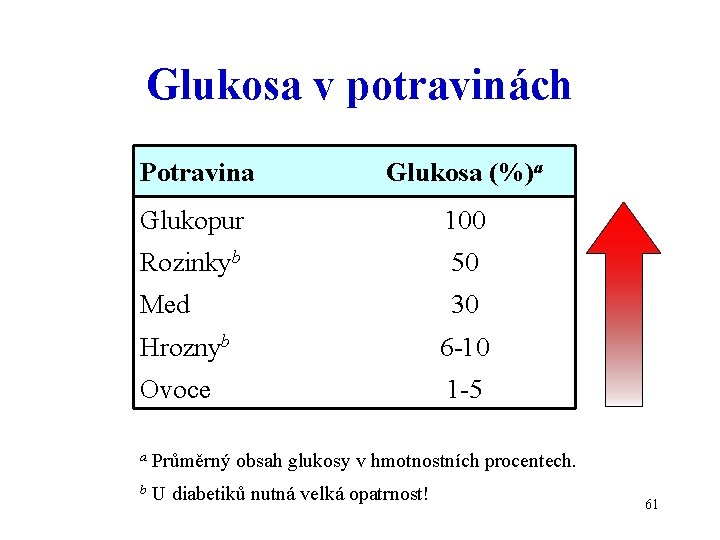
Glukosa v potravinách Potravina Glukosa (%)a Glukopur 100 Rozinkyb 50 Med 30 Hroznyb 6 -10 Ovoce 1 -5 a Průměrný obsah glukosy v hmotnostních procentech. b U diabetiků nutná velká opatrnost! 61
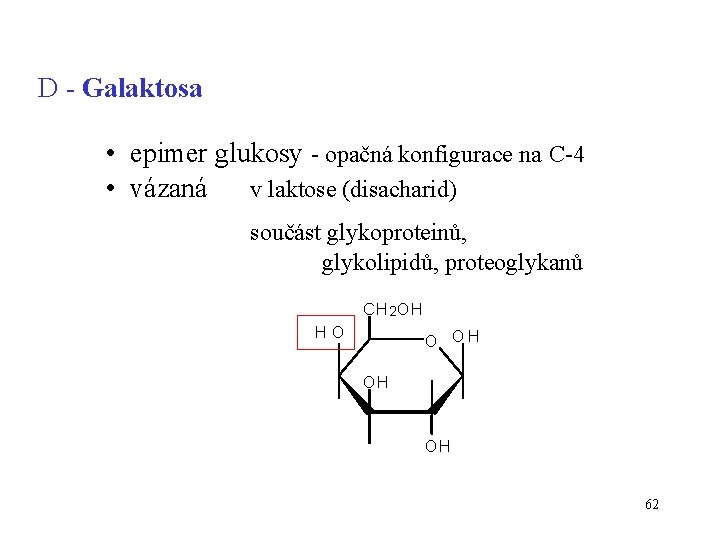
D - Galaktosa • epimer glukosy - opačná konfigurace na C-4 • vázaná v laktose (disacharid) součást glykoproteinů, glykolipidů, proteoglykanů CH 2 OH HO O OH OH OH 62
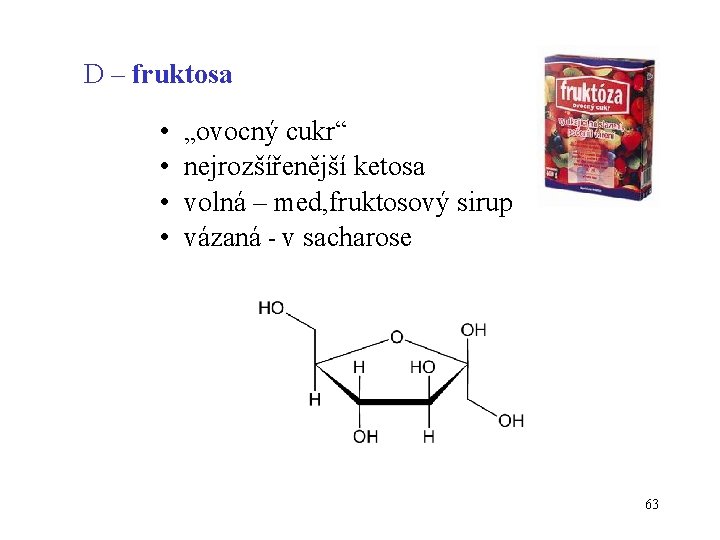
D – fruktosa • • „ovocný cukr“ nejrozšířenější ketosa volná – med, fruktosový sirup vázaná - v sacharose 63
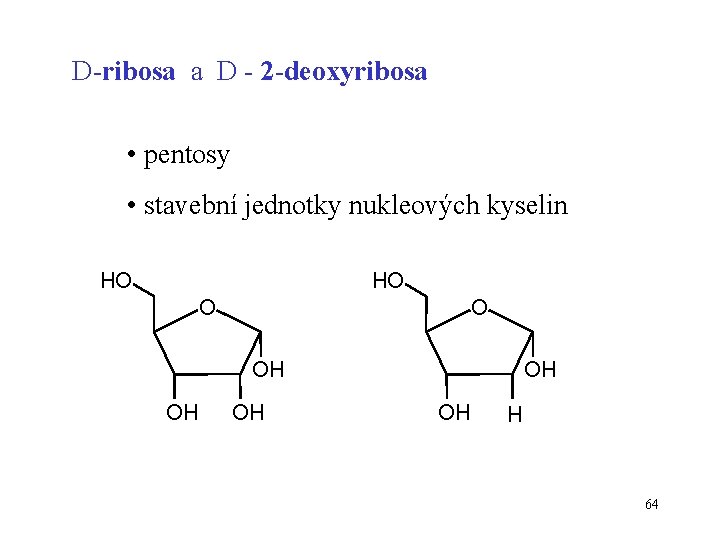
D-ribosa a D - 2 -deoxyribosa • pentosy • stavební jednotky nukleových kyselin HO HO O O OH OH OH H 64
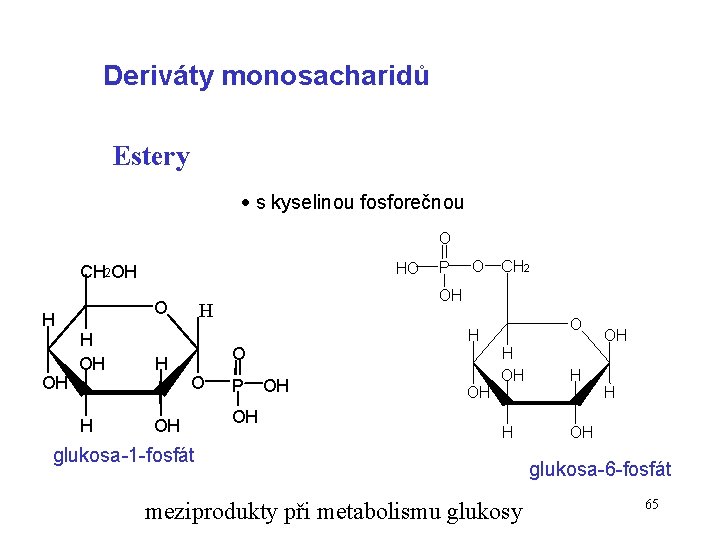
Deriváty monosacharidů Estery s kyselinou fosforečnou O HO CH 2 OH H OH O H OH H O OH O CH 2 OH H O P P OH OH OH O H OH H H OH glukosa-1 -fosfát meziprodukty při metabolismu glukosy OH H glukosa-6 -fosfát 65
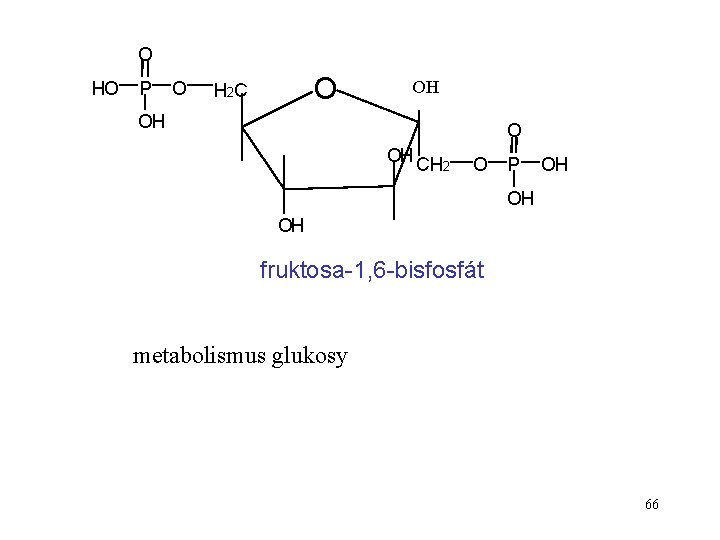
O HO P O O H 2 C OH OH O OH CH 2 O P OH OH OH fruktosa-1, 6 -bisfosfát metabolismus glukosy 66
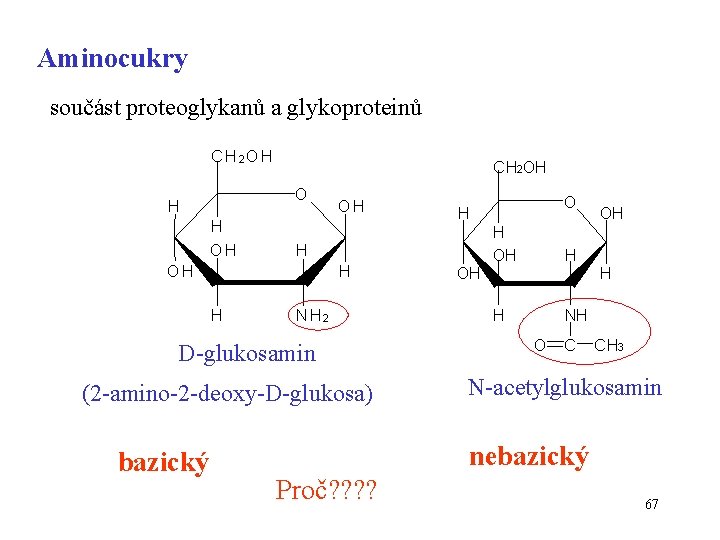
Aminocukry součást proteoglykanů a glykoproteinů C H 2 OH CH 2 OH O H H OH OH H H NH 2 D-glukosamin (2 -amino-2 -deoxy-D-glukosa) bazický H OH O H OH H H NH O C OH H CH 3 N-acetylglukosamin nebazický Proč? ? 67
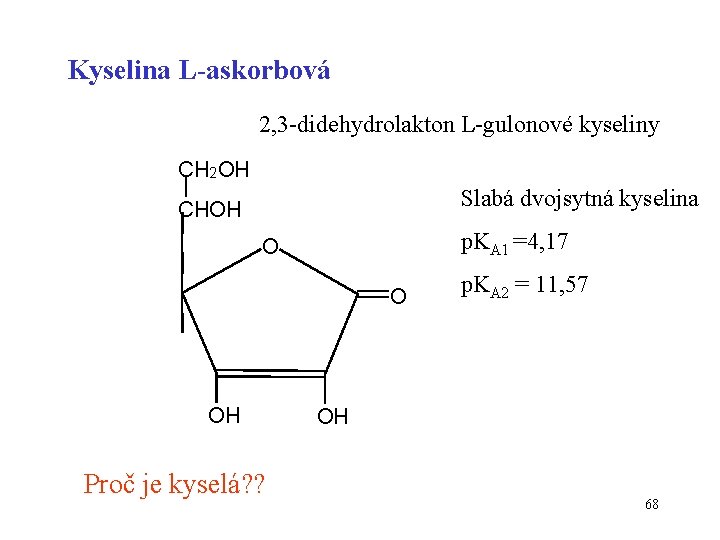
Kyselina L-askorbová 2, 3 -didehydrolakton L-gulonové kyseliny CH 2 OH Slabá dvojsytná kyselina CHOH p. KA 1 =4, 17 O O OH Proč je kyselá? ? p. KA 2 = 11, 57 OH 68
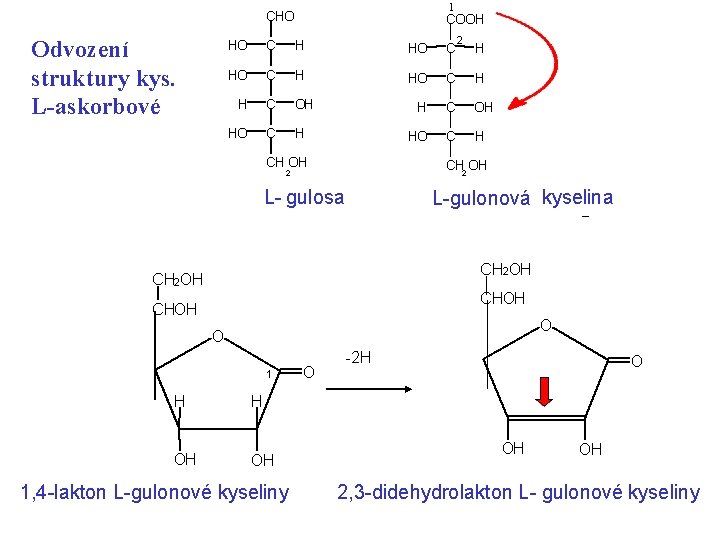
1 CHO Odvození struktury kys. L-askorbové COOH 2 HO C H H C OH HO C H CH OH H CH 2 OH 2 L- gulosa L-gulonová kyselina CH 2 OH CHOH O O 1 H H OH OH 1, 4 -lakton L-gulonové kyseliny O -2 H O OH OH 2, 3 -didehydrolakton L- gulonové kyseliny 69
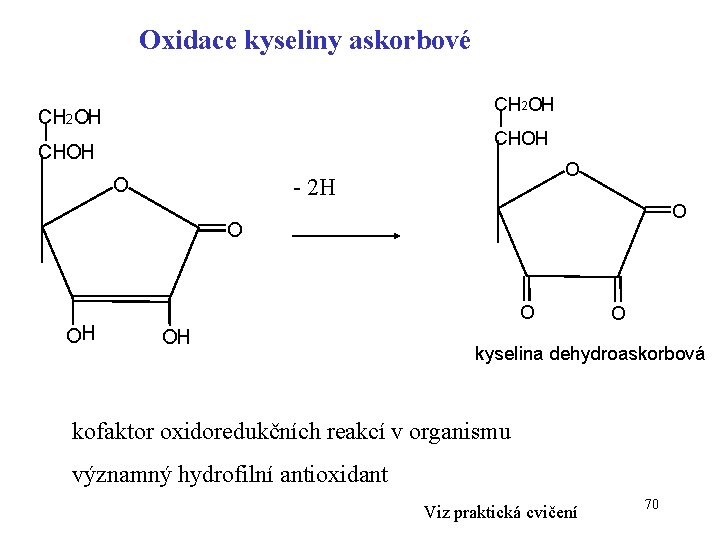
Oxidace kyseliny askorbové CH 2 OH CHOH O - 2 H O OH O kyselina dehydroaskorbová kofaktor oxidoredukčních reakcí v organismu významný hydrofilní antioxidant Viz praktická cvičení 70
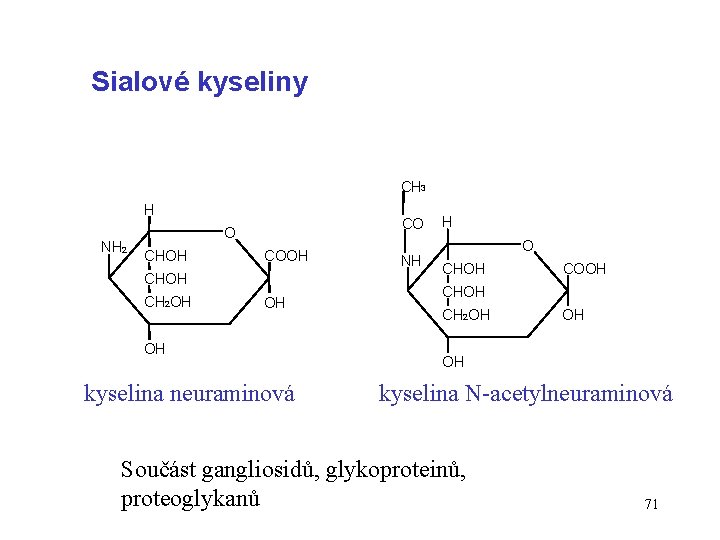
Sialové kyseliny CH 3 H NH 2 CO O CHOH COOH CH 2 OH OH OH kyselina neuraminová NH H O CHOH COOH CH 2 OH OH OH kyselina N-acetylneuraminová Součást gangliosidů, glykoproteinů, proteoglykanů 71
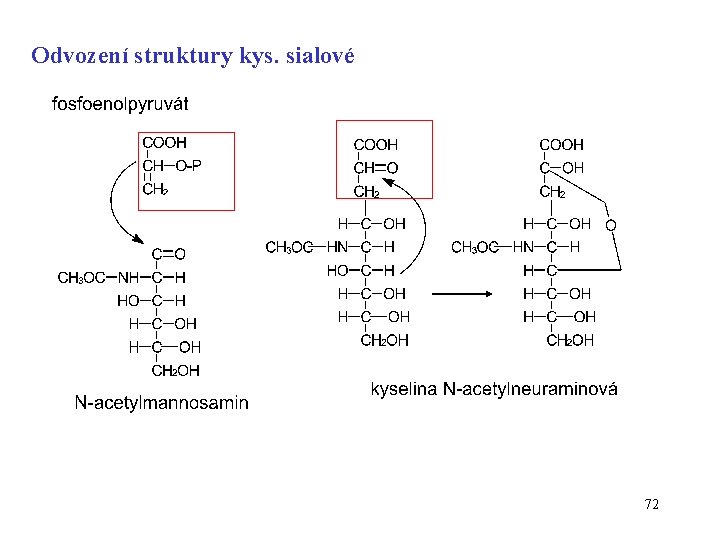
Odvození struktury kys. sialové 72
Glykosidy Deriváty cyklických forem cukrů vznikající reakcí poloacetalového hydroxylu sacharidu : S alkoholovým nebo fenolovým hydroxylem jiné látky O-glykosidy S NH- skupinou jiné látky N-glykosidy 73
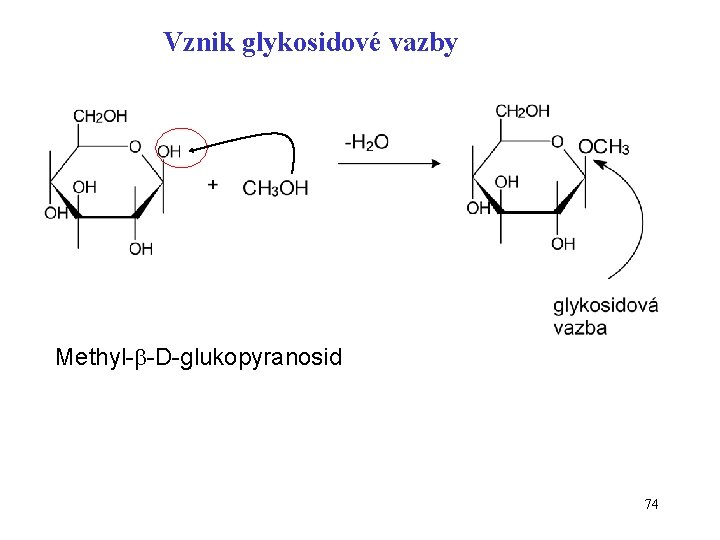
Vznik glykosidové vazby Methyl- -D-glukopyranosid 74
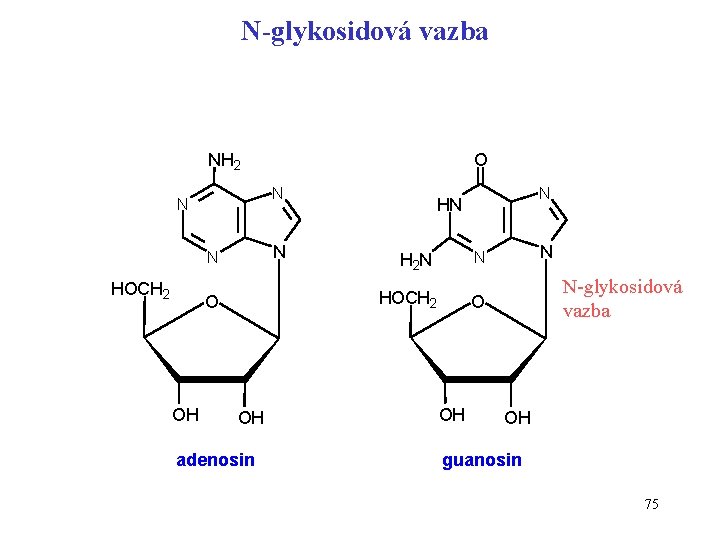
N-glykosidová vazba NH 2 N N HOCH 2 OH adenosin N HN N N H 2 N HOCH 2 O OH O N-glykosidová vazba O OH OH guanosin 75

Názvosloví glykosidů odvozeno od názvu monosacharidu -glukosid, galaktosid, …………. zahrnuje typ anomeru: - D-glukosid - D-galaktosid 76

Typy glykosidů Hologlykosidy Heteroglykosidy vzájemná vazba monosacharidů glykosidovou vazbou Cukerná složka (glykon) + necukerná složka (aglykon) oligosacharidy, polysacharidy Velmi rozšířené v přírodě 77
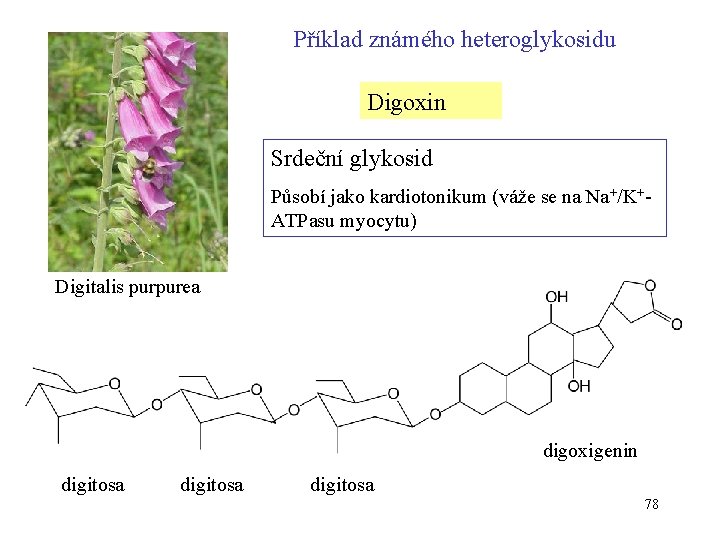
Příklad známého heteroglykosidu Digoxin Srdeční glykosid Působí jako kardiotonikum (váže se na Na+/K+ATPasu myocytu) Digitalis purpurea digoxigenin digitosa 78
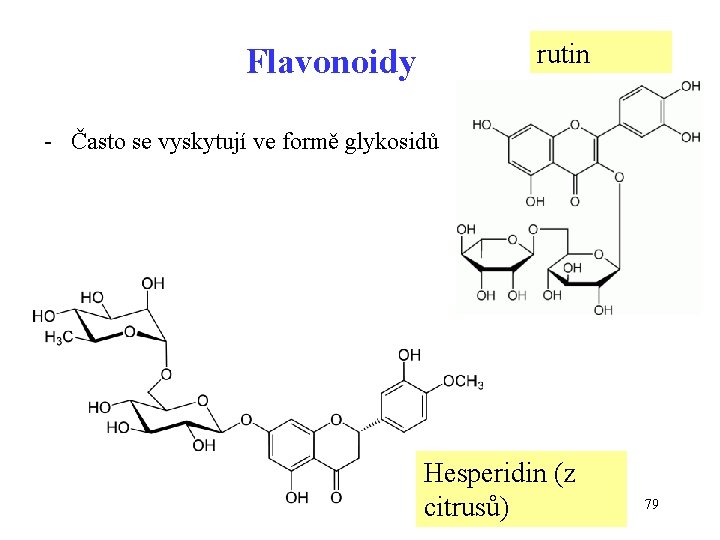
rutin Flavonoidy - Často se vyskytují ve formě glykosidů Hesperidin (z citrusů) 79

Disacharidy 80
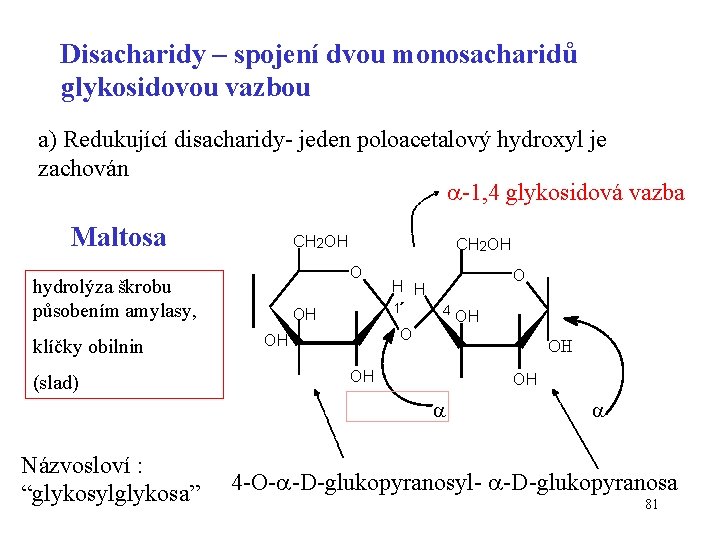
Disacharidy – spojení dvou monosacharidů glykosidovou vazbou a) Redukující disacharidy- jeden poloacetalový hydroxyl je zachován -1, 4 glykosidová vazba Maltosa CH 2 OH O hydrolýza škrobu působením amylasy, klíčky obilnin (slad) CH 2 OH 1´ OH O H H 4 O OH OH Názvosloví : “glykosylglykosa” OH 4 -O- -D-glukopyranosyl- -D-glukopyranosa 81
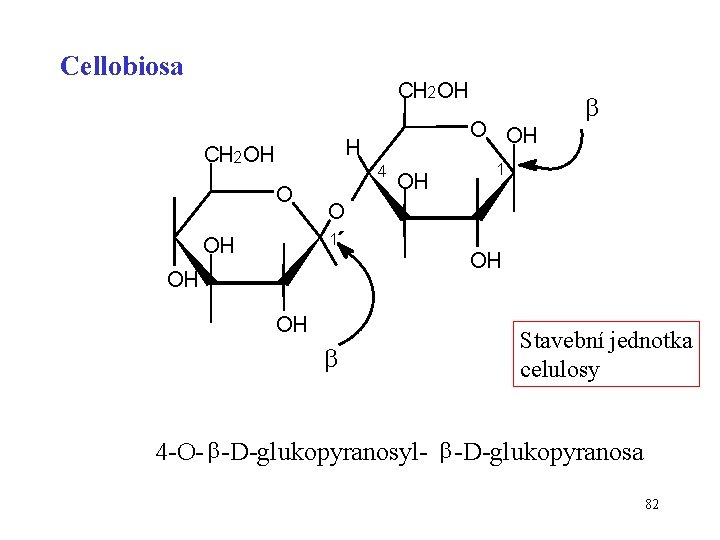
Cellobiosa CH 2 OH O OH H CH 2 OH 4 O 1´ OH OH OH Stavební jednotka celulosy 4 -O- -D-glukopyranosyl- -D-glukopyranosa 82
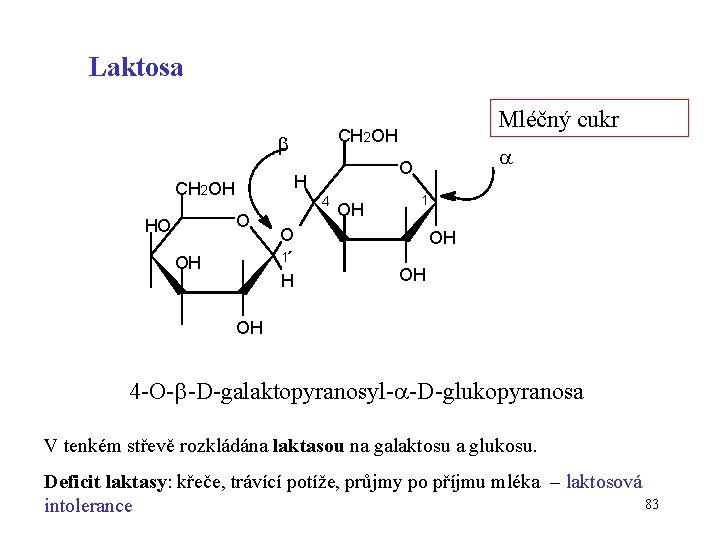
Laktosa CH 2 OH 4 O HO OH 1 O 1´ OH O H CH 2 OH Mléčný cukr H OH OH OH 4 -O- -D-galaktopyranosyl- -D-glukopyranosa V tenkém střevě rozkládána laktasou na galaktosu a glukosu. Deficit laktasy: křeče, trávící potíže, průjmy po příjmu mléka – laktosová 83 intolerance
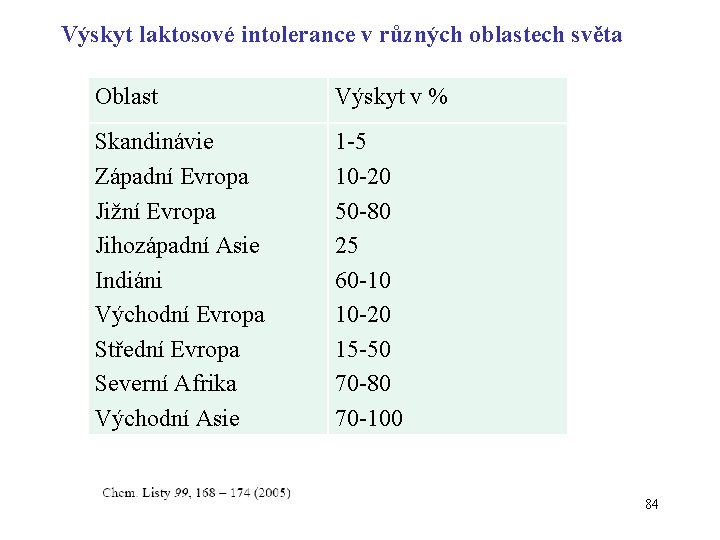
Výskyt laktosové intolerance v různých oblastech světa Oblast Výskyt v % Skandinávie Západní Evropa Jižní Evropa Jihozápadní Asie Indiáni Východní Evropa Střední Evropa Severní Afrika Východní Asie 1 -5 10 -20 50 -80 25 60 -10 10 -20 15 -50 70 -80 70 -100 84
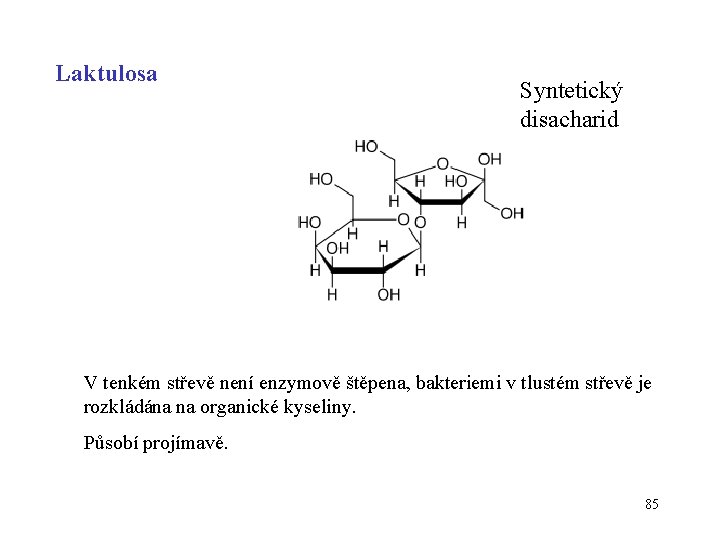
Laktulosa Syntetický disacharid V tenkém střevě není enzymově štěpena, bakteriemi v tlustém střevě je rozkládána na organické kyseliny. Působí projímavě. 85
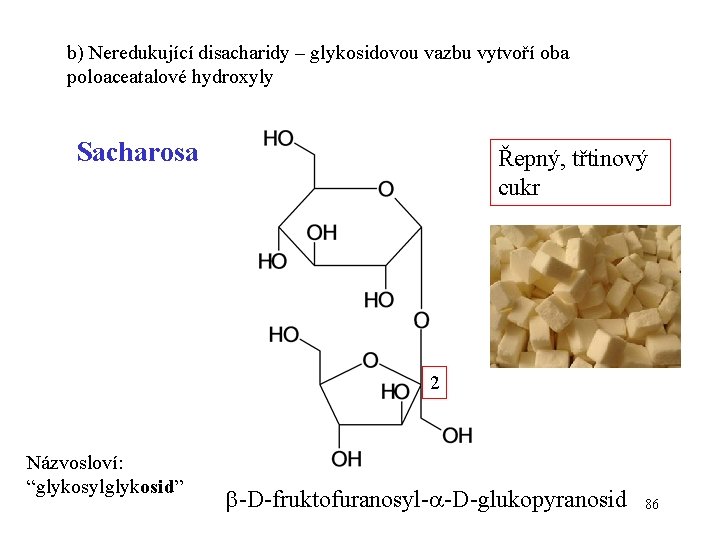
b) Neredukující disacharidy – glykosidovou vazbu vytvoří oba poloaceatalové hydroxyly Sacharosa Řepný, třtinový cukr 2 Názvosloví: “glykosylglykosid” -D-fruktofuranosyl- -D-glukopyranosid 86

Obsah sacharosy v potravinách Kolik váží kostka cukru? Menší kostka – 4 g ( 16 kcal, 68 k. J) Větší kostka 6 -8 g Potravina/nápoj Obsah cukrů vztažený na kostku cukru (4 g) Coca-cola 1 l 27 kostek (1836 k. J) 100% pomerančový džus 1 l 25 kostek Red Bull 250 ml 7 kostek 10 jahod 2 kostky Porce kečupu (17 g) 1 kostka Jogurt Activia jahodová 4 kostky Tyčinka Snickers 14 kostek 87
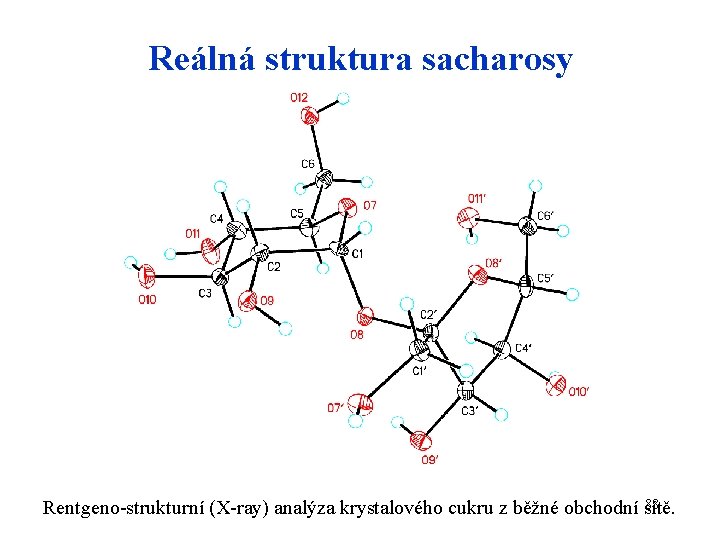
Reálná struktura sacharosy 88 Rentgeno-strukturní (X-ray) analýza krystalového cukru z běžné obchodní sítě.
- Slides: 88