S gio dc o to VNH LONG Tr





















- Slides: 29

Së gi¸o dôc ®µo t¹o VĨNH LONG Tr Ưêng THCS THPT TRƯNG VƯƠNG


Bài 15 HÓA TRỊ VÀ SỐ OXI HÓA

Có mấy loại liên kết hoá học mà các em đã học? LIÊN KẾT HÓA HỌC LIÊN KẾT CỘNG Hãy xác định ION HOÁ TRỊ điện O Na. Cltích. H 2 các nguyên tố trong Ca. F 2 CH 4 hợp chất ion và NH 3 Mg. O viết công thức cấu tạo của hợp chất cộng hóa trị

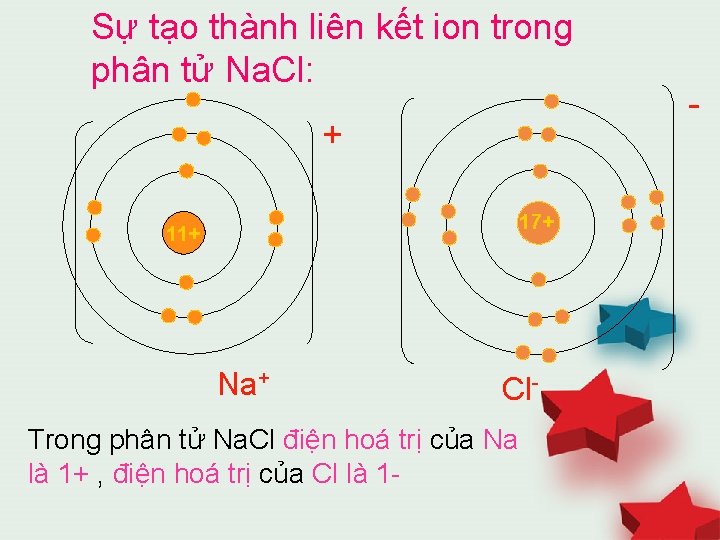
Sự tạo thành liên kết ion trong phân tử Na. Cl: + 17+ 11+ Na+ Cl- Trong phân tử Na. Cl điện hoá trị của Na là 1+ , điện hoá trị của Cl là 1 - -

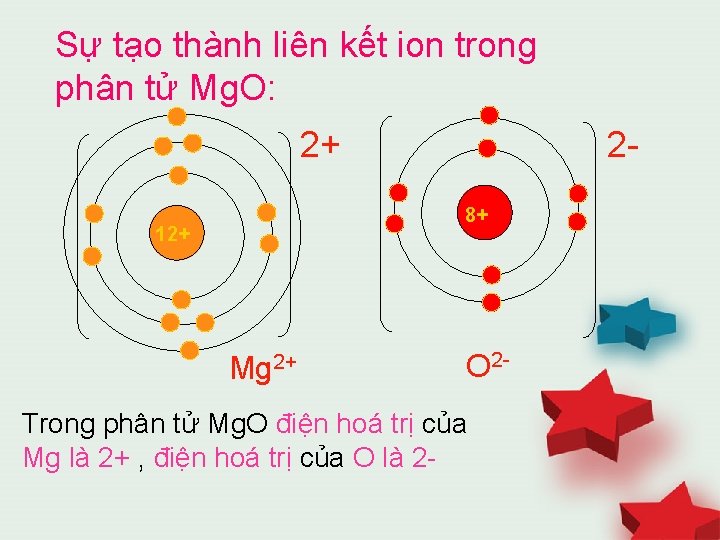
Sự tạo thành liên kết ion trong phân tử Mg. O: 2 - 2+ 8+ 12+ Mg 2+ O 2 - Trong phân tử Mg. O điện hoá trị của Mg là 2+ , điện hoá trị của O là 2 -

1. Hóa trị trong hợp chất ion: Hóa trị của nguyên tố trong hợp chất ion gọi là gì? Cách tính như thế nào? Cách ghi như thế nào?

I HÓA TRỊ: 1. Hóa trị trong hợp chất ion: Hóa trị của nguyên tố trong hợp chất ion gọi là điện hóa trị ► Cách tính: Điện hóa trị = Điện tích ion ► Cách ghi: Ghi số trước , dấu sau

Nhận xét : + Các nguyên tố kim loại thuộc nhóm IA, IIIA có điện hóa trị là 1+, 2+, 3+. + Các nguyên tố phi kim thuộc nhóm VIA, VIIA có điện hóa trị là 2 , 1. 9

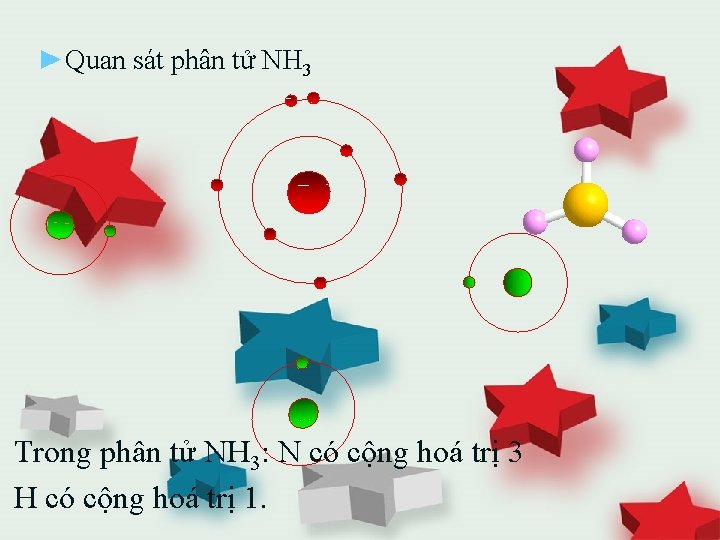
►Quan sát phân tử NH 3 Trong phân tử NH 3: N có cộng hoá trị 3 H có cộng hoá trị 1.

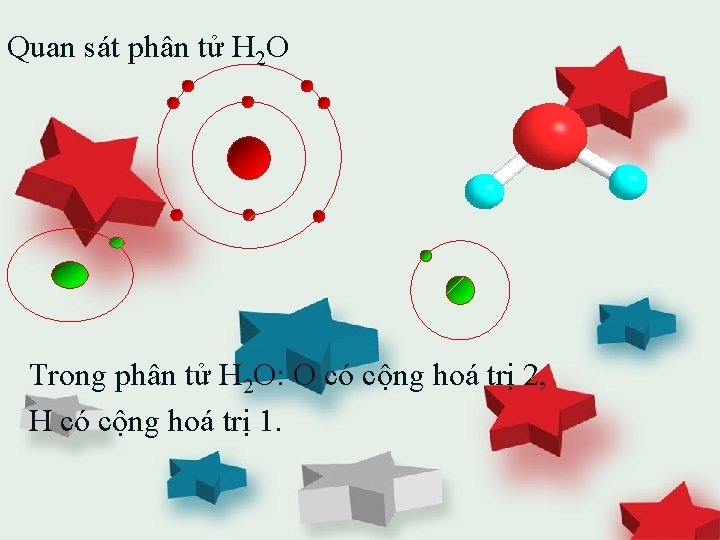
Quan sát phân tử H 2 O Trong phân tử H 2 O: O có cộng hoá trị 2, H có cộng hoá trị 1.

2. Hóa trị trong hợp chất cộng hoá trị: Hóa trị của nguyên tố trong hợp chất cộng hoá trị gọi là gì? Cách tính như thế nào?

2. Hoá trị trong hợp chất cộng hóa trị: • Hóa trị của nguyên tố trong hợp chất cộng hóa trị gọi là cộng hóa trị • Cách tính: Cộng hóa trị = số liên kết = số cặp e chung

Kết luận: các bước xác định hóa trị của nguyên tố ► Xác định chất đó chứa LKCHT hay LK ion ► Nếu là hợp chất ion xác định điện tích của các ion và kết luận hóa trị của các nguyên tố ► Nếu là hợp chất cộng hóa trị thì viết công thức cấu tạo và xác định số liên kết của các nguyên tử và kết luận hóa trị

II. SỐ OXI HÓA: 1. Khái niệm : Số oxi hóa là điện tích của nguyên tử của nguyên tố trong phân tử, nếu giả định rằng liên kết của các nguyên tử trong phân tử là liên kết ion

2. Qui tắc xác định số oxi hóa: Qui tắc 1: Số oxi hoá của nguyên tố trong các đơn chất bằng 0. 0 0 0 Thí dụ: trong đơn chất Na, Cu, Zn, O 2, H 2, N 2 -Cách viết số oxi hoá: dấu trước , số sau và được đặt phía trên kí hiệu hoá học.

Qui tắc 2: Trong hầu hết các hợp chất -Số oxi hoá của H bằng +1 trừ một số trường hợp như hiđrua kim loại (Na. H, Ca. H 2…). -Số oxi hoá của O bằng – 2, trừ trường hợp OF 2 peoxit (H 2 O 2, K 2 O 2. . ), supeoxit ( KO 2 , Na. O 2…. )

Qui tắc 3: Trong một phân tử, tổng số số oxi hoá của các nguyên tố nhân với số nguyên tử của từng nguyên tố bằng 0 Ví dụ: Tính số oxi hoá của nitơ trong các trường hợp sau: -3 x +1 NH 3 , * NH 3 x -2 +1+5 HNO 3 : x + 3*(+1) = 0 x = -3 * HNO 3 : (+1)*1 + x +3*(-2) = 0 x = +5

Qui tắc 4: - Số oxi hoá của các ion đơn nguyên tử bằng điện tích của ion đó. Thí dụ: Số oxi hoá của các nguyên tố ở các ion K+, Ca 2+, Fe 3+ Cl-, S 2 - lần lượt là +1, +2, +3, -1, -2 -Cách viết số oxi hoá: dấu trước , số sau và được đặt phía trên kí hiệu hoá học. Vi du : +2 Ca +3 Fe Ca 2+ , Fe 3+ , Cl-, S 2 -

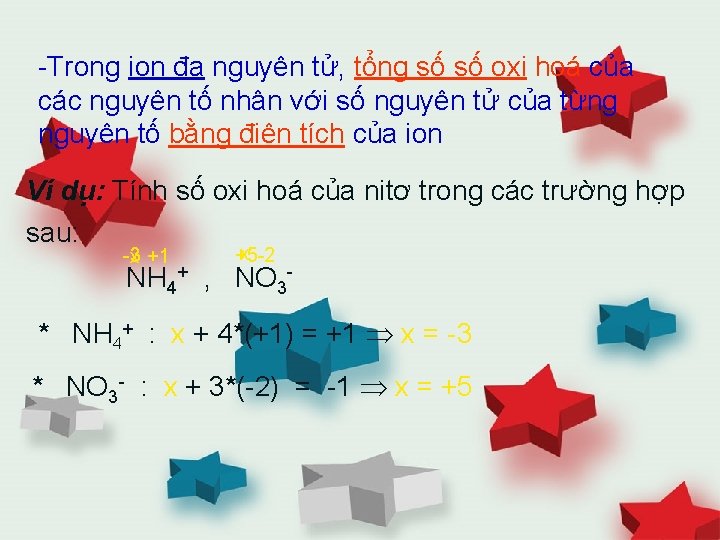
-Trong ion đa nguyên tử, tổng số số oxi hoá của các nguyên tố nhân với số nguyên tử của từng nguyên tố bằng điện tích của ion Ví dụ: Tính số oxi hoá của nitơ trong các trường hợp sau: -3 x +1 x -2 +5 NH 4+ , NO 3 - * NH 4+ : x + 4*(+1) = +1 x = -3 * NO 3 - : x + 3*(-2) = -1 x = +5

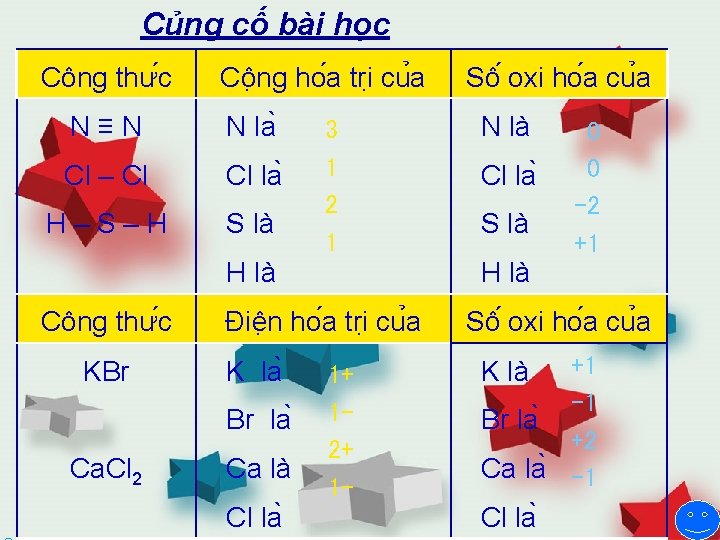
Củng cố bài học Công thư c Cô ng ho a tri cu a N≡N N la Cl – Cl Cl la H–S–H S là 3 1 2 1 H là Công thư c KBr Br la Ca. Cl 2 Ca là Cl la N là Cl la S là 0 0 -2 +1 H là Điê n ho a tri cu a K la Sô oxi ho a cu a 1+ 12+ 1 - Sô oxi ho a cu a +1 -1 Br la +2 Ca la -1 K là Cl la

Tính số oxi hoá của Cr trong các trường hợp sau: a) K 2 Cr 2 O 7 b) Cr. O 42 - Gọi x là số oxi hoá của Cr • 2 *(+1) +2 x + 7*(-2) = 0 => x= +6 • x + 4*(-2) = -2 => x = + 6 Chú ý: Số oxi hoá của các kim loại nhóm IA, IIIA bằng hoá trị của nó Ví dụ : K hoá trị I => số oxi hoá của K = +1

Câu hỏi trắc nghiệm Câu 1: Điện hóa trị của các nguyên tố O, S ( thuộc nhóm VIA) trong các hợp chất với các nguyên tố nhóm IA đều là: A. 2–. B. 2+. C. 6+. D. 4+.

Câu hỏi trắc nghiệm Câu 2: Cộng hóa trị của các nguyên tố H, C trong các phân tử CH 4 lần lượt là: A. 1, 1. B. 4, 1. C. 1, 4. D. 4, 4.

Câu hỏi trắc nghiệm Câu 3: Số oxi hoá của Mn trong hợp chất +1 x -2 KMn. O 4 là : A. +1 B. – 1 C. – 5 D. +7. +1+x+(-2)*4=0

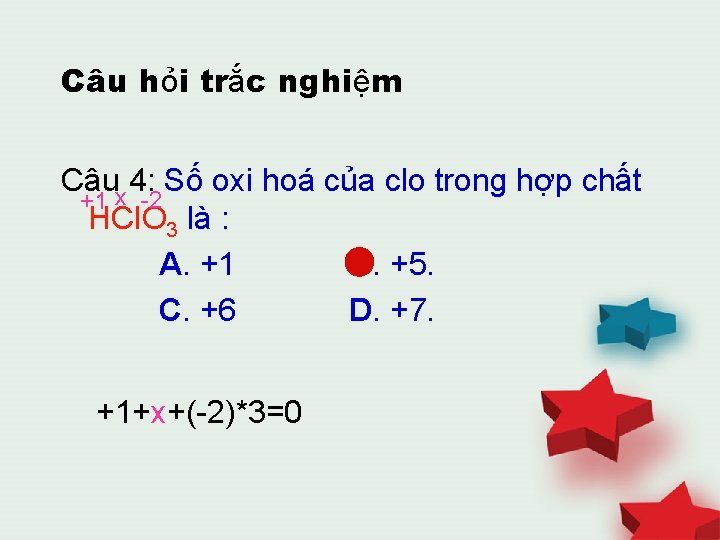
Câu hỏi trắc nghiệm Câux 4: Số oxi hoá của clo trong hợp chất +1 -2 HCl. O 3 là : A. +1 B. +5. C. +6 D. +7. +1+x+(-2)*3=0

Câu 5: Số oxi hóa của Mn , Fe trong Fe 3+, S trong SO 3, P trong PO 43 - lần lượt là: A. 0 , +3 , +6 , +5 B. +3, +5 , 0 , +6 C. 0 , +3 , +5 , +6 D. +5 , +6 , +3 , 0

GiẢI Ô CHỮ 4. ……. hoá trị là hoá trị của các nguyên tố 5. Trong axit HNO thì nguyên tố nào có số oxi 3………………. của đơn chất luôn bằng 0. 3 1. Cộng hoá trị được tính bằng số …………… 2. Số trị oxitrong hoá của bằng …………… ion 6. Hoá hợpion chất có liên kết ion là…… trong hợp chất có liên kết cộng hoá trị hoá là +5 1 2 3 S 4 5 Đ L I E N K E T Đ I E N T I C H O O X I H O A C O N G O A N I T O I E N H 6 HỌC TỐT T R I

Dặn dò: - Học bài - Bài tập SGK trang 90 - Bài tập phần luyện tập chương 3