Roztoky elektrolyt p H hydrolza sol pufry Biochemick

Roztoky elektrolytů: p. H, hydrolýza solí, pufry Biochemický ústav LF MU (E. T. ) 2013 1

Pojmy, jejichž znalost ze střední školy je nezbytná pro porozumění přednášené látce : • elektrolyty, jejich chování, typy elektrolytů • chemická rovnováha, její ovlivnění, rovnovážná konstanta • kyseliny, zásady, konjugované páry, • autoprotolýza vody, p. H • silné a slabé kyseliny a zásady • výpočet p. H silných kyselin a zásad • hydrolýza solí Tyto pojmy jsou zopakovány ve skriptu Lékařská chemie I 2
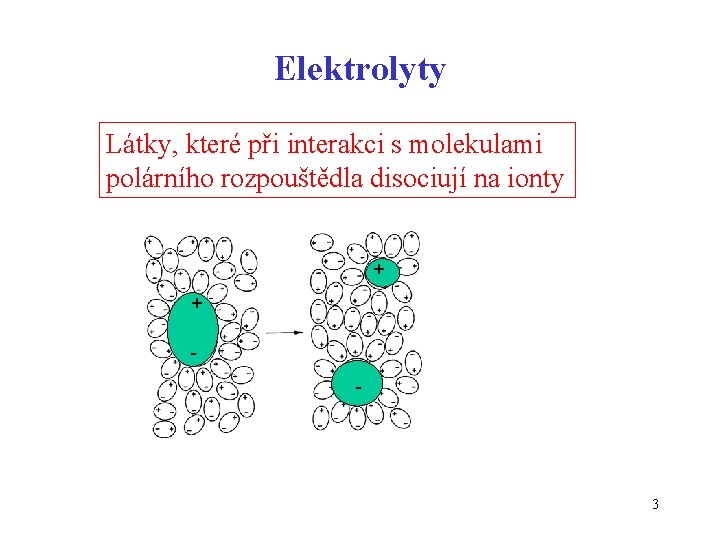
Elektrolyty Látky, které při interakci s molekulami polárního rozpouštědla disociují na ionty + + - 3
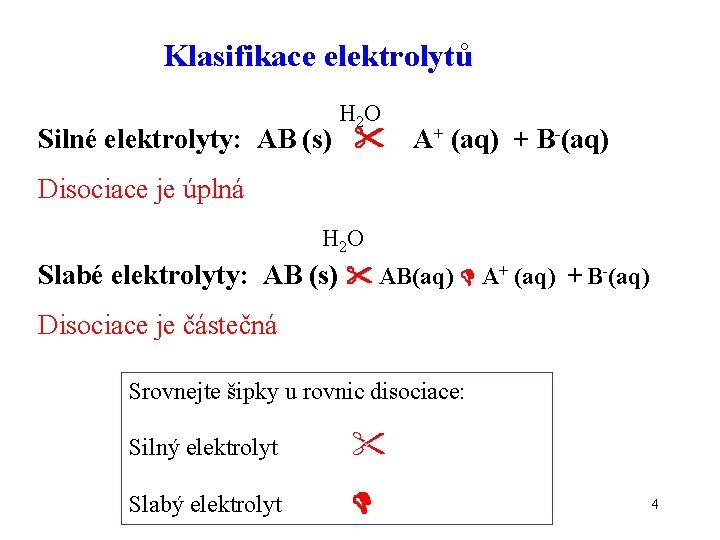
Klasifikace elektrolytů H 2 O Silné elektrolyty: AB (s) A+ (aq) + B-(aq) Disociace je úplná H 2 O Slabé elektrolyty: AB (s) AB(aq) A+ (aq) + B-(aq) Disociace je částečná Srovnejte šipky u rovnic disociace: Silný elektrolyt Slabý elektrolyt 4

Elektrolyty Silné Slabé silné kyseliny slabé kyseliny silné hydroxidy slabé zásady všechny soli Pozor!!! Všechny soli až na několik vyjímek (např. citrát vápenatý) úplně disociují – jsou silné elektrolyty (nezaměňujte s hydrolýzou solí !!!!!!) 5
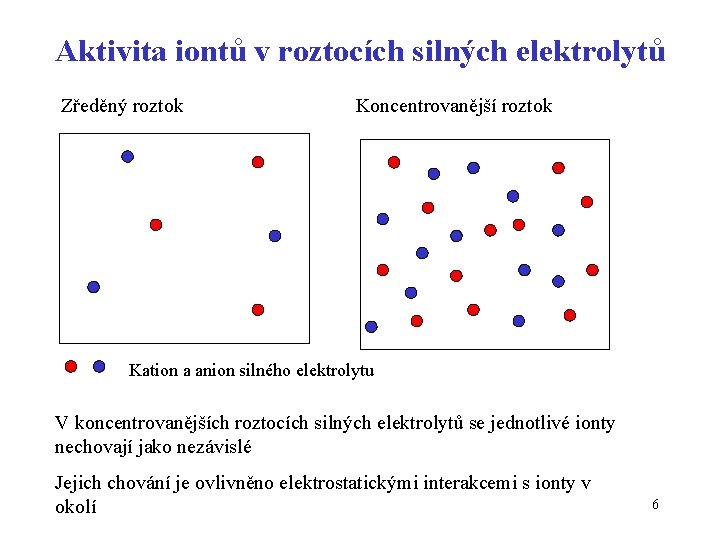
Aktivita iontů v roztocích silných elektrolytů Zředěný roztok Koncentrovanější roztok Kation a anion silného elektrolytu V koncentrovanějších roztocích silných elektrolytů se jednotlivé ionty nechovají jako nezávislé Jejich chování je ovlivněno elektrostatickými interakcemi s ionty v okolí 6

Chování iontů závisející na množství iontů popisuje aktivita Aktivita je mírou interakce iontů v roztoku s okolím ai = i ci i. . . aktivitní koeficient ci……koncentrace 1 Výpočet aktivitního koeficientu z Debye. Hűckelova vztahu: Z- náboj iontu, I-iontová síla roztoku 7
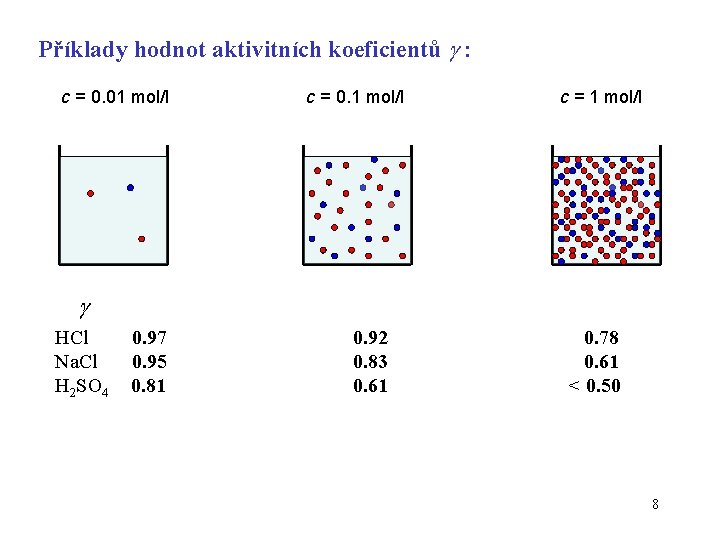
Příklady hodnot aktivitních koeficientů : c = 0. 01 mol/l c = 0. 1 mol/l c = 1 mol/l HCl Na. Cl H 2 SO 4 0. 97 0. 95 0. 81 0. 92 0. 83 0. 61 0. 78 0. 61 < 0. 50 8

Iontová síla roztoku ci – koncentrace daného iontu zi - náboj daného iontu Je funkcí koncentrace a náboje iontů, charakterizuje celkovou „koncentraci náboje” v roztoku. Ovlivňuje aktivitu iontů. 9

Jaká je iontová síla roztoku Na 2 SO 4 o koncentraci 0, 1 mol/l ? Řešení: Na 2 SO 4 Na+ + SO 42 - 2 Na+ + SO 42 c 1= c(Na+) = 2 ∙ 0, 1 = 0, 2 mol/l c 2 = c(SO 42 -) = 0, 1 mol/l z 1= z(Na+) = 1 z 2 = z(SO 42 -) = 2 I = ½ (0, 2 ∙ 12 + 0, 1 ∙ 22) = 0, 1 + 0, 2 = 0, 3 mol/l 10

Koncentrace, koncentrace iontů a iontová síla soli Typ soli koncentrace csoli cčástic Iontová síla I Na+Cl– csoli 2 csoli Ca 2+Cl 2– csoli 3 csoli Zn 2+SO 42– csoli 2 csoli 4 csoli Fe 3+Cl 3– csoli 4 csoli 6 csoli Jakou iontovou sílu má fyziologický roztok Na. Cl? Iontová síla krevní plazmy má prakticky konstantní hodnotu 0, 16 mol/l, naproti tomu iontová síla moče je velmi variabilní 11
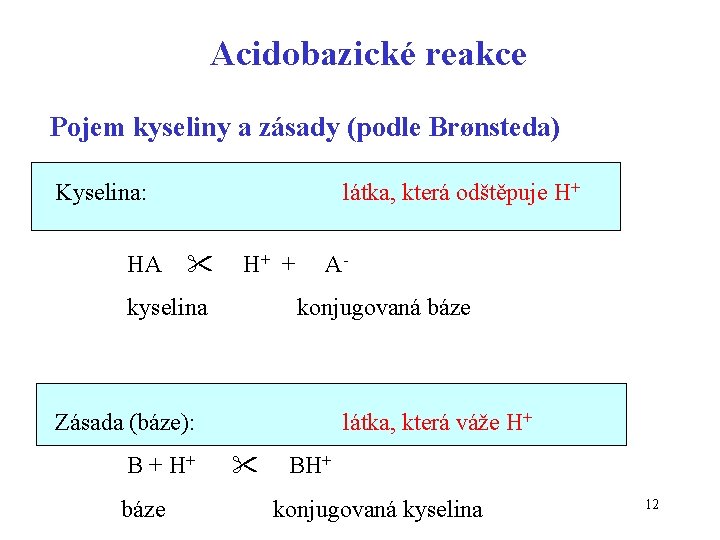
Acidobazické reakce Pojem kyseliny a zásady (podle Brønsteda) Kyselina: HA látka, která odštěpuje H+ + kyselina Akonjugovaná báze Zásada (báze): B + H+ báze látka, která váže H+ BH+ konjugovaná kyselina 12
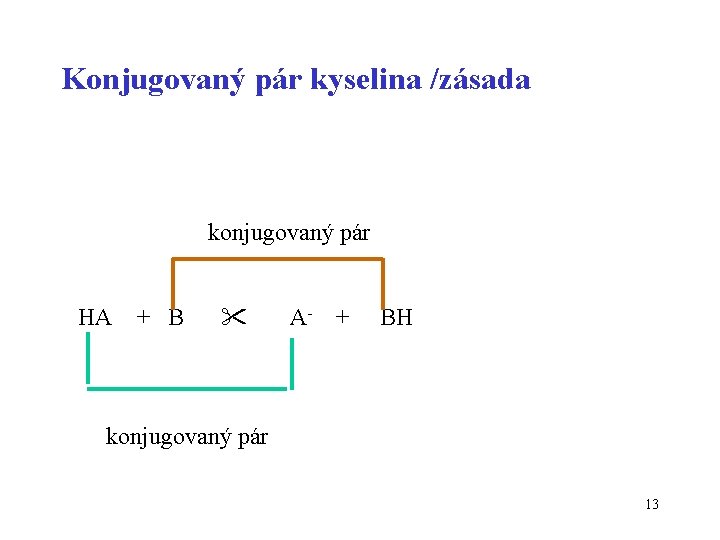
Konjugovaný pár kyselina /zásada konjugovaný pár HA + B A- + BH konjugovaný pár 13

Ionizace vody Voda je velmi slabý elektrolyt Má amfiprotický charakter, může vázat nebo uvolňovat protony Autoprotolýza vody 2 H 2 O H 3 O+ + OH− Kc=1 x 10 -16 Iontový součin vody: Kw = [H 3 O+] x [OH-] = 10− 14 mol 2 l− 2. 14
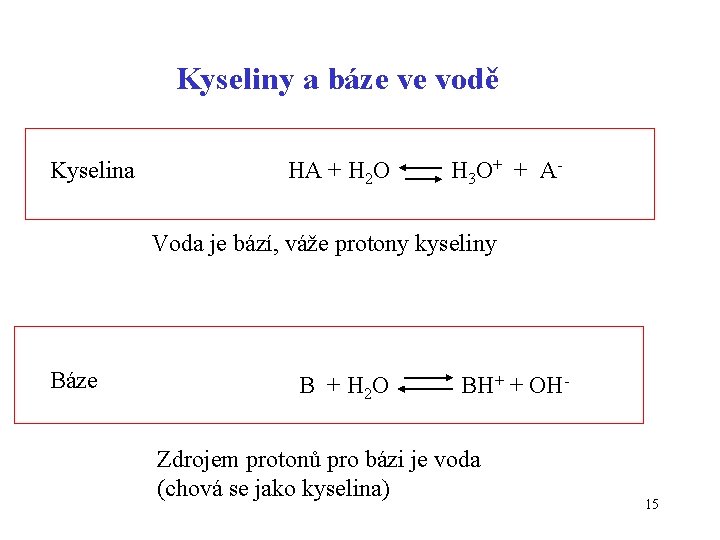
Kyseliny a báze ve vodě Kyselina HA + H 2 O H 3 O+ + A- Voda je bází, váže protony kyseliny Báze B + H 2 O BH+ + OH- Zdrojem protonů pro bázi je voda (chová se jako kyselina) 15

Výpočty p. H silných kyselin a zásad (opakování látky střední školy, bude krátce zopakováno na semináři 2, viz též skripta LCH I, ) Silné kyseliny a silné hydroxidy jsou silnými elektrolyty. Ve zjednodušených výpočtech předpokládáme, že ve vodě zcela disociují HA + H 2 O H 3 O+ + AU jednosytné kyseliny je pak koncentrace H+ stejná jako celková koncentrace c. HA a p. H lze počítat jako p. H = - log H 3 O+ = - log c. HA Obdobně platí pro silné zásady 16

p. H slabých kyselin a zásad Jaké p. H má ocet ? Jaké p. H má roztok kyseliny askorbové? Proč mohu pít roztok kyseliny uhličité, fosforečné a ne roztok kyseliny sírové ? 17

Disociace slabých kyselin a zásad Slabá jednosytná kyselina HA + H 2 O H 3 O+ + A- Slabá jednosytná zásada B + H 2 O BH+ + OH- rovnovážná konstanta disociační konstanta protonizační konstanta 18
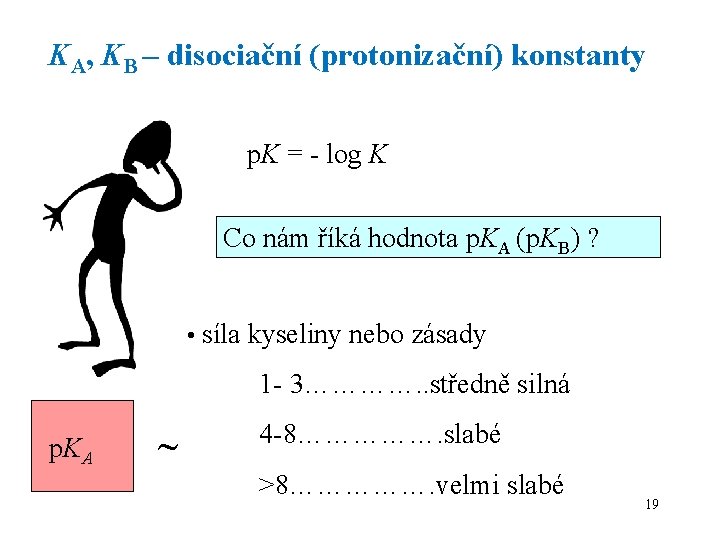
KA, KB – disociační (protonizační) konstanty p. K = - log K Co nám říká hodnota p. KA (p. KB) ? • síla kyseliny nebo zásady 1 - 3…………. . středně silná p. KA 4 -8……………. slabé >8……………. velmi slabé 19
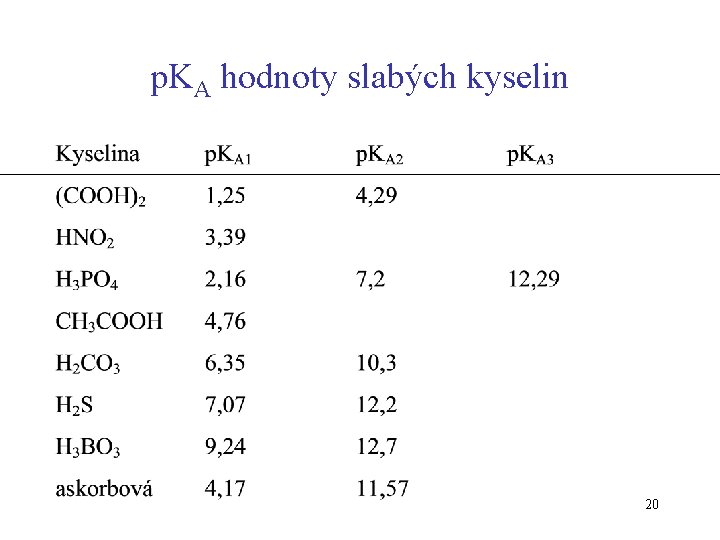
p. KA hodnoty slabých kyselin 20
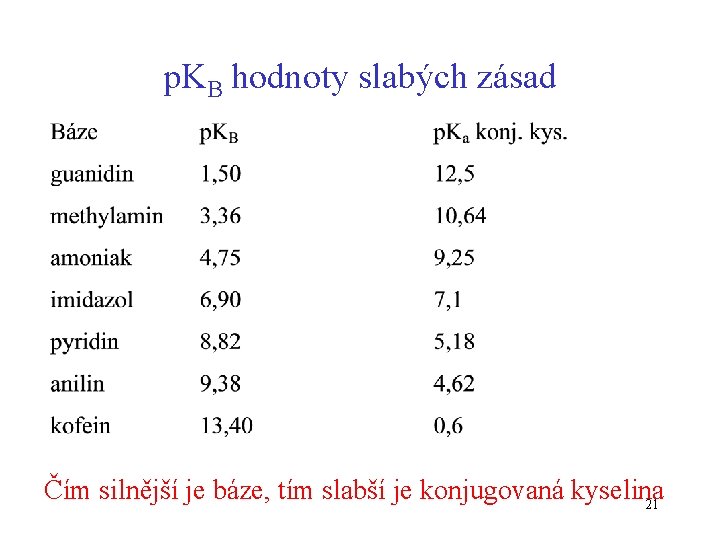
p. KB hodnoty slabých zásad Čím silnější je báze, tím slabší je konjugovaná kyselina 21

Vztah KA a KB ( p. KA a p. KB) KA. KB = Kv = 1. 10 -14 p. KA+ p. KB = 14 22

Příklad: Chování amoniaku NH 3 ve vodě NH 3 + H 2 O NH 4+ + H 2 O NH 4+ + OH- NH 3 jako zásada NH 3 + H 3 O+ NH+4 jako kyselina 23

Zjednodušené výpočty p. H slabých kyselin a zásad Slabá jednosytná kyselina o celkové koncentraci c. HA HA + H 2 O H 3 O + + A - 24
![c. HA-celková koncentrace všech molekul [HA] – koncentrace nedisociovaných molekul Pro úpravu vztahu zavedeme c. HA-celková koncentrace všech molekul [HA] – koncentrace nedisociovaných molekul Pro úpravu vztahu zavedeme](http://slidetodoc.com/presentation_image_h2/77e31bc3ea6bfe385645b40aa7d1fd39/image-25.jpg)
c. HA-celková koncentrace všech molekul [HA] – koncentrace nedisociovaných molekul Pro úpravu vztahu zavedeme 2 zjednodušení: 1. Koncentrace disociovaných molekul u slabé kyseliny je velmi malá ve srovnání s nedisociovanými: c. HA>> H+ [HA] = (c. HA – [H+]) [HA] c. HA 2. Z jedné molekuly vzniká disociací stejný počet kationtů a aniontů: [H+] = [A-] 25

p. H slabé kyseliny závisí na její koncentraci a p. KA hodnotě p. H = - log H+ = - log Pravidla logaritmování: Ølogaritmus součinu x. y= součtu logaritmů (logx + log y) Ølogarimus odmocniny x = 1/2 log x p. KA 26

Porovnání p. H silné a slabé kyseliny o stejné koncentraci HCl c=0, 1 mol/l p. H = -log c. HA = - log 0, 1 = 1 CH 3 COOH c=0, 1 mol/l p. H = 2, 35 + 0, 5 = 2, 85 Hodnotu p. H ovlivňují všechny H+ ionty – kyselina je plně disociována p. KA = 4, 7 Hodnotu p. H ovlivňují pouze disociované H+ ionty 27

Slabá jednosytná báze: B + H 2 O BH+ + OH- 28
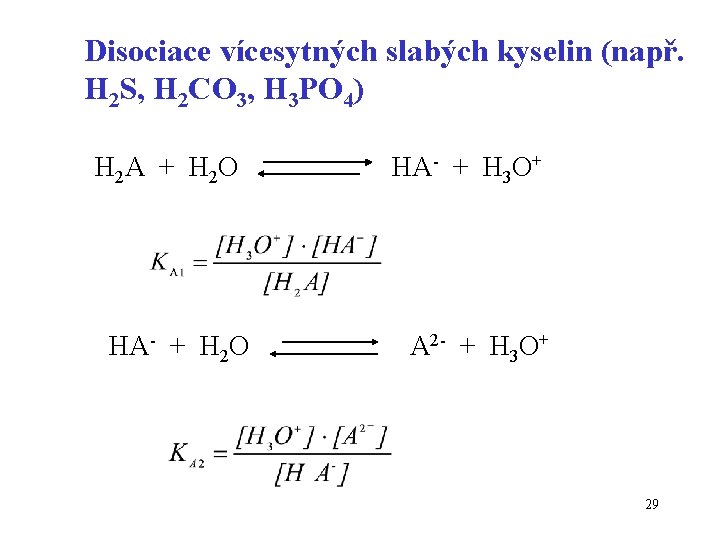
Disociace vícesytných slabých kyselin (např. H 2 S, H 2 CO 3, H 3 PO 4) H 2 A + H 2 O HA- + H 3 O+ A 2 - + H 3 O+ 29

Hodnoty p. KA u vícesytných kyselin se obvykle výrazně liší Pokud koncentrace kyseliny není příliš nízká a rozdíl v p. K je větší jak 3, ionizaci do dalšího stupně lze zanedbat a uvažovat, že ve vodném roztoku převažují ionty z disociace do 1. stupně. Neplatí tedy pro kys. sírovou, kterou zjednodušeně pokládáme za silnou dvojsytnou kyselinu) 30

Hydrolýza solí Soli vznikají reakcí mezi kyselinou a zásadou – neutralizací. Při neutralizační reakci není vždy výsledné p. H neutrální. Všechny soli disociují ve vodném roztoku, ale jen některé hydrolyzují Hydrolýza soli = reakce aniontů slabých kyselin nebo kationtů slabých zásad s vodou ovlivňuje p. H roztoku soli Hydrolyzují pouze ty soli, v nichž je obsažen kation slabé zásady nebo anion slabé kyseliny 31

Rozdíly v reaktivitě iontů („silné“ a „slabé“ ionty*) Cl- animace CH 3 COOH 2 O CH 3 COOH + OH- Cl- je divácký (spectator) anion, nereaguje s vodou CH 3 COO- je anion slabé kyseliny, má tendenci reagovat s vodou a tvořit kyselinu octovou. Reakcí s vodou se vytvoří takové množství CH 3 COOH, aby byla zachována rovnováha daná disociační konstantou *V klinické biochemii se anionty silných kyselin označují jako silné ionty 32

Ion, který reaguje s vodou ovlivňuje p. H roztoku 33

Proč má mýdlo alkalickou reakci ? Proč je roztok sody (Na 2 CO 3) alkalický ? Proč je roztok Na 3 PO 4 alkalický ? 34
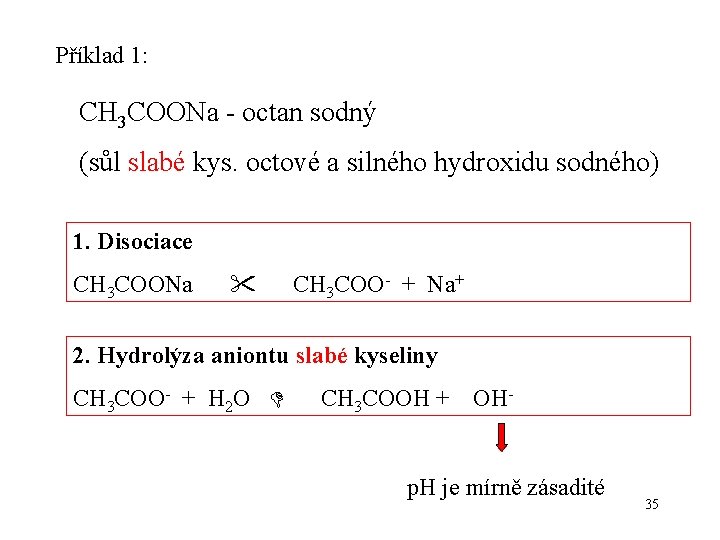
Příklad 1: CH 3 COONa - octan sodný (sůl slabé kys. octové a silného hydroxidu sodného) 1. Disociace CH 3 COONa CH 3 COO- + Na+ 2. Hydrolýza aniontu slabé kyseliny CH 3 COO- + H 2 O CH 3 COOH + OH- p. H je mírně zásadité 35

Příklad 2: NH 4 Cl - chlorid amonný (sůl slabé báze amoniaku a silné kyseliny chlorovodíkové, také např. pyridinium chlorid, pyrrolidinium bromid atd. ) 1. Disociace NH 4 Cl NH 4+ + Cl- 2. Hydrolýza kationtu slabé báze NH 4+ + H 2 O H 3 O+ + NH 3 p. H je mírně kyselé 36

Příklad 3: Cu. Cl 2 - chlorid měďnatý (sůl kationtu Cu 2+ odvozeného od slabého hydroxidu a silné kyseliny chlorovodíkové) 1. Disociace Cu. Cl 2 Cu 2+ + 2 Cl- 2. Vznik aquakomplexu Cu 2+ + 6 H 2 O [Cu(H 2 O)6]2+ 3. Hydrolýza komplexního aquakationtu [Cu(H 2 O)6 ]2+ + H 2 O [Cu(H 2 O)5 OH]+ + H 3 O+ p. H je mírně kyselé 37
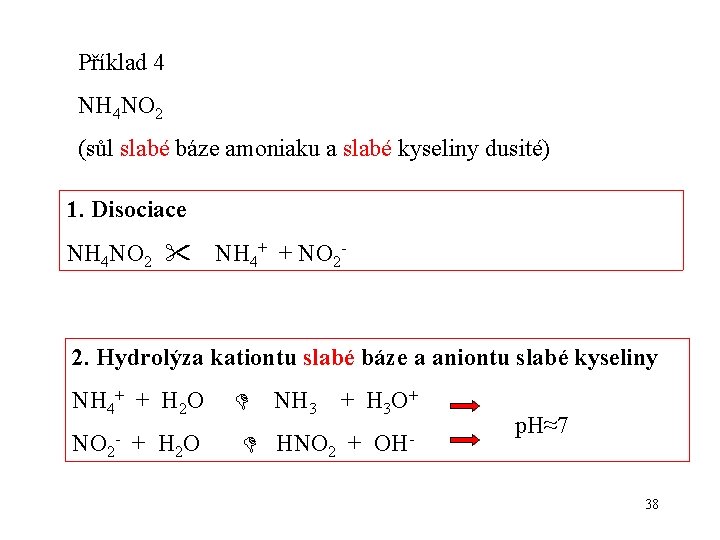
Příklad 4 NH 4 NO 2 (sůl slabé báze amoniaku a slabé kyseliny dusité) 1. Disociace NH 4 NO 2 NH 4+ + NO 2 - 2. Hydrolýza kationtu slabé báze a aniontu slabé kyseliny NH 4+ + H 2 O NO 2 - + H 2 O NH 3 + H 3 O+ HNO 2 + OH- p. H≈7 38
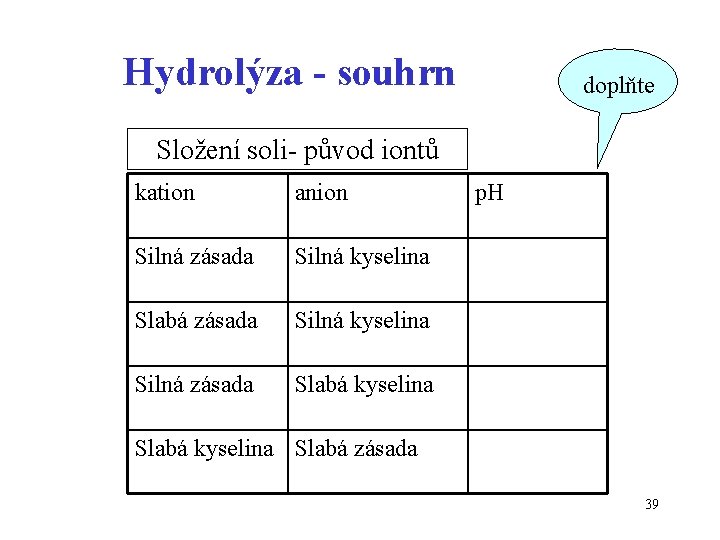
Hydrolýza - souhrn doplňte Složení soli- původ iontů kation anion Silná zásada Silná kyselina Slabá zásada Silná kyselina Silná zásada Slabá kyselina p. H Slabá kyselina Slabá zásada 39

Tlumivé roztoky (pufry) Látky, pomocí kterých lze: • nastavit přesnou hodnotu p. H • udržet dané p. H v určitých mezích • tlumit výkyvy p. H způsobené omezeným přídavkem kyseliny či zásady. 40

Pufry jsou nejčastěji: • směs slabé kyseliny a její soli se silnou zásadou (kys. octová a octan sodný) • směs slabé zásady a její soli se silnou kyselinou (amoniak a chlorid amonný) • směs solí vícesytné kyseliny (hydrogenfosforečnan a dihydrogenfosforečnan sodný) 41
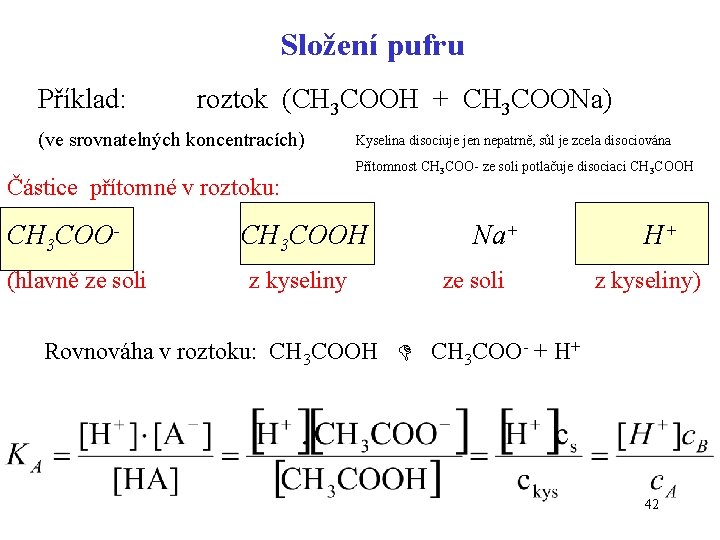
Složení pufru Příklad: roztok (CH 3 COOH + CH 3 COONa) (ve srovnatelných koncentracích) Částice přítomné v roztoku: CH 3 COO(hlavně ze soli Kyselina disociuje jen nepatrně, sůl je zcela disociována Přítomnost CH 3 COO- ze soli potlačuje disociaci CH 3 COOH z kyseliny Na+ ze soli H+ z kyseliny) Rovnováha v roztoku: CH 3 COOH CH 3 COO- + H+ 42

Jak pufr působí Př. : Do roztoku octanového pufru přidáme silnou kyselinu H+ ionty → porušíme rovnováhu Rovnováha v roztoku se opět obnoví, část H+ iontů se sloučí na CH 3 COOH : CH 3 COO- + H+ CH 3 COOH • většina přidaných H+ je vázána jako slabá kyselina, její disociace je potlačena přítomností CH 3 COOhttp: //www. chembio. uoguelph. ca/educmat/chm 19104/chemtoons 8. htm 43

Př. : Do roztoku přidáme silný hydroxid OH- ionty → porušíme rovnováhu CH 3 COOH + OH- CH 3 COO- + H 2 O Sníží se konc. CH 3 COOH, zvýší se koncentrace CH 3 COOAby byla zachována rovnováha, část CH 3 COOiontů se sloučí s H+ na CH 3 COOH • přibylo iontů CH 3 COO-, část se přeměnila na CH 3 COOH 44
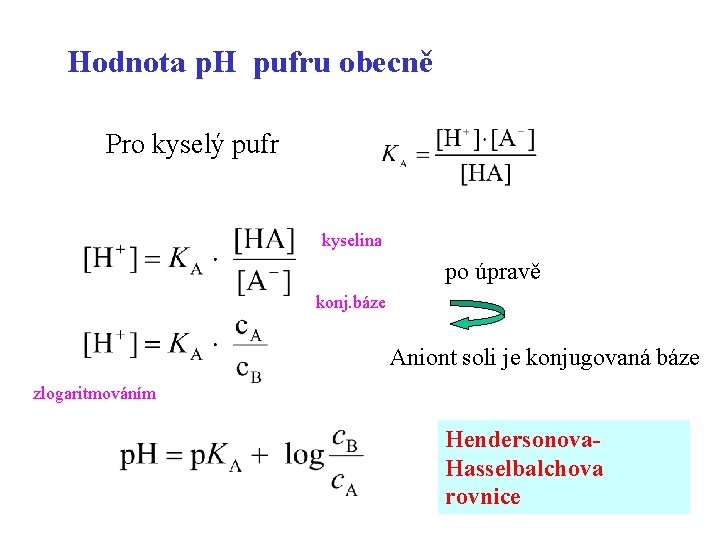
Hodnota p. H pufru obecně Pro kyselý pufr kyselina po úpravě konj. báze Aniont soli je konjugovaná báze zlogaritmováním Hendersonova. Hasselbalchova rovnice 45
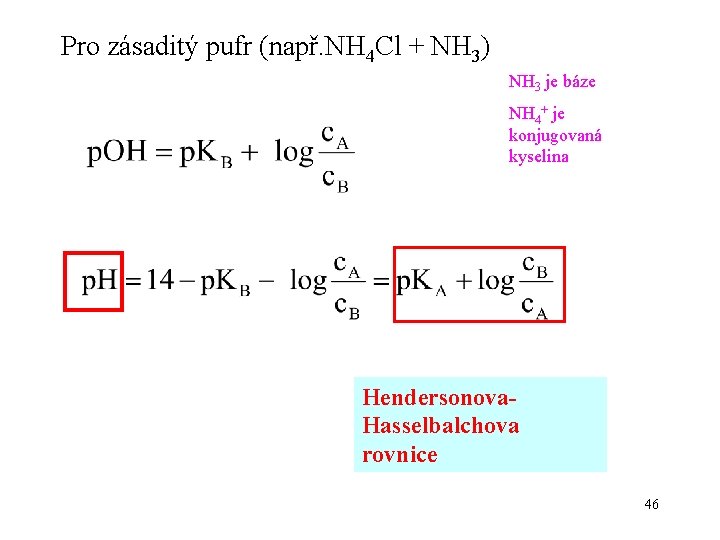
Pro zásaditý pufr (např. NH 4 Cl + NH 3) NH 3 je báze NH 4+ je konjugovaná kyselina Hendersonova. Hasselbalchova rovnice 46
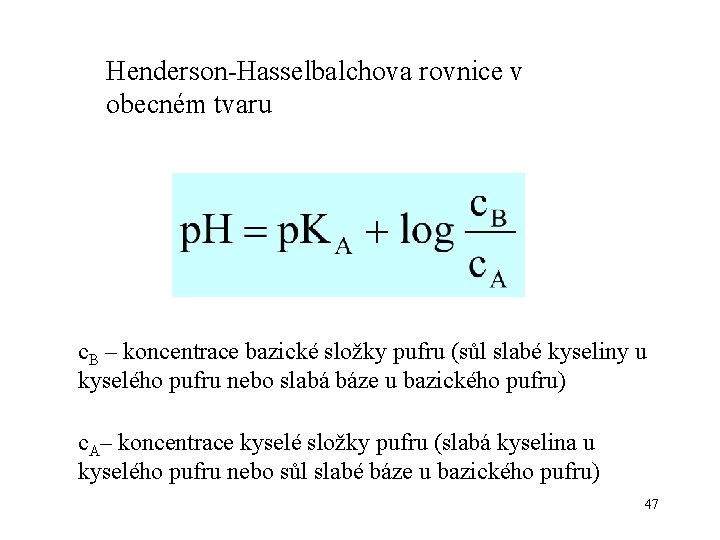
Henderson-Hasselbalchova rovnice v obecném tvaru c. B – koncentrace bazické složky pufru (sůl slabé kyseliny u kyselého pufru nebo slabá báze u bazického pufru) c. A– koncentrace kyselé složky pufru (slabá kyselina u kyselého pufru nebo sůl slabé báze u bazického pufru) 47
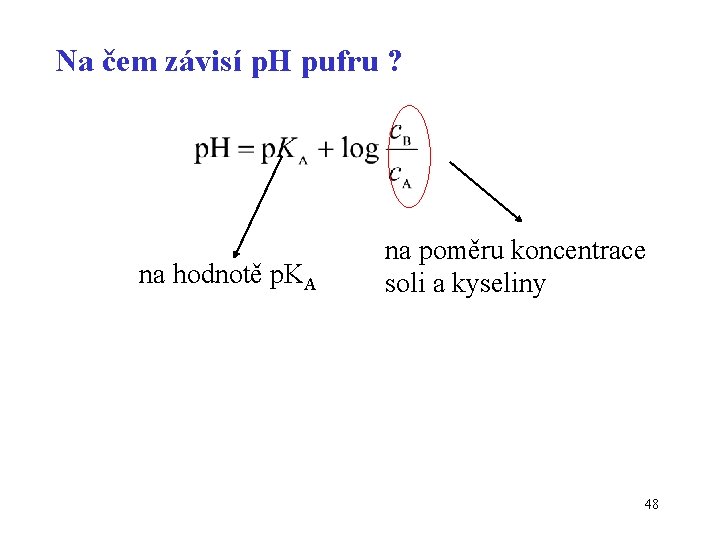
Na čem závisí p. H pufru ? na hodnotě p. KA na poměru koncentrace soli a kyseliny 48

Příklad: Jaké bude p. H octanového pufru připraveného z 0, 2 l kyseliny octové, c=0, 4 mol/l a 0, 3 l octanu sodného c=0, 2 mol/l ? 49 49

Kapacita pufru - vyjadřuje účinnost pufru = množství H+ nebo OH- iontů , které je třeba přidat k 1 l pufru, aby se p. H změnilo o 1 (resp. 0, 1) Na čem závisí kapacita pufru ? • na poměru koncentrací obou složek • na koncentraci obou složek pufru Viz praktická cvičení 50

Závislost kapacity na poměru koncentrací Změna poměru koncentrací po přídavku silné kyseliny nebo báze je nejmenší, jsou-li koncentrace soli i kyseliny stejné Kapacita je nejvyšší, jestliže pak c. B/c. A = 1 log 1 = 0 p. H = p. KA 51

Účinné pufry mají p. H = p. K 1 ( c. B/c. A = 1/10 -10 /1) Tedy p. KA kyselé složky pufru musí být co nejbližší pufrované hodnotě p. H Při stejném poměru obou složek pufru má větší kapacitu pufr s vyšší koncentrací 52

Pro určitý pokus potřebujete upravit p. H vzorku vody na hodnotu p. H = 4. Který z následujících pufrů můžete použít? a) borátový (H 3 BO 3 + Na 2 B 4 O 7, p. KA = 9, 24) b) acetátový (CH 3 COOH + CH 3 COONa, p. KA = 4, 76) c) fosfátový (Na. H 2 PO 4 + Na 2 HPO 4, p. KA = 7, 20) Jak daný pufr připravíte? 53

Vztah pufru k titračním křivkám • titrační křivka vyjadřuje změny p. H v průběhu titrace kyseliny zásadou nebo naopak • je to závislost p. H na objemu přidaného titračního činidla nebo % neutralizace Např. titrace kys. octové hydroxidem sodným CH 3 COOH + Na. OH CH 3 COONa + H 2 O Titrací vzniká sůl, v reakční směsi je v průběhu titrace směs kyseliny a soli – tedy směs je pufrem (na počátku jen kyselina, na konci jen sůl) 54
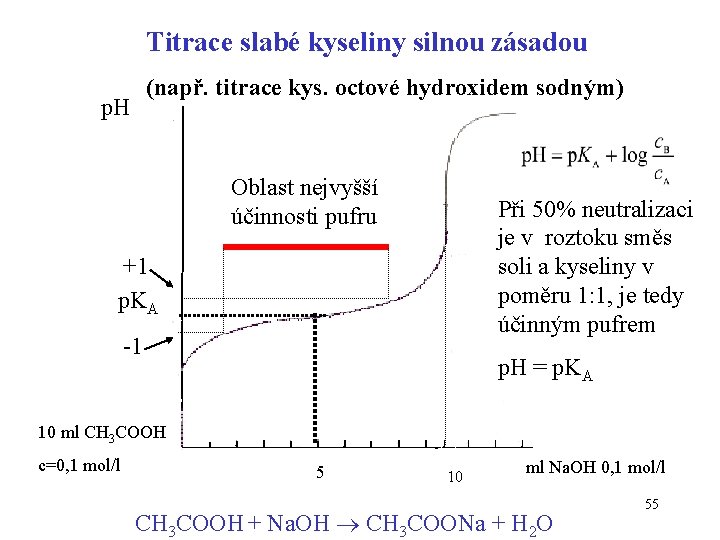
Titrace slabé kyseliny silnou zásadou (např. titrace kys. octové hydroxidem sodným) p. H Oblast nejvyšší účinnosti pufru Při 50% neutralizaci je v roztoku směs soli a kyseliny v poměru 1: 1, je tedy účinným pufrem +1 p. KA -1 p. H = p. KA 10 ml CH 3 COOH c=0, 1 mol/l 5 10 ml Na. OH 0, 1 mol/l CH 3 COOH + Na. OH CH 3 COONa + H 2 O 55

Jak můžeme zjistit p. KA slabé kyseliny? Máme k dispozici p. H metr, příslušnou kyselinu a Na. OH ? ? 56

Vliv p. H na disociaci slabých kyselin a bází Z H. -H. rovnice lze odvodit, jaký bude poměr mezi disociovanou a nedisociovanou formou kyseliny nebo báze při různém p. H Příklad: Kyselina mléčná, p. KA = 3, 86 V jakém stavu disociace se bude kyselina mléčná nacházet při p. H a) 2 b) 3, 86 c) 7, 4 (fyziologické p. H) ? a) p. H=2 Při p. H=2 poměr c. B/c. A 1/100, tedy cca 99% molekul je v nedisociovaném stavu (-COOH) Při p. H 2 převažuje nedisociovaná forma kyseliny 57

b) kys. mléčná, p. H 3, 86 (=p. KA ) Při p. H=p. KA poměr c. B/c. A 1/1, tedy 50 % molekul je v nedisociovaném stavu (COOH) a 50% je disociováno (COO-) c) kys. mléčná, p. H 7, 4 Při p. H=7, 4 poměr c. B/c. A > 1000/1, tedy cca 99% molekul je v disociovaném stavu (-COO-) Při p. H 7, 4 převažuje disociovaná forma kyseliny 58

Vliv p. H na disociaci slabých kyselin p. H Převažuje forma p. H<<p. KA -COOH p. H = p. KA -COOH= -COO- p. H >>p. KA -COO- Závěr: • Při p. H<<p. KA slabá kyselina není téměř disociována • Při p. H = p. KA je kyselina disociována z 50% • Při p. H >> p. KA je kyselina úplně disociována Pufrační účinky se směsí kyselina/sůl se mohou projevit jen při hodnotách p. H blízkých p. KA. (viz též snímek 52) 59
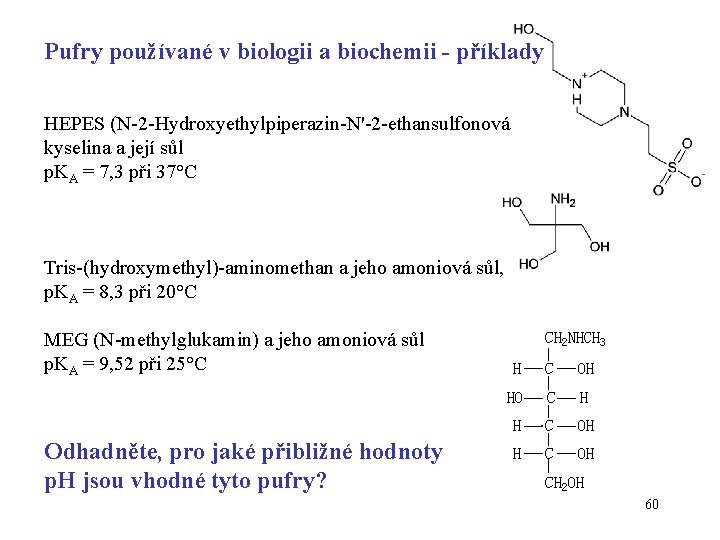
Pufry používané v biologii a biochemii - příklady HEPES (N-2 -Hydroxyethylpiperazin-N'-2 -ethansulfonová kyselina a její sůl p. KA = 7, 3 při 37°C Tris-(hydroxymethyl)-aminomethan a jeho amoniová sůl, p. KA = 8, 3 při 20°C MEG (N-methylglukamin) a jeho amoniová sůl p. KA = 9, 52 při 25°C Odhadněte, pro jaké přibližné hodnoty p. H jsou vhodné tyto pufry? 60

Jak se v těle udržuje konstantní hodnota p. H ? p. H citron pepsikola pomeranč 2, 3 2, 5 3, 7 buňky prostaty buňky kost. svalů trombocyty erytrocyt osteoblasty 8, 5 4, 5 6, 9 7, 0 7, 3 KREV 7, 36– 7, 44 žaludeční šťáva duoden. šťáva žluč moč 1, 2– 3 6, 5– 7, 6 6, 2– 8, 5 4, 8– 8 61
![Hraniční hodnoty p. H (plná krev) p. H = 7, 4 [H+] 40 nmol. Hraniční hodnoty p. H (plná krev) p. H = 7, 4 [H+] 40 nmol.](http://slidetodoc.com/presentation_image_h2/77e31bc3ea6bfe385645b40aa7d1fd39/image-62.jpg)
Hraniční hodnoty p. H (plná krev) p. H = 7, 4 [H+] 40 nmol. l-1 p. H = 6, 80 [H+] 160 nmol. l-1 p. H = 7, 70 [H+] 20 nmol. l-1 62

Pufrační systémy v organismu p. H krve Pufr 7, 40 0, 04 plná krev HCO 3−/H 2 CO 3 + CO 2 50 % IST ICT HCO 3− Protein−/HProtein 45 % – proteiny HPO 42−/H 2 PO 4− 5% anorg. fosfáty Všechny pufrační systémy působí koordinovaně 63

Hydrogenuhličitanový pufr (hydrogenkarbonátový) CO 2 + H 2 O H 2 CO 3 H+ + HCO 3 - • CO 2 se rozpouští ve vodě a jeho malá část vytváří H 2 CO 3 • Koncentrace H 2 CO 3 závisí na koncentraci CO 2 • Do rovnováhy zahrnujeme i CO 2 (voda, 25 C) p. KAef = 6, 37 [CO 2 + H 2 CO 3] = [H 2 CO 3]ef efektivní koncentrace Její mírou je p. CO 2 nad roztokem 64
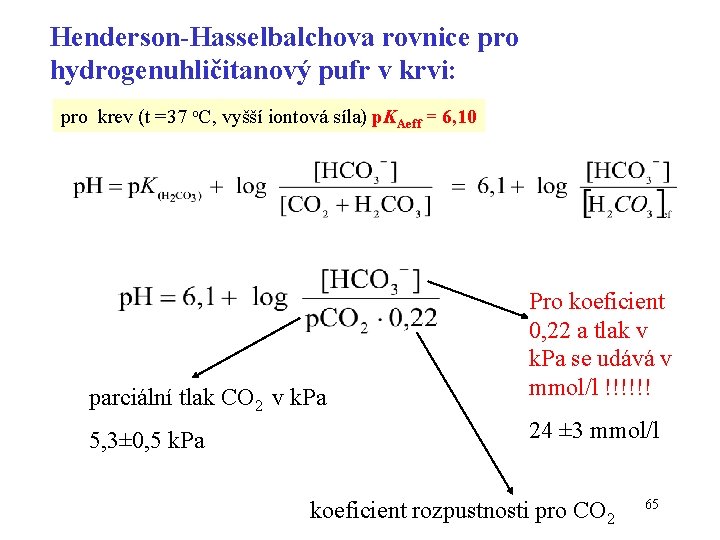
Henderson-Hasselbalchova rovnice pro hydrogenuhličitanový pufr v krvi: pro krev (t =37 o. C, vyšší iontová síla) p. KAeff = 6, 10 parciální tlak CO 2 v k. Pa 5, 3± 0, 5 k. Pa Pro koeficient 0, 22 a tlak v k. Pa se udává v mmol/l !!!!!! 24 ± 3 mmol/l koeficient rozpustnosti pro CO 2 65
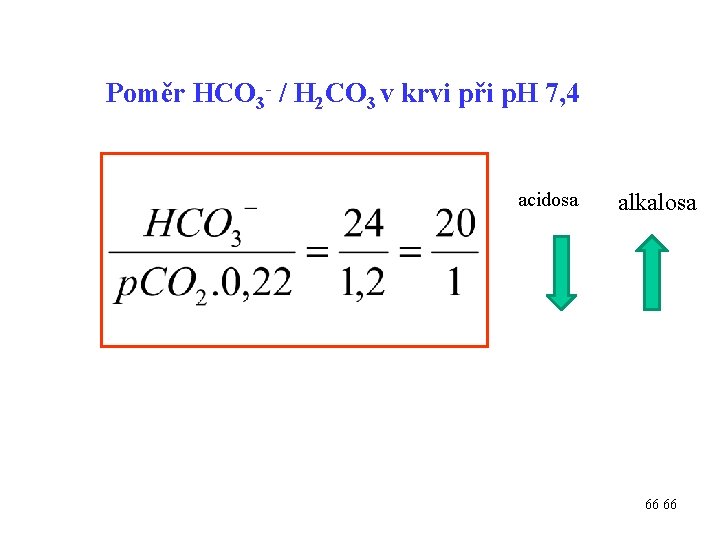
Poměr HCO 3 - / H 2 CO 3 v krvi při p. H 7, 4 acidosa alkalosa 66 66
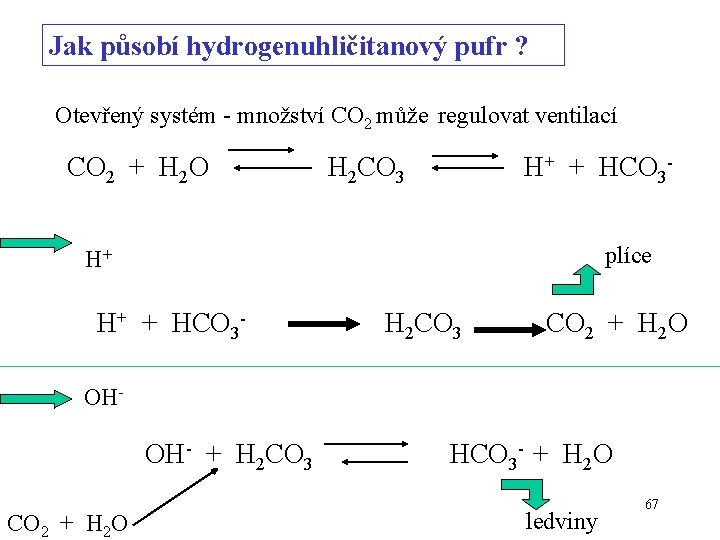
Jak působí hydrogenuhličitanový pufr ? Otevřený systém - množství CO 2 může regulovat ventilací CO 2 + H 2 O H 2 CO 3 H+ + HCO 3 plíce H+ H+ + HCO 3 - H 2 CO 3 CO 2 + H 2 O OH- + H 2 CO 3 CO 2 + H 2 O HCO 3 - + H 2 O ledviny 67
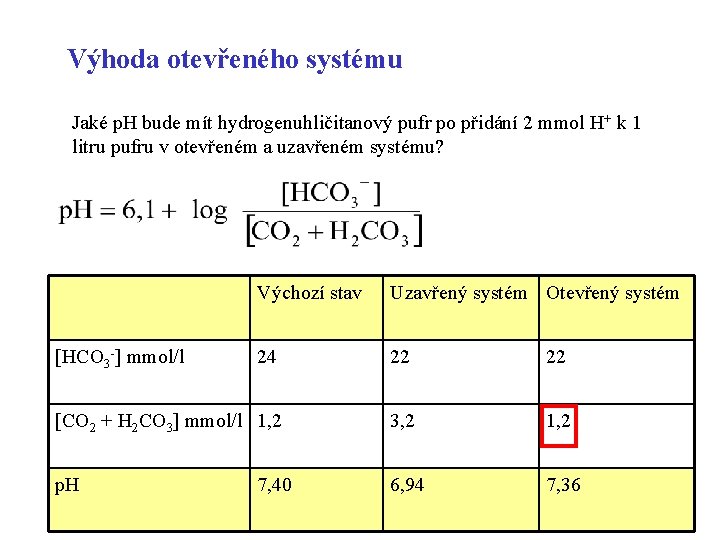
Výhoda otevřeného systému Jaké p. H bude mít hydrogenuhličitanový pufr po přidání 2 mmol H+ k 1 litru pufru v otevřeném a uzavřeném systému? Výchozí stav Uzavřený systém Otevřený systém 24 22 22 [CO 2 + H 2 CO 3] mmol/l 1, 2 3, 2 1, 2 p. H 6, 94 7, 36 [HCO 3 -] mmol/l 7, 40 68
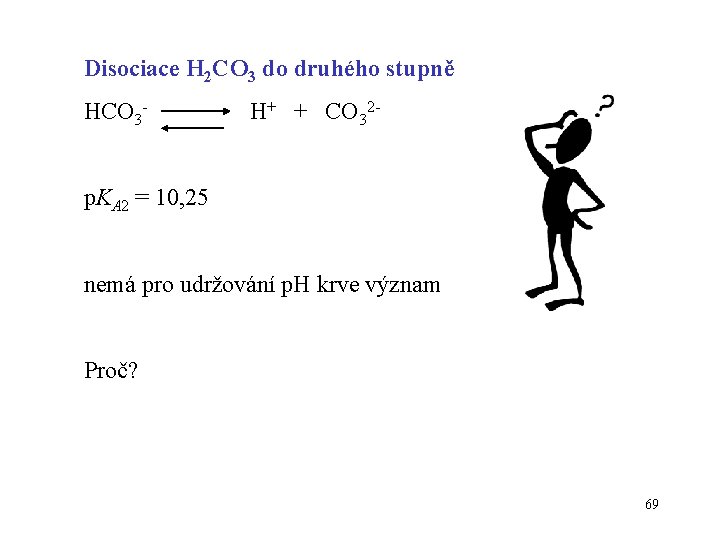
Disociace H 2 CO 3 do druhého stupně HCO 3 - H+ + CO 32 - p. KA 2 = 10, 25 nemá pro udržování p. H krve význam Proč? 69
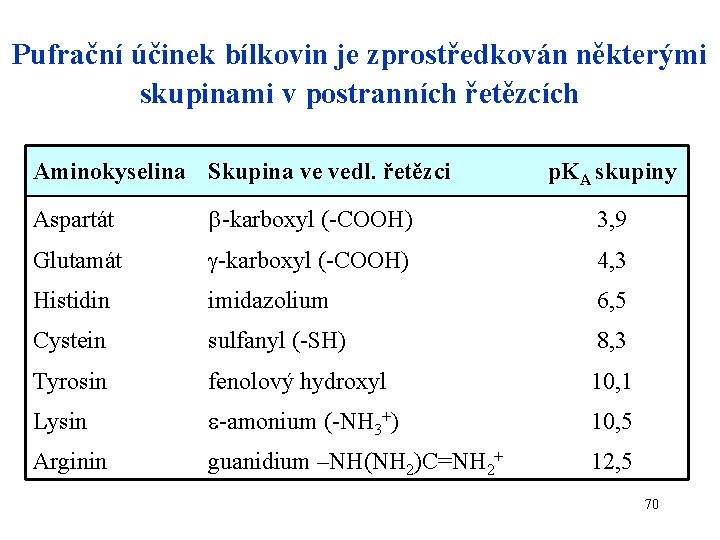
Pufrační účinek bílkovin je zprostředkován některými skupinami v postranních řetězcích Aminokyselina Skupina ve vedl. řetězci p. KA skupiny Aspartát -karboxyl (-COOH) 3, 9 Glutamát -karboxyl (-COOH) 4, 3 Histidin imidazolium 6, 5 Cystein sulfanyl (-SH) 8, 3 Tyrosin fenolový hydroxyl 10, 1 Lysin -amonium (-NH 3+) 10, 5 Arginin guanidium –NH(NH 2)C=NH 2+ 12, 5 70

Která z uvedených AK se může efektivně podílet na udržení p. H 7, 4 ? 71
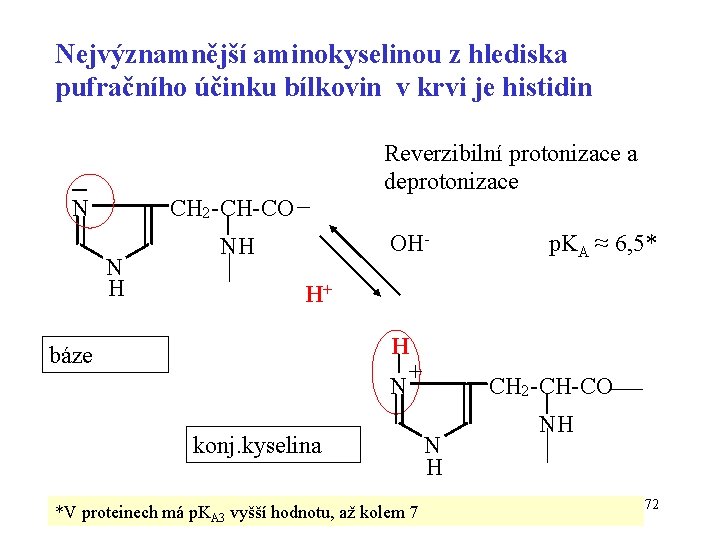
Nejvýznamnější aminokyselinou z hlediska pufračního účinku bílkovin v krvi je histidin N Reverzibilní protonizace a deprotonizace CH 2 -CH-CO N H OH- NH p. KA ≈ 6, 5* H+ H + N báze konj. kyselina *V proteinech má p. KA 3 vyšší hodnotu, až kolem 7 CH 2 -CH-CO N H NH 72

Nejvýznamnějším bílkovinným pufrem v krvi je hemoglobin, je to hlavní bílkovina krve Obsahuje histidinové zbytky: např. hemoglobin A (tetramer) má 38 histidinových zbytků Pufrační účinky má také albumin (hlavní bílkovina plazmy) a ostatní bílkoviny. 73
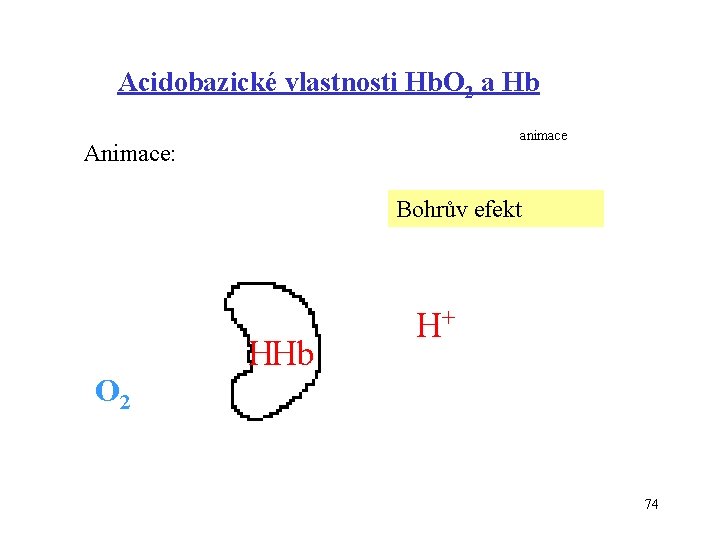
Acidobazické vlastnosti Hb. O 2 a Hb animace Animace: Bohrův efekt O 2 HHb H+ 74
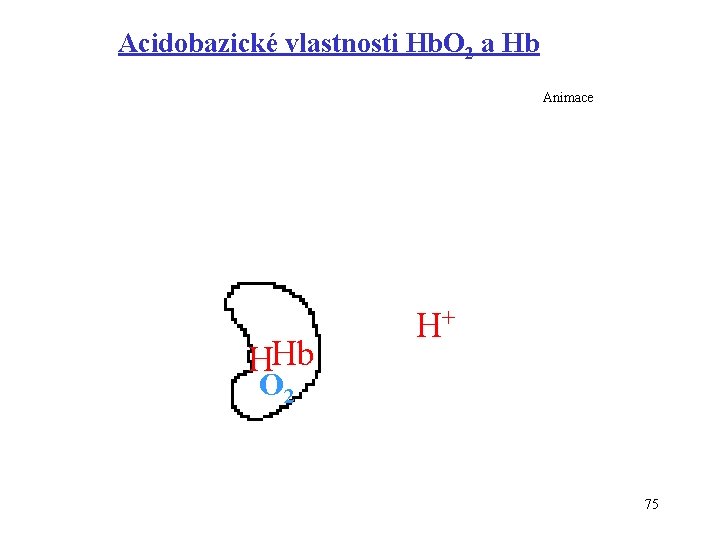
Acidobazické vlastnosti Hb. O 2 a Hb Animace HHb H+ O 2 75
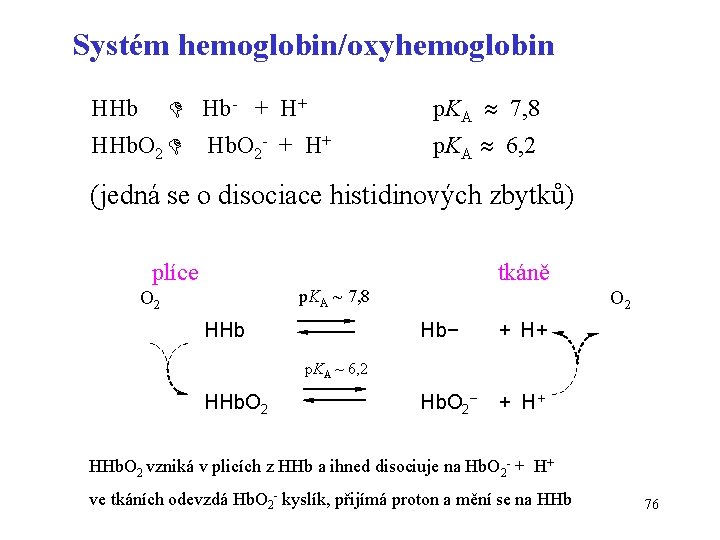
Systém hemoglobin/oxyhemoglobin Hb- + H+ HHb. O 2 Hb. O 2 - + H+ p. KA 7, 8 p. KA 6, 2 (jedná se o disociace histidinových zbytků) plíce tkáně p. KA ~ 7, 8 O 2 HHb O 2 Hb− + H+ Hb. O 2− + H+ p. KA ~ 6, 2 HHb. O 2 vzniká v plicích z HHb a ihned disociuje na Hb. O 2 - + H+ ve tkáních odevzdá Hb. O 2 - kyslík, přijímá proton a mění se na HHb 76

Hydrogenfosfátový pufr H 2 PO 4 - - kyselá složka HPO 42 - - bazická složka p. KA 2 = 6, 8 koncentrace fosfátů v krvi je nízká působí jako účinný pufr v moči a v buňkách 77
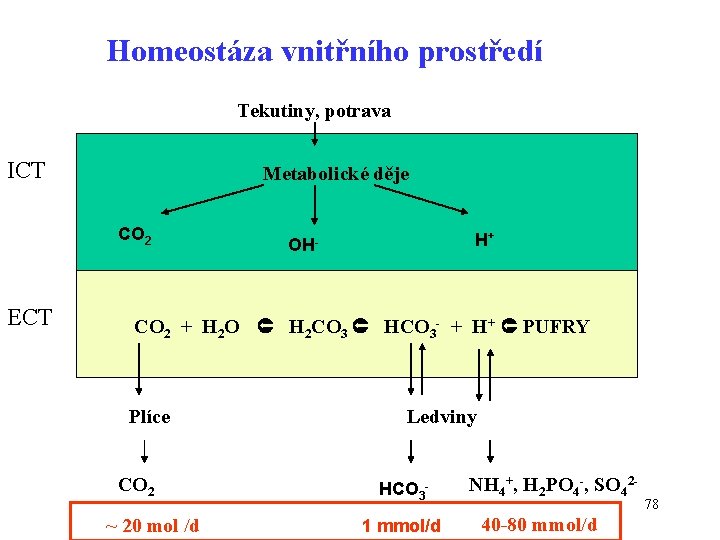
Homeostáza vnitřního prostředí Tekutiny, potrava ICT Metabolické děje CO 2 ECT H+ OH- CO 2 + H 2 O H 2 CO 3 HCO 3 - + H+ PUFRY Plíce CO 2 ~ 20 mol /d Ledviny HCO 31 mmol/d NH 4+, H 2 PO 4 -, SO 4240 -80 mmol/d 78
- Slides: 78