RISONANZA DALLA CHIMICA INORGANICA LO IONE CARBONATO CO

RISONANZA
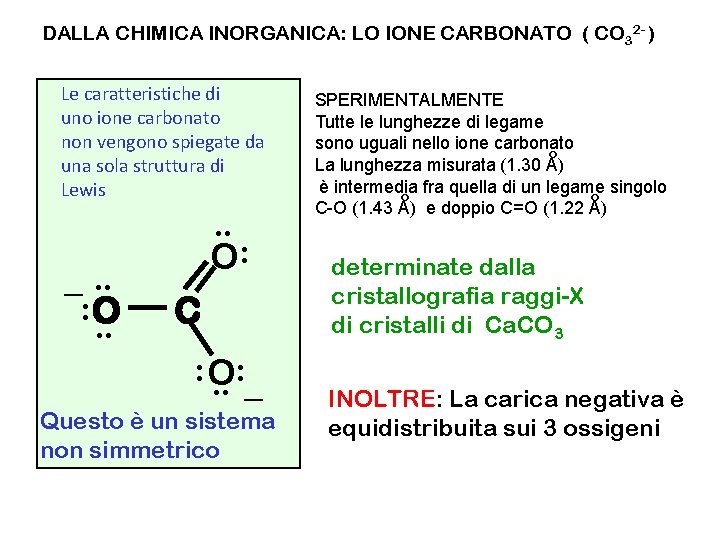
DALLA CHIMICA INORGANICA: LO IONE CARBONATO ( CO 32 - ) Le caratteristiche di uno ione carbonato non vengono spiegate da una sola struttura di Lewis _. . : O. . O: C : O. . : _ Questo è un sistema non simmetrico SPERIMENTALMENTE Tutte le lunghezze di legame sono uguali nello ione carbonato o La lunghezza misurata (1. 30 A) è intermedia fra quella di un legame singolo o o C-O (1. 43 A) e doppio C=O (1. 22 A) determinate dalla cristallografia raggi-X di cristalli di Ca. CO 3 INOLTRE: La carica negativa è equidistribuita sui 3 ossigeni
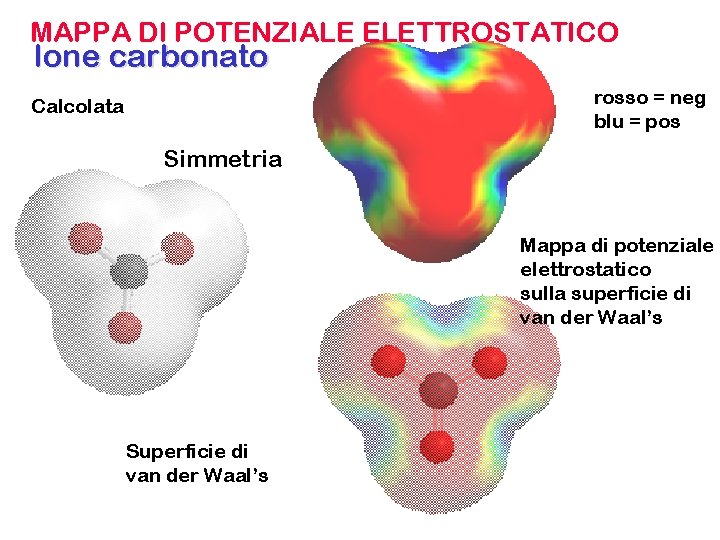
MAPPA DI POTENZIALE ELETTROSTATICO Ione carbonato rosso = neg blu = pos Calcolata Simmetria Mappa di potenziale elettrostatico sulla superficie di van der Waal’s Superficie di van der Waal’s
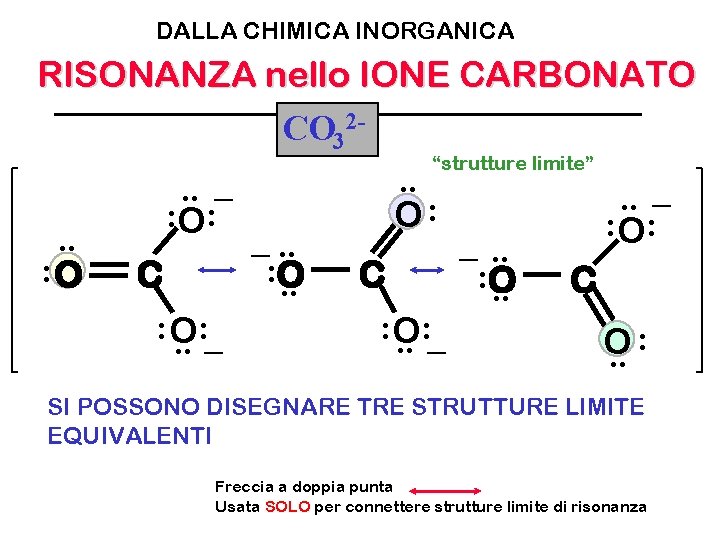
DALLA CHIMICA INORGANICA RISONANZA nello IONE CARBONATO CO 32“strutture limite”. . _. . : O: O: : : O _. . : O C. . : O : : : O _ : . . _. . O. . SI POSSONO DISEGNARE TRE STRUTTURE LIMITE EQUIVALENTI Freccia a doppia punta Usata SOLO per connettere strutture limite di risonanza
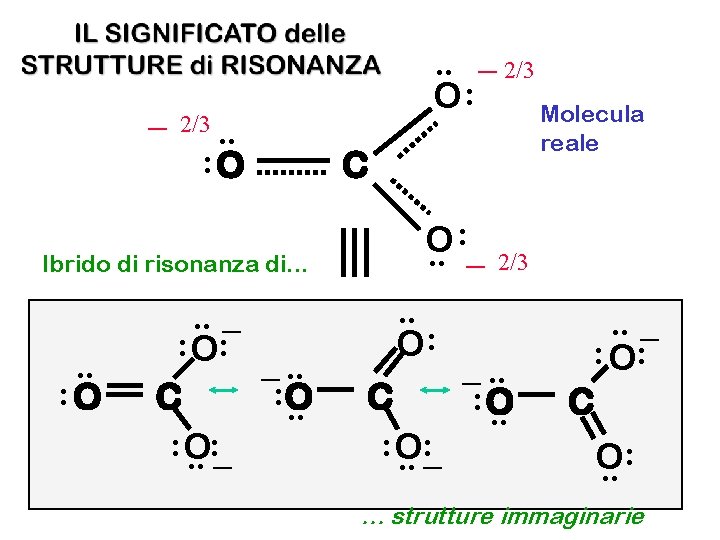
_ 2/3 . . : O Ibrido di risonanza di. . . : O . . _ 2/3 O: Molecula . . _ : O: _. . : O C. . : O : . . _ reale C : _ O. . O: C : O : . . _ 2/3 _. . : O. . _ : O: C : O. . … strutture immaginarie
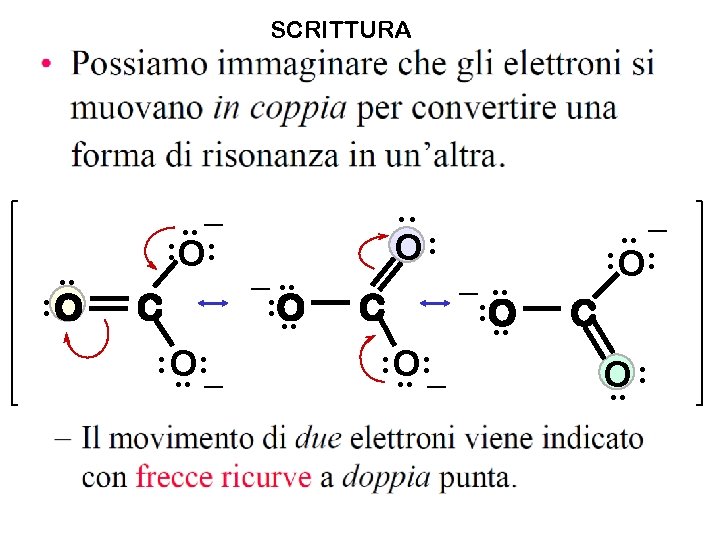
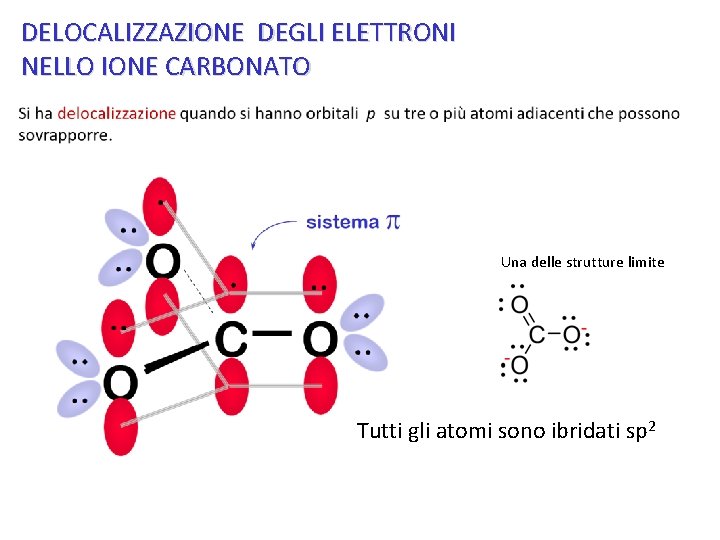
DELOCALIZZAZIONE DEGLI ELETTRONI NELLO IONE CARBONATO Una delle strutture limite Tutti gli atomi sono ibridati sp 2
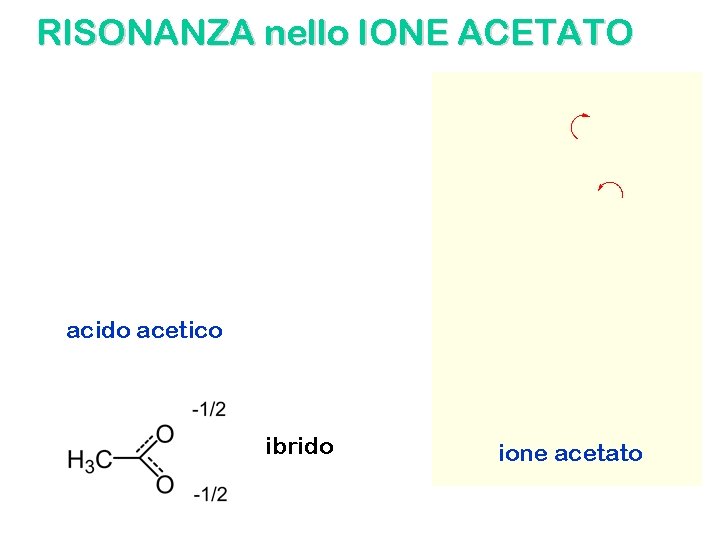
RISONANZA nello IONE ACETATO acido acetico ibrido ione acetato
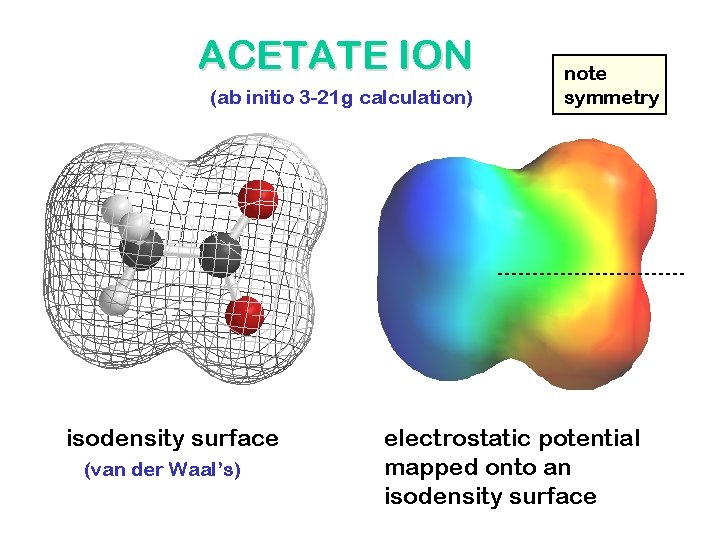
ACETATE ION (ab initio 3 -21 g calculation) isodensity surface (van der Waal’s) note symmetry electrostatic potential mapped onto an isodensity surface
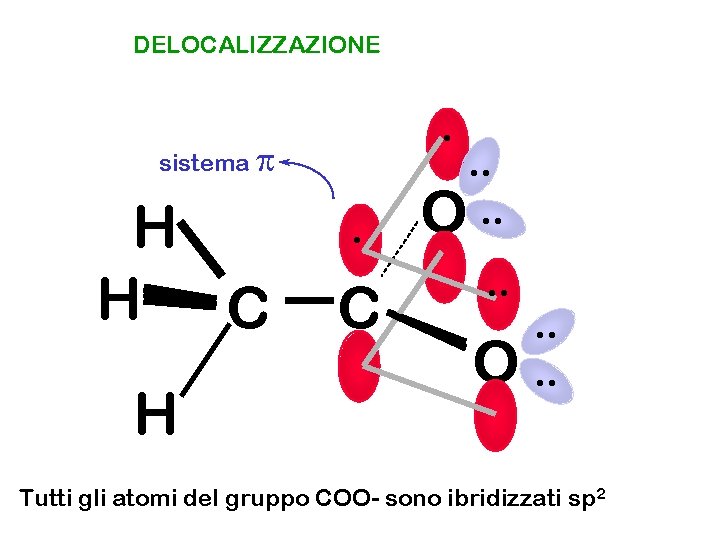
DELOCALIZZAZIONE . sistema p H H C H . C . . O. . O . . Tutti gli atomi del gruppo COO- sono ibridizzati sp 2

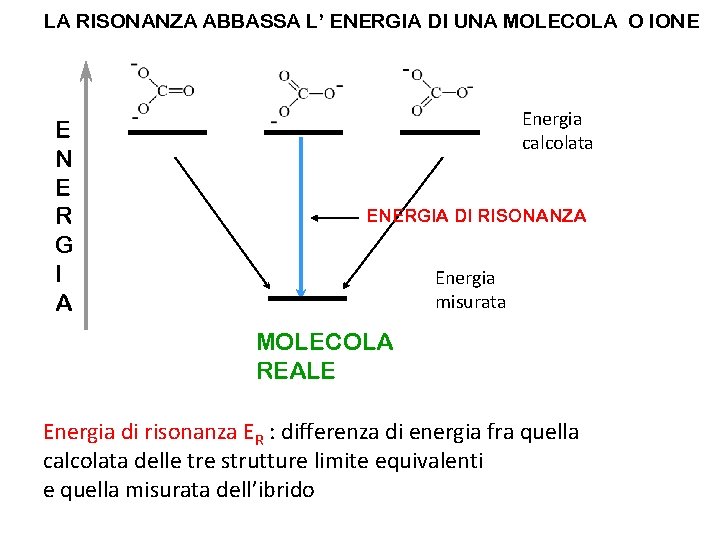
LA RISONANZA ABBASSA L’ ENERGIA DI UNA MOLECOLA O IONE E N E R G I A Energia calcolata ENERGIA DI RISONANZA Energia misurata MOLECOLA REALE Energia di risonanza ER : differenza di energia fra quella calcolata delle tre strutture limite equivalenti e quella misurata dell’ibrido


Si ha risonanza quando una molecola può essere rappresentata da due o più strutture, dette STRUTTURE LIMITE , che si differenziano soltanto per la distribuzione elettronica, ma che hanno la stessa disposizione degli atomi. La molecola reale è un IBRIDO di tutte queste strutture, ognuna delle quali contribuisce all’ ibrido, ma nessuna delle quali lo rappresenta compiutamente L’ ibrido di risonanza è più stabile di ognuna delle strutture limite che vi contribuiscono. Il contributo di ogni struttura all’ ibrido dipende dalla sua stabilità. La struttura più stabile è quella che contribuisce di più all’ ibrido
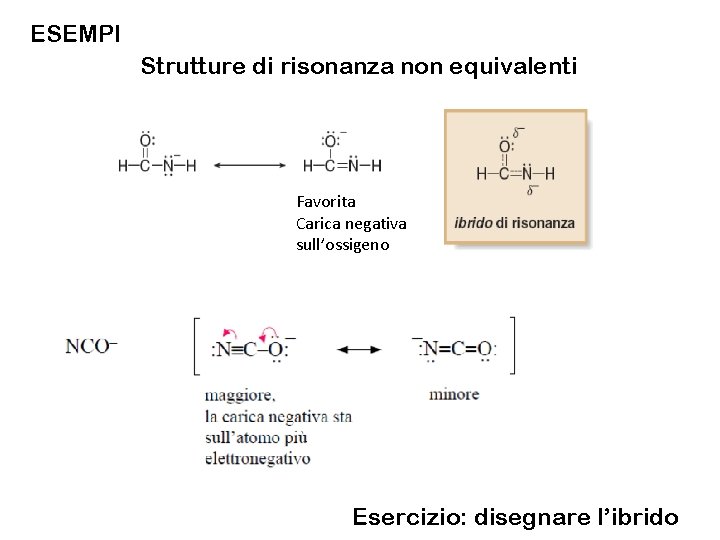
ESEMPI Strutture di risonanza non equivalenti Favorita Carica negativa sull’ossigeno Esercizio: disegnare l’ibrido
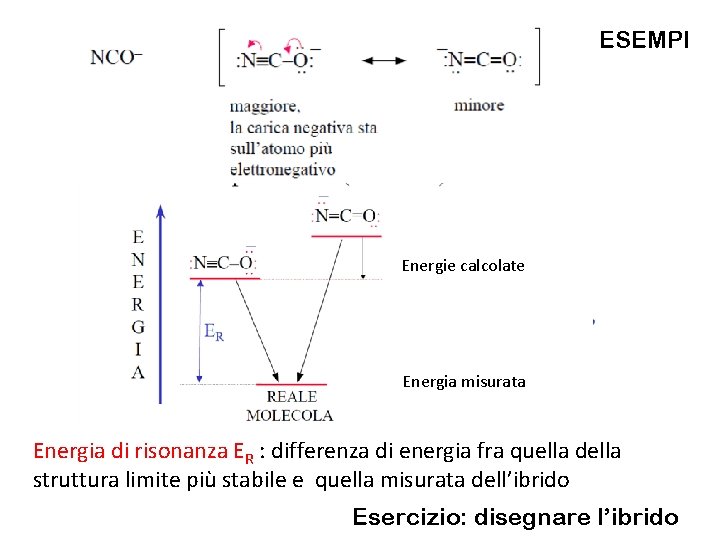
ESEMPI Energie calcolate Energia misurata Energia di risonanza ER : differenza di energia fra quella della struttura limite più stabile e quella misurata dell’ibrido Esercizio: disegnare l’ibrido

Riconoscere i sistemi descritti da forme di risonanza
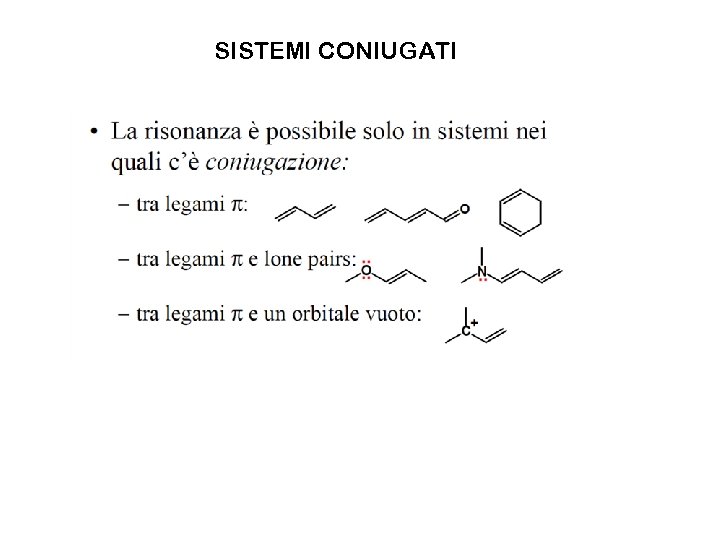
SISTEMI CONIUGATI
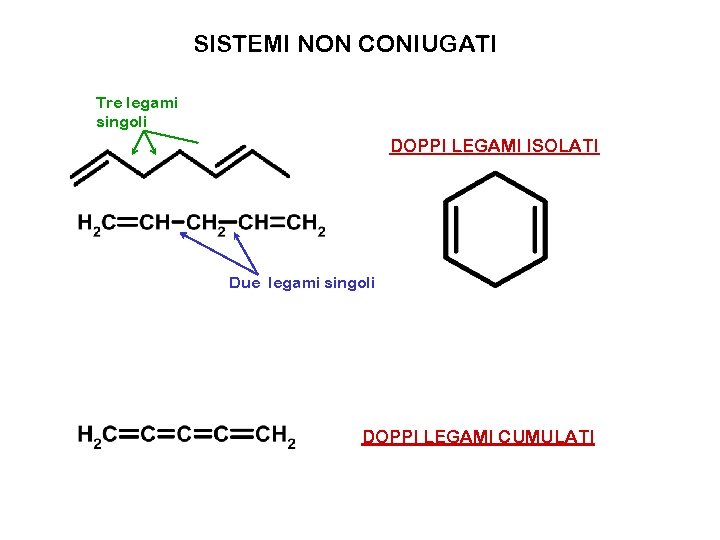
SISTEMI NON CONIUGATI Tre legami singoli DOPPI LEGAMI ISOLATI Due legami singoli DOPPI LEGAMI CUMULATI
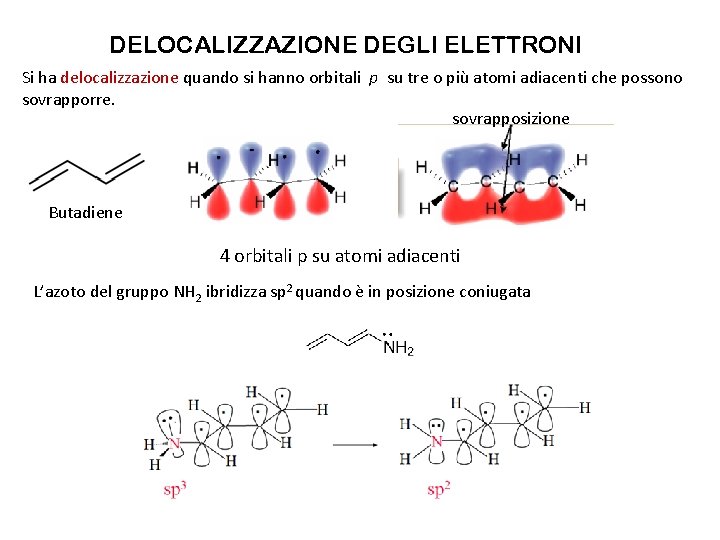
DELOCALIZZAZIONE DEGLI ELETTRONI Si ha delocalizzazione quando si hanno orbitali p su tre o più atomi adiacenti che possono sovrapporre. sovrapposizione Butadiene 4 orbitali p su atomi adiacenti L’azoto del gruppo NH 2 ibridizza sp 2 quando è in posizione coniugata
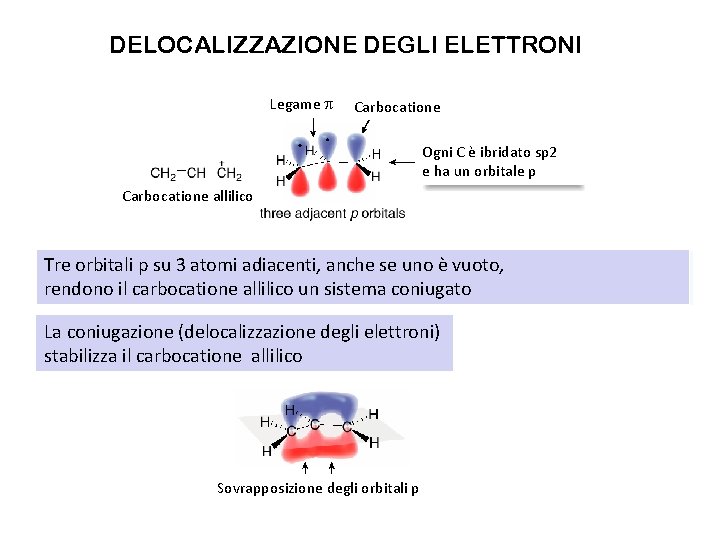
DELOCALIZZAZIONE DEGLI ELETTRONI Legame p Carbocatione Ogni C è ibridato sp 2 e ha un orbitale p Carbocatione allilico Tre orbitali p su 3 atomi adiacenti, anche se uno è vuoto, rendono il carbocatione allilico un sistema coniugato La coniugazione (delocalizzazione degli elettroni) stabilizza il carbocatione allilico Sovrapposizione degli orbitali p

Sistemi descritti da forme di risonanza Sistema «allilico» Doppi legami coniugati
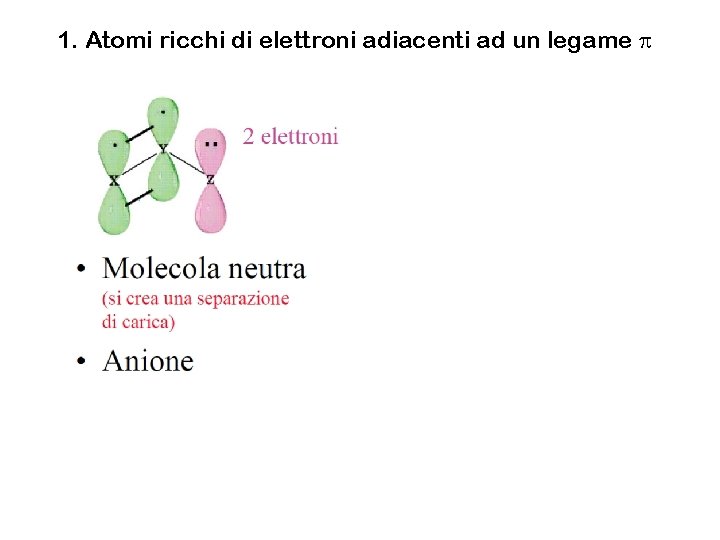
1. Atomi ricchi di elettroni adiacenti ad un legame p
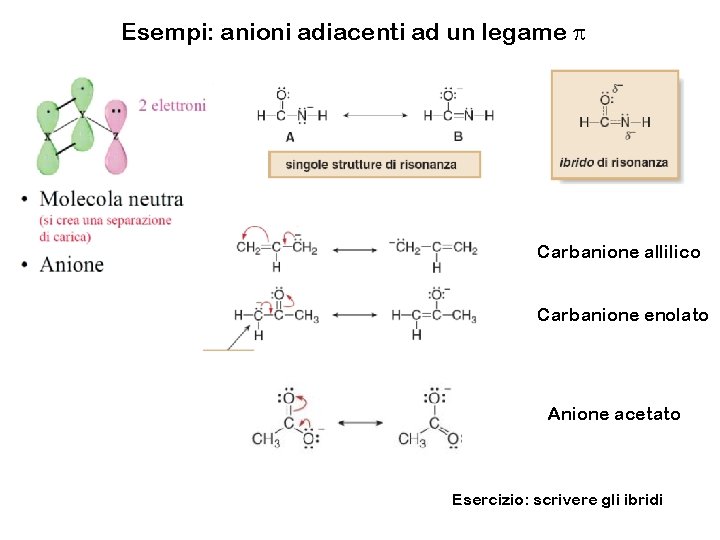
Esempi: anioni adiacenti ad un legame p Carbanione allilico Carbanione enolato Anione acetato Esercizio: scrivere gli ibridi
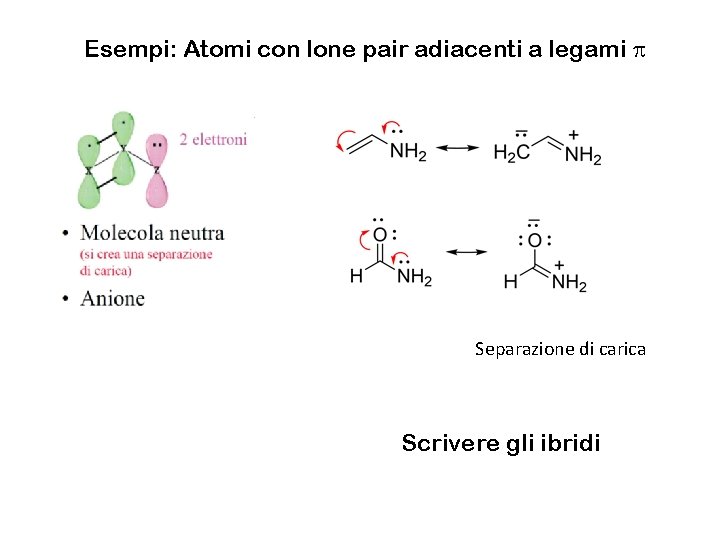
Esempi: Atomi con lone pair adiacenti a legami p Separazione di carica Scrivere gli ibridi
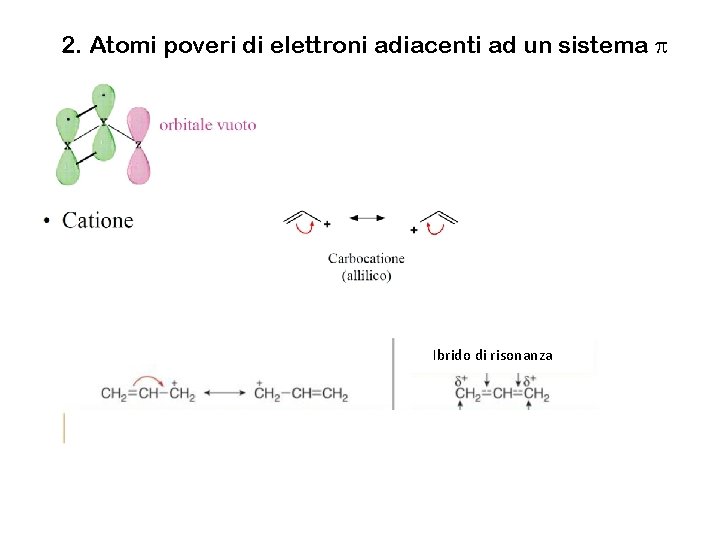
2. Atomi poveri di elettroni adiacenti ad un sistema p Ibrido di risonanza
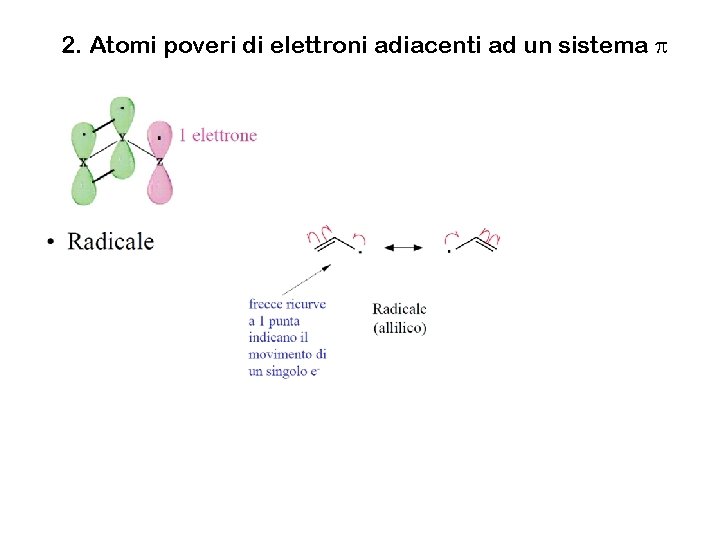
2. Atomi poveri di elettroni adiacenti ad un sistema p
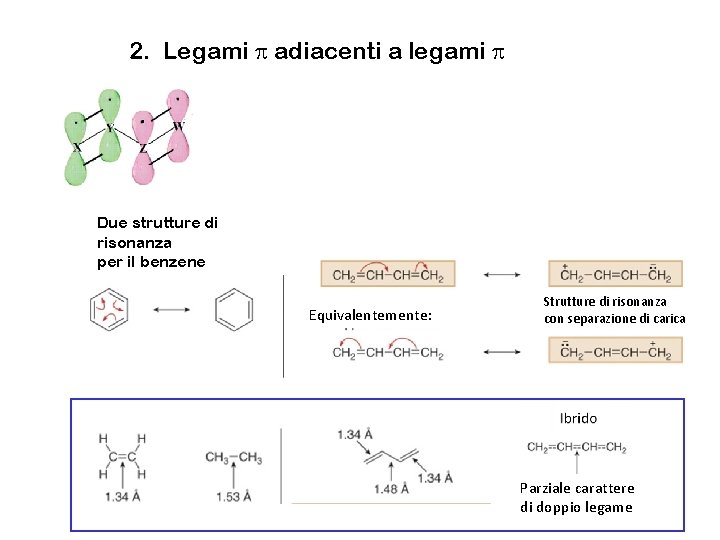
2. Legami p adiacenti a legami p Due strutture di risonanza per il benzene Equivalentemente: Strutture di risonanza con separazione di carica Parziale carattere di doppio legame
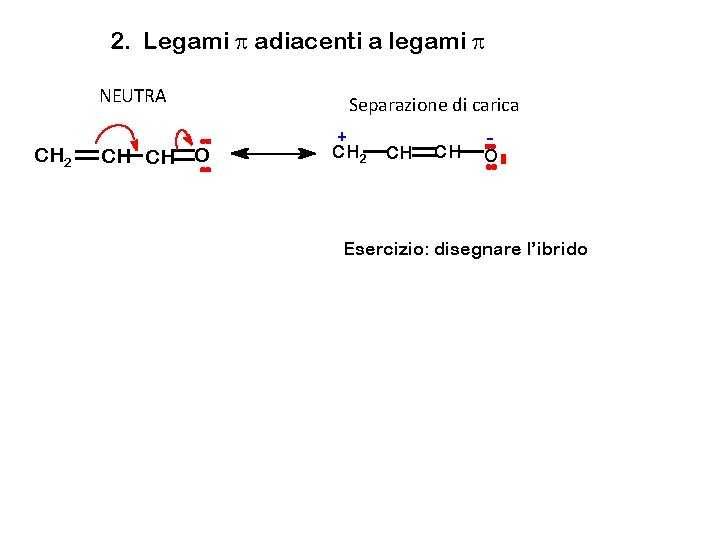
2. Legami p adiacenti a legami p NEUTRA CH 2 CH CH O Separazione di carica + CH 2 CH CH - O Esercizio: disegnare l’ibrido
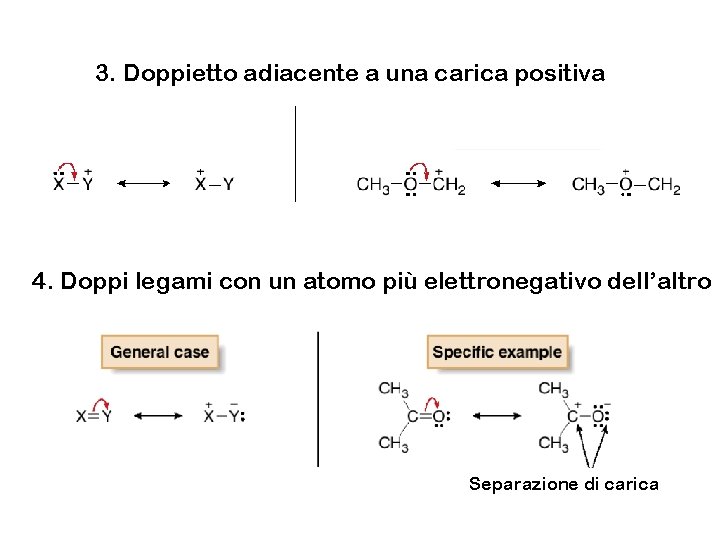
3. Doppietto adiacente a una carica positiva 4. Doppi legami con un atomo più elettronegativo dell’altro Separazione di carica
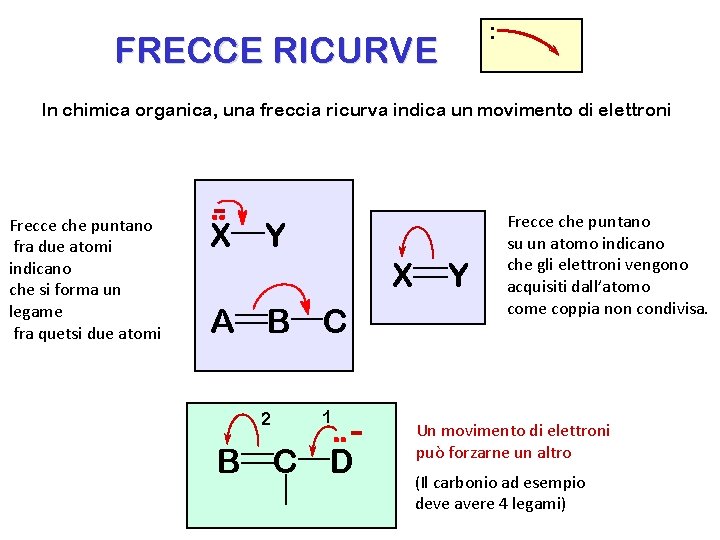
: FRECCE RICURVE In chimica organica, una freccia ricurva indica un movimento di elettroni Frecce che puntano fra due atomi indicano che si forma un legame fra quetsi due atomi - X Y X A B C 2 1 - B C D Y Frecce che puntano su un atomo indicano che gli elettroni vengono acquisiti dall’atomo come coppia non condivisa. Un movimento di elettroni può forzarne un altro (Il carbonio ad esempio deve avere 4 legami)





EFFETTI DELLA RISONANZA ACIDITA’
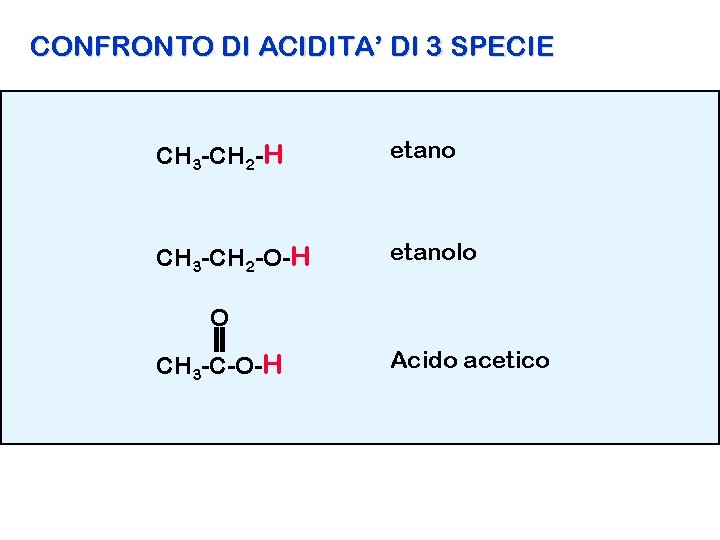
CONFRONTO DI ACIDITA’ DI 3 SPECIE CH 3 -CH 2 -H etano CH 3 -CH 2 -O-H etanolo O CH 3 -C-O-H Acido acetico
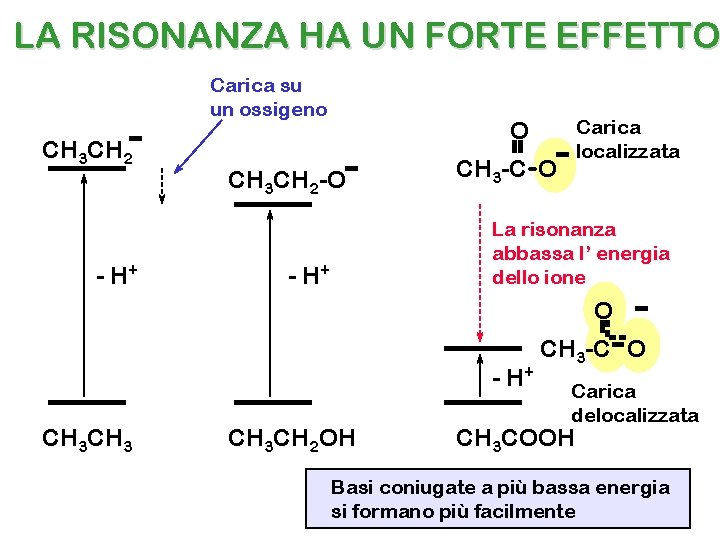
LA RISONANZA HA UN FORTE EFFETTO Carica su un ossigeno CH 3 CH 2 - H+ Carica localizzata O CH 3 CH 2 -O CH 3 -C-O La risonanza abbassa l’ energia dello ione - H+ O - H+ CH 3 CH 2 OH CH 3 -C O Carica delocalizzata CH 3 COOH Basi coniugate a più bassa energia si formano più facilmente

- Slides: 39