RESONANCIA MAGNTICA NUCLEAR Mriam Onrubia Laura Plaza Patricia

RESONANCIA MAGNÉTICA NUCLEAR Míriam Onrubia Laura Plaza Patricia Resa

Resonancia Magnética Nuclear La RMN es un fenómeno que ocurre cuando el núcleo de ciertos átomos inmersos en un campo magnético estático, son expuestos a un segundo campo magnético. 1 H, 13 C, 15 N, 31 P

Características RMN Uso de muestras no cristalizadas estructura en solución Posibilidad de aplicar a moléculas sin cristales disponibles. Amplio rango de condiciones experimentales PDB: 16% de proteínas determinadas por RMN Determinación de estructuras de tamaño limitado (3540 KDa)

Mecánica Clásica y Cuántica µ = momento magnético dipolar B = Campo magnético e = carga del em = massa del átomo o e. L = Σ momentos angulares γ = cte giromagnética M = magnetización ml = momento angular de spin

Mecánica Cuántica Niveles cuánticos de la energía en B 0: DE
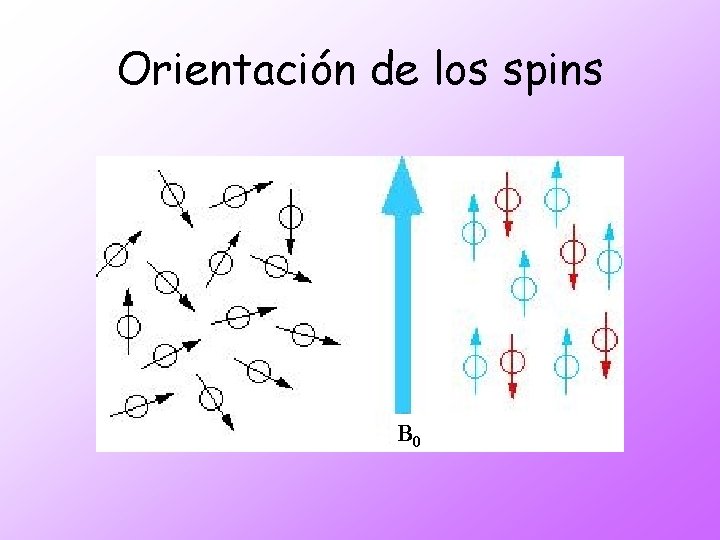
Orientación de los spins B 0

Población de niveles energéticos Frecuencia de Larmor Nα > Nβ
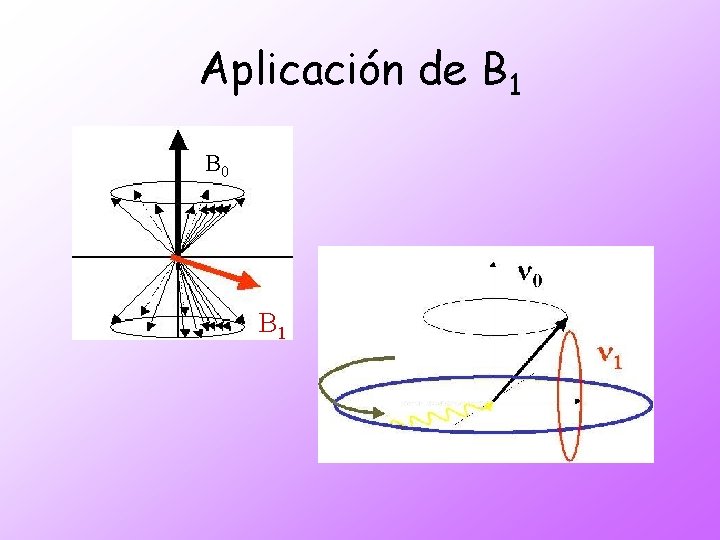
Aplicación de B 1 B 0 B 1

Relajación

Ecuaciones de Bloch ¶L T = = M x B ¶t ¶L ¶M = γT = γ (M x B) ¶t ¶t

Ecuaciones de Bloch Soluciones
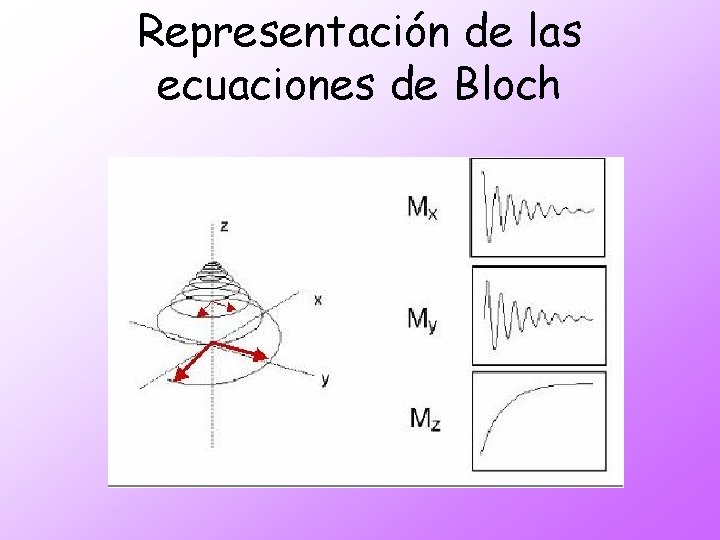
Representación de las ecuaciones de Bloch

Ecuaciones de Bloch Soluciones
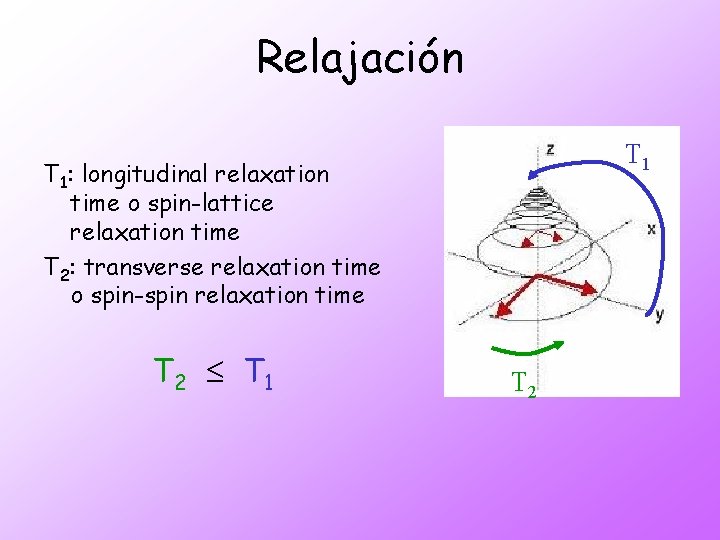
Relajación T 1: longitudinal relaxation time o spin-lattice relaxation time T 2: transverse relaxation time o spin-spin relaxation time T 2 T 1 T 2
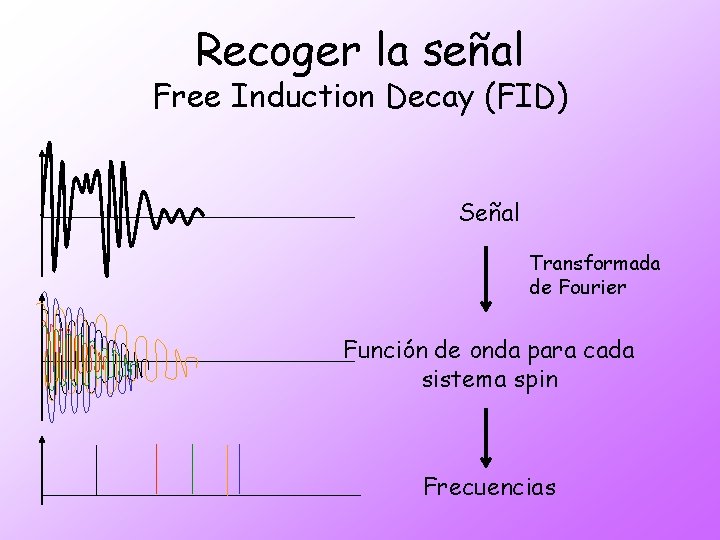
Recoger la señal Free Induction Decay (FID) Señal Transformada de Fourier Función de onda para cada sistema spin Frecuencias
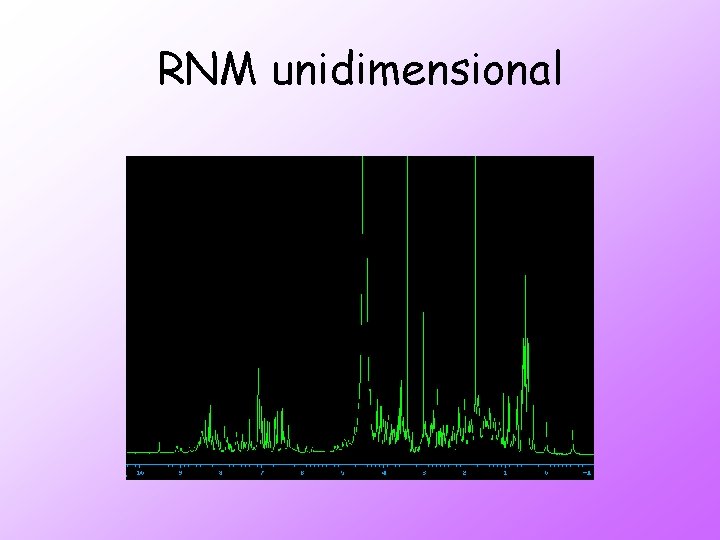
RNM unidimensional

Determinación estructural de proteínas para RMN Proteínas pequeñas (< 10 k. Da) – RMN bidimensional basada en experimentos de 1 H – La estructura se puede obtener sin necesidad de enriquecimiento isotópico. Proteínas pequeñas-medianas (< 20 k. Da) – Marcaje isotópico (15 N i 13 C) – Experimentos de RMN multidimensionales (3 D) de triple resonancia (1 H/13 C/15 N) Proteínas grandes (> 20 k. Da) – Marcaje isotópico (15 N i 13 C) + deuteración (50%-70% 2 H) – Experimentos de RMN multidimensionales (3 D i 4 D) de triple resonancia (1 H/13 C/15 N) sofisticados

RMN bidimensional 1. Obtención de los espectros de COSY, TOCSY y NOESY. 2. Asignación : determinar que Aa hay en los espectros 3. Determinación de las distancias entre Aa 4. Reconstrucción 3 D
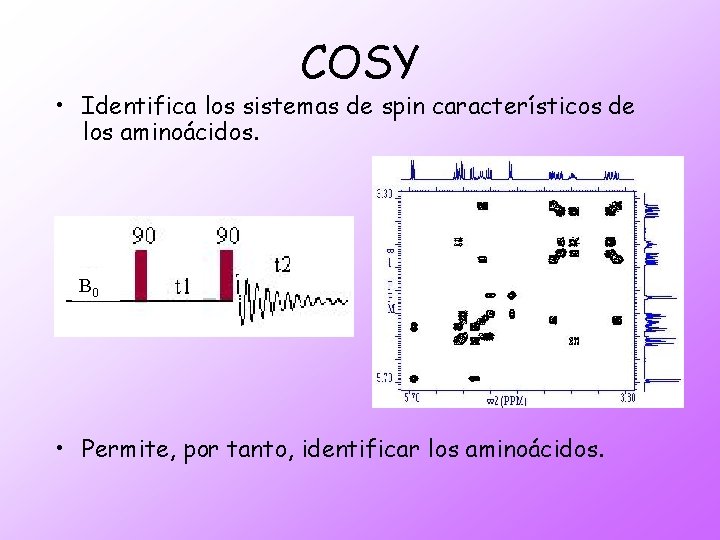
COSY • Identifica los sistemas de spin característicos de los aminoácidos. B 0 • Permite, por tanto, identificar los aminoácidos.
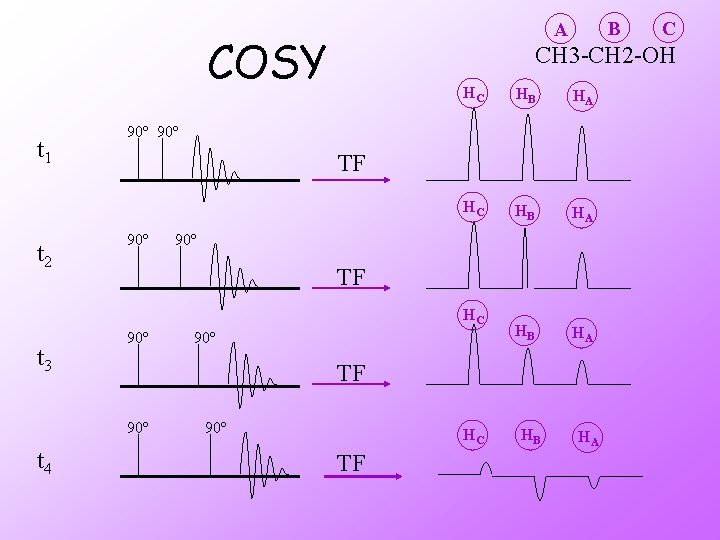
COSY t 1 t 2 HC HB HA 90º 90º TF 90º t 4 90º TF 90º C CH 3 -CH 2 -OH HC t 3 B A 90º HC TF HB HA
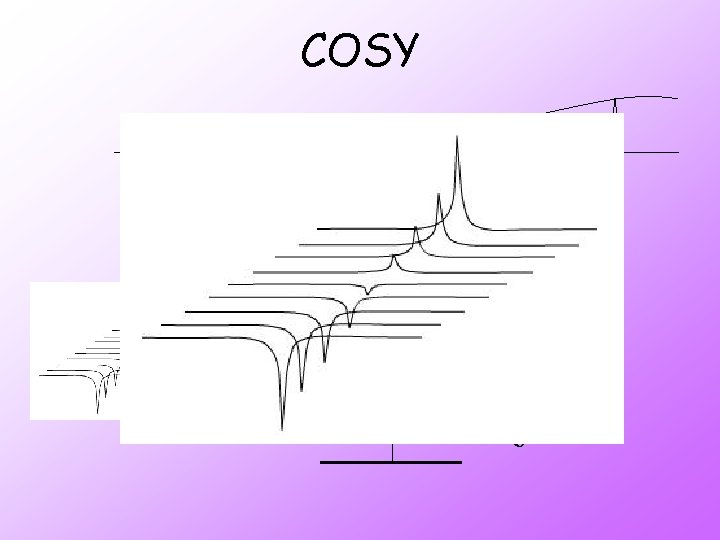
COSY Tiempo de evolución (t 1) Transformada de Fourier υ

t 1 t 2 1ª transformada de Fourier 2ª transformada de Fourier t 3 t 4

NOESY • Técnica para correlacionar núcleos en el espacio que se encuentran a una distancia menor de 5Å. • La diferencia entre los espectros con y sin efecto NOE da lugar al espectro NOESY. Cuanto mayor es el efecto menor es la distancia. B 0 • Permite la identificación de la posición específica de cada aminoácido en la secuencia.

Efecto NOE: Nuclear Overhauser Effect La irradiación sobre un núcleo produce variaciones en la resonancia en los núcleos vecinos. Condiciones: • distancia < 5Å • Saturación de la resonancia

RMN bidimensional 1. Obtención de los espectros de COSY, TOCSY y NOESY. 2. Asignación : determinar que Aa hay en los espectros 3. Determinación de las distancias entre Aa 4. Reconstrucción 3 D

Asignación Identificar tipos de Aa en COSY y TOCSY Identificar en NOESY los Aa de la secuencia Desplazamientos químicos en COSY

Asignación de los sistemas de spin de los Aa
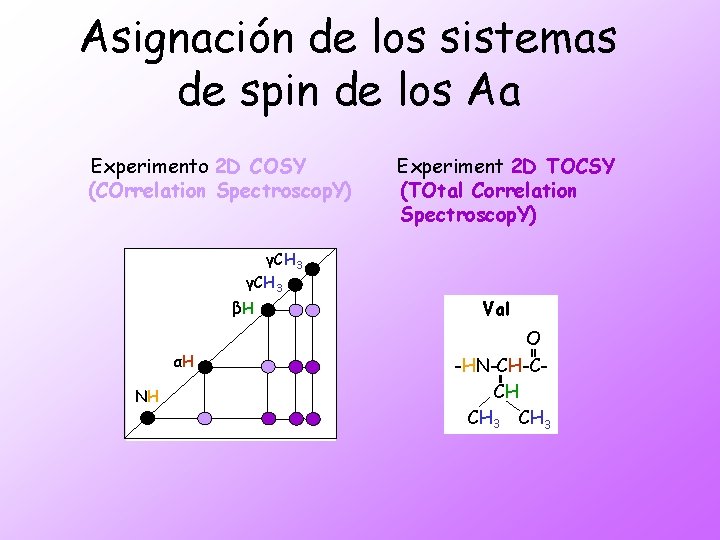
Asignación de los sistemas de spin de los Aa Experimento 2 D COSY (COrrelation Spectroscop. Y) γCH 3 βH αH NH Experiment 2 D TOCSY (TOtal Correlation Spectroscop. Y) Val O -HN-CH-CCH CH 3
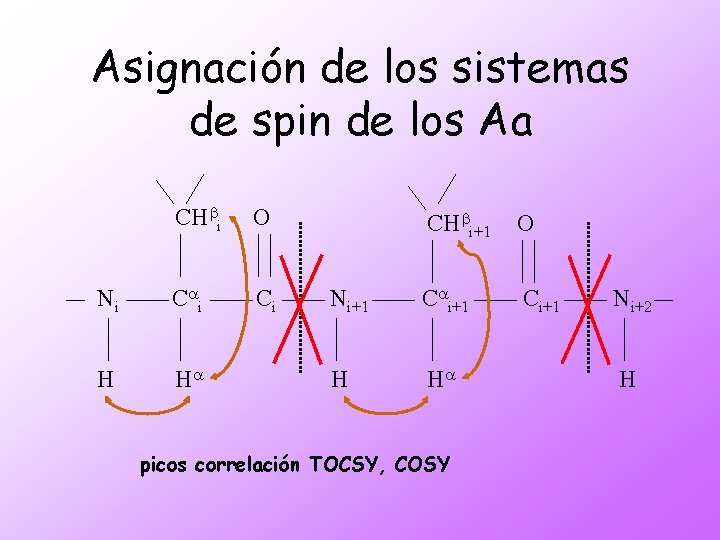
Asignación de los sistemas de spin de los Aa CHbi O Ni C ai Ci H Ha CHbi+1 O Ni+1 Cai+1 Ci+1 H Ha picos correlación TOCSY, COSY Ni+2 H

Asignación de los sistemas de spin de los Aa
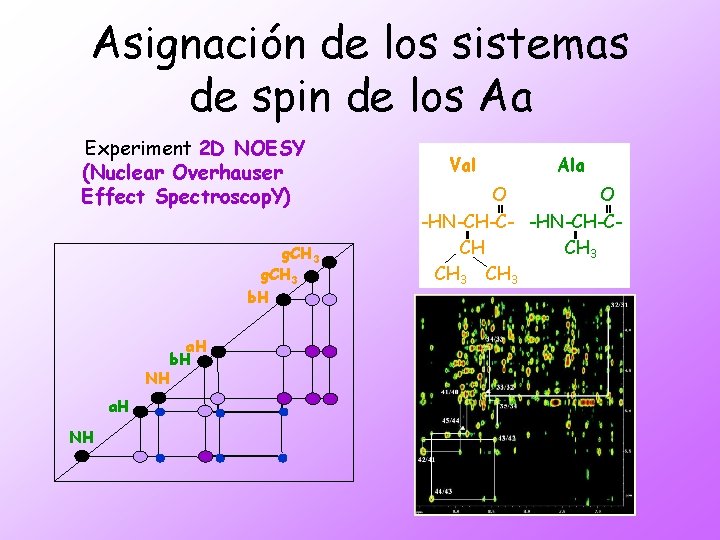
Asignación de los sistemas de spin de los Aa Experiment 2 D NOESY (Nuclear Overhauser Effect Spectroscop. Y) g. CH 3 b. H a. H b. H NH a. H NH Val Ala O O -HN-CH-C- -HN-CH-CCH 3
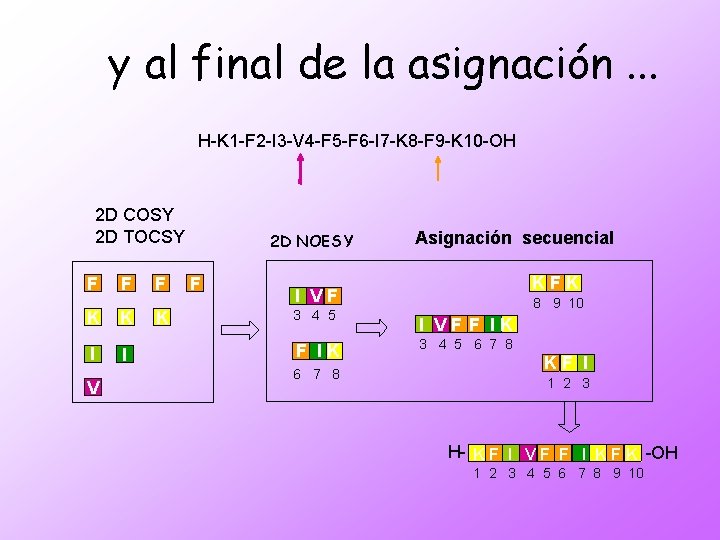
y al final de la asignación. . . H-K 1 -F 2 -I 3 -V 4 -F 5 -F 6 -I 7 -K 8 -F 9 -K 10 -OH 2 D COSY 2 D TOCSY F F K K I I V F K 2 D NOESY F Asignación secuencial KFK I VF 3 4 5 F IK 6 7 8 8 9 10 I VF F IK 3 4 5 6 7 8 KF I 1 2 3 H- K F I V F F I K F K -OH 1 2 3 4 5 6 7 8 9 10

RMN bidimensional 1. Obtención de los espectros de COSY, TOCSY y NOESY. 2. Asignación : determinar que Aa hay en los espectros 3. Determinación de las distancias entre Aa 4. Reconstrucción 3 D

Determinación de las distancias entre Aa NOE distancias NOEs intensos: NOEs medios: NOEs débiles: 1. 8 < r. HH < 2. 8 Å 1. 8 < r. HH < 3. 5 Å 1. 8 < r. HH < 5 Å H H H

RMN bidimensional 1. Obtención de los espectros de COSY, TOCSY y NOESY. 2. Asignación : determinar que Aa hay en los espectros 3. Determinación de las distancias entre Aa 4. Reconstrucción 3 D

Reconstrucción 3 D ángulos diedros puentes disulfuro límites de distancias entre 1 H Secuencia proteína Longitudes y ángulos de enlace geometría covalente restricciones experimentales Coordenadas De los átomos de la proteína Estructura 3 D quiralidad, planaridad Interacciones no covalentes: van der Waals, electrostáticas, enlaces d’H
Estructura de proteínas enlace
Estructura de proteínas ángulo enlace
Estructura de proteínas dihedro ángulo enlace
Estructura de proteínas dihedro ángulo enlace van der Waals
Estructura de proteínas dihedro ángulo enlace + - electrostático van der Waals
Estructura de proteínas dihedro ángulo enlace puente de hidrógeno + - electrostático van der Waals

Estructura de proteínas NOE dihedro ángulo enlace puente de hidrógeno + - electrostático van der Waals


Fin de la presentación, haga click si tiene dudas

Parámetros espectrales con información sobre la estructura secundaria de la proteína 1. NOE 2. Constantes de acoplamiento (J) 3. Desplazamientos químicos (δ) 4. Velocidades de intercambio H 5. Coeficientes de temperatura D
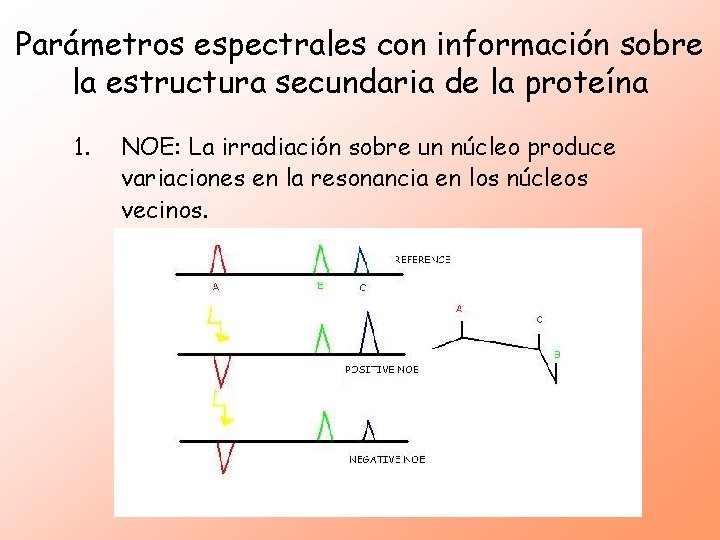
Parámetros espectrales con información sobre la estructura secundaria de la proteína 1. NOE: La irradiación sobre un núcleo produce variaciones en la resonancia en los núcleos vecinos. Condiciones: • distancia < 5Å • Saturación de la resonancia para igualar estados alfa y beta. Es el método de elucidación de características estructurales en 3 D y estereoquímica, usando RMN junto con información de los acoplamientos escalares spin-spin.
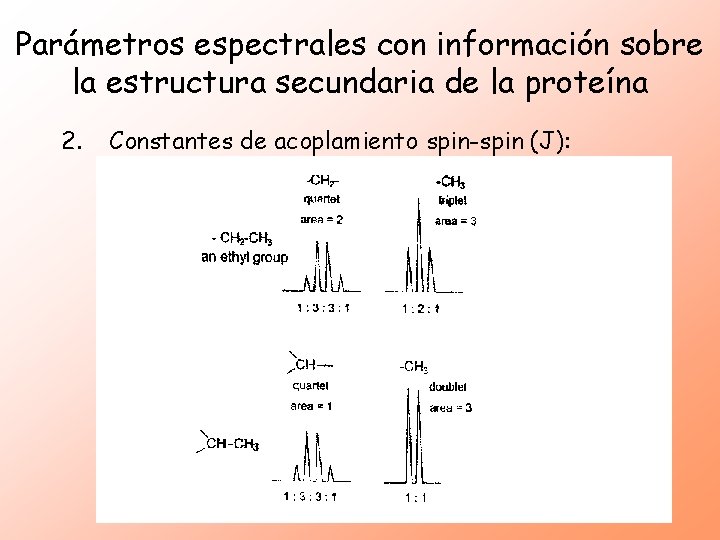
Parámetros espectrales con información sobre la estructura secundaria de la proteína 2. Constantes de acoplamiento spin-spin (J): Las interacciones escalares entre núcleos unidos a través de un pequeño número de enlaces covalentes causan desacoplamiento en las señales de RMN. Dependen de la geometría de los enlaces que unen los spins nucleares.
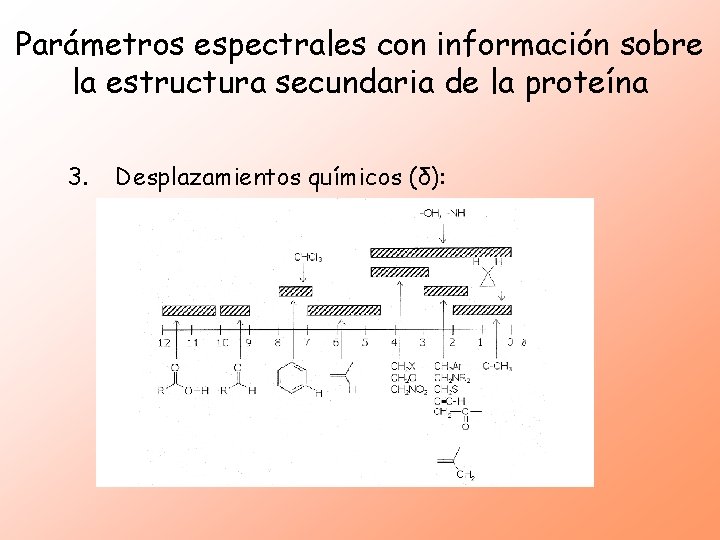
Parámetros espectrales con información sobre la estructura secundaria de la proteína 3. Desplazamientos químicos (δ): Los diferentes protones de una molécula presentan frecuencias de resonancia característica en función de su entorno químico.

Parámetros espectrales con información sobre la estructura secundaria de la proteína 4. Velocidades de intercambio 1 H 5. Coeficientes de temperatura: permite saber si se forman puentes de hidrógeno intramoleculares. 2 H:

1. Cita las características más importantes de la técnica RMN y su definición. La RMN es un fenómeno q ocurre cuando el núcleo de ciertos átomos inmersos en un campo magnético estático, son expuestos a un segundo campo magnético. Solo sufren este fenómeno los núcleos que tiene la propiedad llamada SPIN. Núcleos q tienen esta propiedad de spin son 1 H, 13 C, 15 N. Solo los q tienen spin distinto de 0 son detectables por RMN. Características: - Las estructuras a estudiar están en solución, como suelen estar en su medio habitual. - Posibilidad de aplicar a moléculas sin cristales disponibles. - Amplio rango de condiciones experimentales. Esto permite aumentar las posibilidades de estudios comparativos en soluciones de condiciones naturales o desnaturalizantes. - También se pueden estudiar con esta técnica proteínas no solubles: con RMN sólido o con micelas. (para por ejemplo el estudio de prot. Transmembrana). - PDB: 16% de proteínas determinadas por RMN - Determinación de estructuras de tamaño limitado (35 -40 KDa)

2. ¿En que consiste el efecto NOE y que aplicaciones podemos encontrarle? Efecto NOE: la saturación de un sistema spin mediante irradiación producirá variaciones en la señal emitida por los sistemas spin vecinos. Se basa en saturar uno de los sistemas spin de la muestra. Si seguimos irradiando este sistema spin concreto durante un periodo de tiempo más largo, este no puede absorber esta energía de más y la cede a los sistema spin vecinos situados a menos de 5 amstrongs que sí podrán absorber esta energía. Comparando las frecuencias obtenidas habiendo producido o no efecto NOE, podremos deducir que sistemas spin están a 5 amstrongs o menos de distancia. Aplicaciones Experimento NOESY: Nos permite comparar espectros obtenidos habiendo producido el efecto NOE y sin producirlo, de manera que podemos comparar que sistemas de spin quedan afectados por otros sistemas de spin cercanos. Teniendo en cuenta que cada aminoácido tienen un sistema de spin característico, podemos relacionar sistemas spins vecinos separados por enlaces peptídicos ( doble enlace), es decir, podemos relacionar aminoácidos vecinos. Esto nos permite conocer la secuencia de una proteína.

• • • 1. 2. 3. 4. • • • • PEM: 1. Señala les opciones correctas: a) Solo los átomos con sistema de spin diferente de 0 son detectables por RMN. b) Tienen propiedad de spin los átomos con un número de electrones impar y/o con un número de neutrones impar. c) Las dos anteriores son correctas. d) Cualquier tipo de átomo presenta propiedad de spin. e) Todas las anteriores son correctas. 2. Señala las verdaderas. Sobre RMN (Resonancia Magnético Nuclear). . . Una de las principales ventajas del RMN es que no es necesario cristalizar la molécula en estudio. Se pueden hacer RMN en medio sólido. El hecho de que se puedan hacer RMN con micelas, permite el estudio de proteínas transmembrana en un medio similar al que se encuentran en condiciones normales. Uno de los principales inconvenientes es que el tamaño de las proteínas que se pueden estudiar es limitado. a) 1, 2 i 3 b) 1 i 3 c) 2 i 4 d) 4. e) 1, 2, 3 i 4 3. ¿Cuál de estas es una característica de la RMN? indica la opción correcta: a) Las muestras deben estar cristalizadas. b) Las condiciones experimentales vienen muy detalladas y las condiciones son muy limitadas. c) Es posible para cualquier tipo de moléculas sin importar el tamaño. d) Se pueden utilizar micelas para proteínas no solubles. e) Ninguna de las anteriores es una característica del RMN.

• • • • • • • 4. Indica la opción correcta. El RMN unidimensional nos sirve para. . . a) Determinar si existe mucho solapamiento entre frecuencias, indicando si debemos hacer RMN 3 D. b) Se usa como indicativo de la calidad que tendrá el estudio en 2 D. c) Indica frecuencias y su posición depende del desplazamiento químico. d) Todas las anteriores son correctas. e) Ninguna de las anteriores es correcta. 5. Señala la afirmación incorrecta: a) Las ecuaciones de Bloch describen la relajación del sistema de spin al dejar de aplicar el segundo campo magnético b) La frecuencia a la que precesan (giran) los sistemas de spin es completamente irrelevante. c) El nivel energético en el que se encuentre un átomo sometido a una campo magnético depende del momento angular de spin. d) El momento magnético bipolar ( ) es directamente proporcional a la carga e inversamente proporcional a la masa. e) Todas las anteriores son correctas. 6. Señala las verdaderas. Sobre RMN (Ressonància Magnètico Nuclear). . . 1. El experimento COSY permite ver interacciones entre sistemas de spin de distintos Aminoácidos. 2. El experimento NOESY permite ver interacciones entre sistemas de spin de distintos Aminoácidos. 3. El experimento COSY permite ver interacciones entre sistemas de spin alejados más de 5 amstrongs. 4. El experimento NOESY permite ver interacciones entre sistemas de spin separados por un doble enlace. a) 1, 2 i 3 b) 1 i 3 c) 2 i 4 d) 4 e) 1, 2, 3 i 4

• • • • • • • 7. Indica las verdaderas. a) Un experimento NOESY proporciona más información que uno COSY. b) El primer paso del análisis de los resultados de los experimentos de RMN es la asignación ( saber cada sistema de spin a que aminoácido corresponde). c) Las dos anteriores son correctas. d) El experimento NOESY nos proporciona las restricciones de distancia entre amnoácidos, de manera que es el que realmente nos da la información sobre la estructura secundaria y terciaria de la proteína. e) Todas las anteriores son correctas. 8. En el experimento NOESY: 1. Dado que las proteínas tienen cierto movimiento en solución, las distancias no van a ser números exactos 2. La lista de distancias obtenidas con un NOESY va a ser esencial para hacer la reconstrucción 3 D. 3. Se utilizan una serie de rangos para definir las distancias entre sistemas de spin, el mínimo de los cuales coincide con la suma de los radios de las fuerzas de Van der Wals. 4. Cuanto más intenso sea el pico obtenido en un espectro NOESY, más lejos están los aminoácidos implicados. a) 1, 2 i 3 b) 1 i 3 c) 2 i 4 d) 4 e) 1, 2, 3 i 4 9. ¿Qué información no va a utilizar el ordenador para hacer la reconstrucción 3 D? a) La geometría covalente (longitudes y ángulos de enlace, quiralidad y polaridad). b) La secuencia de la proteína. c) Una lista con el número de aminoácidos de cada tipo obtenida con el TOCSY. d) Las interacciones no covalentes (fuerzas de Van der Wals, enlaces de H. . . ) e) Los límites de distancias obtenidos con el NOESY.

• • • • 10. En cuanto a la asignación en RMN: 1. Con los espectros de COSY identificaremos qué y cuántos aminoácidos hay en nuestra proteína problema. 2. El NOESY nos permitirá determinar los aminoácidos vecinos por estructura y por secuencia. 3. El NOESY es útil para distinguir entre hélices alfa y beta. 4. Cada aminoácido tiene una distribución de picos característica en un espectro COSY. a) 1, 2 i 3 b) 1 i 3 c) 2 i 4 d) 4. e) 1, 2, 3 i 4
- Slides: 56