Resistenz von Mikroorganismen M Kresken 1 AntibiotikaResistenz Resistenz

Resistenz von Mikroorganismen M. Kresken 1

Antibiotika-Resistenz Ø Resistenz ist ein natürliches Phänomen. Ø Einige Erreger sind natürlicherweise gegen bestimmte Antibiotikaklassen resistent. Ø Alle Bakterien haben die Fähigkeit, Resistenzen zu entwickeln oder zu erwerben. Ø Der Gebrauch von Antibiotika erzeugt einen selektiven Druck, der die Resistenzausbreitung begünstigt. M. Kresken 2

Der Multiplikatoreffekt Antibiotika-Gebrauch verstärkt die Selektion resistenter Stämme erhöht das Risiko, dass Patienten sich mit resistenten Stämmen infizieren x Ausbreitung der resistenten Stämme von einem Menschen zu anderen multipliziert die Resistenz M. Kresken 3
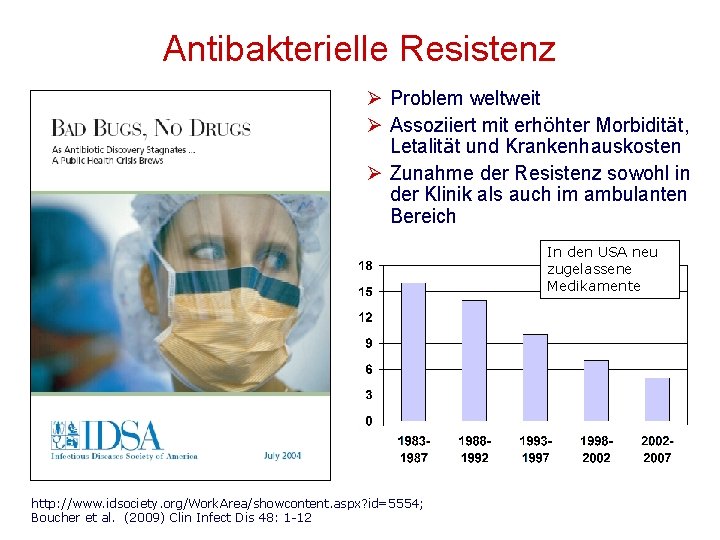
Antibakterielle Resistenz Ø Problem weltweit Ø Assoziiert mit erhöhter Morbidität, Letalität und Krankenhauskosten Ø Zunahme der Resistenz sowohl in der Klinik als auch im ambulanten Bereich In den USA neu zugelassene Medikamente http: //www. idsociety. org/Work. Area/showcontent. aspx? id=5554; Boucher et al. (2009) Clin Infect Dis 48: 1 -12

M. Kresken 5
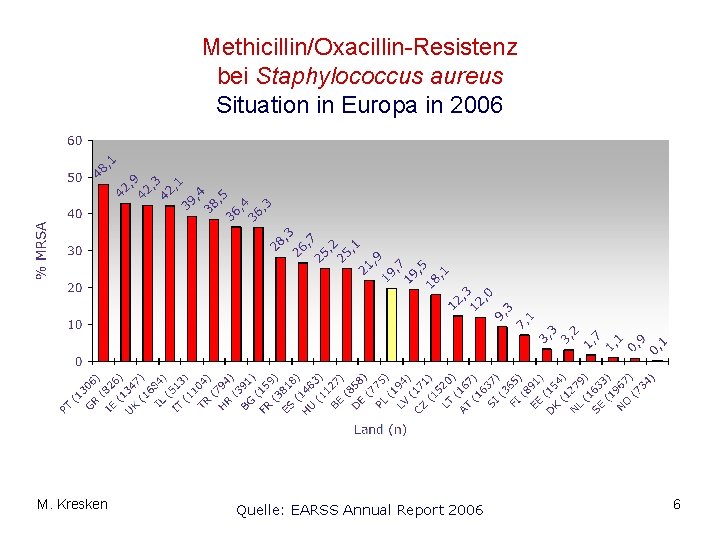
Methicillin/Oxacillin-Resistenz bei Staphylococcus aureus Situation in Europa in 2006 M. Kresken Quelle: EARSS Annual Report 2006 6

PEG-Resistenzstudie Ø Longitudinalstudie seit 1975 Ø 20 bis 30 Labore in Deutschland, Schweiz und Österreich (vorwiegend an Krankenhäusern der Maximalversorgung) Ø 200 klinische Isolate / Labor Ø Enterobacteriaceae, Pseudomonas aeruginosa, Staphylokokken, Enterokokken Ø Einheitliche Methodik der Identifizierung der Bakterienstämme und Empfindlichkeitsprüfung (Bestimmung von MHK-Werten) M. Kresken 7

PEG-Resistenzstudie Trends der Resistenzentwicklung Ø Zeitraum 1975 bis Mitte der 80 er Jahre Þ unveränderte Resistenzlage oder rückläufige Tendenz bei den meisten Bakteriengruppen Ø Zeitraum Mitte der 80 er Jahre bis 2004 Þ bei den meisten Bakteriengruppen Zunahme der Resistenz gegenüber vielen Antibiotika M. Kresken 8

Resistenzentwicklung bei E. coli gegen Ampicillin PEG-Resistenzstudie, 1975 -2007 Anstieg 1984 -2007: ~1, 4%/Jahr n 987 1129 1344 1573 1401 1381 520 381 834 431 1323 783 619 745 648 M. Kresken 9

Risiko - Konstellation Ø Zahlreiche Faktoren begünstigen das Auftreten von resistenten Bakterien Ø Wichtigste Faktoren sind: - Existenz von Resistenzgenen - Ausmaß des Gebrauchs von Antibiotika M. Kresken 10

Resistente Staphylococcus aureus Ø 1944 Ø 1949 Ø 1950+ Ø 1960 Ø 1961 Ø 1980+ Ø 1996 Ø Juni 2002 M. Kresken Einführung von Penicillin G 50% Penicillin-resistente Stämme (bla-Gen) Resistenz gegen Cycline, Makrolide, Aminoglykoside, Chloramphenicol Einführung von Methicillin, Oxacillin MRSA (Methicillin/Oxacillin-resistenter SA) Epidemische Ausbreitung von MRSA; Multiresistenz, Zunahme des Vancomycinverbrauches VISA / GISA VRSA / GRSA 11

Spezies-spezifische Entwicklung der Resistenz gegenüber Penicillin Ø Ø Ø Staphylococcus aureus: bei niedrigem Selektionsdruck 50% resistente Stämme nach 5 Jahren; heute weltweit 70 -80% Streptococcus pneumoniae: erstmals 1962 beschrieben; heute regional unterschiedlich <1 bis 50% resistente Stämme Streptococcus pyogenes: bei hohem Selektionsdruck weltweit kein resistenter Stamm beschrieben M. Kresken 12

Spezifität der Resistenz Ø Substanz Ø Bakterien-Spezies Ø Region M. Kresken 13

Resistenz Ø Natürliche Resistenz Ø Erworbene Resistenz M. Kresken 14
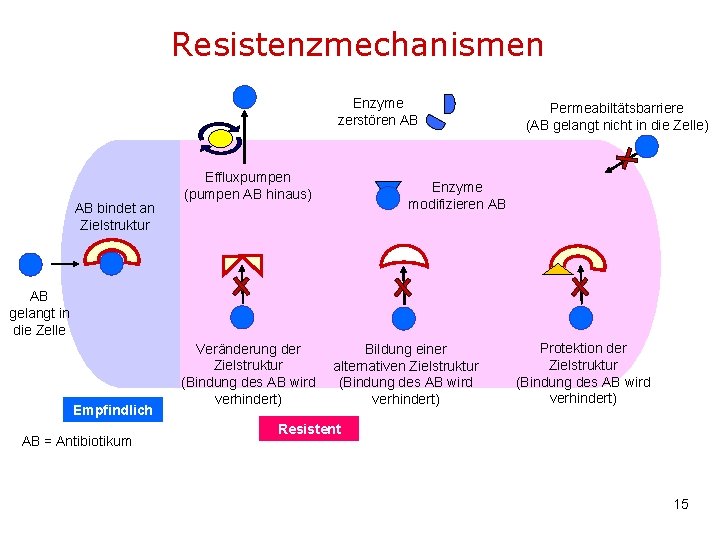
Resistenzmechanismen Enzyme zerstören AB AB bindet an Zielstruktur Effluxpumpen (pumpen AB hinaus) Permeabiltätsbarriere (AB gelangt nicht in die Zelle) Enzyme modifizieren AB AB gelangt in die Zelle Empfindlich AB = Antibiotikum Veränderung der Zielstruktur (Bindung des AB wird verhindert) Bildung einer alternativen Zielstruktur (Bindung des AB wird verhindert) Protektion der Zielstruktur (Bindung des AB wird verhindert) Resistent 15

Treibende Kräfte für den Erwerb von Resistenzeigenschaften Ø Veränderung vorhandener genetischer Information (z. B. Punktmutation, Deletion, Insertion) Ø Aufnahme neuer genetischer Information (z. B. Plasmide, chromosomale Fragmente) Ø Selektion Ø Klonale Ausbreitung M. Kresken 16
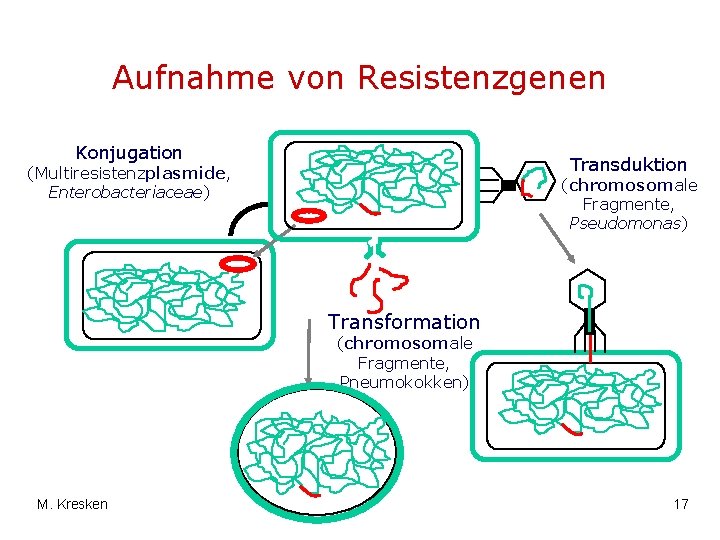
Aufnahme von Resistenzgenen Konjugation Transduktion (Multiresistenzplasmide, Enterobacteriaceae) (chromosomale Fragmente, Pseudomonas) Transformation (chromosomale Fragmente, Pneumokokken) M. Kresken 17
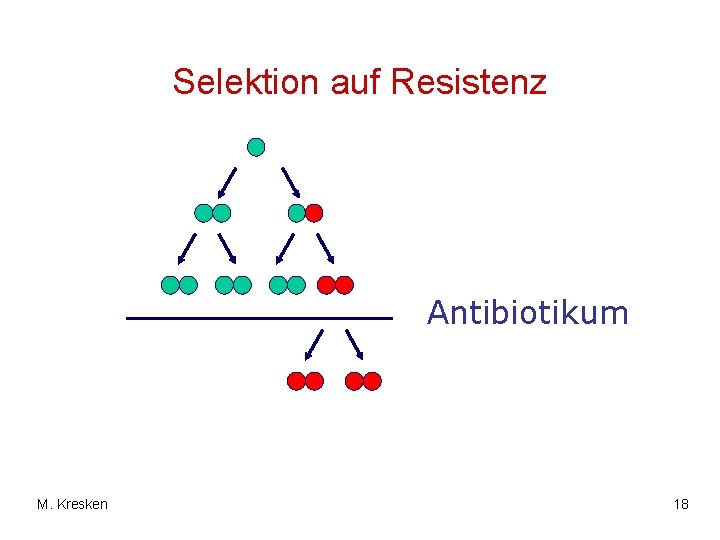
Selektion auf Resistenz Antibiotikum M. Kresken 18

Verbrauch von Antibiotika in USA Bereich Verwendung Humanmedizin (50%) 20% Klinik Veterinärbereich (50%) M. Kresken 80% Praxis 20% Therapie 80% Prophylaxe / Leistungsförderung Harrison & Lederberg, 1998 Zweifelhafte Verwendung 20 -50% unnötig 40 -80% sehr fraglich 19

Selektion von Resistenz Ø 7 Probanden erhielten Ciprofloxacin 2 mal tgl. 750 mg über 7 Tage Ø Fluorchinolon-resistente S. epidermidis wurden im Durchschnitt nach 2, 7 Tagen im Axillarbereich nachgewiesen. M. Kresken Hoiby et al. (1997) Lancet 349(9046): 167 -9 20

Ausbreitungstypen der Resistenz Ø Ausbreitung bei einem einzelnen Patienten (Patientenstamm) - Escherichia coli, Staphylococcus epidermidis Ø Ausbreitung in einer Region (Krankenhausstamm, Epidemiestamm) - Pseudomonas aeruginosa, Staphylococcus aureus Ø Globale Entwicklung (Weltstamm) - Neisseria gonorrhoeae, Streptococcus pneumoniae M. Kresken 21
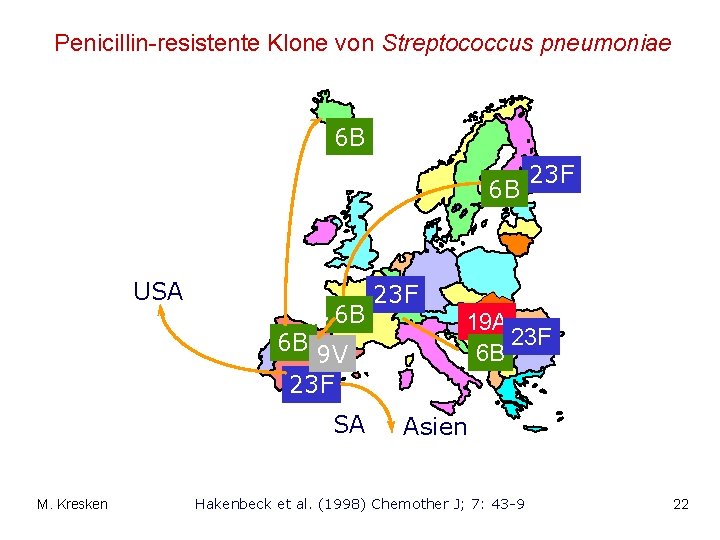
Penicillin-resistente Klone von Streptococcus pneumoniae 6 B 6 B USA 6 B 6 B 9 V 23 F SA M. Kresken 23 F 19 A 23 F 6 B Asien Hakenbeck et al. (1998) Chemother J; 7: 43 -9 22

Klonale Ausbreitung der Resistenz Ø Krankenhäuser, Tageseinrichtungen, Altersheime etc. Ø Fäkal-oral (sanitäre Einrichtungen, Tierprodukte) Ø Sexuelle Übertragung Ø Aerogene Übertragung (Tröpfcheninfektion) Ø Reisetätigkeit M. Kresken 23
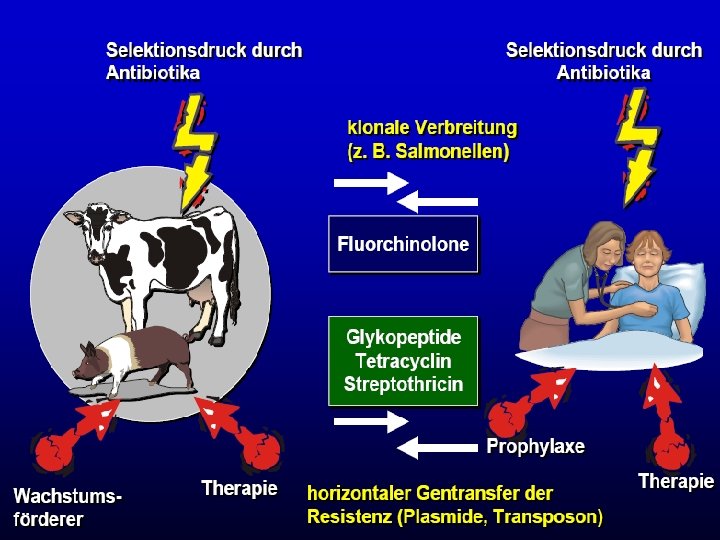
24

Multiresistenz Ø Wahres Gefahrenpotential geht von mehrfach resistenten Stämmen aus. Ø Resistente Bakterien können offensichtlich schneller (weitere) Resistenzgene erwerben als sensible Bakterien. M. Kresken 25

Multiresistente Erreger Ø Methicillin-resistente S. aureus (MRSA) Ø Glykopeptid-resistente Enterokokken (GRE) Ø Penicillin-resistente S. pneumoniae (PRSP) Ø Mehrfach-resistente gramnegative Bakterien M. Kresken 26
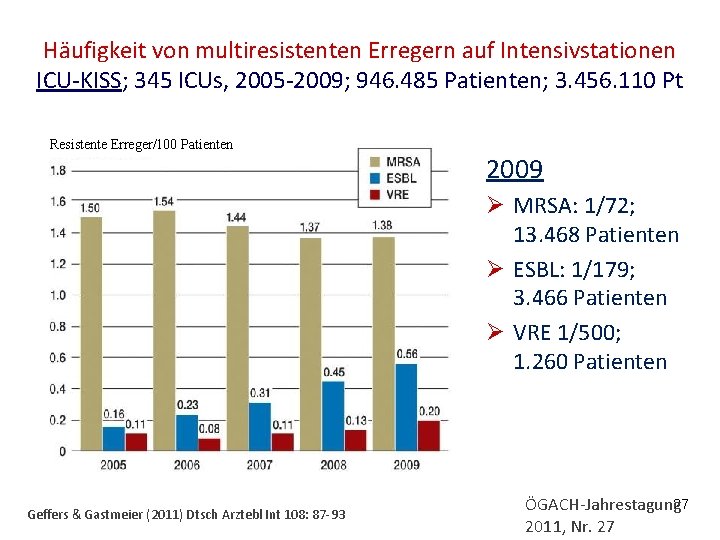
Häufigkeit von multiresistenten Erregern auf Intensivstationen ICU-KISS; 345 ICUs, 2005 -2009; 946. 485 Patienten; 3. 456. 110 Pt Resistente Erreger/100 Patienten 2009 Ø MRSA: 1/72; 13. 468 Patienten Ø ESBL: 1/179; 3. 466 Patienten Ø VRE 1/500; 1. 260 Patienten Geffers & Gastmeier (2011) Dtsch Arztebl Int 108: 87 -93 ÖGACH-Jahrestagung 27 2011, Nr. 27

The bacterial challenge: time to react A call to narrow the gap between multidrug-resistant bacteria in the EU and the development of new antibacterial agents http: //www. emea. europa. eu/pdfs/hu man/antimicrobial_resistance/EMEA 576176 -2009. pdf 28
- Slides: 28