Repetition Svaga syror och baser i vattenlsning Rknar

Repetition - Svaga syror och baser i vattenlösning Räknar exempel senare! - Polyprotolyter Principen för beräkning av speciering – H 3 PO 4 som mall - Buffertsystem Konstruera och avläsa fördelningsdiagram - Mkt utspädda lösningar av starka syror Problem: vattnets autoprotolys kan ej försummas Kan ej räkna på vanligt sätt! Redskap: 1. Massbalans, 2. Laddningsbalans, 3. Vattnets autoprotolys - Exakt lösning av 2: a –grads ekvation KEMA 02/ © Sofi Elmroth 2011

JV FLS 1(3) KEM A 02 Allmän- och oorganisk kemi JÄMVIKT i LÖSNING A: Kap 12 sid. 475 – 508 p. H och lite till! KEMA 02/ © Sofi Elmroth 2011

BLANDADE LÖSNINGAR OCH BUFFERTAR Egentligen inget nytt men nu räknar vi på mer komplexa system! KEMA 02/ © Sofi Elmroth 2011

12. 1 Buffertegenskaper EXEMPEL PÅ NATURLIGA BUFFERTSYSTEM och p. H Blodplasma: p. H ca 7. 4 (fosfat) Havsvatten (oceaner): p. H ca 8. 4 (karbonat- och silikat) BUFFERT - Innehåller alltid ett syra/bas par - Halterna av syra och bas är jämförbara, dvs inom samma tiopotens - Vanliga buffertar: KEMA 02/ © Sofi Elmroth 2011 fosfat-, karbonat-, sulfit- (se tidigare föreläsning) ättikssyra/acetat, ammoniak/ammonumjon

12. 2 Att designa en buffert HAc + Ac- EXEMPEL 12. 1: Tillreda acetatbuffert med visst p. H ÖNSKAR: p. H ca 4 genom att blanda 0. 080 M HAc och 0. 040 M Na. Ac VAD BLIR p. H? (exakt!) JÄMVIKT HAc(aq) + H 2 O(l) Ac-(aq) + H 3 O+(aq) [Ac-(aq)] [H 3 O+(aq)] Ka = [HAc(aq)] [H 3 O+(aq)] = Ka [HAc(aq)] [Ac-(aq)] = 1. 8 E-5 0. 08 0. 04 p. Ka =4. 75 Ka = 1. 8 E-5 M = 3. 6 E-5 M p. H = 4. 44 (-log(3. 6 E-5)) KEMA 02/ © Sofi Elmroth 2011

Hur tålig är bufferten? 1(2) HAc + OH- EXEMPEL 12. 2: 1. 2 g Na. OH löses i HAc/Ac-buffert p. H 4. 44* (EX 12. 1) 0. 030 mol i 0. 5 dm 3 [OH-] = 0. 060 M VAD FÖRVÄNTAR VI OSS? - Liten tillsats av bas (OH-) kan reagera med HAc höjning av p. H - Antag att all OH- reagerar med HAc [rimligt!] och att jämvikten sedan sker REAKTION 1: Den starka basen OH- reagerar fullständigt med HAc (svag) FB Ny start HAc(aq) + OH-(aq) 0. 080* 0. 060 0. 020 0 * Sammansättningen given i Ex 12. 1 KEMA 02/ © Sofi Elmroth 2011 Ac-(aq) 0. 040* 0. 10 + H 2 O(aq)

Hur tålig är bufferten? 2(2) HAc + OH- NY JÄMVIKT ATT BERÄKNA: HAc(aq) + H 2 O(aq) FB VJ 0. 020 -x - Ac-(aq) + H 3 O+(aq) Ka 0. 10+x ANTAGANDE: x << 0. 020 M Ka [Ac-(aq)][H 3 O+(aq)] = = 0. 10 x/0. 02 [HAc] x = 0. 02 Ka / 0. 10 x = 0. 02 1. 8 E-5 /0. 10 = 3. 6 E-6 M antagandet OK! p. H = 5. 44 (-log (3. 6 E-6)) KEMA 02/ © Sofi Elmroth 2011 x
![Henderson-Hasselbach ekvationen OBS! Gäller då [syra] och [bas] >> [OH-], [H 3 O+] [HA] Henderson-Hasselbach ekvationen OBS! Gäller då [syra] och [bas] >> [OH-], [H 3 O+] [HA]](http://slidetodoc.com/presentation_image_h2/60984e04b25dc0212e91e1f1d88d837d/image-8.jpg)
Henderson-Hasselbach ekvationen OBS! Gäller då [syra] och [bas] >> [OH-], [H 3 O+] [HA] p. H = p. Ka – log [A-] HÄRLEDNING: HA(aq) + H 2 O(l) A-(aq) + H 3 O+ (aq) [A-(aq) ][H 3 O+ (aq)] Ka = [HA(aq) ] [H 3 O+ [HA(aq) ] (aq)] = Ka [A (aq) ] -log [H 3 O+ (aq)] = -log Ka - log p. H KEMA 02/ © Sofi Elmroth 2011 p. Ka [HA(aq) ] [A-(aq) ]

F 6 start KEMA 02/ © Sofi Elmroth 2011

Hur skall sammansättningen se ut? HÄR: fixerat p. H EXEMPEL 12. 3 Vilket förhållande mellan HCO 3 - och CO 32 ger p. H = 9. 50? KEMA 02/ © Sofi Elmroth 2011
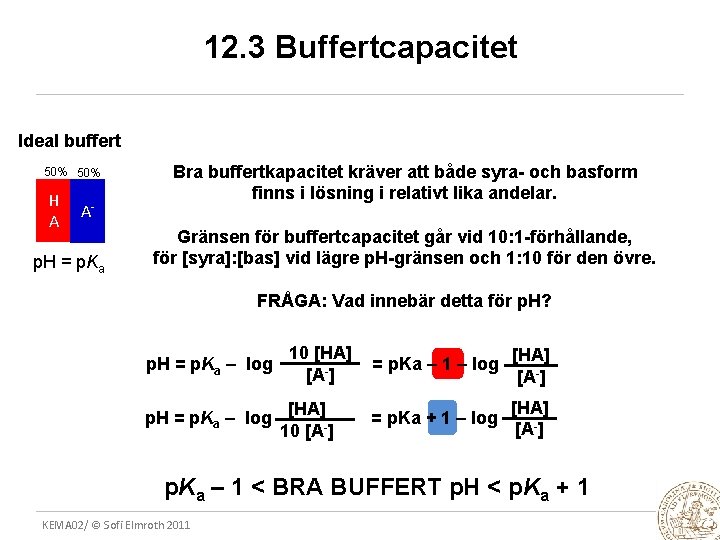
12. 3 Buffertcapacitet Ideal buffert 50% H A A- p. H = p. Ka Bra buffertkapacitet kräver att både syra- och basform finns i lösning i relativt lika andelar. Gränsen för buffertcapacitet går vid 10: 1 -förhållande, för [syra]: [bas] vid lägre p. H-gränsen och 1: 10 för den övre. FRÅGA: Vad innebär detta för p. H? p. H = p. Ka – log 10 [HA] [A-] p. H = p. Ka – log [HA]10 [A ] = p. Ka – 1 – log [HA] [A-] = p. Ka + 1 – log [HA] [A-] p. Ka – 1 < BRA BUFFERT p. H < p. Ka + 1 KEMA 02/ © Sofi Elmroth 2011

TITRERINGAR Nomenklatur TITRANT(TITRATOR) det som tillsätts t. ex från byrett ANALYT(TITRAND) det som analyseras i kolven STÖKIOMETRISKA PUNKTEN EKVIVALENSPUNKTEN lika mängd (mol) H 3 O+ och OH- KEMA 02/ © Sofi Elmroth 2011
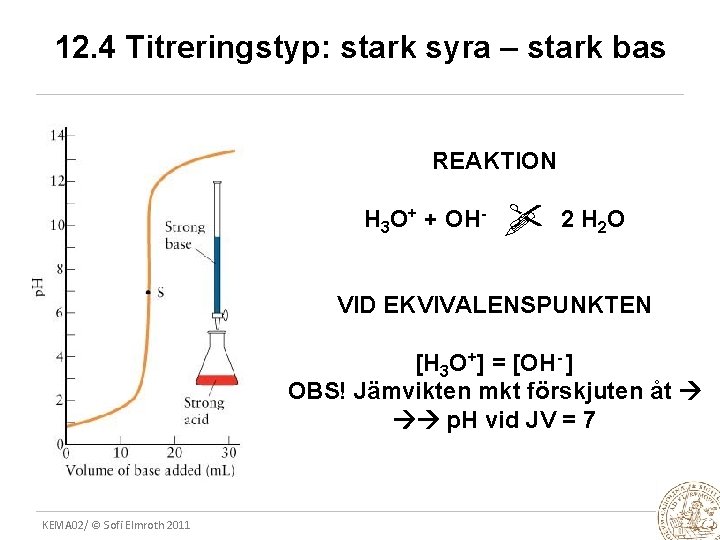
12. 4 Titreringstyp: stark syra – stark bas REAKTION H 3 O+ + OH- 2 H 2 O VID EKVIVALENSPUNKTEN [H 3 O+] = [OH- ] OBS! Jämvikten mkt förskjuten åt p. H vid JV = 7 KEMA 02/ © Sofi Elmroth 2011

Titreringstyp: stark syra – stark bas EXEMPEL 12. 4 Titrering av Na. OH med HCl Vad är start-p. H? , Vad blir slut-p. H? KEMA 02/ © Sofi Elmroth 2011
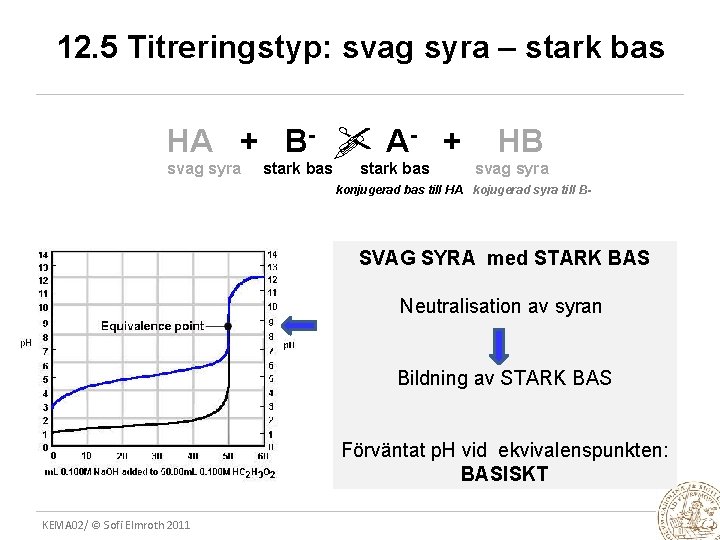
12. 5 Titreringstyp: svag syra – stark bas A- + HA + B- svag syra stark bas HB svag syra konjugerad bas till HA kojugerad syra till B- SVAG SYRA med STARK BAS Neutralisation av syran Bildning av STARK BAS Förväntat p. H vid ekvivalenspunkten: BASISKT KEMA 02/ © Sofi Elmroth 2011
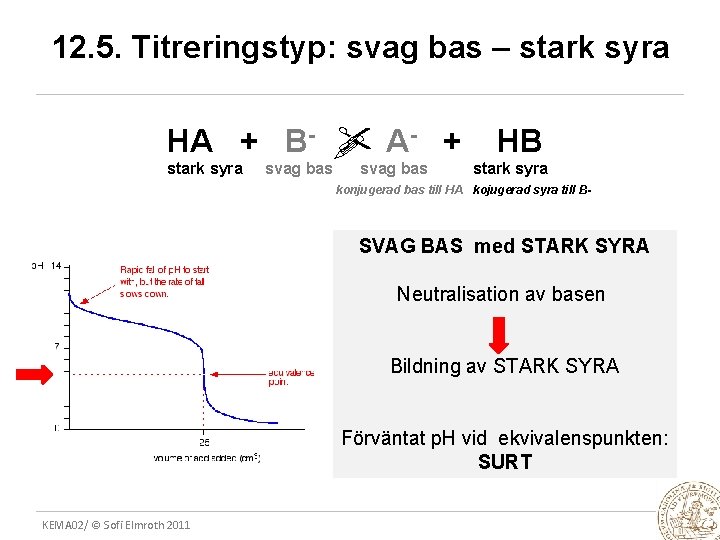
12. 5. Titreringstyp: svag bas – stark syra A- + HA + B- stark syra svag bas HB stark syra konjugerad bas till HA kojugerad syra till B- SVAG BAS med STARK SYRA Neutralisation av basen Bildning av STARK SYRA Förväntat p. H vid ekvivalenspunkten: SURT KEMA 02/ © Sofi Elmroth 2011

Titrering svag syra + stark bas EXEMPEL 12. 5 Titrering av en myrsyra med Na. OH Vad blir p. H vid ekvivalenspunkten? Myrsyra, HCOOH KEMA 02/ © Sofi Elmroth 2011

KEM A 02 Allmän- och oorganisk kemi JÄMVIKT i LÖSNING A: Kap 12 mer p. H, indikatorer och löslighetsprodukt KEMA 02/ © Sofi Elmroth 2011
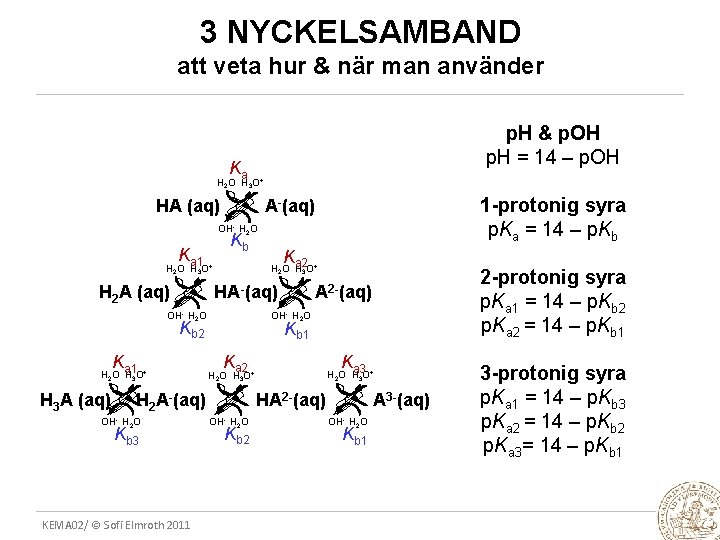
3 NYCKELSAMBAND att veta hur & när man använder p. H & p. OH p. H = 14 – p. OH Ka H 2 O H 3 O+ HA (aq) 1 -protonig syra p. Ka = 14 – p. Kb - OH- H 2 O Kb Ka 1 H 2 A (aq) OH- K H 2 O a 2 H 3 O+ H 2 O H 3 O+ HA-(aq) H 2 O OH- H 2 O Kb 2 Kb 1 Ka 2 Ka 1 H 2 O H 3 O+ Ka 3 H 2 O H 3 O+ H A (aq) HA H 3 A (aq) 2 - OH- H 2 O Kb 3 KEMA 02/ © Sofi Elmroth 2011 2 -protonig syra p. Ka 1 = 14 – p. Kb 2 p. Ka 2 = 14 – p. Kb 1 A 2 -(aq) OH- H 2 O Kb 2 2 -(aq) A OH- H 2 O Kb 1 3 -(aq) 3 -protonig syra p. Ka 1 = 14 – p. Kb 3 p. Ka 2 = 14 – p. Kb 2 p. Ka 3= 14 – p. Kb 1

Beräkning av p. H innan eq-punkten Titreringstyp: svag syra – stark bas EXEMPEL 12. 6 Titrering av en myrsyra med Na. OH Vad blir p. H om vi slutar innan ekvivalenspunkten? Myrsyra, HCOOH KEMA 02/ © Sofi Elmroth 2011

12. 6 Syra-bas indikatorer FRÅGA: Hur detekterar man p. H & p. H-förändringar? FÖLJDFRÅGA: Ekvivalenspunkten nås vid olika p. H – hur vet man när omslaget kommer? METOD 1: METOD 2: p. H meter p. H indikator - mäter noga i hela p. H intervallet - ger dålig framförvarning map ekvivalenspunkten - Mycket data kan samlas in om automatiserad - mäter ”dåligt” utom vid omslag - ger bra framförvarning map ekvivalenspunkten - Datainsamling kan ej göras utan Indirekt mätning (UV/vis) KEMA 02/ © Sofi Elmroth 2011
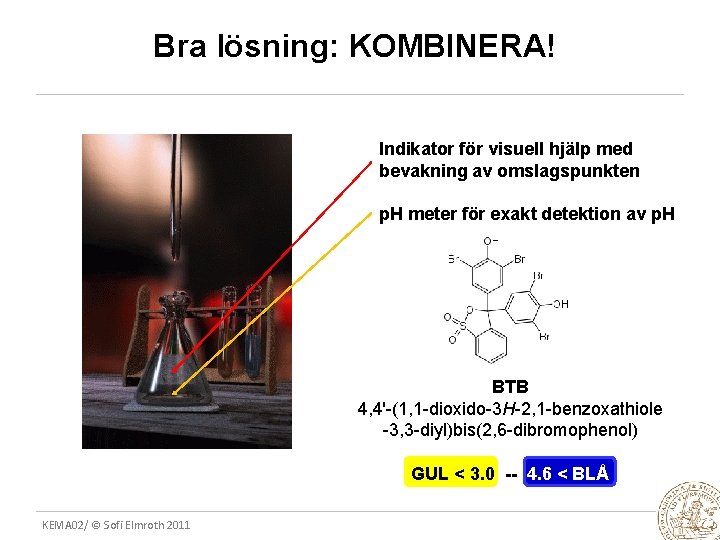
Bra lösning: KOMBINERA! Indikator för visuell hjälp med bevakning av omslagspunkten p. H meter för exakt detektion av p. H BTB 4, 4'-(1, 1 -dioxido-3 H-2, 1 -benzoxathiole -3, 3 -diyl)bis(2, 6 -dibromophenol) GUL < 3. 0 -- 4. 6 < BLÅ KEMA 02/ © Sofi Elmroth 2011

Exempel på indikatorer; omslagsintervall och färgförändring Indikator Indicator Gentian violet (Methyl violet 10 B) BTB Färg FÖRE OMSLAG Omslag (p. H) Low p. H color Transition p. H range Färg EFTER OMSLAG High p. H color yellow 0. 0– 2. 0 blue-violet Leucomalachite green (first transition) yellow 0. 0– 2. 0 green Leucomalachite green (second transition) green 11. 6– 14 colorless Thymol blue (first transition) red 1. 2– 2. 8 yellow Thymol blue (second transition) yellow 8. 0– 9. 6 blue Methyl yellow red 2. 9– 4. 0 yellow Bromophenol blue yellow 3. 0– 4. 6 purple Congo red Methyl orange blue-violet 3. 0– 5. 0 3. 1– 4. 4 red Bromocresol green yellow 3. 8– 5. 4 blue Methyl red Azolitmin red yellow red 4. 4– 6. 2 4. 5– 5. 2 4. 5– 8. 3 Bromocresol purple yellow 5. 2– 6. 8 purple Bromothymol blue yellow 6. 0– 7. 6 blue Phenol red Neutral red yellow 6. 8– 8. 4 6. 8– 8. 0 red Naphtholphthalein colorless to reddish 7. 3– 8. 7 greenish to blue Cresol Red yellow 7. 2– 8. 8 reddish-purple Phenolphthalein colorless 8. 3– 10. 0 fuchsia Thymolphthalein colorless 9. 3– 10. 5 blue Alizarine Yellow R yellow 10. 2– 12. 0 red Litmus red 4. 5 -8. 3 blue KEMA 02/ © Sofi Elmroth 2011 red orange green blue yellow KÄLLA: http: //en. wikipedia. org/wiki/PH_indicator
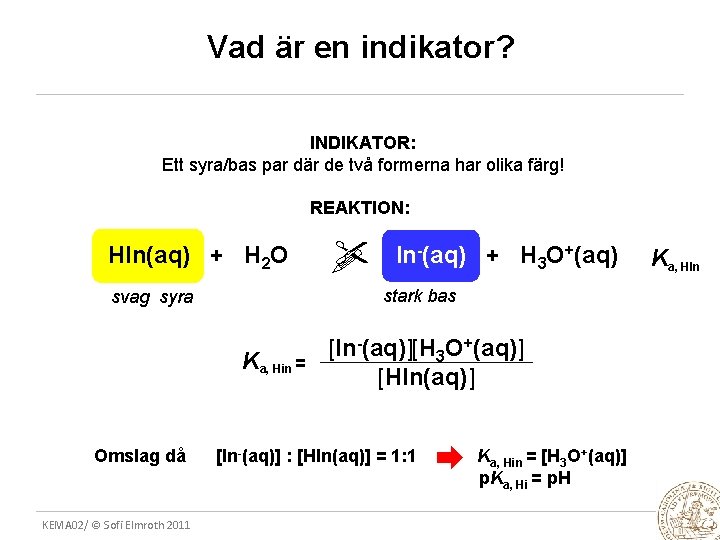
Vad är en indikator? INDIKATOR: Ett syra/bas par där de två formerna har olika färg! REAKTION: HIn(aq) + H 2 O Ka, Hin = KEMA 02/ © Sofi Elmroth 2011 In-(aq) + H 3 O+(aq) stark bas svag syra Omslag då [In-(aq)][H 3 O+(aq)] [HIn(aq)] [In-(aq)] : [HIn(aq)] = 1: 1 Ka, Hin = [H 3 O+(aq)] p. Ka, Hi = p. H Ka, HIn
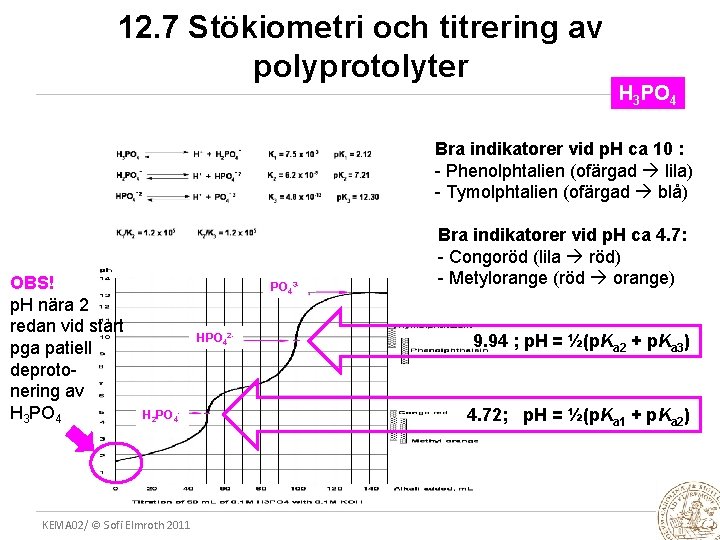
12. 7 Stökiometri och titrering av polyprotolyter H 3 PO 4 Bra indikatorer vid p. H ca 10 : - Phenolphtalien (ofärgad lila) - Tymolphtalien (ofärgad blå) OBS! p. H nära 2 redan vid start pga patiell deprotonering av H 3 PO 43 - HPO 42 - H 2 PO 4 - KEMA 02/ © Sofi Elmroth 2011 Bra indikatorer vid p. H ca 4. 7: - Congoröd (lila röd) - Metylorange (röd orange) 9. 94 ; p. H = ½(p. Ka 2 + p. Ka 3) 4. 72; p. H = ½(p. Ka 1 + p. Ka 2)

LÖSLIGHETSJÄMVIKTER Salter – en kombination av katjoner och anjoner – kan vara mycket olika lösliga i vatten! “…. A barium sulphate suspension in water is the universal contrast medium used for examination of the upper gastrointestinal tract. ” KÄLLA: http: //www. e-radiography. net/ contrast_media/contrast_ media_introduction. htm Na. Cl – ”salt” mkt lättlösligt KEMA 02/ © Sofi Elmroth 2011

Löslighetsjämvikter & biorelevans TYPISKA OMRÅDEN & FRÅGESTÄLLNINGAR: några exempel. . . det finns mycket mer! Vattenkvalitet Fe(II/III), Cr(III-VII), Pb(II), Al(III) ”Bioavailability” av spårmetaller Cu(II), Ni(II), Mn(II) Läckage av metalljoner från gruvmiljö/deponier Metallothioniner är svavel-innehållande protein som används för att transportera tex Cu(II) och Hg(II). Fe(II/III), Ni(II/III), Pb(II/IV), Hg(I/II), Ag(I), Au(III/I) Toxicitet Fe(II/III), Ni(II/III), Pb(II/IV), Hg(I/II), Ag(I), Cd(II) Ksp (Cu. S) = 1. 3 E-36* Ksp (Hg. S) = 1 E-53* Sofi Elmroth 2011 *dvs. KEMA 02/ mkt liten©tendens till frisläppning av M(II) – mer om detta senare! Funktion Na(I), K(I)

12. 8 Löslighetsprodukt BEGREPP: Löslighetsprodukt – ett mått på lösligheten en jämvikt som alla andra! EXEMPEL: Upplösning av Bi 2 S 3(s) 2 Bi 3+(aq) + 3 S 2 -(aq) Ksp = a(Bi 3+(aq))2 a(S 2 -(aq))3 Ksp = [Bi 3+(aq)]2 [S 2 -(aq)]3 Ksp litet för svårlösliga salter; Ksp (Bi 2 S 3(s)) = 1. 0 E-97 M 4 KEMA 02/ © Sofi Elmroth 2011 Ksp
Bestämning av löslighetsprodukt EXEMPEL 12. 7 Vad är Ksp för silverkromat (Ag 2 Cr. O 4) Användning: Fotografi - framkallning (Ag+) Inmärkning av neuroner(nerver)! - kontrastreagens Ag+ KEMA 02/ © Sofi Elmroth 2011

Hur mycket löser sig? EXEMPEL 12. 8 Beräkna lösligheten av Cr 3+ och IO 3 - då Cr(IO 3)3(s) blandas med vatten Förekomst – IO 3 -: Synthetic Sea Salt* Content in ug/L Iodate 550 ± 5. 0 Iodide 197 ± 2. 7 KÄLLA: Dionex application note 236 (HPLC-tillverkare) *Synthetic Sea Salt Commercially available synthetic sea salt was prepared following package directions (1/2 cup of salt per gallon of deionized water). A 1 L portion was prepared with 30 g of aquarium salt. A sea salt density of approximately 2. 2 g/cm 3 was used to convert KEMA 02/ © Sofi Elmroth 2011 JOD och oxidationstal: -I Ijodid 0 I 2 +I +III +V IO- IO 2 - IO 3 - jod hypojodit jodat +VII IO 4 perjodat
- Slides: 30