Reovirus Virus de ARN de cadena doble Reoviridae

Reovirus
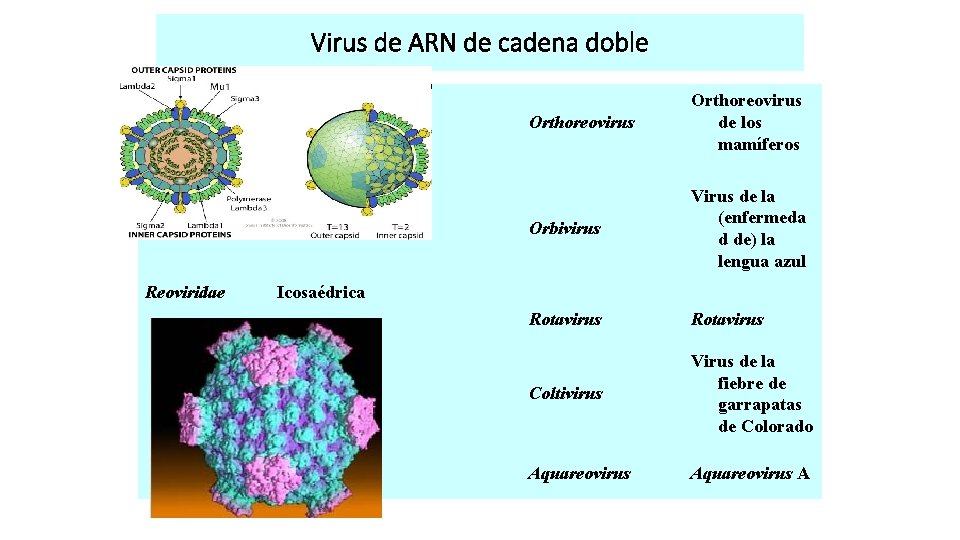
Virus de ARN de cadena doble Reoviridae Icosaédrica Orthoreovirus de los mamíferos Orbivirus Virus de la (enfermeda d de) la lengua azul Rotavirus Coltivirus Virus de la fiebre de garrapatas de Colorado Aquareovirus A

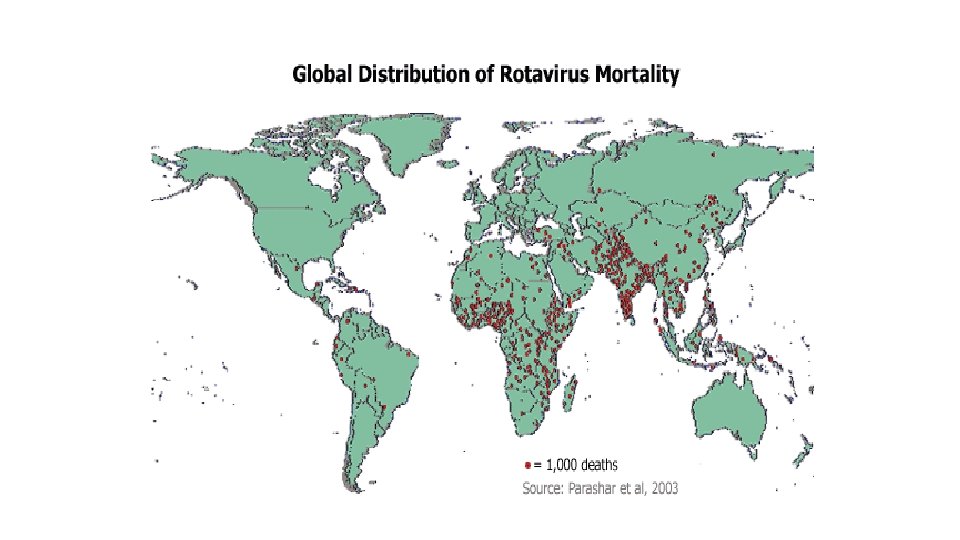
Rotavirus • Distribución geográfica: Mundial • Causa más común de gastroenteritis y deshidratación graves en niños pequeños de países industrializados y vías de desarrollo. • Estudios recientes han calculado que entre 500. 000 y 600. 000 niños mueren c/año

Rotavirus • Descrito 7 grupos • Identificado 3 en humanos • A, B y C • A mas frecuente • 11 serotipos • 1 a 4 mas frecuentes • Contagio: interhumano vía fecal oral
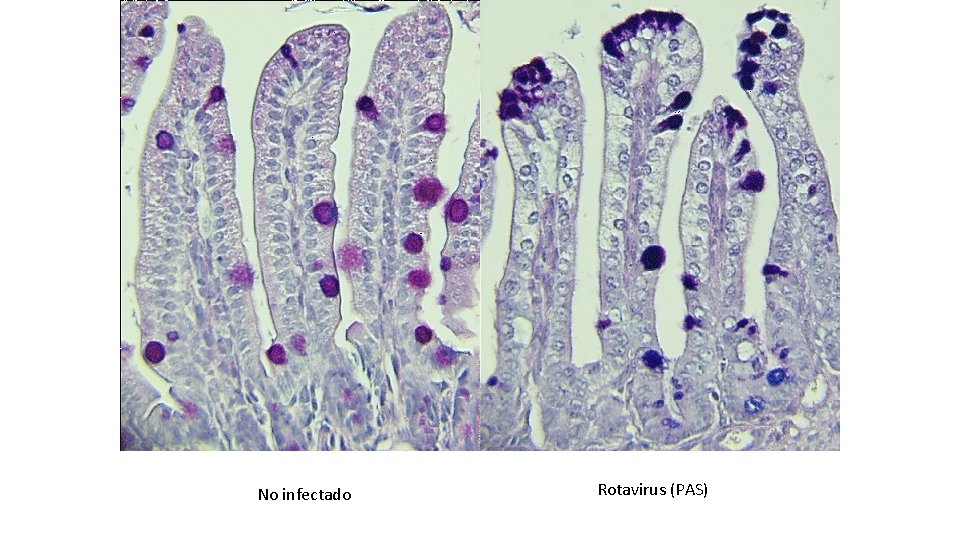
No infectado Rotavirus (PAS)
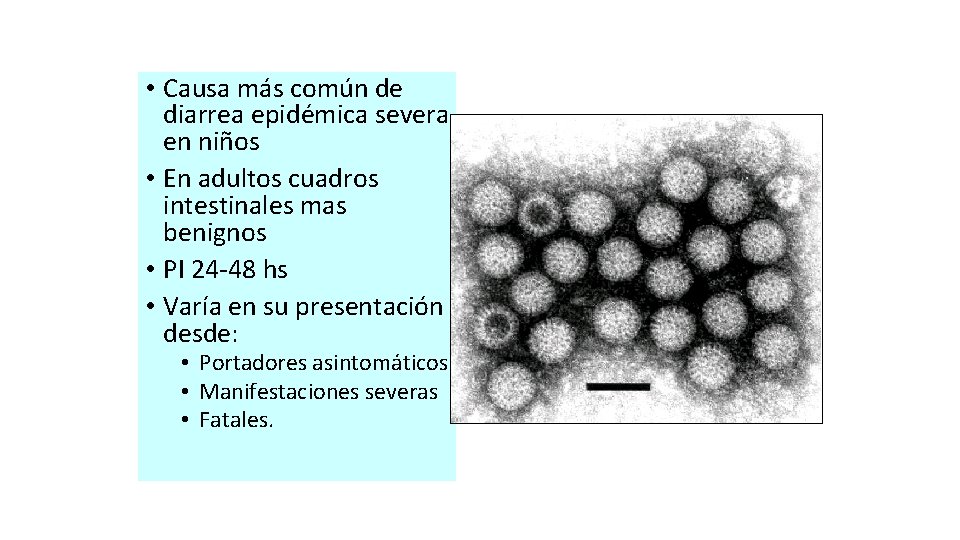
• Causa más común de diarrea epidémica severa en niños • En adultos cuadros intestinales mas benignos • PI 24 -48 hs • Varía en su presentación desde: • Portadores asintomáticos • Manifestaciones severas • Fatales.

• Anorexia • Astenia • Adinamia • Vómito
• Diarrea • • • Evacuaciones 3 -12/d Acuosa Abundante Líquida Mucho gas • Dolor abdominal • Fiebre • Cuadro convulsivo: • Deshidratación: 50% (leve) • PR: 5 a 8 días

• E directo : en heces ME , IFD, FC, CIE ELISA: elección. • Rápido • Práctico • Sensibilidad y especificidad. Detección rápida por aglutinación de partículas de látex. • E Indirecto: serológicos detectando Ac. FC, RIE, ELISA, IFI
• Tto: • Sistemas inmune saludable: • auto-limitada, no tto • No es específico: • Rehidratación oral • Aprox 1/40 niños requiere hospitalización x adm fluidos intravenosos.

• Prevención: • FDA 1998: aprobó una vacuna de virus vivo (Rotashield) para niños.

Familia Togaviridae Comprende 2 géneros de importancia humana: 1. Alfavirus: Arbovirus 2. Rubivirus. Virus de Rubeola

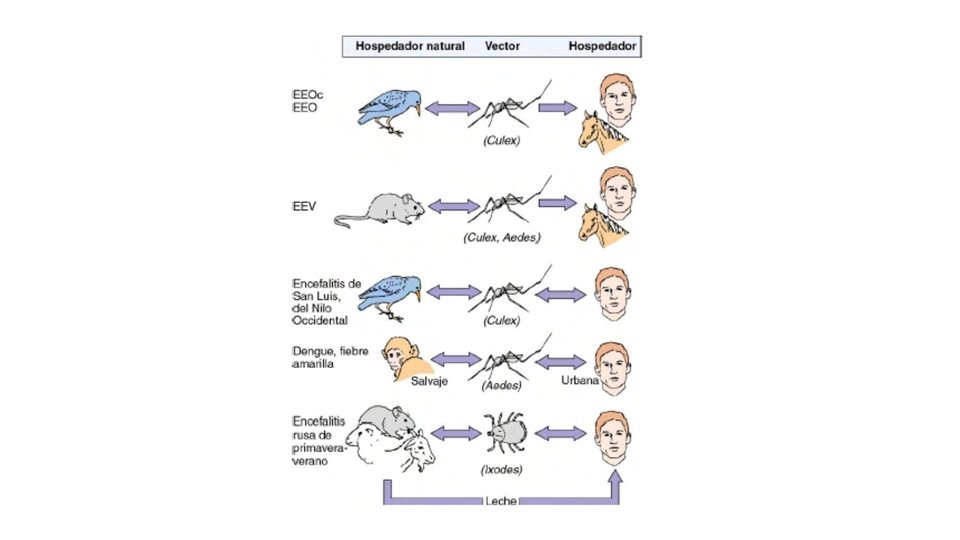
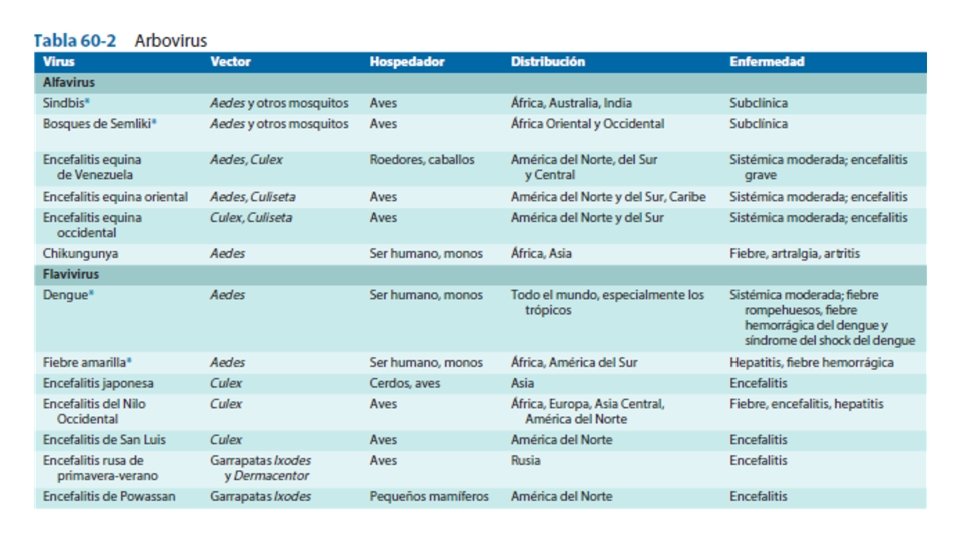
Alfavirus y Flavivirus • Los alfavirus y los flavivirus se clasifican como arbovirus pues suelen transmitirse a través de vectores artrópodos. • No obstante, estos virus tienen un amplio abanico de hospedadores, como organismos vertebrados (p. ej. , mamíferos, aves, anfibios, reptiles) e invertebrados (p. ej. , mosquitos, garrapatas). Las enfermedades transmitidas por los animales o que tienen un reservorio animal se denominan zoonosis

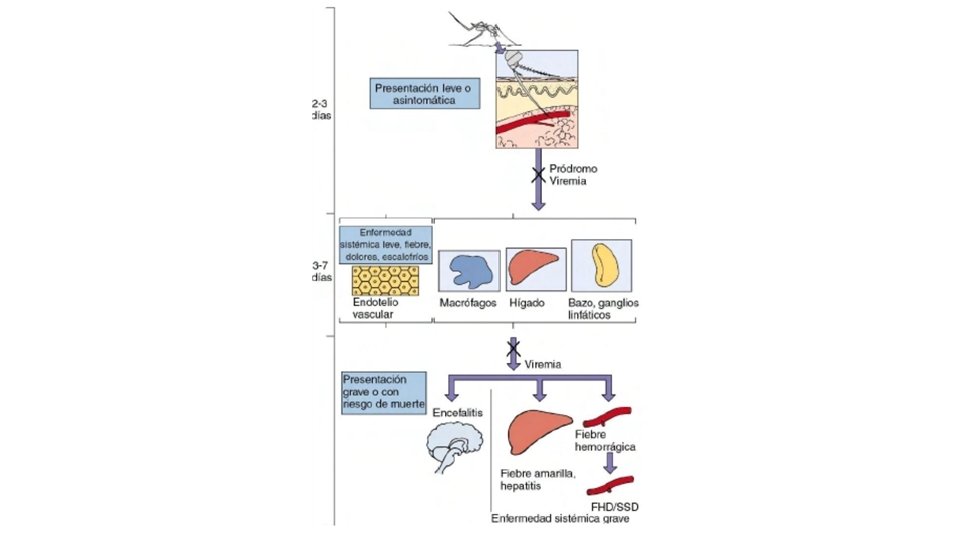

DENGUE • . La fiebre del dengue tambien se conoce como fiebre rompehuesos los sintomas y signos consisten en fiebre elevada, cefalea, eritema y dolor de espalda y de huesos que duran de 6 a 7 dias. • Cuando se produce un nuevo contacto con alguna de las otras cuatro cepas relacionadas con el, el dengue tambien puede provocar FHD y síndrome de shock del dengue (SSD). Los anticuerpos no neutralizantes estimulan la entrada de los virus en los macrofagos, lo que activa los linfocitos de memoria T, provoca la secrecion de citocinas e inicia las reacciones inflamatorias. • Estas reacciones provocan debilidad y rotura de los vasos sanguineos, hemorragia interna y perdida de plasma, lo que da lugar a sintomas de shock y hemorragia interna. En • Cuba, en 1981, el virus dengue-2 infecto a una poblacion

• Las infecciones de fiebre amarilla se caracterizan por una enfermedad sistemica grave con degeneracion de higado, riñones y corazon, asi como hemorragias. La afectacion hepática provoca ictericia de la que se deriva el nombre de la enfermedad, aunque tambien pueden producirse hemorragias gastrointestinales masivas (≪vomito negro≫).

Diagnóstico de laboratorio Estudios citopatologicos, Inmunofluorescencia Hemadsorcion de eritrocitos de ave. RT-PCR del ARN genomico o del ARN virico en sangre u otro tipo de muestras. Inhibición de la hemaglutinacion, Analisis de inmunoadsorcion ligada a enzimas Aglutinacion con latex.
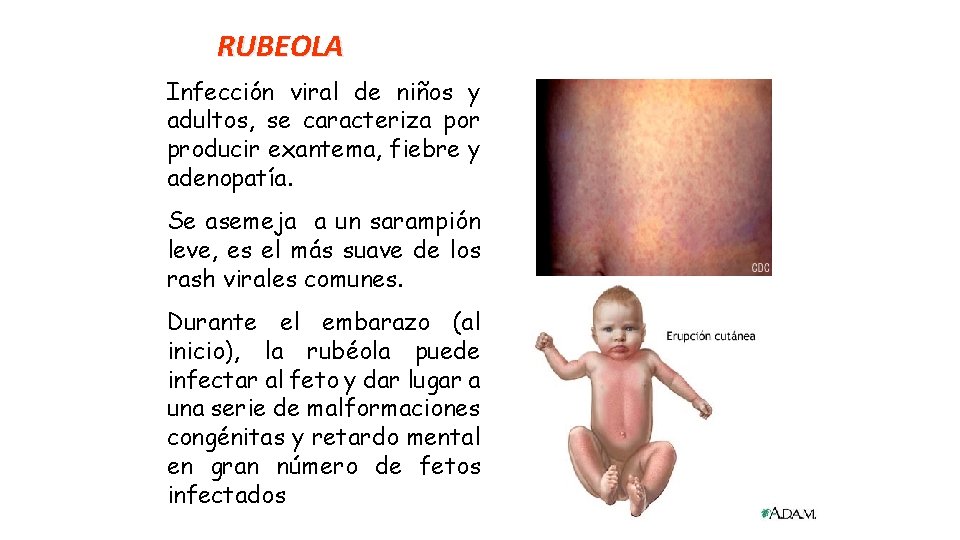
RUBEOLA Infección viral de niños y adultos, se caracteriza por producir exantema, fiebre y adenopatía. Se asemeja a un sarampión leve, es el más suave de los rash virales comunes. Durante el embarazo (al inicio), la rubéola puede infectar al feto y dar lugar a una serie de malformaciones congénitas y retardo mental en gran número de fetos infectados

Agente Etiológico • Estructura icosaedrica, con envoltura 60 -70 nm • Formado por cápside interna helicoidal de ARN y proteínas • Esta formado por un solo tipo serológico

Epidemiología • Es una enfermedad contagiosa sea esta con síntomas o subclínicas • Periodo de incubación de 18 d (12 a 23 d) • Contagio interhumano; • Vía rinofaringea; se propaga por las gotitas expelidas con las secreciones respiratorias, infecta el aparato respiratorio luego pasa a la corriente sanguínea • Tb vía transplacentaria • Más frecuente en primavera, aunque se presenta durante todo el año

Rubéola • Enfermedad sumamente leve o subclínica • Infección en lactantes , niños y adultos. • Ocurre a través de la mucosa de las vías respiratorias superiores • La reaplicación viral se inicia en el aparato respiratorio, la multiplicación ocurre en los ganglios linfáticos • De 5 a 7 dura la viremia, persiste hasta la aparición de Ac (13 a 15 d) • La aparición de Ac es coincidente con la aparición de Rash • 25% de la infección primaria es subclínica
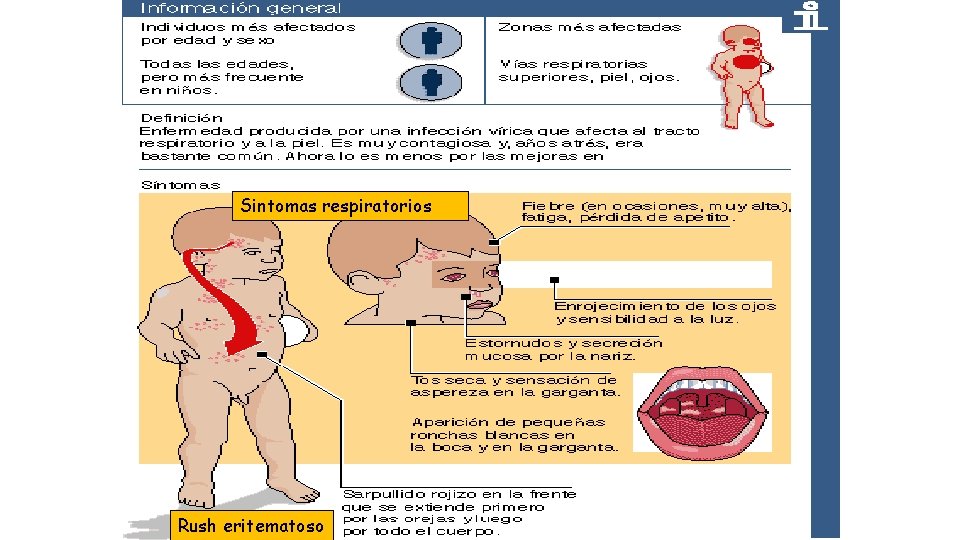
Sintomas respiratorios Rush eritematoso
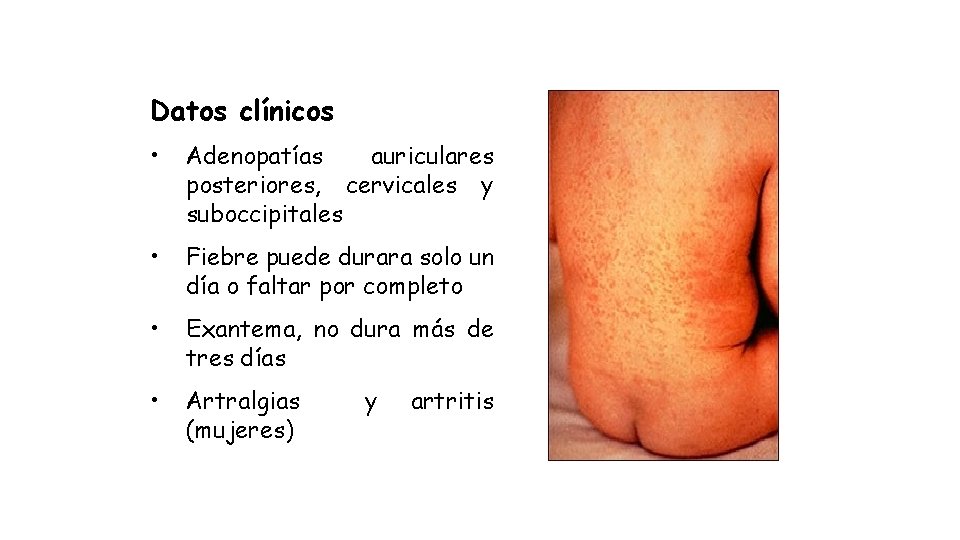
Datos clínicos • Adenopatías auriculares posteriores, cervicales y suboccipitales • Fiebre puede durara solo un día o faltar por completo • Exantema, no dura más de tres días • Artralgias (mujeres) y artritis

Síndrome de la Rubéola Congénita • Infección de la madre puede ser transmitida al feto en gestación • Infección de la placenta y el feto (Viremia) • Factor patogénico más importante gestación del feto • Cuando ocurre en el 1º trimestre, las malformaciones fetales son más frecuentes y graves afectando a órganos y aparatos la edad de
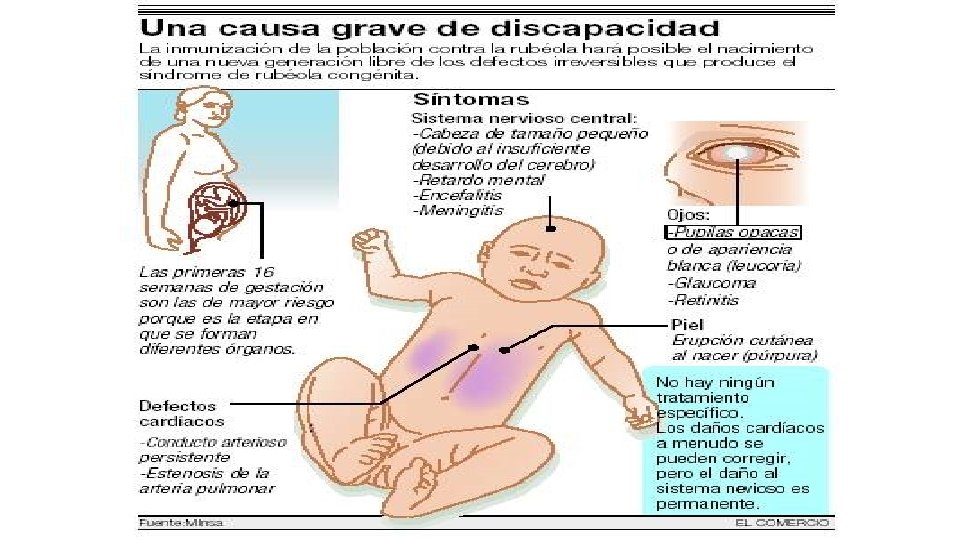
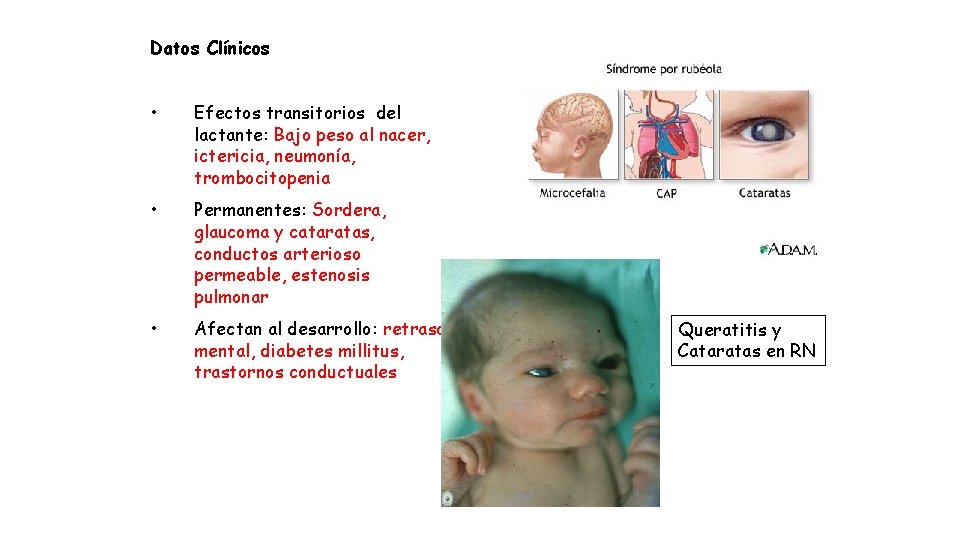
Datos Clínicos • Efectos transitorios del lactante: Bajo peso al nacer, ictericia, neumonía, trombocitopenia • Permanentes: Sordera, glaucoma y cataratas, conductos arterioso permeable, estenosis pulmonar • Afectan al desarrollo: retraso mental, diabetes millitus, trastornos conductuales Queratitis y Cataratas en RN
Inmunizacion • La enfermedad deja inmunidad para toda la vida • Vacuna a virus atenuados (triple viral)

Diagnostico • Aislamiento del virus. (muy poco utilizado) • Serologia. Ac anti-rubeola IFI IHA FC ELISA

Arenaviridae Arenavirus: Sus huéspedes naturales son una variedad de roedores, que están persistentemente infectados sin que haya una respuesta inmunológica efectiva por parte del huésped ni enfermedad sintomática. El virus se excreta por la orina, que es la fuente de infección humana La transmisión interhumana se observa con regularidad sólo en el caso del virus Lassa, en general entre personal sanitario expuestos a líquidos corporales (autopsias)

• Virus de la coriomeningitis linfocitaria(LCM): meningitis aséptica en el hombre, cuadro febril con mialgia semejante a la gripe • Virus de las fiebres hemorrágicas: • Virus de la fiebre de Lassa: en África Occidental es la mejor conocida. Fiebre coagulopatías, petequias y a veces hemorragias viscerales, así como necrosis hepática y esplénica. Hemorragias con shock, y en ocasiones con lesión cardiaca y hepática. La faringitis y los vómitos son frecuentes. La mortalidad llega al 50%

• • Virus Machupo (fiebre hemorrágica boliviana) Virus Junín (fiebre hemorrágica argentina) Virus Guanarito (fiebre hemorrágica venezolana) Sabiá (fiebre hemorrágica brasileña)

Familia Bunyaviridae
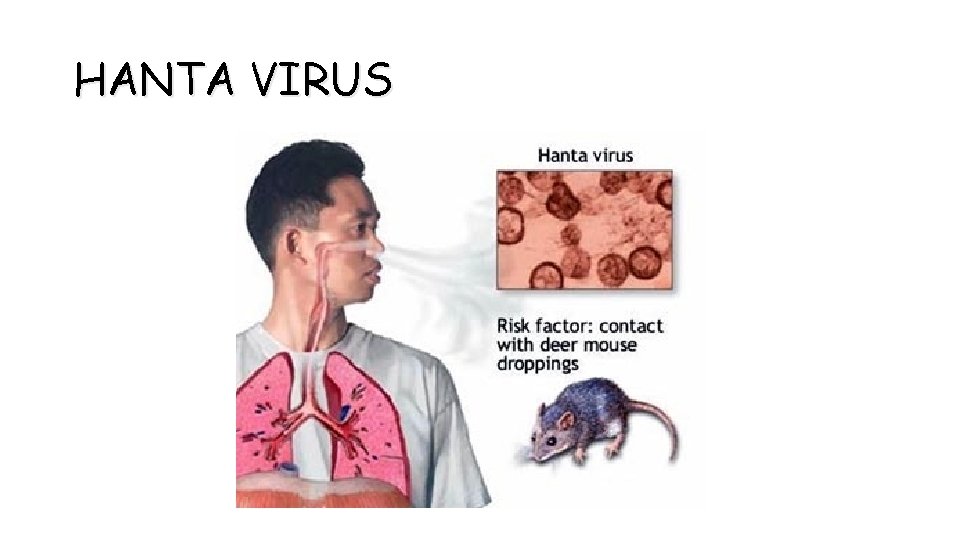
HANTA VIRUS
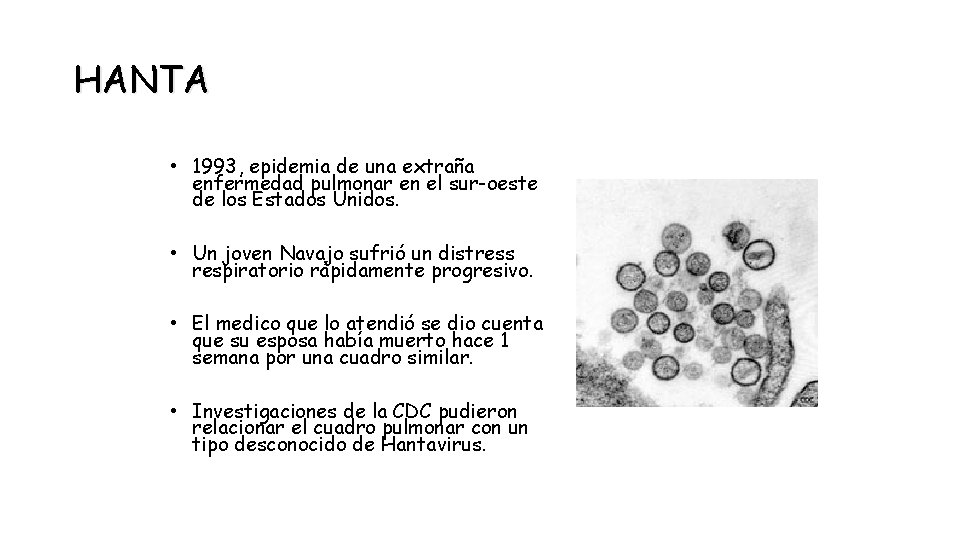
HANTA • 1993, epidemia de una extraña enfermedad pulmonar en el sur-oeste de los Estados Unidos. • Un joven Navajo sufrió un distress respiratorio rápidamente progresivo. • El medico que lo atendió se dio cuenta que su esposa había muerto hace 1 semana por una cuadro similar. • Investigaciones de la CDC pudieron relacionar el cuadro pulmonar con un tipo desconocido de Hantavirus.
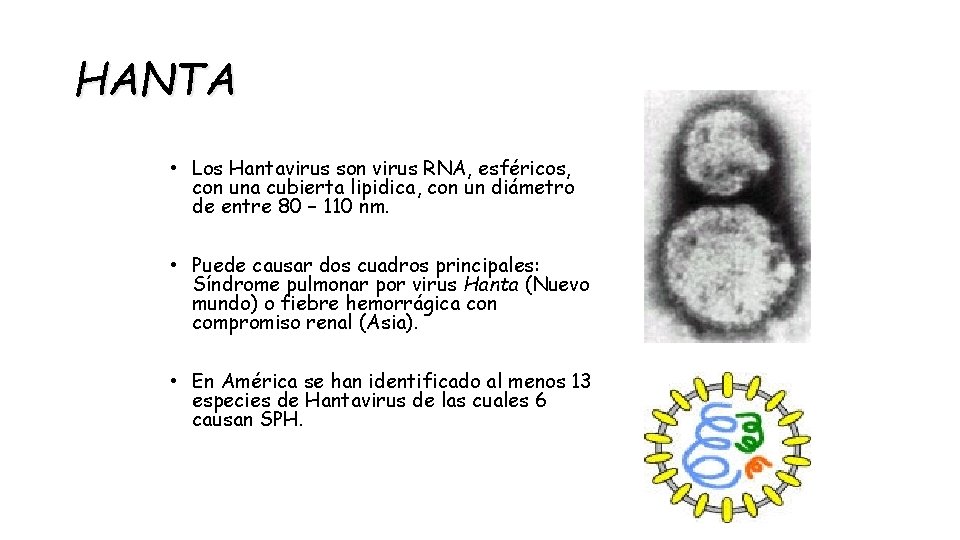
HANTA • Los Hantavirus son virus RNA, esféricos, con una cubierta lipidica, con un diámetro de entre 80 – 110 nm. • Puede causar dos cuadros principales: Síndrome pulmonar por virus Hanta (Nuevo mundo) o fiebre hemorrágica con compromiso renal (Asia). • En América se han identificado al menos 13 especies de Hantavirus de las cuales 6 causan SPH.

HANTA • Vector es el Oligoryzomis Longicaudatus o “Ratón de cola larga”. • El virus esta presente en orina, saliva y lagrimas de roedores infectados.

HANTAVIRUS

Familia Bunyaviridae

HANTAVIRUS – Epidemiología Trasmisión: aspiración de aerosoles contaminados a partir de saliva, orina o materias fecales de roedores infectados. Interhumano en población de riesgo. Heridas y mordeduras de ratones infectados. Población de riesgo: trabajadores rurales, granjeros. limpieza o ingreso a habitaciones cerradas con alta probabilidad de presencia de roedores (galpones, cabañas, graneros) roedores. zonas de alta poblaciones de

HANTAVIRUS – Epidemiología Distribución geográfica: mundial >China Reservorio: roedores (salvajes o domésticos) asintomáticos lo trasmiten en forma horizontal. Cada género presenta una especie de roedor. Brotes: 1. Cambios estacionales año a año 2. Cambios en la dinámica de los roedores (depredadores) 3. Intervenciones humanas (ecosistema) despoblación rural.
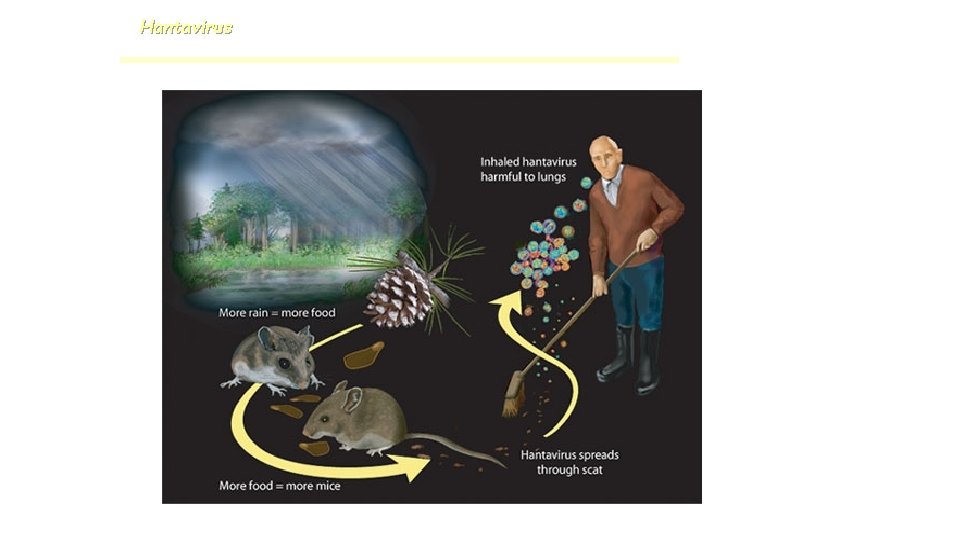
Hantavirus

HANTA • Periodo de incubación: No esta claro, entre 3 -45 días. • Cuadro clínico: Desde cuadro similar a gripe hasta síndrome Cardiopulmonar. • Fase Prodrómica (3 -5 días): • CEG, fiebre, Mialgias, Cefalea, manifestaciones gastrointestinales. • HMG: trombocitopenia, hematocrito aumentado, aumento recuento de blancos con linfocitos atípicos. • Rx Tx: Normal o infiltrado intersticial escaso. • Fase Cardiopulmonar: • • Aparición brusca de tos, disnea, hipotensión. Rápida progresión Causado por aumento de la permeabilidad capilar pulmonar. Falla respiratoria severa y shock cardiogenico refractario. Mortalidad 40% • Fase Convalecencia: • Recuperación total.
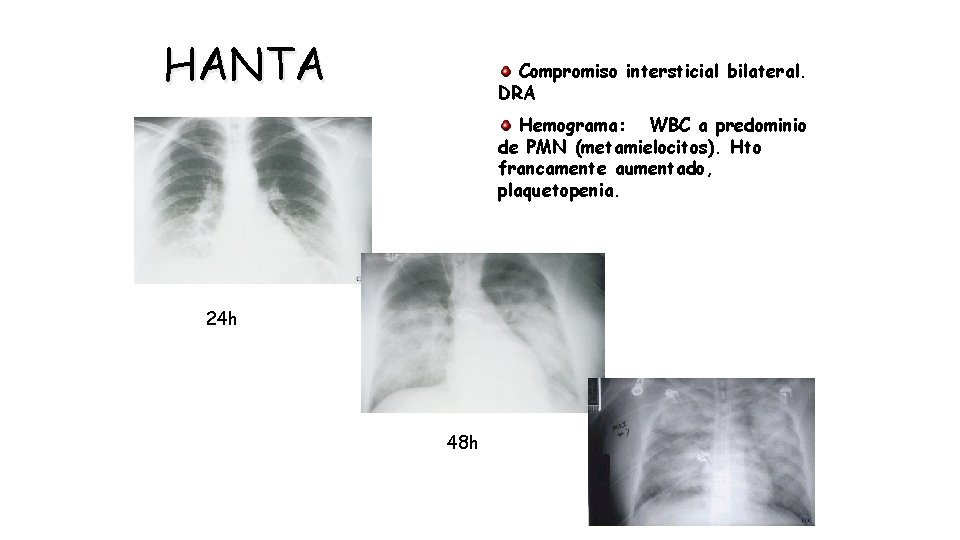
HANTA Compromiso intersticial bilateral. DRA Hemograma: WBC a predominio de PMN (metamielocitos). Hto francamente aumentado, plaquetopenia. 24 h 48 h
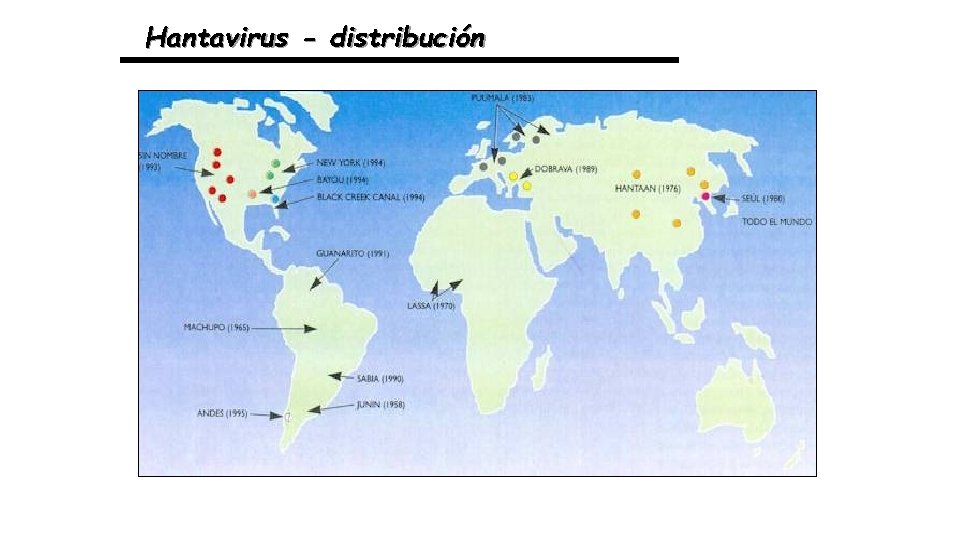
Hantavirus - distribución
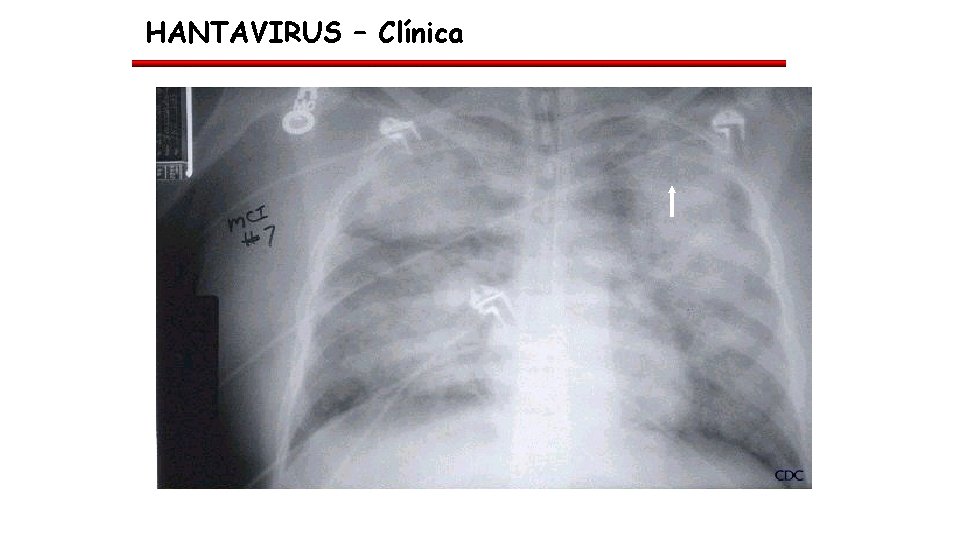
HANTAVIRUS – Clínica
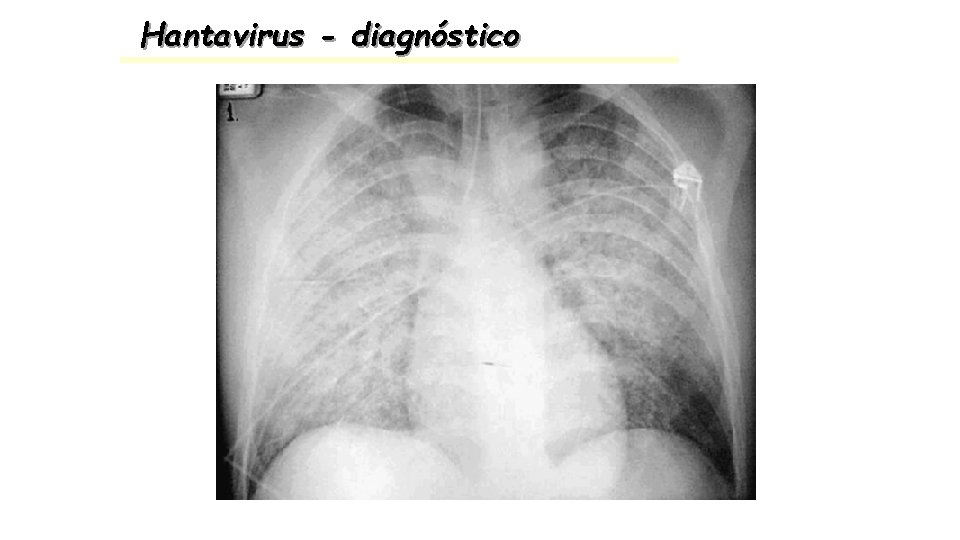
Hantavirus - diagnóstico

HANTAVIRUS – Diagnóstico microbiológico Técnicas serológicas: Ig. M en suero por ELISA de captura utiliza un antígeo de la cepa Andes y la combinación antigénica de otros tipos. El ascenso de los antígenos en suero coincide con la etapa de estado.
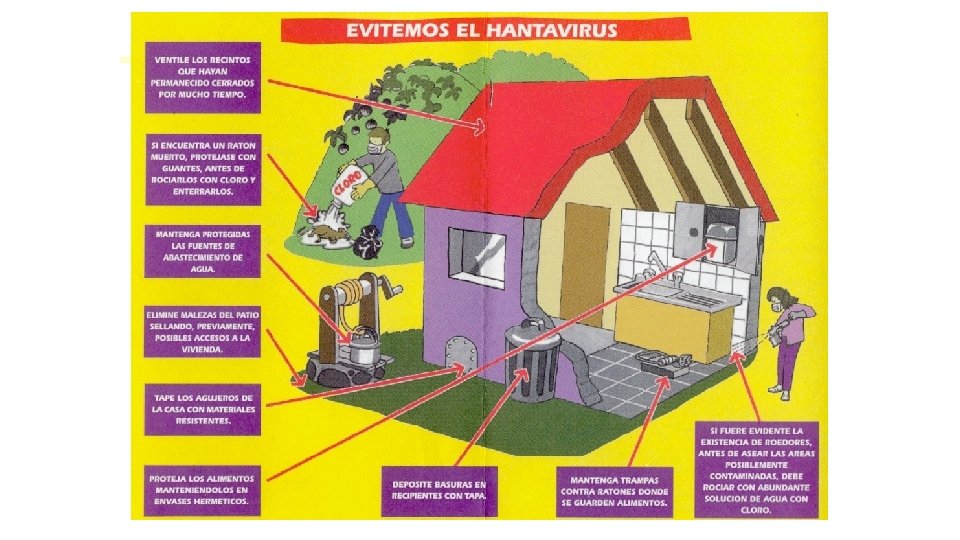
Hantavirus - recomendaciones

HANTAVIRUS – Epidemiología 1951 rió Hantang guerra de Corea (Hantavirus del viejo mundo) 1993 EEUU IRA, shock , mortalidad 80% (SPH) (Hantavirus del nuevo mundo) 1995 Chile y Argentina 1996 nueva especie Andes 1997 SPH Uruguay. 38 casos hasta 2002.

HANTAVIRUS - taxonomía Flia: Bunyaviridae Géneros: Hantan Bunyavirus Phlebovirus Nairovirus Tospovirus > 14 especies o tipos

HANTAVIRUS – Morfología y estructura Envuelto cápside helicoidal ARN –, trisegmentado, circular 2 proteínas de superficie G 1 y G 2 (adherencia y fusión), antígenos neutralizantes.

FAMILIA RETROVIRIDAE

• Son virus ARN de cadena positiva. • Codifican una ADN polimerasa ARN dependiente. (Retrotranscriptasa). • La copia del ADN viral se integra al cromosoma del hospedador.
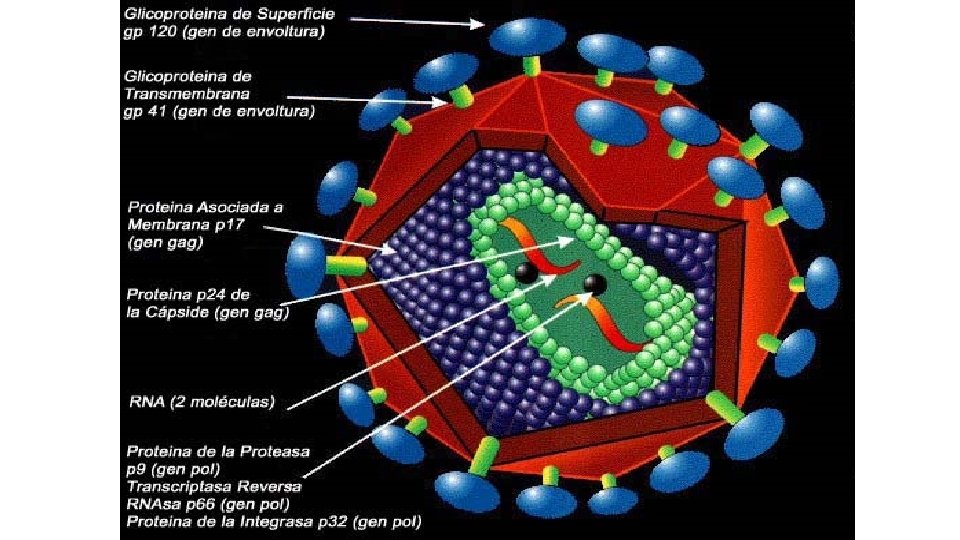
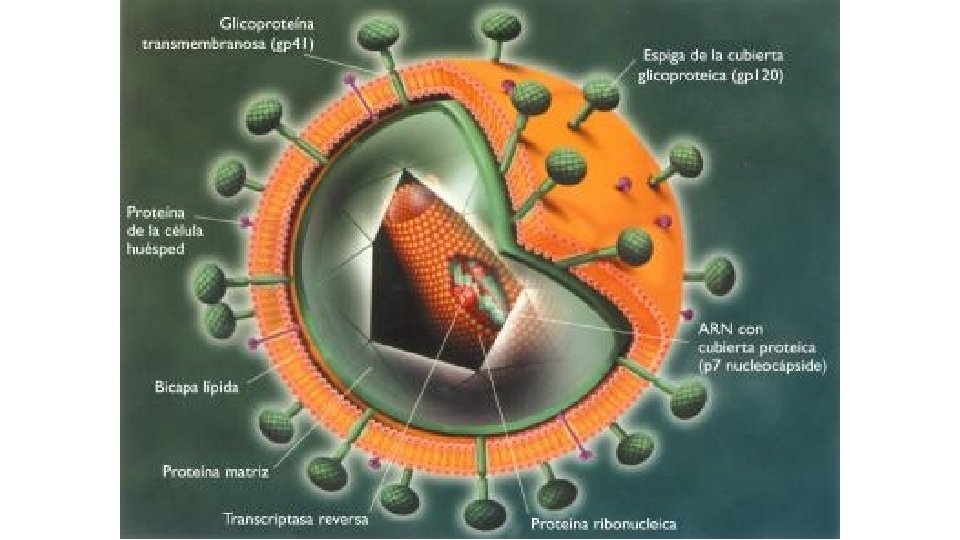

CLASIFICACIÓN Tres subfamilias: • Oncovirinae ( virus linfotrópos humanos). • Spumavirinae (no asociado a patologias). • Lentivirinae (virus de la inmunodeficiencia humana)

• Los retrovirus endógenos son conocidos como los “parásitos perfectos” • El primer retrovirus humano aislado fue el virus de la leucemia de linfocitos T humana (VLTH-1)

Retrovirus de interés médico: • VLTH-1 y VLTH-2 (oncovirus). • VIH-1 y VIH-2 (lentivirus). VLTH-1 y VIH-1 infectan linfocitos T CD 4+, se contagian de manera similar y tienen largos periodos de latencia.

ESTRUCTURA • Son virus ARN con envoltura de diámetro 80 -120 nm • La envoltura posee glucoproteínas • La cápside posee dos copias idénticas del genoma ARN de cadena positiva • Posee 10 a 50 copias de la transcriptasa inversa • Posee la integrasa, la proteasa y dos ARNt
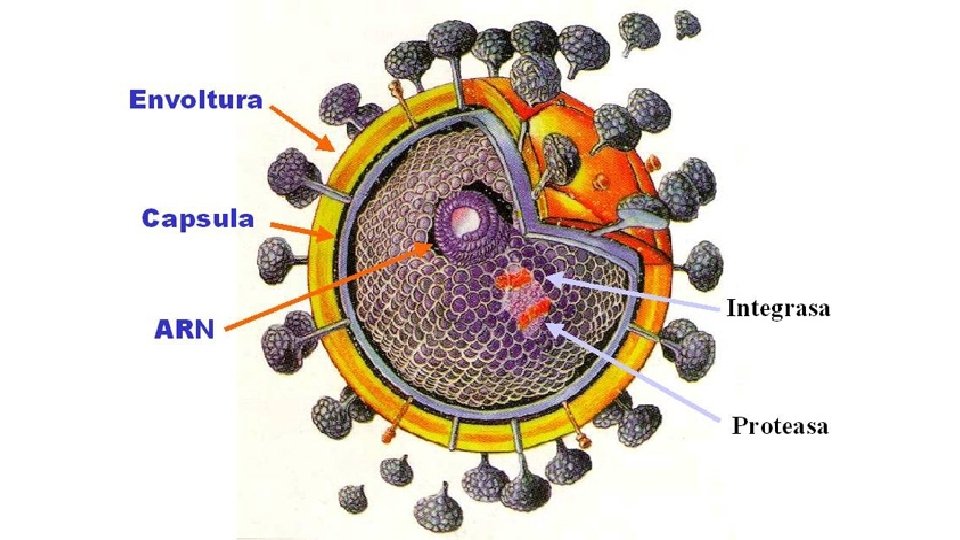

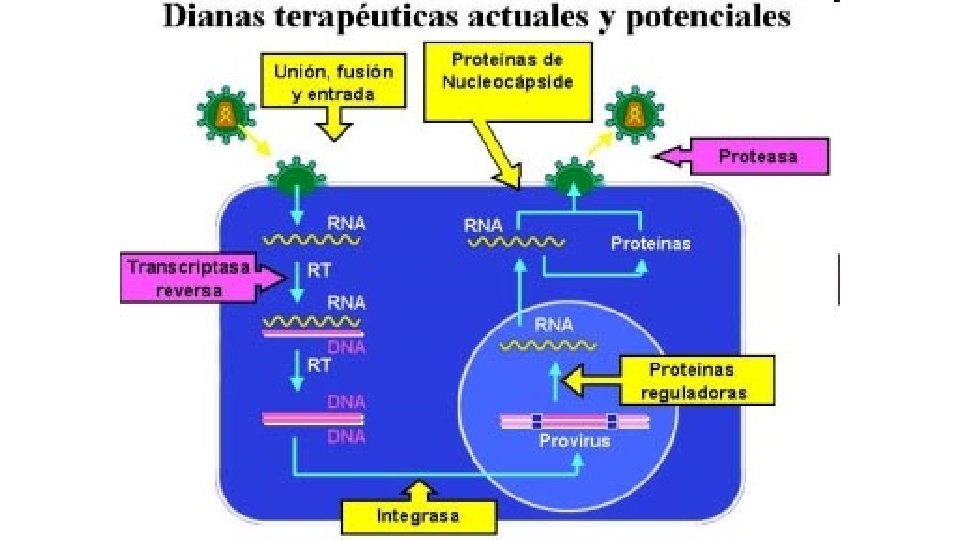
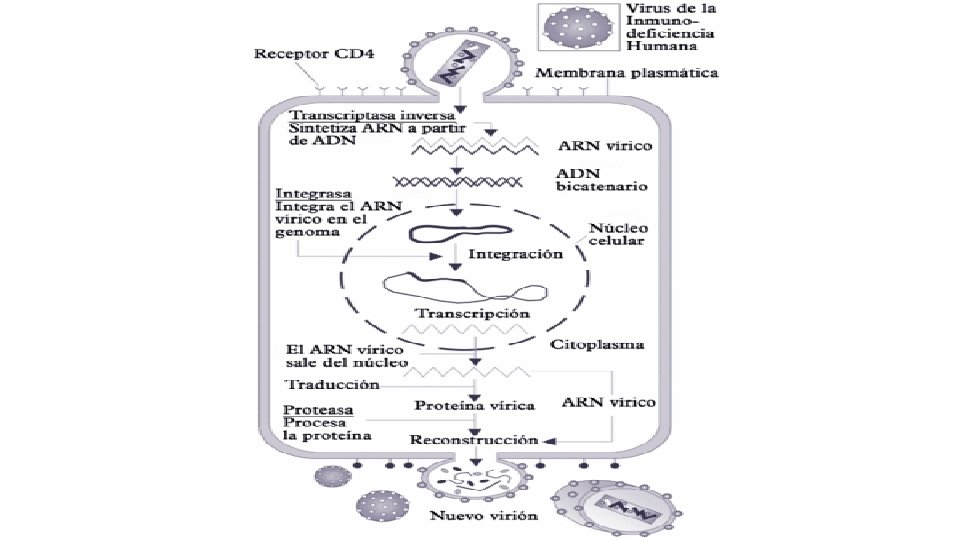
CICLO VITAL • La replicación comienza con la unión de las glucoproteínas del virus a receptores específicos de la superficie celular del hospedador
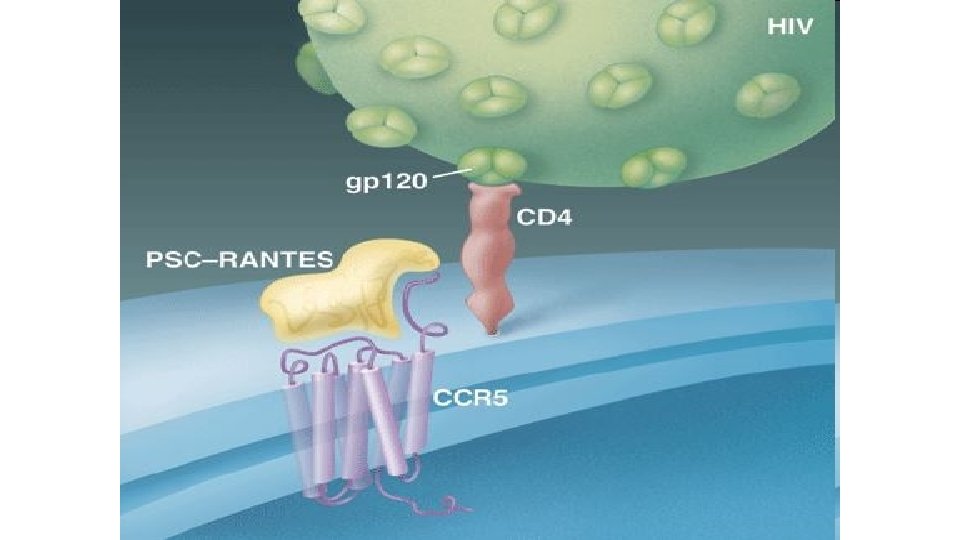
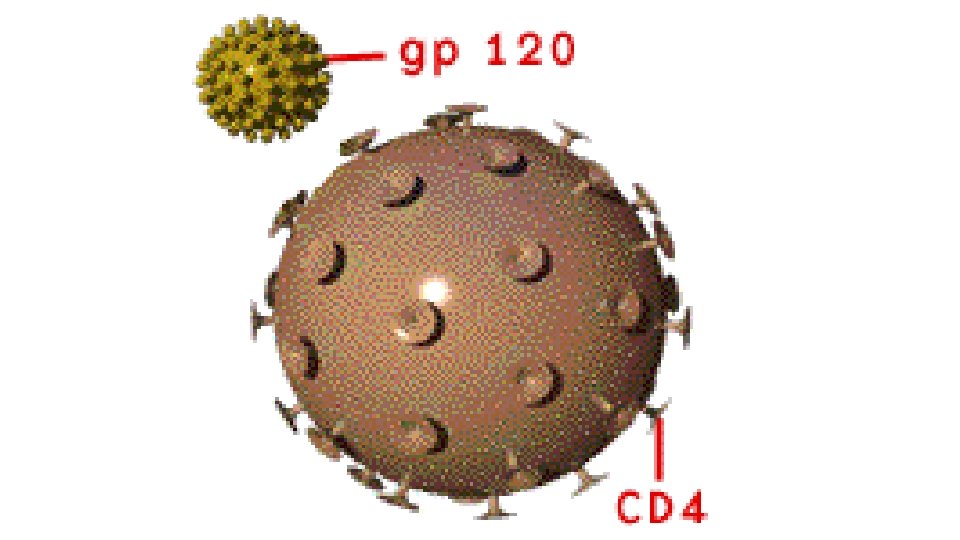

• Una vez en el citoplasma, la transcriptasa inversa sintetiza ADN de cadena negativa utilizando el ARNt del virión como cebador • La transcriptasa inversa actúa también como una ARNasa degradando el genoma ARN • Luego, sintetiza la cadena de ADN positiva, la cual pasa al núcleo

• La integrasa integra al azar esta cadena en el genoma • El ADN integrado se transcribe como un gen cualquiera por la ARN polimerasa II • Se produce ARNm a partir del cual se sintetizan poliproteínas

• Estas poliproteínas, por medio de la proteasa, se dividen en proteínas funcionales más pequeñas que luego se glicosidan • Todo esto ocurre en el RE y Golgi • Estos compuestos formados migran a la membrana plasmática, donde por gemación son liberados nuevos viriones
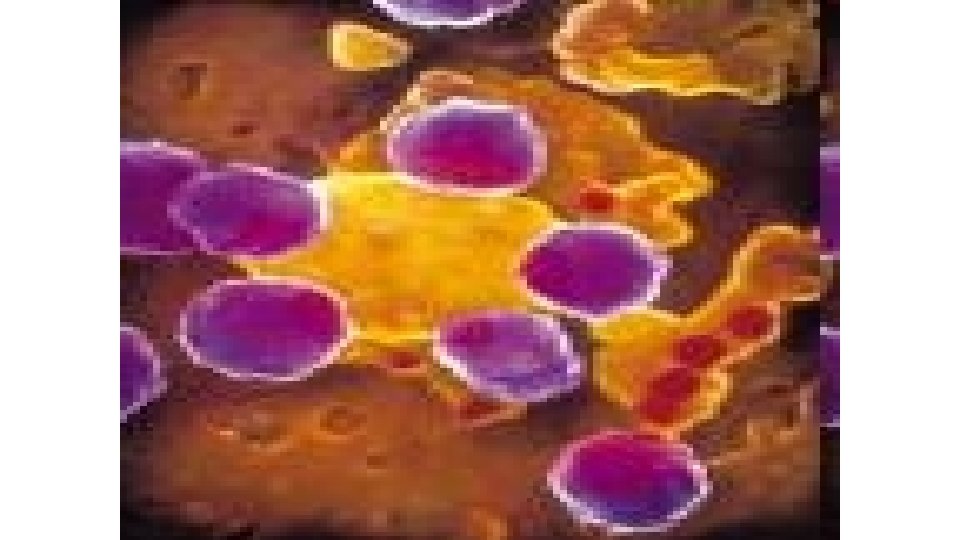


VIH • Es un virus que se adaptó al ser humano • Está comprobado que provienen evolutivamente del mono verde africano • Existen dos tipos: VIH-1 y VIH-2, ambos capaces de infectar a seres humanos • El VIH es bastante frágil en el medio ambiente

• Es rápidamente inactivado por el calor, sustancias bactericidas como el Na. Cl. O, formaldehído, glutaraldehído, alcohol y agua oxigenada. • Una de sus principales características es la extrema variabilidad genética que posee y su consecuente capacidad de mutación

• Se describen varios subtipos de VIH-1 y VIH-2 • VIH-1 se divide en grupos M, N y O • El grupo M posee 9 subtipos • Los grupos N y O poseen 1 solo subtipo

TRANSMISIÓN Puede ser transmitida de una persona infectada a otra a través de: • Sangre (incluyendo flujo menstrual) • Semen • Fluidos vaginales • Transmisión vertical

• La saliva, lágrima, sudor, heces y la orina a pesar de contener partículas virales, no son considerados fluidos transmisores

CONDUCTAS DE RIESGO

• Relaciones sexuales vaginal y anal: El VIH puede infectar la membrana mucosa de los genitales y del recto directamente o través de microtraumas causados durante la relación

• Relaciones sexuales orales (boca-pene, boca-vagina) La boca es considerada un ambiente inadecuado para el VIH, siendo menor el riesgo de transmisión que a través de la mucosa vaginal o anal

• Inyección de agujas y jeringas contaminadas • Transfusiones no controladas de sangre y derivados

• Transmisión vertical Es posible la transmisión de la madre al hijo, antes y durante el parto y a través de la leche materna. Aproximadamente el 80 % de los casos es durante el parto


DIAGNÓSTICO CLÍNICO • Se puede dividir en 4 fases: • Infección aguda • Fase asintomática • Fase sintomática • SIDA
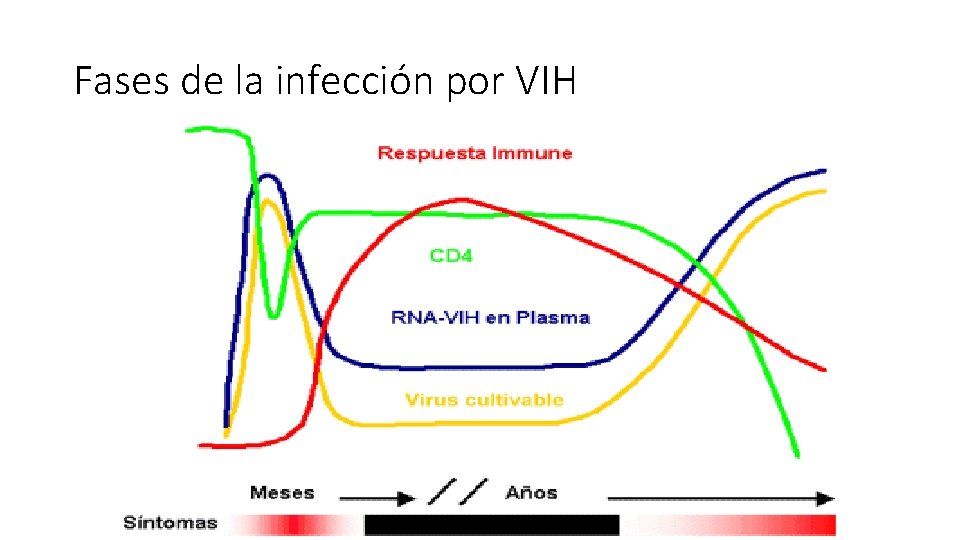
Fases de la infección por VIH

INFECCIÓN AGUDA • Se observa una rápida elevación de la viremia y amplia diseminación del virus a los órganos linfoides y al SNC • Es un cuadro clínicamente autolimitado • Las manifestaciones clínicas pueden variar desde un resfrío hasta un cuadro de mononucleosis infecciosa • Estos síntomas aparecen a las 2 -3 semanas

• La frecuencia de los síntomas es: • Fiebre: 95 % • Fatiga: 90 % • Lesiones en la piel: 90 % • Cefalea y faringitis: 70 % • La inmunidad celular cumple un papel fundamental en el control de la viremia. Se observa una disminución del los LTCD 4+

FASE ASINTOMÁTICA • Varía de una persona a otra. De 7 -10 años • Hay una marcada reducción de la viremia y un aumento de los LTCD 4+ haciendo que la enfermedad entre a un estado asintomático • En esta fase son importantes los controles complementarios

• La producción de viriones es de varios miles de millones y el intercambio de LT es de millones al día • Esto puede ayudar a explicar la naturaleza fluctuante y progresiva de la depleción de los LT

FASE SINTOMÁTICA • Representa el desequilibrio inmunológico • Hay un aumento de la viremia y una disminución de los LTCD 4+ • Aparecen los síntomas constitucionales: sudoración nocturna, fatiga, enflaquecimiento, diarrea, candidiasis oral o vaginal, herpes simple, herpes zóster y trombocitopenia

SIDA • Se caracteriza por la aparición de enfermedades oportunistas graves o de algunos tipos de cáncer • El recuento de LTCD 4+ debe ser menor a 350 por mm 3 más el diagnóstico de por lo menos una de las siguientes enfermedades:

• Criptococosis extrapulmonar • Cáncer cervical invasivo • Candidiasis de esófago • Candidiasis de tráquea, bronquios o pulmones • Citomegalovirus (exc. Hígado, bazo o ganglios) • Criptosporidiasis intestinal crónica • Herpes simple mucocutáneo (por más de 1 mes) • Histoplasmosis diseminada • Isospodidiosis intestinal crónica § Leucoencefalopatía multifical progresiva § Linfoma no Hodking de células B § Linfoma primario de cerebro § Neumonía por Pneumocystis carinii § Cualquier enfermedad por micobacterias § Reactivación del mal de Chagas § Sepsis recurrentes por Salmonella § Toxoplasmosis del SNC

• Alrededor de la mitad de todos los pacientes infectados por VIH desarrollarán una enfermedad neurológica durante el curso de la infección • Las presentaciones más comunes son: el complejo demencia-SIDA, la neuropatía vascular y la neuropatía periférica
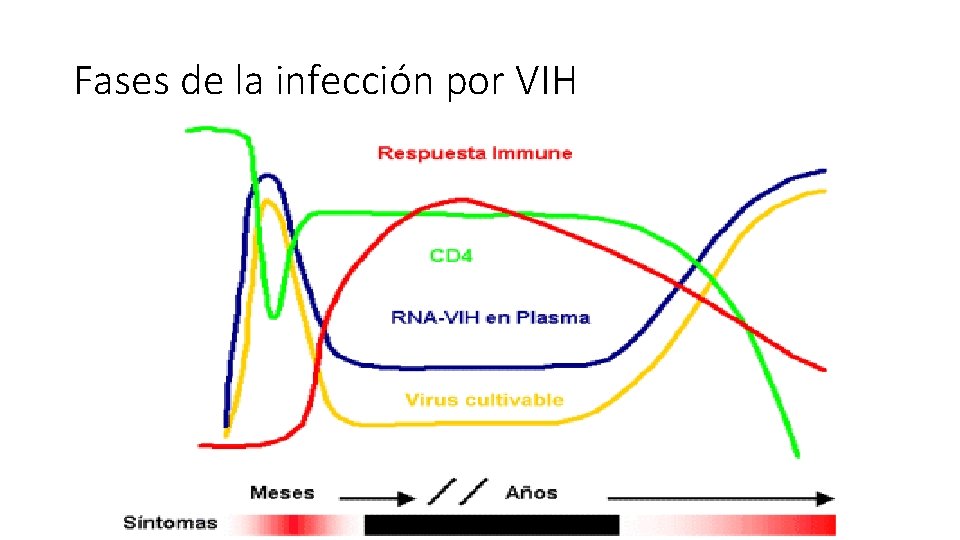
Fases de la infección por VIH


CAMBIEMOS LA “S” DE SIDA POR LA “V” DE VIDA

PRIONES • Virus lentos, no convencionales, que provocan encefalopatías espongiformes (enfermedad neurodegenerativa). • Proteínas modificadas del hospedador que puede transmitir la enfermedad. • Prión: pequeña partícula infecciosa proteica. Humanos Kuru Enfermedad de Creutzfeldt-Jakob (ECJ) Animales Scrapie Encefalopatía espongiforme bovina (vacas locas)

COMPARACION VIRUS VS PRIONES VIRUS PRION Filtrable (infeccioso) Sí No Presencia Acido Nucleico Presencia de proteínas Sí Sí No? Sí Desinfección con Formaldehído Sí No Algunos No La mayoría Sí No No Sí Dep. virus Sí Sí No Largo No No Proteasas Calor (80ºC) Radiaciones ionizantes y UV Patología Efecto citopatológico Periodo de incubación Respuesta inflamatoria Respuesta inmunitaria

ESTRUCTURA Y FISIOLOGIA • El prototipo de estos microorganismos es la scrapie o Pr. PSc (prión proteico de la scrapie). • Tanto humanos como algunos animales codifican una proteina Pr. PC (prión proteico celular). COMPARACION Pr. PSc VS Pr. Pc Estructura Resistencia a la proteasa Presencia de Scrapie en fibrillas Localización dentro o sobre las células Multiplicación Pr. PSc Pr. PC Globular Extendida Sí No Vesículas Citoplamáticas Mbna Plasmáticas Días Horas

PATOGENESIS Características patogénicas de los virus lentos. La encefalopatía espongiforme describe: • El aspecto de las neuronas vacuoladas • La pérdida de función. • Falta de antigenicidad /ausencia de reacción inmunitaria. • Ausencia de inflamación. • Síntomas pérdida de control muscular, escalofríos, temblores, demencia.
Una proteína aberrante provoca la enfermedad: Pr. Pc Pr. PSc

• Pr. PSc se une a la Pr. Pc que hay en la superficie celular
• Pr. PSc hace que Pr. Pc se transforme en Pr. PSc y se desprenda de la célula.

• A continuación la célula repone Pr. Pc.

• Las neuronas y los fagocitos absorben la Pr. PSc, difícil de degradar, lo que contribuye a la vacuolización del tejido cerebral y destrucción tisular.

PATOGENESIS Una proteína aberrante provoca la enfermedad: • Pr. PSc se une a la Pr. Pc que hay en la superficie celular y hace que se transforme en Pr. PSc, se desprenda de la célula y se acumule en las placas mieloides del cerebro. • Al ser proteinas del hospedador no se produce respuesta inmunitaria) • A continuación la célula repone Pr. Pc. • Las neuronas y los fagocitos absorben la Pr. PSc, difícil de degradar, lo que contribuye a la vacuolización del tejido cerebral y destrucción tisular. • Los priones se pueden aislar de distintos tejidos del cerebral pero solamente el cerebro presenta alguna lesión.

DIAGNOSTICO DE LABORATORIO • No existe métodos para detectar directamente el virus en el tejido. • No existe análisis serológico para detectar el anticuerpo viral • El diagnóstico debe basarse en la clínica, confirmándose con los cambios histológicos característicos del tejido cerebral. • Los priones se pueden aislar de distintos tejidos del cerebral pero solamente el cerebro presenta alguna lesión. • La identificación de Pr. P resistente a la cinasa K (Western blot) puede confirmar un caso de ECJ.

TRATAMIENTO, PREVENCION Y CONTROL • No existe tratan¡miento contra el Kuru o la ECJ. • Los agentes causales son resistentes a los procesos de desinfección utilizados para otros virus (Formaldehídos, detergentes. . . ) • Eliminación por autoclave, hipoclorito sódico (5%) o hidróxido sódico (1 M)
- Slides: 117