Rencontres Jeunes Chercheurs Annecy 2010 Le carbone 12

Rencontres Jeunes Chercheurs, Annecy, 2010 Le carbone 12 au profit de l’hadronthérapie Didier JULIANI Directeur : Christian FINCK Co-encadrant: Marc ROUSSEAU

• Choix du carbone 12 • Expériences passées • Expériences à venir

Le cancer correspond à la multiplication anarchique de certaines cellules de l’organisme. En outre, ces cellules sont capables : Ø D’envahir le tissu normal avoisinant en le détruisant, Ø Puis de migrer à distance pour former des métastases. 1

Traitements Localiser les cellules tumorales, puis les éliminer ou les tuer avec 3 armes thérapeutiques complémentaires: • Chirurgie • Chimiothérapie (médicaments) • Radiothérapie (rayonnements ionisants) 2

Historique La radiothérapie: une spécialité médicale qui existe depuis plus d’un siècle … • 1895: Découverte des rayons X par Wilhelm Conrad RONTGEN • 1896: Découverte de la radioactivité par Henri BECQUEREL 3

Objectif biologique La radiothérapie: une spécialité médicale qui existe depuis plus d’un siècle … • On cherche à détruire les cellules tumorales en cassant leur ADN par rayonnements ionisants. • Lorsqu’ils traversent les tissus biologiques, les rayonnements ionisants subissent de nombreuses collisions atomiques. • Chaque collision correspond à un dépôt d’énergie, qui produit un effet biologique en particulier en réalisant des cassures de l’ADN. • L’effet des rayonnements sur les cellules tumorales est généralement plus important que sur les cellules normales. 4
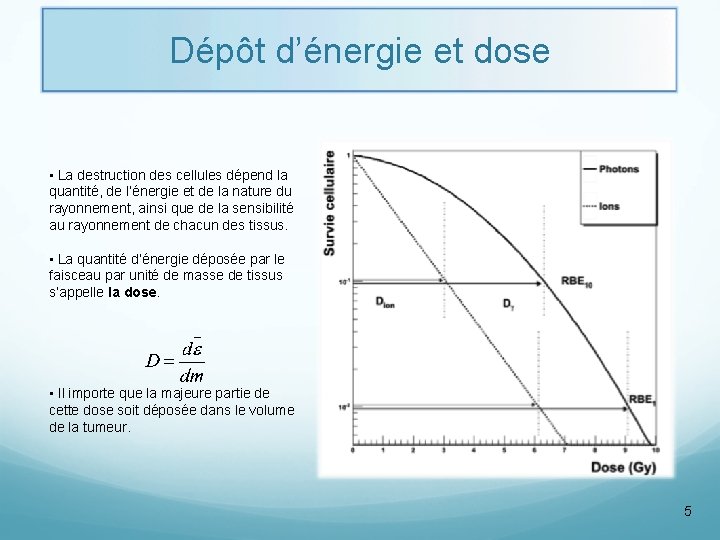
Dépôt d’énergie et dose • La destruction des cellules dépend la quantité, de l’énergie et de la nature du rayonnement, ainsi que de la sensibilité au rayonnement de chacun des tissus. • La quantité d’énergie déposée par le faisceau par unité de masse de tissus s’appelle la dose. • Il importe que la majeure partie de cette dose soit déposée dans le volume de la tumeur. 5

Dose biologique • 6 Dose biologique = RBE x D • Taux de survie dépendant du taux d’oxygène dans la cellule • => Oxygen Enhancement Ratio
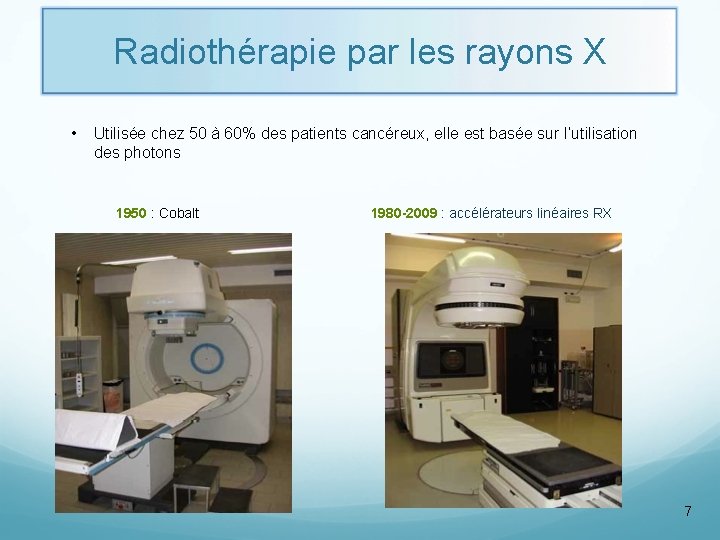
Radiothérapie par les rayons X • Utilisée chez 50 à 60% des patients cancéreux, elle est basée sur l’utilisation des photons 1950 : Cobalt 1980 -2009 : accélérateurs linéaires RX 7
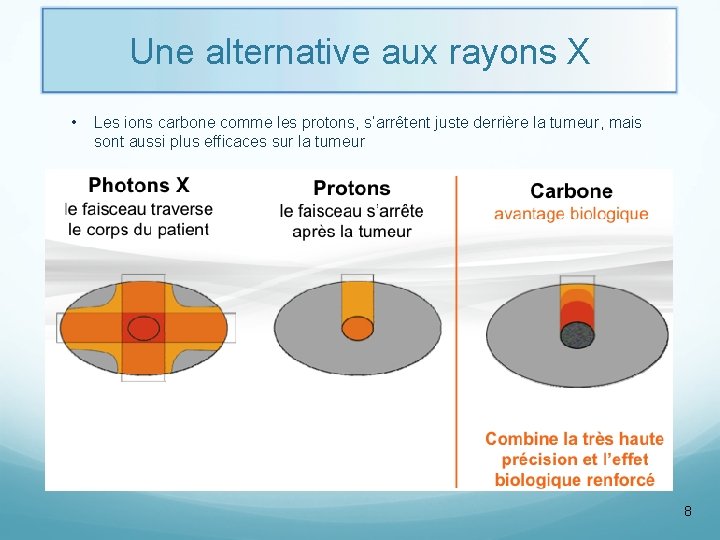
Une alternative aux rayons X • Les ions carbone comme les protons, s’arrêtent juste derrière la tumeur, mais sont aussi plus efficaces sur la tumeur 8
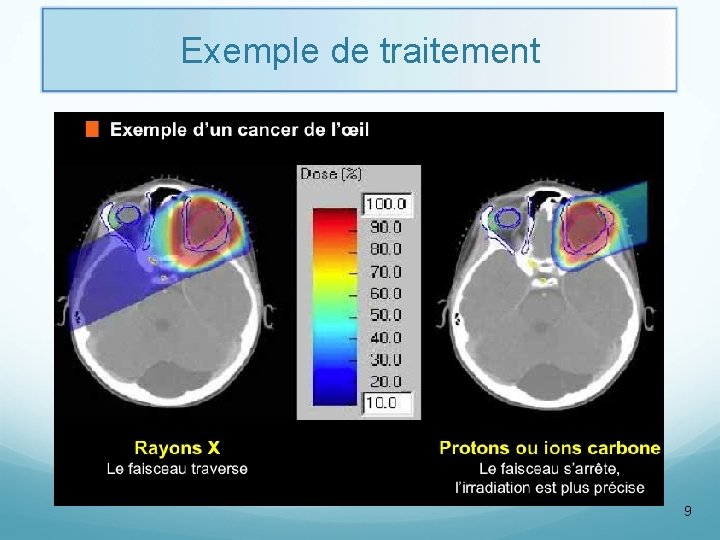
Exemple de traitement 9

Interêt physique des ions carbone Pourquoi ces rayonnements sont-ils différents ? 10

Interactions ion-matière • 3 modes d’intéraction pour les ions dans la matière: a. Collision avec les électrons de la cible b. Collision nucléaire élastique a. Collision nucléaire inélastique 11

Collisions Coulombiennes Transfert d’énergie des ions chargés de grande énergie aux électrons du milieu =>Excitation du milieu si changement de couche électronique =>Ionisation si énergie assez grande pour l’arracher de son atome 12

Perte d’énergie électronique Pouvoir d’arrêt : Formule de Bethe-Bloch (Fano 1963): transfert d’énergie lorsque vitesse projectile perte d’énergie spécifique lorsque charge Zp projectile (vitesse constante) perte d’énergie spécifique lorsque densité matériau 13
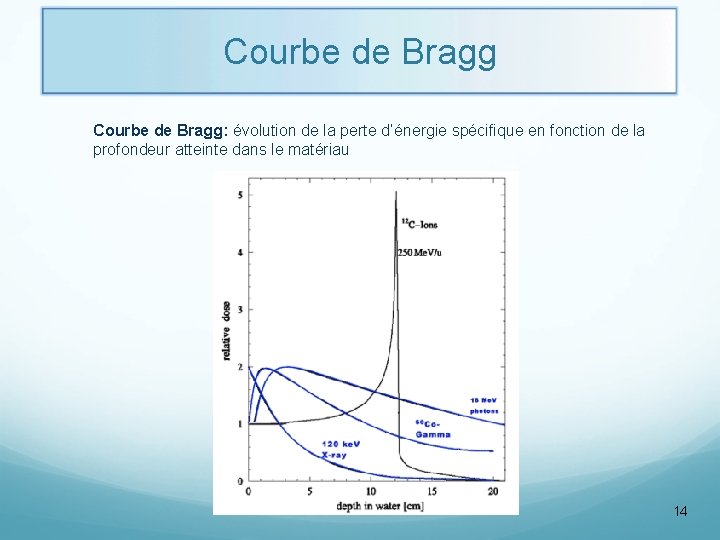
Courbe de Bragg: évolution de la perte d’énergie spécifique en fonction de la profondeur atteinte dans le matériau 14

Collisions élastiques noyau-noyau • Dispersion angulaire régie par la répulsion coulombienne, dépendant de la charge des noyaux et du paramètre d’impact Angle de diffusion lorsque paramètre d’impact • Les collisions centrales sont les moins probables (section efficace géométrique) • Dispersion angulaire lorsque charge cible 15
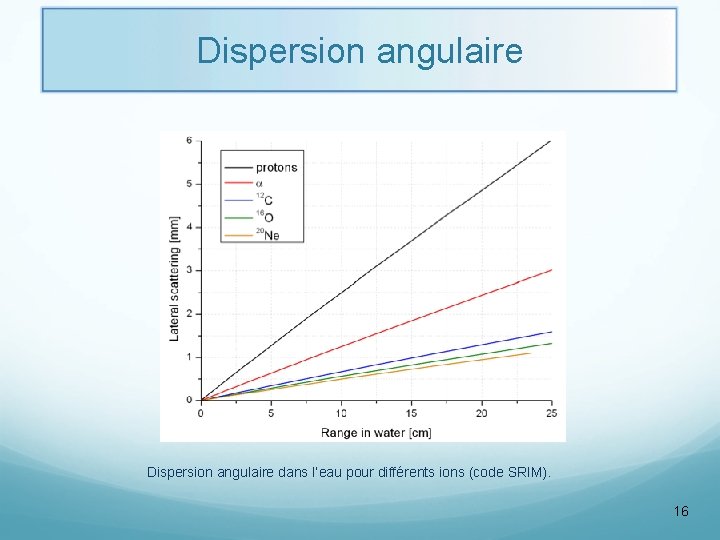
Dispersion angulaire dans l’eau pour différents ions (code SRIM). 16

Pouvoir d’arrêt nucléaire • Perte d’énergie par collisions élastiques entre le projectile et les noyaux atomiques de la cible • Dépend: 1. Du nombre d’atomes cible par unité de volume 2. De l’énergie cinétique du projectile 3. De la section efficace différentielle en énergie de diffusion élastique 17

Collisions inélastiques - Fragmentation • Energie cinétique du projectile suffisante pour franchir la barrière coulombienne du noyau cible • Zone dite « participante » : interaction des nucléons de chaque noyau => Changement de nature du projectile et de la cible (fragmentation partielle) => émission de particules plus légères 18

Consommation du projectile 19
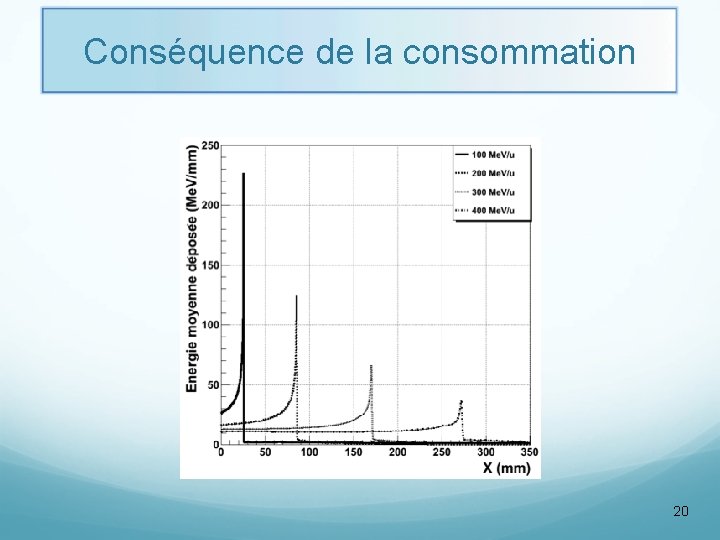
Conséquence de la consommation 20
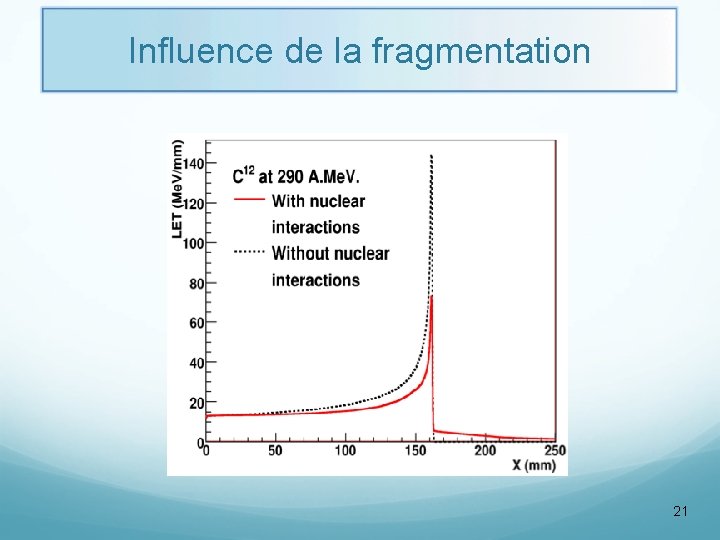
Influence de la fragmentation 21

Choix du carbone 12 comme projectile Bon compromis entre les effets bénéfiques suivants: • • • Balistique précise Dépôt d’énergie maximum en profondeur RBE entre 1, 5 et 3 selon la tumeur OER faible Rapport entre le dépôt d’énergie à l’entrée et le dépôt au pic de Bragg faible et les inconvénients: • • • Consommation des ions primaires conduisant à un dépôt d’énergie au-delà du pic de Bragg Dispersion angulaire Dégradation du faisceau 22

Expérience GANIL 2008 Motivations: • Manque de données dans les réactions nucléaires 12 C dans le domaine de la hadronthérapie pour les “basses” énergies (80 -200 Me. V) • Les codes de simulation ne reproduisent pas la dose déposée avec une bonne précision Objectifs: • Simuler correctement la dose déposée par des ions 12 C dans des tissus humains à 2, 5% près (ETOILE 2014) • Base de données de sections efficaces doublement différentielles mesurées pour le calcul des doses • Contraindre les modèles nucléaires pour le 12 C 23
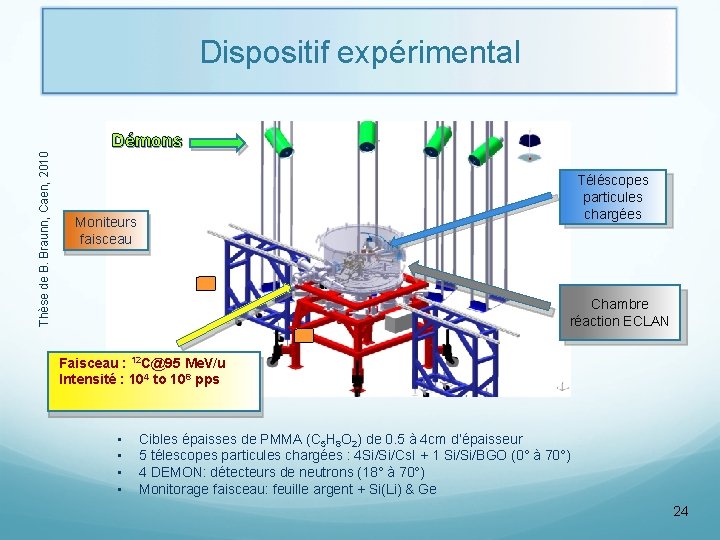
Dispositif expérimental Thèse de B. Braunn, Caen, 2010 Démons Téléscopes particules chargées Moniteurs faisceau Chambre réaction ECLAN Faisceau : 12 C@95 Me. V/u Intensité : 104 to 108 pps • • Cibles épaisses de PMMA (C 5 H 8 O 2) de 0. 5 à 4 cm d’épaisseur 5 télescopes particules chargées : 4 Si/Si/Cs. I + 1 Si/Si/BGO (0° à 70°) 4 DEMON: détecteurs de neutrons (18° à 70°) Monitorage faisceau: feuille argent + Si(Li) & Ge 24
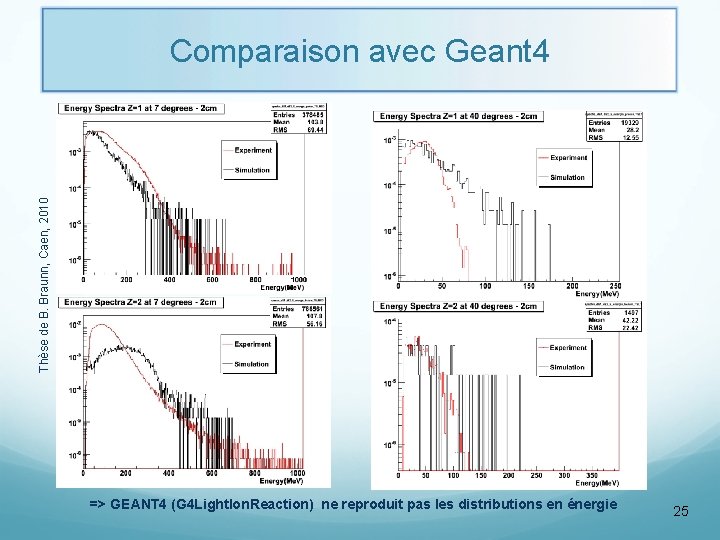
Thèse de B. Braunn, Caen, 2010 Comparaison avec Geant 4 => GEANT 4 (G 4 Light. Ion. Reaction) ne reproduit pas les distributions en énergie 25

Expériences futures • E 600: 12 C à 95 Me. V/nucléon sur cible mince PMMA, avril 2011 Equivalent tissus humains PMMA (C 5 H 8 O 2) : 0, 5 mg/cm 2 5 téléscopes similaires à l’expérience de 2008 C + (C, O, CH 2, Al …) • SPEG: 12 C à 95 Me. V/nucléon sur cible mince PMMA, proposition Mesures à 0º degré 26

Fragmentation of Ions Relevant for Space and Therapy Motivations de l’expérience FIRST Effets des rayonnements cosmiques sur les humains Fragmentation d’ions lourds Protections dans l’environnement de l’accélérateur Traitement des cancers par ions légers ( Z<9 and E<400 Me. V/u) =>Hadronthérapie Les codes de transport Monte Carlo (FLUKA, GEANT 4…) sont utilisés aussi bien en hadronthérapie qu’en radioprotection La précision du transport Monte Carlo dépend de la disponibilité des sections efficaces doublement différentielles pour les réactions d’ions lourds sur différentes cibles Les modèles physiques dans les différents codes doivent être validés en observant comment ils reproduisent les mesures expérimentales 27
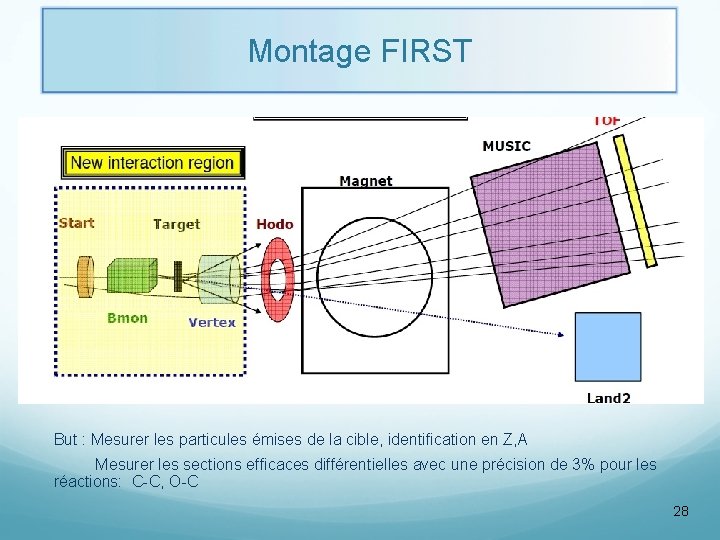
Montage FIRST But : Mesurer les particules émises de la cible, identification en Z, A Mesurer les sections efficaces différentielles avec une précision de 3% pour les réactions: C-C, O-C 28

M. Winter, in 2 p 3 Strasbourg Montage FIRST Quelques conditions pour le vertex: • Angle d’acceptance le plus grand possible • Résolution angulaire de 0. 3° ( pour l’hadronthérapie) • Temps de lecture << 1 ms 29

MIMOSA 26 • Contribution Strasbourg : Ø Développement des CMOS du télescope Ø “Digitizer” pour la partie CMOS Ø Développement du code d’analyse (tracking + d. E/dx) -> mi 2011 Ø Simulation de différentes géométrie pour les besoins de la hadronthérapie -> courant 2011 30

Conclusion et perspectives • Expérience E 600 (GANIL) : Ø Participation à la préparation et l’installation Ø Participation au traitement des données acquises • Collaboration FIRST : Ø Développement d’un télescope (vertex) • Collaboration ARCHADE : Ø Développement d’un télescope (ΔE-E) Ø Monitorage faisceau (mesure de l’intensité) 31
- Slides: 33