Rekombinant DNA teknolojisi Kathleen Danna ve Daniel Nathans
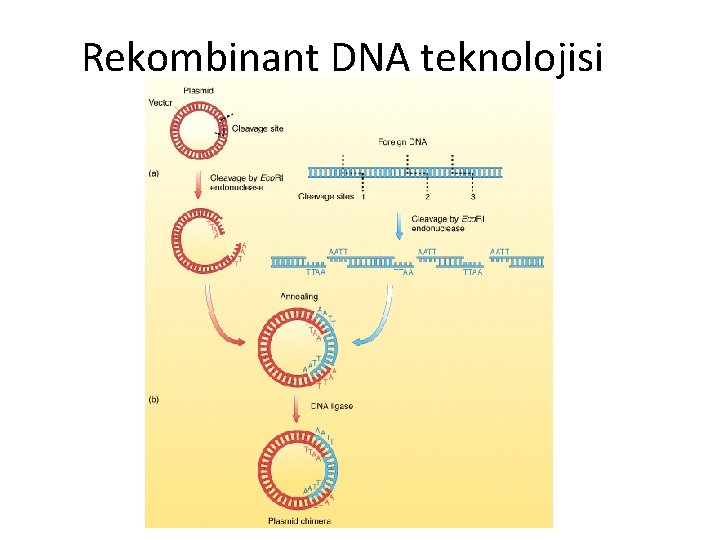
Rekombinant DNA teknolojisi

Kathleen Danna ve Daniel Nathans tarafından 1971’de yayınlanan bir makale, rekombinant DNA çağının başlangıcını işaret etmiştir. • Makale, bir bakteri suşundan bir enzimin ayrıştırılmasını ve enzimin viral DNA’yı, özgül nükleotit dizilerinden kesmek için kullanılışını tanımlar. • Bu proteinler “restriksiyon enzimleri” olarak adlandırılır.
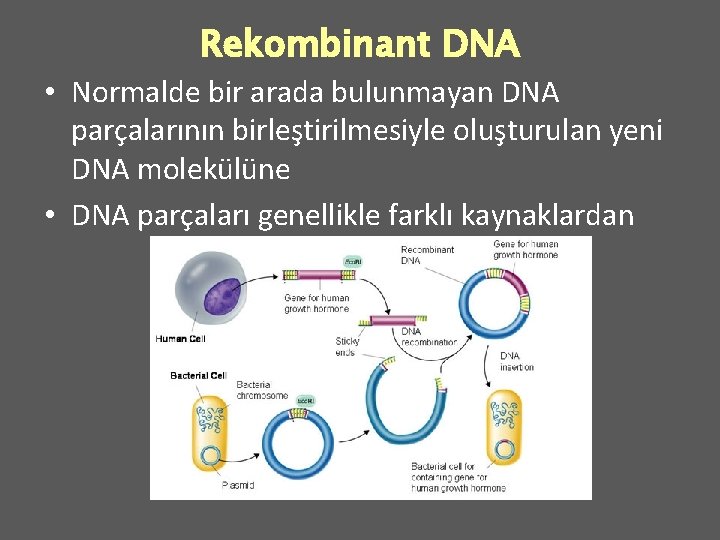
Rekombinant DNA • Normalde bir arada bulunmayan DNA parçalarının birleştirilmesiyle oluşturulan yeni DNA molekülüne • DNA parçaları genellikle farklı kaynaklardan

Bazı terimler • Genom: bir organizmanın genlerinin bütününe • Gen: kromozomlar üzerinde bulunan bireyin genetik bilgilerini taşıyan ve fonksiyonel bir ürünü (RNA veya protein) kodlayan DNA parçacığıdır. • Genotip: bireyin her türlü çevre etkisinden bağımsız olarak sahip olduğu nükleotit dizilerinin tümü • Fenotip: genetik (genotip) ve çevresel etkenlerin oluşturduğu özelliklerin canlının dış görünüşündeki yansıması • Nükleik asit: Organizmanın çoğalmasını ve işlevini kontrol eden genetik materyaller (DNA-RNA)
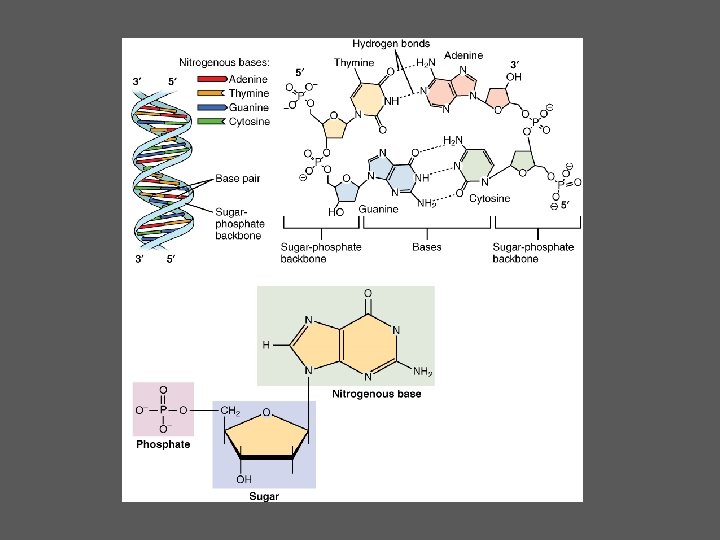

Nükleik asitler • Genetik bilgiyi aktarır DNA ve RNA Yaşayan bütün canlılarda ve virüslerde bulunur

• Rekombinant DNA teknolojisi, bir genomdaki binlerce gen arasından tek bir genin ayrıştırılmasını, tanımlanmasınıve bu genin klonlanmış DNA molekülü olarak büyük miktarlarda üretilmesinimümkün kılmaktadır. • Bu teknoloji, bir genin potansiyel olarak sınırsız miktarda üretilmesi için güçlü bir araçtır.

Uygulamaları • • • Gen izolasyonu ve sentezi Sekanslama/Genomiks/Proteomiks PCR Mutagenesis İfade analizleri (transkripsiyonel ve translasyon seviyesinde) Restriction fragment length polymorphisms (RFLPs) Biyokimya/Moleküler modelleme Gen terapisi Rekombinant aşılar

• • • Genetiği değiştirilmiş organizmalar Biyosensörler Hücre/doku kültürü Biyotemizleme Yeni nesil antibiyotiklerin üretimi Suç bilimleri

• Bilim adamları, genleri doğrudan çalışabilmek için, gen boyutundaki DNA parçalarının çok sayıda kopyasının elde edildiği yöntemlerin geliştirilmesine gereksinim duymuştur. • Diğer bir deyişle, bilim adamları gen klonlamasıile ilgili tekniklere ihtiyaç duymuştur.

• Gen klonlama: Bir genin birçok kopyasının oluşturulmasını ve izolasyonunu ifade eder. • Bir genin klonlanması için gerekli laboratuar yöntemleri 1970’lerde bulunmuştur. Bu tekniklerin geliştirilmesiyle bulunan yöntemler hücre biyologları, biyokimyacılar, bitki biyologları ve mikrobiyologlar tarafından kullanılmıştır.

• Klonlanmış DNA konak hücrelerden izole edilip incelenebilir, transkripsiyona uğratılabilir, m. RNA’sıtranslasyonasokulabilir ve kodlanan gen ürünü izole edilerek araştırma için ya da ticari amaçlarla satılmak için kullanılabilir. • Klonlanan genlerin potansiyel kullanımı 2 genel kategoride toplanır : 1. Protein ürünü elde etmek 2. Genin çok sayıda kopyasını hazırlamak

• Kopyalanacak olan DNA parçaları konak hücresine doğrudan giremezler. Ancak, restriksiyon enzimiyle kesilmiş bir DNA parçası “vektör”adı verilen başka bir DNA molekülü ile birleşirse konak hücreye girebilir. • Vektörler, kendilerine takılan DNA parçasını nakleden ve replike eden taşıyıcı DNA molekülleridir.

Bir DNA molekülünün vektör olarak kullanılabilmesi için birtakım özelliklere sahip olması gerekir; • Kendini ve taşıdığı herhangi bir DNA parçasını bağımsız olarak eşeleyebilmelidir. • Klonlanacak DNA parçasının yerleştirilmesine imkan tanıyan birçok kesim dizisi içermelidir. • Vektörde seçicilik sağlayan “marker genler” bulunmalıdır. Bunlar, vektör taşıyan ve taşımayan konak hücreleri ayırmak için gereklidir. • Konakçı hücre karşı toksik etkiye sahip olmamalı.

Vektör çeşitleri • • Plasmidler Bakteriyofajlar Cosmidler Bakteri Yapay Kromozomları (BAC) Maya Yapay Kromozomları (YAC) Memeli Yapay Kromozomları (MAC) İnsan Yapay Kromozomları (HAC) İfade Vektörleri
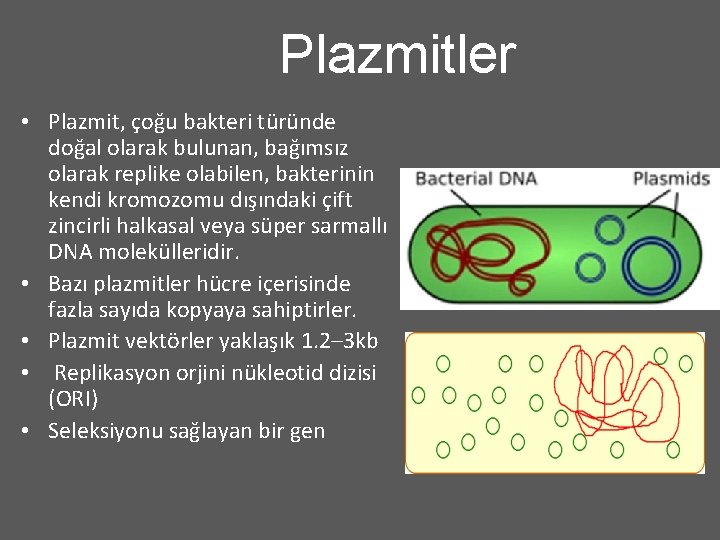
Plazmitler • Plazmit, çoğu bakteri türünde doğal olarak bulunan, bağımsız olarak replike olabilen, bakterinin kendi kromozomu dışındaki çift zincirli halkasal veya süper sarmallı DNA molekülleridir. • Bazı plazmitler hücre içerisinde fazla sayıda kopyaya sahiptirler. • Plazmit vektörler yaklaşık 1. 2– 3 kb • Replikasyon orjini nükleotid dizisi (ORI) • Seleksiyonu sağlayan bir gen

Plazmit Vektörler • Plazmitler, vektör olarak kullanılabilmeleri için genetik mühendisliği ile çok fazla değişikliğe uğratılmıştır. • Plazmit vektörler genellikle 10 kb’a kadar insert DNA taşırlar. • Plazmitler, ilk geliştirilen vektörlerdir ve hala klonlama için yaygın olarak kullanılmaktadır. • Kullanan ilk plazmit vektör, p. BR 322 olarak adlandırılmıştır. Bu vektörün büyüklüğü 4361 bp’dir.


Seçici Markör • Seçici markör, plazmidin hücre içinde korunmasını sağlar. Çünkü markör genin varlığında plazmit hücre için yarar sağlamaktadır. • Seçici koşullarda sadece seçici markör genini taşıyan hücreler yaşayabilir. • Çeşitli antibiyotiklere dayanıklılık sağlayan genler kullanılır. • Anficilin, neomisin veya kloronfenikol

Replikasyon orjini • Replikasyon orjini hücresel DNA replikasyon enzimleri tarafından tanınan DNA bölgesidir. • Replikasyon orjini olmadan DNA hücre içinde kendini eşleyemez.

Çoklu klonlama bölgesi • Birçok klonlama vektörü çoklu klonlama bölgesi veya polylinker içerir. Bu bölgelerde yanyana birçok restriksiyon enzimi kesim bölgesi mevcuttur. • Çoklu klonlama bölgesinde yer alan kesim enzimi bölgesi plazmidin diğer kısımlarında yer almaz. • Bu bölgede yer alan enzimlerle plazmit kesildiği zaman plazmidin diğer özellikleri etkilenmez.
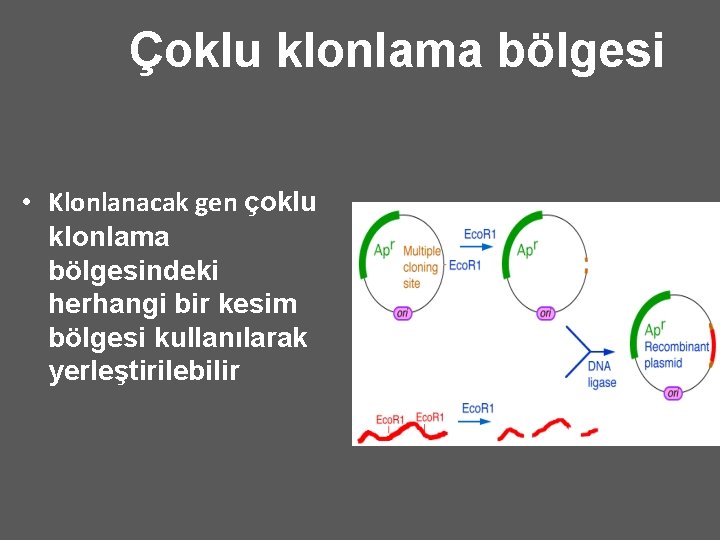
Çoklu klonlama bölgesi • Klonlanacak gen çoklu klonlama bölgesindeki herhangi bir kesim bölgesi kullanılarak yerleştirilebilir

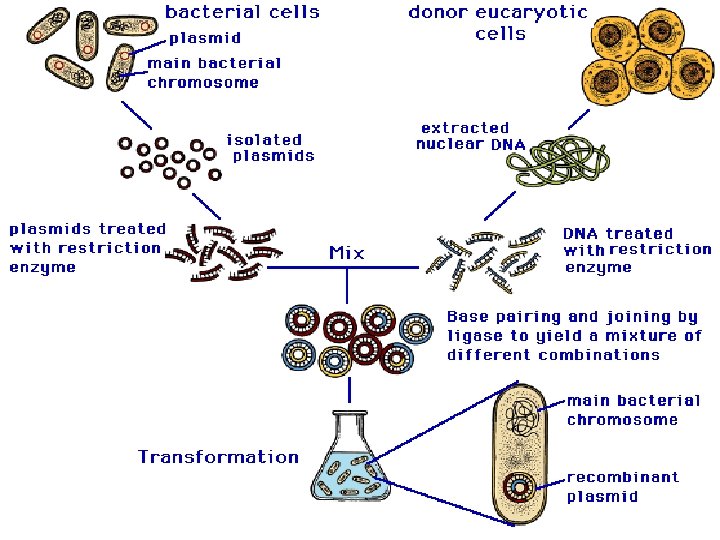
Ökaryotik bir genin izole edilmesi ve klonlanması • • Vektör ve gen-kaynağı DNA’nın izolasyonu DNA’nın vektöre takılması Klonlama vektörünün hücrelere aktarılması İstenen geni taşıyan hücre klonlarının ayrımı • Gen-kaynağı DNA, laboratuar kültüründe gelişmekte olan insan doku hücrelerinden elde edilir. • Plasmid ise, E. coli bakterisinden elde edilir. Plasmid DNA’sın da ampisilindirenç geni ve lac. Zgeni bulunur. Ayrıca, restriksiyon enzimi için tek bir tanıma dizisi bulundurur ve bu dizi lac. Zgeni içerisinde yer alır.
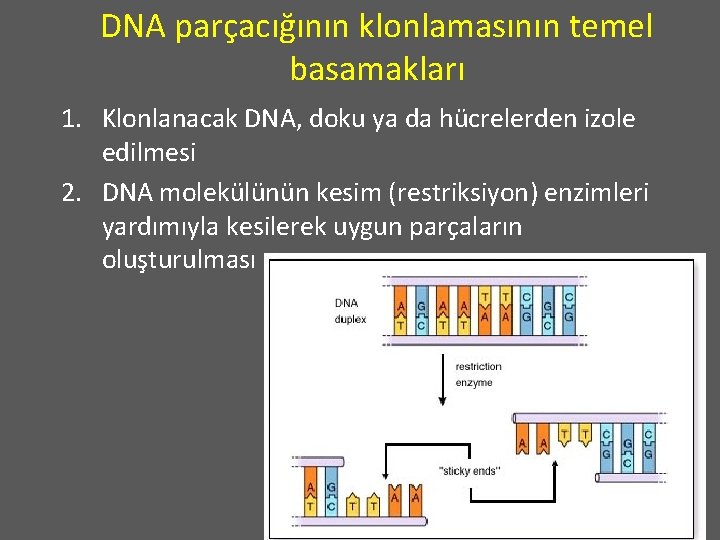
DNA parçacığının klonlamasının temel basamakları 1. Klonlanacak DNA, doku ya da hücrelerden izole edilmesi 2. DNA molekülünün kesim (restriksiyon) enzimleri yardımıyla kesilerek uygun parçaların oluşturulması
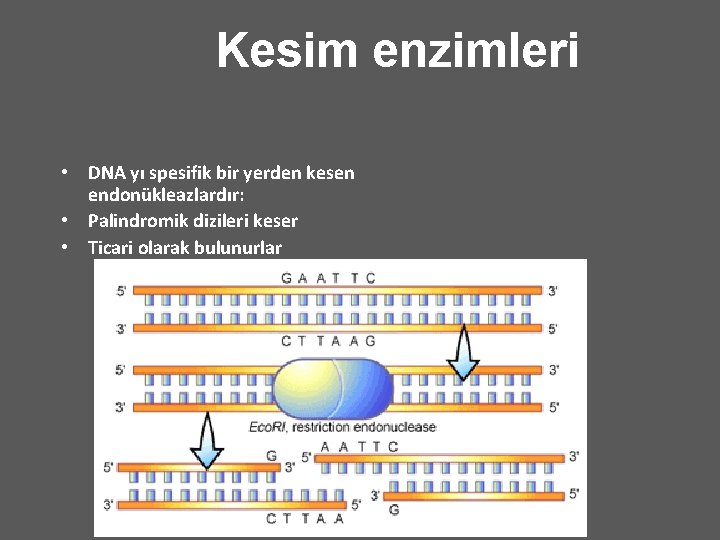
Kesim enzimleri • DNA yı spesifik bir yerden kesen endonükleazlardır: • Palindromik dizileri keser • Ticari olarak bulunurlar


3. Kesilen parçanın uygun vektöre yerleştirilmesi. Plasmid yapışkan uçları, DNA fragmentlerinin komplementer yapışkan uçları ile baz çiftleri oluşturur. Bunun yanı sıra, iki plasmidin bir araya gelmesi, plasmidin kendine kapanması ya da plasmidin çeşitli DNA parçalarıyla birleşmesi gibi kombinasyonlar da ortaya çıkabilir. DNA moleküllerini kovalentbağlarla birleştirmek üzere DNA ligazenzimi uygulanır. Sonuç olarak, rekombinant DNA’lardan oluşan bir karışım oluşur

4. Rekombinant DNA molekülünün uygun konakçı hücreye aktarılması – – Transformasyon Her hücre r. DNA = KLON Replikasyon sonucu binlerce r. DNA molekülü Konakçı hücre bölündükçe yeni oluşan hücrelere de r. DNA aktarılması • Transformeedilen bakteriler, antibiyotik seleksiyonu ve X-gal bulunan katı besiyerine ekilir. • Çoğalan bakteriler bir hücre klonu oluştururlar. • Bu şekilde, plasmidlertarafından taşınan insan genleri aynı zamanda klonlanmış olur. • Rekombinant plasmidleri taşıyan hücre kolonilerini seçmede plasmidin kendi genlerinden yararlanılır.
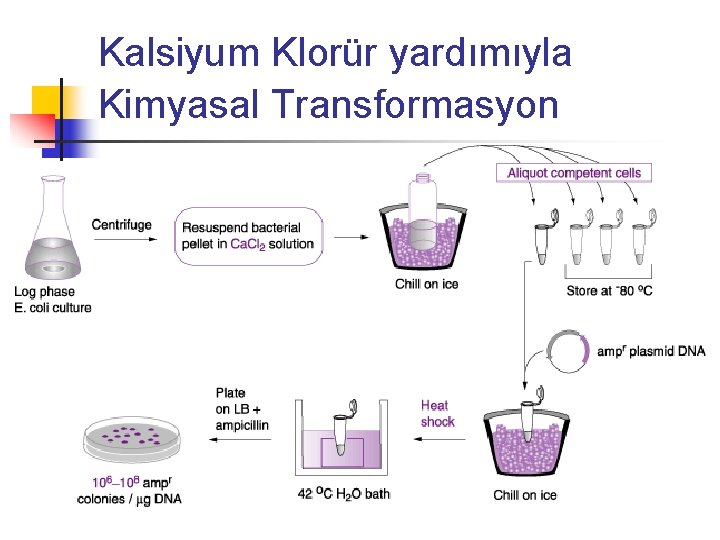
Kalsiyum Klorür yardımıyla Kimyasal Transformasyon
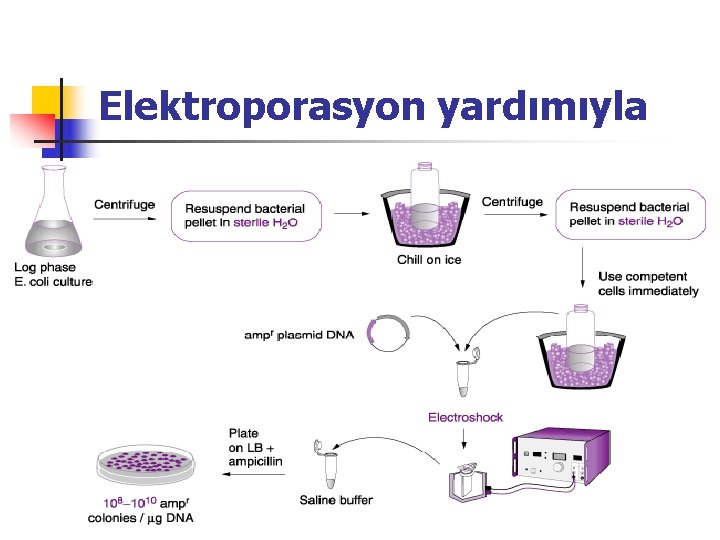
Elektroporasyon yardımıyla
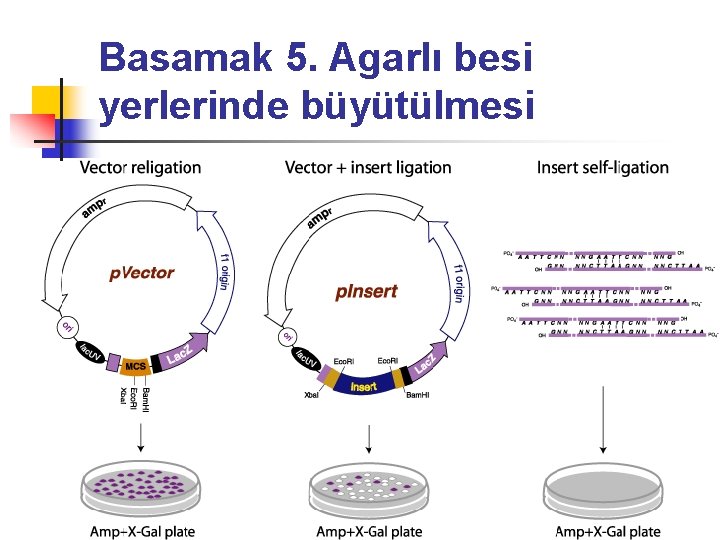
Basamak 5. Agarlı besi yerlerinde büyütülmesi

Basamak 5 n Mavi koloniler Anficiline dirençli ve p. Vector bulunduran bakterileri göstermektedir. Bunlar parçalanmamış Lac. Z alfa kodlama bölgesindeki fonksiyonel alfa parçasını ifade etmektedir. Beyaz koloniler ise Anficiline dirençli olup p. Insert içeren ve Lac. Z alfa parçacığını içermeyen bakterileri gösterir.
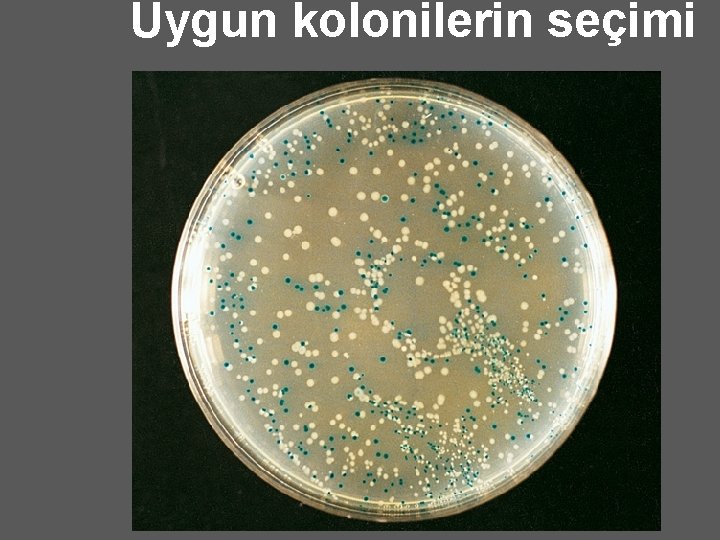
Uygun kolonilerin seçimi

• 4. r. DNA aktarılan hücrelerin çoğalması. – Amplification – Moleküler analizler için DNA izolasyonu • Genlerin organizasyonunun incelenmesi • Yapı / Fonksiyon • Aktivasyon

Lambda fajı • Lambda fajı genlerinin hepsi tanımlanmış, tüm genomunun haritası çıkarılmış ve nükleotit dizisi belirlenmiştir. ʎ fajının genetik olarak değiştirilmiş suşları vektör olarak kullanılır. • Bakterileri enfekte eden virüsler…. Lizis • Bakteriyel virüs, E. coli konakçı olarak kullanır. • Tipik bir faj yapısına sahiptir: baş, kuyruk , boyun bölgesi. • Lambda virüs genom: 48. 5 kb düz DNA (her iki ucta 12 bazlık tek zincirli ss. DNA yapışkan uç…. cos bölgesi) • Enfeksiyon : lambda kuyrukları hücre reseptörlerine bağlanır ve DNA enjekte edilir. DNA cos bölgelerinde dairesel yapı kazanarak E. coli içinde yaşamaya başlar. • Virüslerde sitoplazma ve enzim sistemleri yoktur
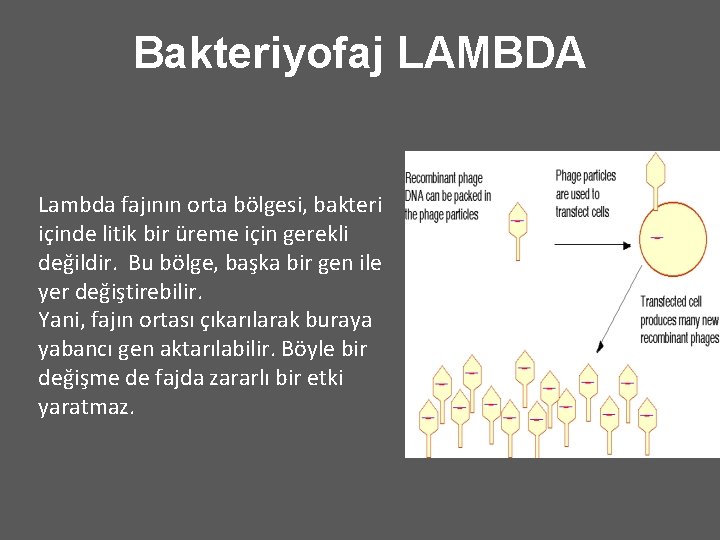
Bakteriyofaj LAMBDA Lambda fajının orta bölgesi, bakteri içinde litik bir üreme için gerekli değildir. Bu bölge, başka bir gen ile yer değiştirebilir. Yani, fajın ortası çıkarılarak buraya yabancı gen aktarılabilir. Böyle bir değişme de fajda zararlı bir etki yaratmaz.

Kozmit Vektör • Amaç: Büyük DNA parçalarının klonlanması DNA: büyüklük~ 45 kb Özellikler: Kozmidler bir yada iki Lamda Cos bölgesi içeren plazmitlerdir. Kozmit vektörler, bir bakteriye ait ve replikasyon orjin bölgesine sahip plazmitle, buna birleştirilmiş lamda fajı yapışkan ucundan (cos, cohesive ends) oluşturulmuşlardır (hibrit vektörler). • Cos bölgelerinin bulunması kozmit DNA’sının Lamda fajının içine yerleştirilebilmesini sağlar.

Bakteriyel yapay vektörler (BAC) • Ökaryotik genomların analiz ve haritalanmasında ihtiyaç duyulan büyük DNA parçalarının klonlanabilmesi için geliştirilmiş vektörlerdir. • BAC’lar, bakterinin üreme plazmidi olan F faktörü ile oluşturulur. • F faktörleri, bakteri konjugasyonu sırasında genetik bilgiyi transfer eden, bağımsız olarak kendini eşleyebilen plasmidlerdir • BAC’lar yaklaşık 300 kb DNA taşıyabilir. • Replikasyon için F faktör genlerini, markır olarak antibiyotik direnç genlerini ve çoklu klonlama bölgesini taşırlar.

Maya yapay kromozomları (YAC) • Bir YAC her iki uçta telomer yapısı, bir replikasyon orjini (otonom olarak replike olan diziler) ve mayaya ait bir sentromer içerir. • İki adet markır (TRP 1 ve URA 3) bulunur. • Çoklu klonlama bölgesi mevcuttur. • 2 megabaz (2 milyon bç) uzunluğunda DNA parçaları YAC’ların içine girebilir. • Hem bakteride hem de mayada replike olabilir.

PCR İlk kez 1985'de bilim dünyasına sunulduğundan itibaren polimeraz zincir reaksiyonu (PCR); hem araştırmada hem de klinik laboratuarlarda tanıda yeni bir çığır açmıstır. ABD'de Cetus şirketin'de çalisan Henry A. Erlich, Kary Mullis ve Randall K. Saiki tarafindan gelistirilmistir. Metod basitçe tüpte nükleik asitlerin uygun kosullarda çogaltilmasidir. (Science, 1985: 230, 1350). Bu bulusundan dolayi K. Mullis, 1993 yili Nobel Kimya Ödülüne hak kazanmistir.

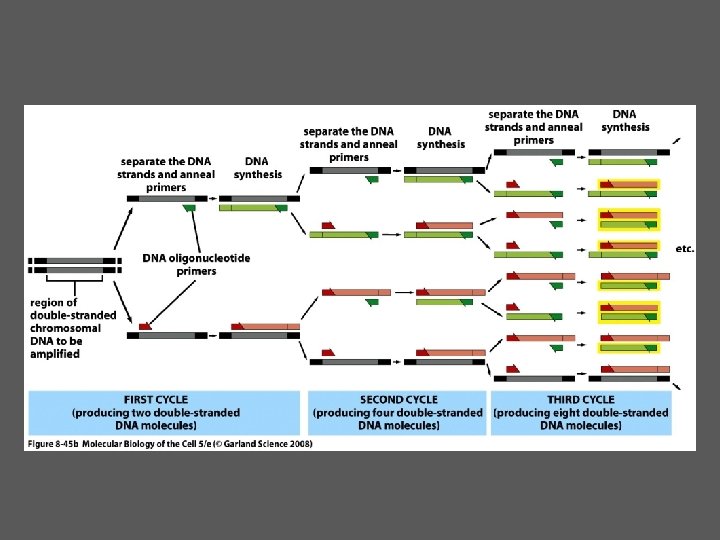
PCR Reaksiyonu? PCR reaksiyonunda üç temel basamak vardır ve çoğaltılmış ürün miktarı, bu üç adımın tekrarına bağlıdır. 1) Denatürasyon (90 -95 °C) 2) Primer bağlanması (50 -70 °C) 3) DNA sentezi (70 -75 °C) Bu üç adım bir PCR siklüsünü oluşturur (Genetik Kavramlar S-515)

İlk adımda, çoğaltılacak DNA denatüre edilerek tek zincirli hale getirilir. Herhangi bir materyal kullanılabilir. Bitki, kurumuş kan gibi adli tıp örnekleri, uzun süre saklanmış tıbbi örnekler, tek bir saç teli, mumya kalıntıları, fosil gibi değişik kaynaklardan elde edilebilir Çift zincirli DNA ısıtılarak tek zincirli hale getirilir.
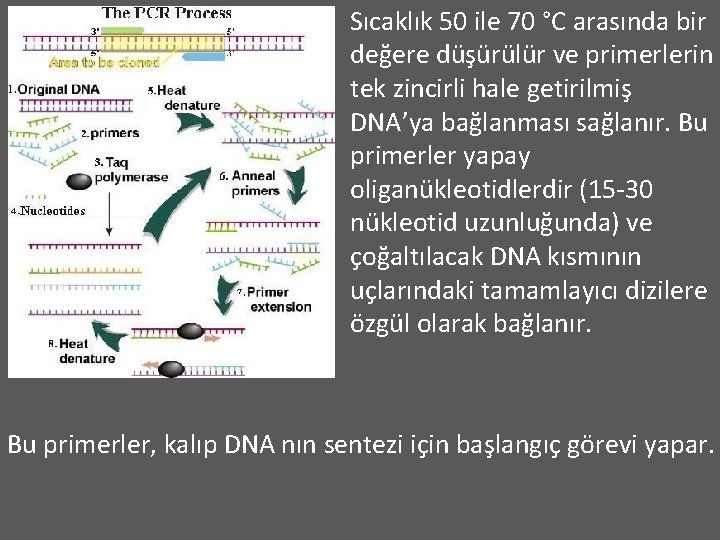
Sıcaklık 50 ile 70 °C arasında bir değere düşürülür ve primerlerin tek zincirli hale getirilmiş DNA’ya bağlanması sağlanır. Bu primerler yapay oliganükleotidlerdir (15 -30 nükleotid uzunluğunda) ve çoğaltılacak DNA kısmının uçlarındaki tamamlayıcı dizilere özgül olarak bağlanır. Bu primerler, kalıp DNA nın sentezi için başlangıç görevi yapar.
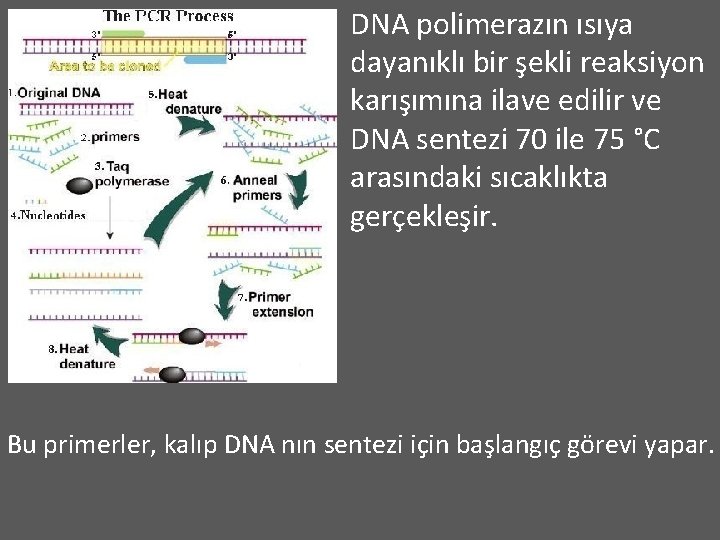
DNA polimerazın ısıya dayanıklı bir şekli reaksiyon karışımına ilave edilir ve DNA sentezi 70 ile 75 °C arasındaki sıcaklıkta gerçekleşir. Bu primerler, kalıp DNA nın sentezi için başlangıç görevi yapar.
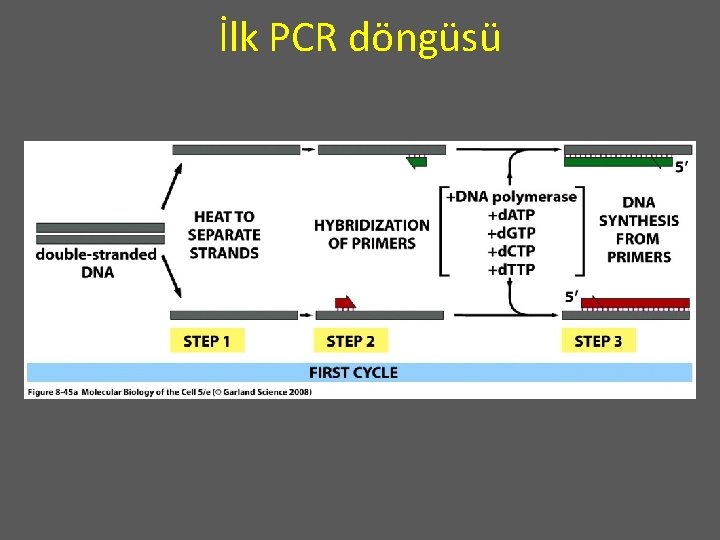
İlk PCR döngüsü 94°C 37 -65°C 70 -75°C

Thermus aquaticus Taq DNA polymerase


PCR da kullanılan malzemeler 1) Kalıp DNA 2) Reaction buffer (x 2, 5 µl) 3) forward primer (x 0, 5 µl) 4) reverse primer (x 0, 5 µl) 5) d. NTP (x 4 µl) 6) Mg. Cl 2 (x 2, 5 µl) 7) Taq Polimraz (x 0, 25 µl)

PCR’ın Sınırlılıkları • Kısa ürünlerin elde edilmesi • Kontaminasyona açık olma • Taq DNA polymerase giderek inaktive olur. Taq DNA Polimerazin, yari ömrü 92. 5°'de 130 dk; 95°C'de 40 dk'dir. Bu nedenledir ki PCR'in sonlarina dogru olan sikluslarda aktivitesi sinirlanmaktadir. • Ortamda Fenol kalıntılarının bulunması PCR ı inhibe eder.

Real Time PCR Son yılllarda PCR reaksiyonlarında sıcaklık döngüleri sağlamak için kullanılan cihazların (thermocycler) hassas ölçüm aletleriyle birleştirilmesi, real-time PCR olarak adlandırılan yeni bir yöntemin gelişmesine neden olmuştur. Real-time PCR’da ürünlerin analizi reaksiyon sırasında yapılmaktadır. Bu nedenle, agaroz jel elektroforezi, DNA bantlarının mor ötesi ışık altında görüntülenmesi gibi işlemlerin uygulanmasına gerek kalmamaktadır. Real-time PCR ürünlerinin kalitatif ve kantitatif analizlerinde, diziye özgün olmayan floresan boyalardan ya da diziye özgün problardan yararlanılmaktadır.

Real-Time PCR Real-time PCR monitors the fluorescence emitted during the reaction as an indicator of amplicon production at each PCR cycle (in real time) as opposed to the endpoint detection Real-Time PCR Real-time PCR Reaksiyon esnasında her bir PCR siklüsünde yeterli miktarda ürünün verdiği floresans ışığa göre çalışıp reaksiyonu aşama sonuna kadar oluşan ürünü kontrol eden bir sistemdir.

Gerçek Zamanlı PCR ( Real Time PCR ) Işıma özelliğine sahip moleküller kullanarak PCR’ı oluşurken izleme ve miktar belirleme yöntemidir.

*Sinyal üretimi Amplikon miktarını PCR’ın linear fazında izlemek Primer/prob/amplikonların florojenik moleküllerle İşaretlenmesi *Cihaz Sinyali saptamak ve değerlendirmek Thermal cycler +Eksitasyon. Emisyon sistemleri+Bilgisayar
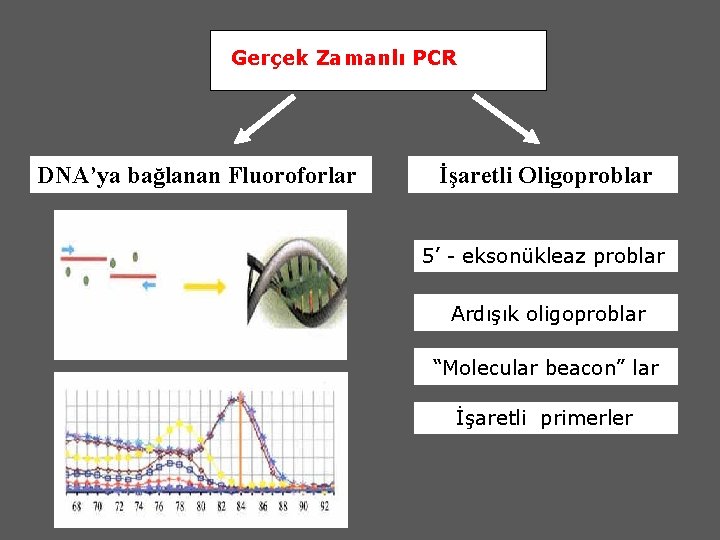
Gerçek Zamanlı PCR DNA’ya bağlanan Fluoroforlar İşaretli Oligoproblar 5’ - eksonükleaz problar Ardışık oligoproblar “Molecular beacon” lar İşaretli primerler

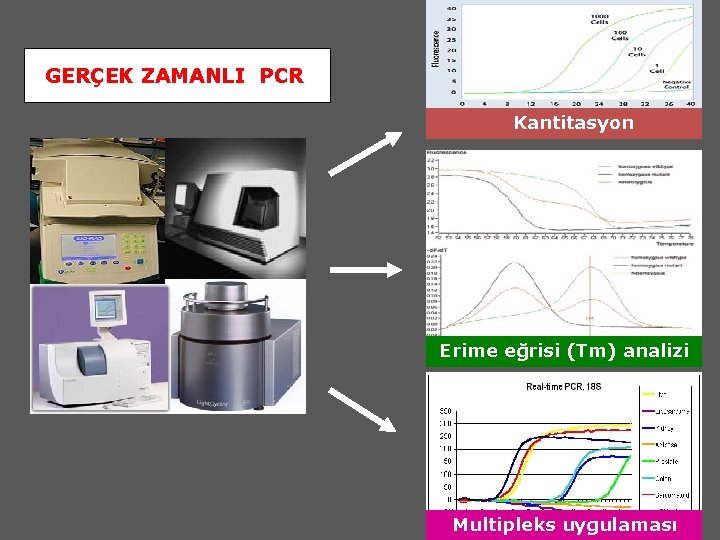
GERÇEK ZAMANLI PCR Kantitasyon Erime eğrisi (Tm) analizi Multipleks uygulaması


KLASİK PCR àPCR sonundaki ürünler (amplikonlar) saptanır; analiz edilir. “REAL TIME PCR” (GERÇEK ZAMANLI PCR) PCR devam ederken ortaya çıkan ürünler saptanmaya başladığı anda değerlendirmeye alınır.

Real-time PCR’ın Prensipleri v Bir flöresan röporterin kantitasyonu ve tanısı üzerine kurulu v PCR ürünlerinin miktarındaki ilk önemli artış (CT - threshold cycle) hedef template’in başlangıç miktarı ile orantılıdr

Klasik PCR’da Problemler v. Primer seçimi ve dizaynı v. Termalcycler programları v. Reaksiyon şartları v. Zaman alan analiz işlemleri v. Bir testin optimizasyonu v. Agaroz jel elektroforezi, Blotlama v. Kontaminasyon riski

Real-time PCR’ın avantajları v Spesifik olmayan amplifikasyonlardan etkilenmiyor v Reaksiyon boyunca veri toplanarak aynı anda analiz imkanı v PCR sonrası ürünlerin ikincil bir işlemi gerekmiyor (yüksek verimlilik, düşük kontaminasyon riski) v ultra-rapid siklus (30 dak. to 2 saat) v 10¹º katı bulan geniş dinamik aralık v İki kat değişikliği hızla tanımlayabilmekte v Spesifik erime eğrisi analizleri ile spesifik amplifikasyonların tanımlanması v Duyarlılığı, özgüllüğü ve tekrarlanabilirliği yüksek v Konvensiyonel PCR’dan daha pahalı değil

Real-time PCR’ın dezavantajları v teknik donanım, alt yapı, beceri ve tecrübe gerektiriyor v Yüksek ekipman ihtiyacı v Aynı ve farklı laboratuvar’lar arasında sonuçlar arası faklılıklar v Standardizasyon problemi
- Slides: 65