REIRRADIACIN EN TUMORES DE CABEZA Y CUELLO Manuel

RE-IRRADIACIÓN EN TUMORES DE CABEZA Y CUELLO Manuel de las Heras González

Tumores avanzados de Cabeza y Cuello: Pobre escenario - La mayoría de pacientes se presentan UN IMPORTANTE NÚMERO en estadios avanzados (65%-70%). DE PACIENTES VAentre A NECESITAR - A los 2 años desarrollan 30%-60% UN(10 -15% SEGUNDO CURSO recidiva local mts sistémicas). DEde. TRATAMIENTO - La incidencia 2 as neoplasias oscila entre (REIRRADIACIÓN) 25%-30% a los 10 años de los tumores controlados previamente del campo). (Braakhuiset et al. Head & Neck 2002) PARA (cancerización DISPONER DE ALGUNA - 50% mueren por problemas locales exclusivamente y el POSIBILIDAD 80% de los que mueren por enfermedad sistémica tienen DE SUPERVIVENCIA enfermedad local - La Toxicidades, agudas y tardías son importantes.

Escenario Clínico de la Re-irradiación: Variables a tener en cuenta - Fracaso local exclusivo ( primitivo vs cuello). - Recidiva cervical aislada (5%-7%) (mejores resultados) (Chopra: Re-irradiation in the management of isolated neck recurrences. Systematic review. Radioth & Oncol 2006) - Toxicidades tardías severas (Esogagitis G 3 -4, Mucositis G 34 - etc) - Resecabilidad variable entre los cirujanos e instituciones - La mayoría de los estudios publicados (antes de los 90), son previos a la quimioirradiación, a los fraccionamientos alterados y a la conformación en 3 D. - Tras los tratamientos de quimio-irradiación menor fracaso local, pero cuando se produce los tumores son más resistentes a los nuevos intentos terapeúticos.

Escenario terapeútico • Causa del Problema: • El fracaso a la Radioterapia puede haberse debido a: – Radioresistencia del tumor. – Fallo en la dosis aplicada (insuficiente: < 70 Gy) – Fallo en la técnica (errores geogáficos o “cold spots”) • Metástasis /2 os primarios en zona previamente tratada • Solución: – Cirugía – Quimioterapia y/o agentes biológicos. (Mediana de sup 7 -9 m y 5 -10% de largos supervivientes). – Reirradiación – Tratamientos combinados

Recaida local: Radioresistencia y. Fenotipo agresivo 1. 2. 3. (Ginos, 2004) Activación de oncogenes (Ras, Myc, EGFR, ciclina D 1), Inactivación de supresores (TP 53, p 16) Pérdida de la heterozigosidad Repoblación acelerada (Tpot 3 -4 días), gran hipoxia, apoptosis inhibida, etc.

SEGUNDOS PRIMARIOS
Tratamientos tras el fracaso o 2 dos tumores en el campo de Radioterapia: CIRUGÍA DE RESCATE • La cirugía es el tratamiento de elección en: Pacientes irradiados, Recidiva local única y 2 dos primarios. • Sólo el 25% de los fracasos son operables con una gran variabilidad entre los cirujanos. Taussky et al. Head & Neck 2005. • La cirugía previa influye sobre el rescate quirúrgico (mejor si no hay vaciamiento cervical previo). • Localización del Primario influye en el rescate: laringe / hipofaringe / cuello vs cavidad oral /orofaringe /s. paranasales. • En general supervivencia a 5 años entre 15%-35%. • ECOG (1 -2 mejor que 3 -4) y co-morbilidades empeoran (diabetes, EPOC etc).

Quimioterapia de rescate Es el tratamiento convencional aunque: • Menos del 50% (10%-35%) responden a la QT de rescate. • Las respuestas completas son anecdóticas (< 4%) y poco mantenidas. • La supervivencia a los 5 años es < del 5%. • No se distingue en las series entre tumores diseminados y fallos locales. • Los nuevos esquemas de QT apenas mejoran a los clásicos en supervivencia (Supervivencia del 10% pero a sólo 2 años). • Ensayos en marcha: Fase III E 1395 (CDDP 5 -Fu ) vs Paclitaxel

PRINCIPIOS GENERALES DE LA REIRRADIACIÓN: Definición Re-irradiación es la administración de un segundo curso de irradiación sobre un volumen previamente irradiado, después de un intervalo de tiempo que oscila entre meses y años. Reirradiación es definida por las siguientes características: 1. VOLUMEN DE TRATAMIENTO SUPERPONIBLE generalmente SUBSTANCIAL 2. ACUMULACIÓN DE DOSIS Generalmente por encima de los NIVELES DE TOLERANCIA (>TD 50/5) (Dosis capaz de producir 50% de toxicidades graves a los 5 años)
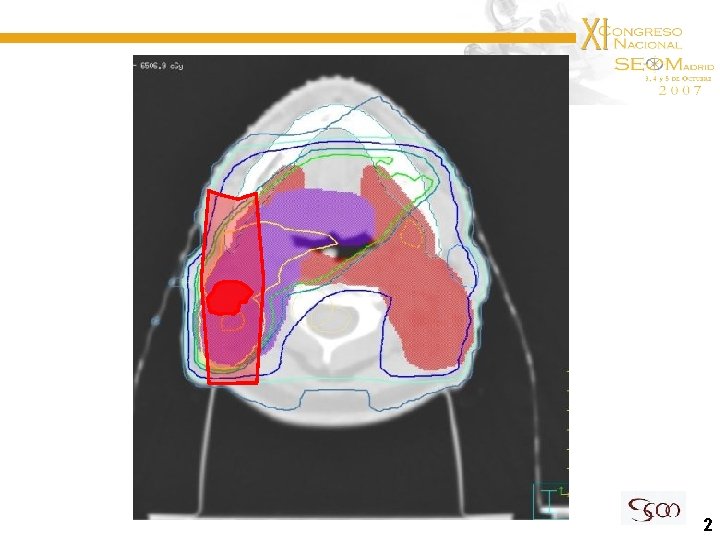
APBI 2004 32 Gy/8 Rx WBI 2000 50 Gy/25 Rx 2

Re-irradiación No es un concepto nuevo (Pierquin, 1970) pero ha sido poco utilizado por: • Miedo a las toxicidades graves (G 3 -4). • Gran incertidumbre de la tolerancia medular. • Pocas disponibilidades tecnológicas anteriormente. Co-60, apenas conformación, no planificación con fusión RM-PET-TAC, gran variabilidad en el depósito de la dosis etc. Ahora se ha retomado sus indicaciones por: • Datos de laboratorio, animales y pequeñas series de pacientes indican que existe una reparación del daño radio-inducido entre el 1º y la 2º tratamiento. • Grandes avances tecnologicos y de imagen (PET-TAC, IMRT, IGRT, Tomo, Protones etc) • Ayuda gracias a mejores tratamientos sistémicos.

PRINCIPIOS GENERALES DE REIRRADIACIÓN Evaluación del paciente A) CLÍNICA ¿ VER SI EL PACIENTE ES UN POSIBLE CANDIDATO PARA RE-IRRADIATION? 1. 2. 2. Valoración cuidadosa del daño severo causado por la primer tratamiento. Esperar que la re-irradiación, sea la mejor alternativa y que la calidad de vida del paciente será aceptable. B) CONSIDERAR QUE OTROS FACTORES PUEDEN AFECTAR LA TOLERANCIA DE LOS TEJIDOS SANOS 1. Tipo, esquema, secuencia & dosis de quimioterapia. 2. Edad y co-morbilidades del paciente

PRINCIPIOS GENERALES DE REIRRADIACIÓN C) TÉCNICA DE RADIOTERAPIA ¿ QUE CONOCEMOS DEL PLAN DE RADIOTERAPIA ANTERIOR? 1. Histogramas Dosis Volumen (DVHs) del tumor y de los diferentes Organos en Riesgo (OARVs), Planning Target Volume (PTV), y volumen Irradiado. 2. Dosis por fracción, tiempo entre los cursos de irradiación. 3. Modalidad de tratamiento (fotones, electrones, braquiterapia, . . . ) 4. Porta films o Rx de simulación para valoración cuidadosa. D) VALORAR CUIDADOSAMENTE LOS TEJIDOS EN EL VOLUMEN IRRADIADO. 1. Tejidos QUE NO muestran intervalo de recuperación: corazón, riñones, vejiga, etc 2. Tejidos QUE SÍ muestran intervalo de recuperación: piel, mucosas, pulmón, médula espinal, etc. LA MEJOR OPCIÓN ES QUE EL PACIENTE SEA EVALUADO EN EL CENTRO EN QUE SE HIZO EL PRIMER TRATAMIENTO (!!!)
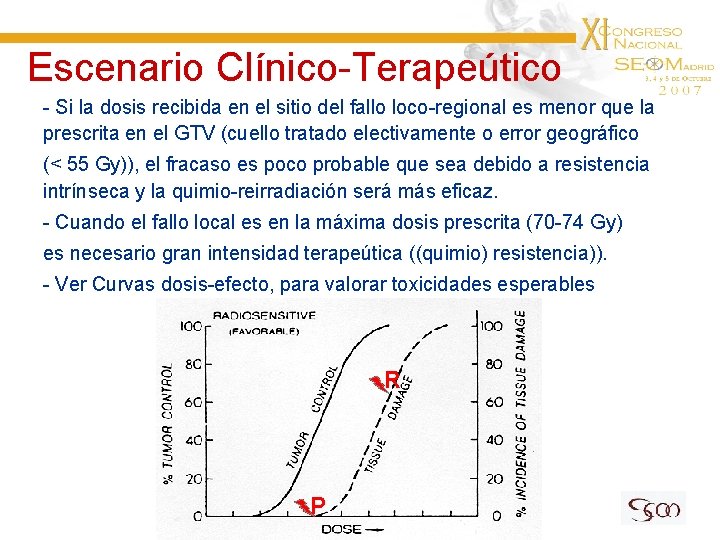
Escenario Clínico-Terapeútico - Si la dosis recibida en el sitio del fallo loco-regional es menor que la prescrita en el GTV (cuello tratado electivamente o error geográfico (< 55 Gy)), el fracaso es poco probable que sea debido a resistencia intrínseca y la quimio-reirradiación será más eficaz. - Cuando el fallo local es en la máxima dosis prescrita (70 -74 Gy) es necesario gran intensidad terapeútica ((quimio) resistencia)). - Ver Curvas dosis-efecto, para valorar toxicidades esperables R P

PRINCIPIOS GENERALES DE REIRRADIACIÓN Decisiones terapeúticas 1. VOLUMEN IRRADIADO 1. 1. Mantener el volumen a irradiar TAN PEQUEÑO como sea posible. 1. 2. Utilizar técnicas de la máxima conformación. IMRT, Tomoterapia, Cyber. Knife, Protones, Radiocirugía, Braquiterapia, etc. 2. FRACIONAMIENTO 2. 1. Usar pequeñas dosis por fracción: Menor toxicidad tardía y permite una potenciación del efecto radiosensibilizante de la QT. 3. RADIOPROTECTORES 3. 1. (Atractivo) Deben ser validados en ensayos clínicos. 4. DOSIS TOTAL 4. 1. Depende de los objetivos y los riesgos a asumir.
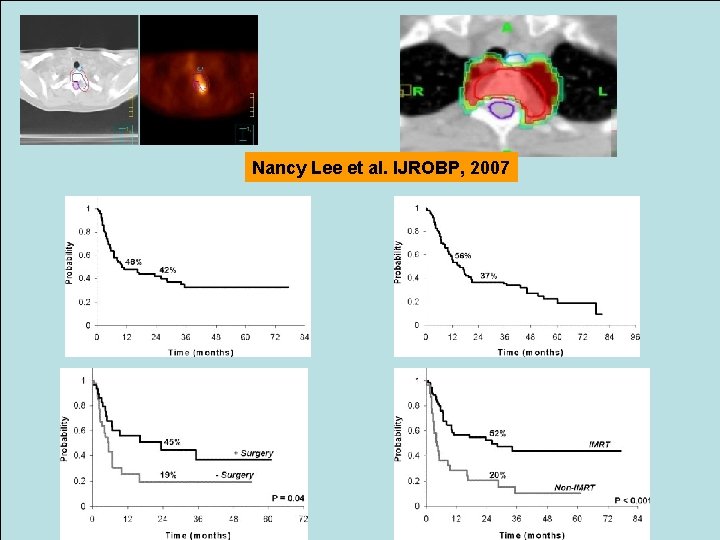
Conceptos en la re-irradiación Nancy Lee et al. IJROBP, 2007 Ø Planificación con PET-TAC. Ø Máxima conformación al GTV. Máximas Ø Hiperfraccionamiento y/o dosis pequeñas por fracción. Ø Quimio concomitante: Si es posible Ø Criterios clínicos aceptables

Modelo lineal cuadrático: Tejidos sanos Respuesta aguda y tumores Respuesta tardía La toxicidad de los tejidos sanos depende del: Tiempo de tratamiento: Toxicidad Aguda Dosis por fracción: Toxicidad Tardía. El tiempo de tratamiento influye sobre la repoblación (toxicidad aguda) y la QT aumenta los efectos agudos al inhibir la reploblación. El cociente a/b es diferente según la capacidad de reparación del tejido Tejidos Tardíos: Reparación Mayor curvatura / baja. - Mucha dependencia dosis por fracción: mantenerla 1. 5 -1. 8 Gy. Poca dependencia del tiempo total de tratº: Poca repoblación. Menos dependencia de la dosis total.

PRINCIPIOS GENERALES DE REIRRADIACIÓN Paradigma de la Médula Espinal Organo en serie: No depende del volumen tratado sino de su dosis de tolerancia. LA MÉDULA ESPINAL MUESTRA UN INTERVALO DE RECUPERACIÓN DOSIS-DEPENDIENTE. El riesgo de mielitis es PEQUEÑO sí: 50 Gy/2 Gy (BED= 100 Gy 2) 1. La dosis equivalente biológica- BED no es mayor de 135 Gy 2 2. BED de cada curso de irradiación NO ES MAYOR de 98 Gy 2 3. Intervalo mayor de 6 meses.

Efectos tardíos. Médula Espinal. Investigación Existe una recuperación a largo plazo que se inicia a las 8 semanas y que aumenta con el tiempo. Estudios en roedores. La magnitud de la recuperación depende dosis inicial, edad, especie animal. Aproximadamente 1/2 o 2/3 del daño inicial oculto es recuperado entre 20 -28 semanas. Monos: 3/4 dosis se recupera en 1 -2 años. Médula Torácica y lumbar se recuperan mejor que la cervical. Más evidente en animales jóvenes.
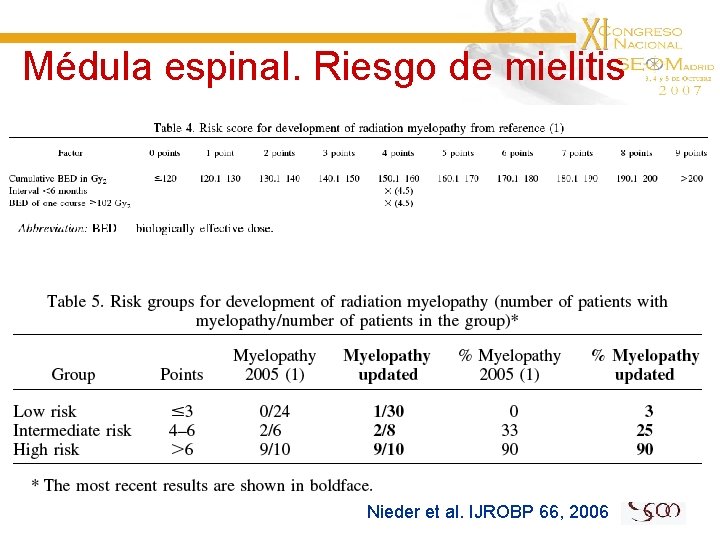
Médula espinal. Riesgo de mielitis Nieder et al. IJROBP 66, 2006
Herramientas – Braquiterapia – IMRT y IG-IMRT – Combinacion terapéutica (RIO) – Partículas pesadas

¿ COMO VENCER LA RESISTENCIA ? 1. Escalada de Dosis 2. - Hiperfraccionamiento. (MARCH. Bourhis. Lancet 2006). 3. - Quimioradioterapia dependiendo de la 1ª RT (MACH-NC. Pignon. Lancet 2000) 2. Nuevos Desarrollos. 3. - Qumioterapia de Inducción (TPF). 4. - Máxima conformación (IMRT, IGRT, Tomoterapia, Cyber. Knife, Braquiterapia etc). 5. 6. 7. - Sólo tratamiento de GTV (Planificar con fusión PET-TAC). 3. “Targeted Therapy” - Bortezomib concomitante

Criterios de selección para la Re-Irradiación. • Factores relacionados con el paciente – Sitio anatómico • Nasofaringe y laringe más favorables. • La re-irradiación del cuello mayor riesgo que la del tumor primitivo (20% vs 3%). Ohizumi et al, Am J Otol 2002. – Segundo primario vs recurrencia • Segundos primarios más favorables por menor radioresistencia. – Intervalo de 24 meses mejor • Spencer: intervalo > 24 m, mediana sv= 15 m vs. 6, 5 m <24 m. • Factores relacionados con el tratamiento – – Cirugía “debulking” mejor. Radioquimioterapia previa peor que RT exclusiva. Volumen de tratamiento previo limitado mejor. Efecto dosis-respuesta: Dosis Total. • Dtotal>58 Gy LRC@3 a y OS fueron 56% y 30%, que D< 58 Gy, LRC and OS fue 33% y 6% (Salama et al).

Resultados. Series seleccionadas Estudio # Dosis Sensibilizador MST %SV@2 (Gy) RTOG 9610 EX 83 r 60 Fu/HU 8, 8 Medianas. EXde supervivencia: 10 meses 105 (60) r 60 CP/Fu 13 RTOG 9911 RTOGSeries 0421 quirúrgicas: algo superior EX pendiente r 60 Supervivencias: 25% ar 60 los Crevoisier EX 169 Salama (UChic)quirúrgicas EX 115 Series Chen. Toxicidad: (UCSF) RIO 2 QT años 27, 5 CP/T ? - 21 ? ac 131 QTúnica: 11 superior 22 @3 a 30 -40 % de recidiva 137 83% Importante pero asumible Martinez (CUN) BQ 25 Cohen 25 r 72 Gy CP/Tirapa EX 17 4 Gy bid x 8 52 14 46 @4 a 27
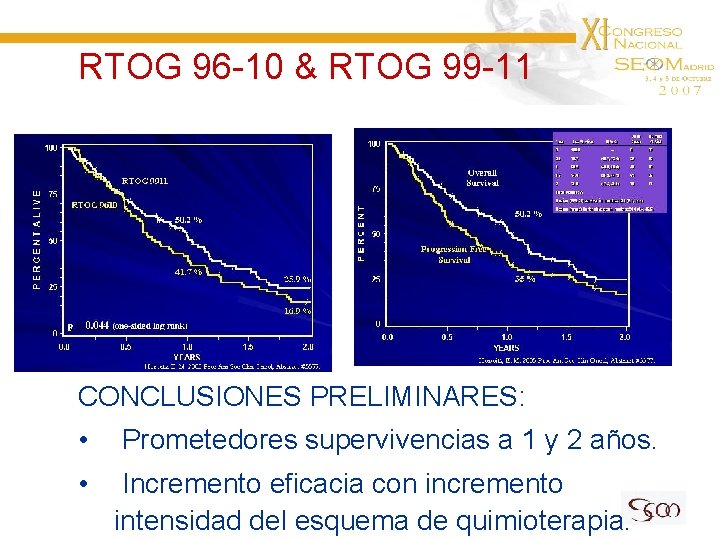
RTOG 96 -10 & RTOG 99 -11 CONCLUSIONES PRELIMINARES: • Prometedores supervivencias a 1 y 2 años. • Incremento eficacia con incremento intensidad del esquema de quimioterapia.

RTOG 99 -11: TOXICIDADES OTRAS TOXICIDADES: • Osteoradionecrosis. • Necrosis de tejidos blandos. • Tox. Vascular. • Toxicidades funcionales (tragar, hablar etc).
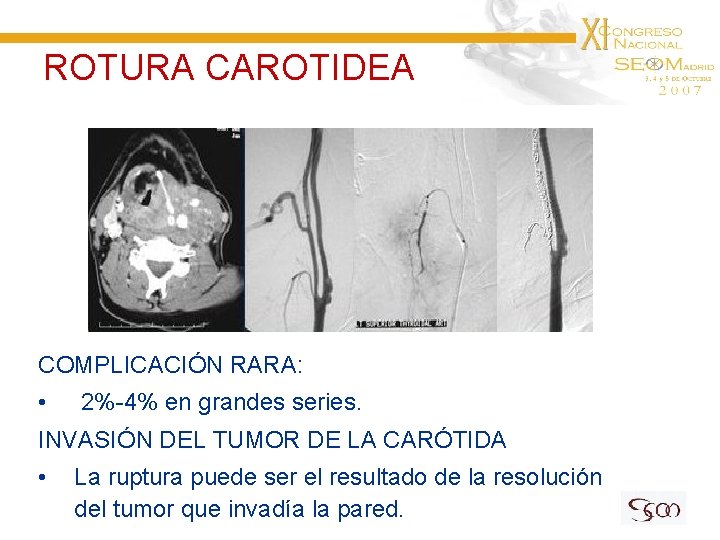
ROTURA CAROTIDEA COMPLICACIÓN RARA: • 2%-4% en grandes series. INVASIÓN DEL TUMOR DE LA CARÓTIDA • La ruptura puede ser el resultado de la resolución del tumor que invadía la pared.

COMPARACIÓN RETROSPECTIVA DE LOS ESTUDIOS DE QT EXCLUSIVA CON RADIOQUIMIOTERAPIA

FASES III QUE COMPARAN LA QT vs RQT
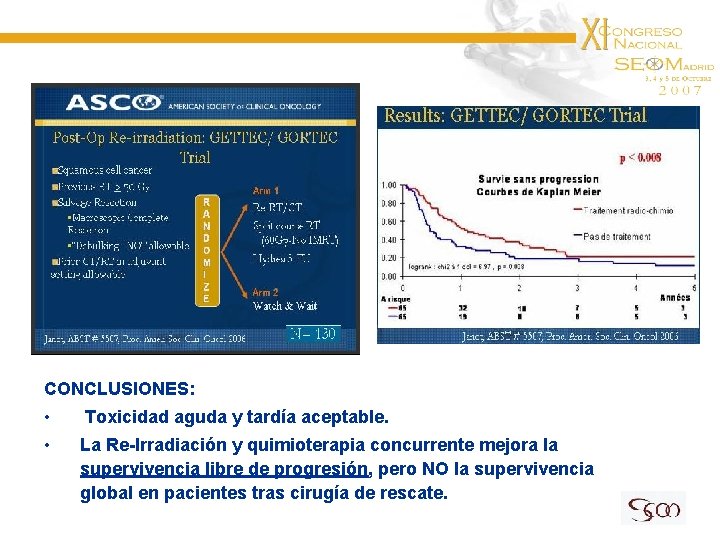
CONCLUSIONES: • Toxicidad aguda y tardía aceptable. • La Re-Irradiación y quimioterapia concurrente mejora la supervivencia libre de progresión, pero NO la supervivencia global en pacientes tras cirugía de rescate.

Conclusiones • Es un tratamiento complicado y necesita un equipo interdisciplinario. Más no siempre es mejor. • Las variables de la irradiación previa deben ser LA MEJOR RE-IRRADIACIÓN ES perfectamente conocidas. • • UN ÓPTIMO TRATAMIENTO Deben. DEL asumirse unos costos TUMOR EN en LAtoxicidades. PRIMERA OPORTUNIDAD Se necesitan excelentes medios técnológicos y equipos experimentados (Grupos de referencia). referencia • Necesitamos más investigación clínica y aplicada en este campo.

La investigación tecnológica va a ayudar a la Re-irradiación
¡¡ Gracias !!
- Slides: 33