REGULACIN DE PRECIOS DE MEDICAMENTOS EN COLOMBIA AURELIO

REGULACIÓN DE PRECIOS DE MEDICAMENTOS EN COLOMBIA AURELIO MEJÍA Dirección de Medicamentos y Tecnologías en Salud Ministerio de Salud y Protección Social

2 1. METODOLOGÍA DE LA REGULACIÓN DE PRECIOS 2. RESULTADOS 3. REGULACIÓN DE PRECIOS A LA ENTRADA

3 METODOLOGÍA

4 HERRAMIENTAS DE REGULACIÓN METODOLOGÍA La regulación del mercado farmacéutico para la contención del gasto en Colombia utiliza varias herramientas de política que están disponibles y son complementarias: • • • Control de precios a medicamentos Compra centralizada Información para los actores Promoción de la competencia Evaluación de tecnologías en salud

5 TERMÓMETRO DE PRECIOS METODOLOGÍA • Se puede consultar por principio activo y concentración. • Se observan las diferentes alternativas comerciales. • Los precios se ordenan de menor (verde) a mayor (rojo). • Información SISMED dispuesta de forma amigable.

6 CONTROL DE PRECIOS A MEDICAMENTOS METODOLOGÍA Ejecutada por la Comisión Nacional de Precios de Medicamentos y Dispositivos Médicos (tripartita: Ministerio de Salud, Ministerio de Comercio y Presidencia). Regulación que, a partir de 2013, se basa en referenciación internacional de 17 países. El mecanismo de fijación de precio es transparente y predecible. Sigue reglas de decisión contenidas en la Circular 03 de 2013.

7 CONTROL DE PRECIOS A MEDICAMENTOS METODOLOGÍA

MERCADOS RELEVANTES SUJETOS A REGULACIÓN 8 OBJETIVO ¿QUÉ INTERVENIR? Intervenir cuando se presenta falla de mercado en cuanto a la 1. Top SISMED Concentrados concentración, con el propósito de alcanzar 2. Pareto del pago y monopólicos reducción de precios de por medicamentos. Se no PBS. regula el punto mayorista. ¿CUÁNDO INTERVENIR? ¿CÓMO INTERVENIR? 1. Menos (<=) 3 oferentes O 2. Índice de Herfindahl. Hirschman>2. 500 PRI (Percentil 25) Criterios: *PRN 1>PRI 2 = Regulado *PRN<PRI = No Regulado 1. Precio de Referencia Nacional: Promedio ponderado por participación en las ventas totales, medidas en valor normalizado por unidad mínima de concentración 2. Precio de Referencia Internacional: Para cada país se obtiene el promedio simple de los precios, se ordenan de mayor a menor y se calcula el percentil 25.

9 RESULTADOS
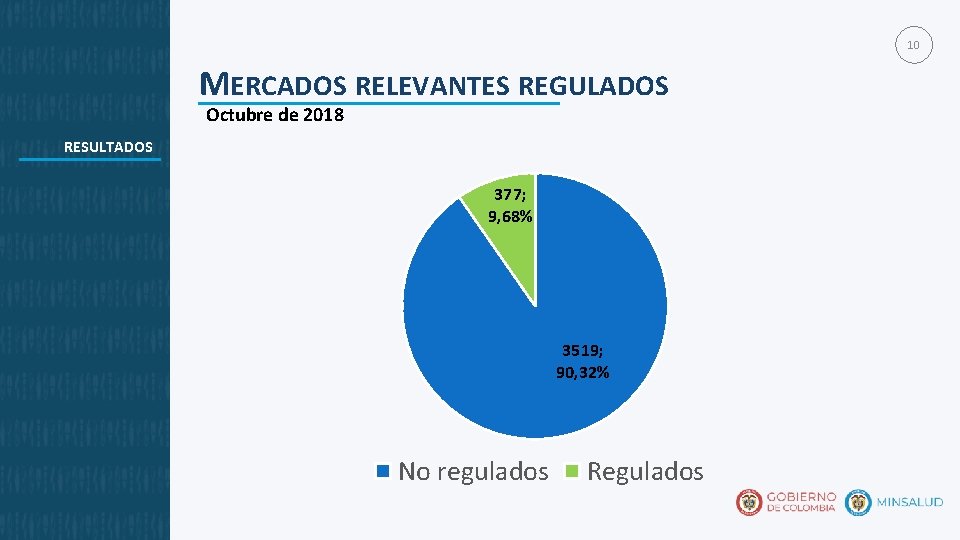
10 MERCADOS RELEVANTES REGULADOS Octubre de 2018 RESULTADOS 377; 9, 68% 3519; 90, 32% No regulados Regulados
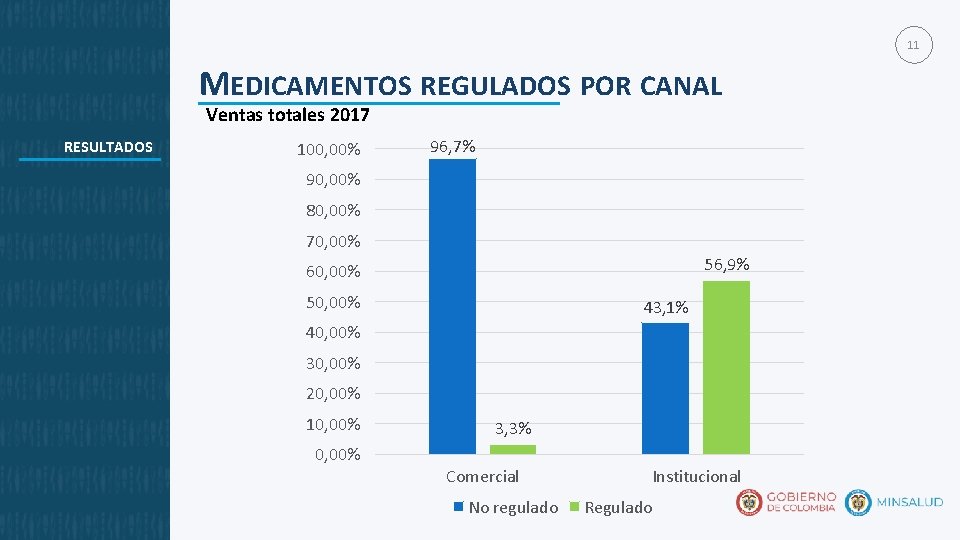
11 MEDICAMENTOS REGULADOS POR CANAL Ventas totales 2017 RESULTADOS 100, 00% 96, 7% 90, 00% 80, 00% 70, 00% 56, 9% 60, 00% 50, 00% 43, 1% 40, 00% 30, 00% 20, 00% 10, 00% 3, 3% Comercial No regulado Institucional Regulado

12 DESDE 2013: RESULTADOS 1039 +902 Medicamentos Regulados en enero de 2019 42% Reducción promedio de precio de los medicamentos regulados
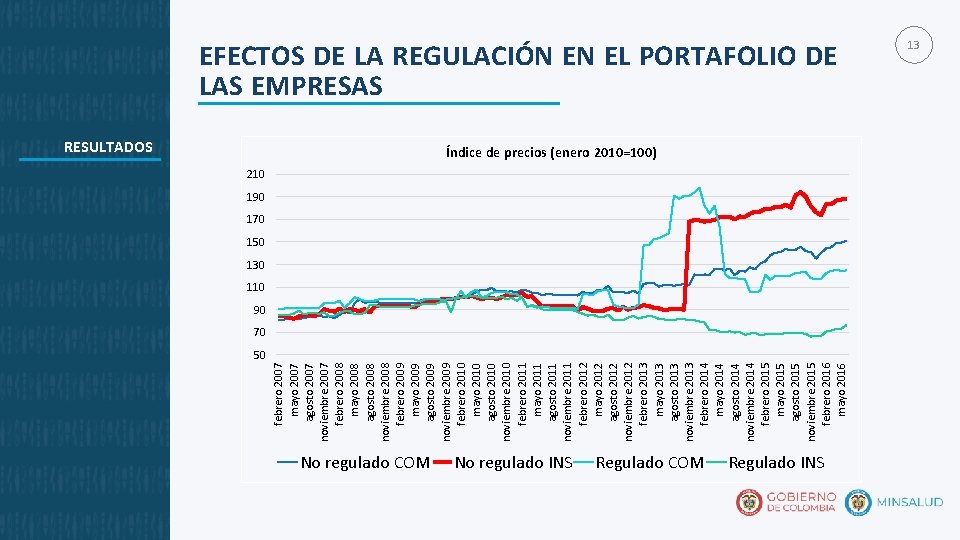
febrero 2007 mayo 2007 agosto 2007 noviembre 2007 febrero 2008 mayo 2008 agosto 2008 noviembre 2008 febrero 2009 mayo 2009 agosto 2009 noviembre 2009 febrero 2010 mayo 2010 agosto 2010 noviembre 2010 febrero 2011 mayo 2011 agosto 2011 noviembre 2011 febrero 2012 mayo 2012 agosto 2012 noviembre 2012 febrero 2013 mayo 2013 agosto 2013 noviembre 2013 febrero 2014 mayo 2014 agosto 2014 noviembre 2014 febrero 2015 mayo 2015 agosto 2015 noviembre 2015 febrero 2016 mayo 2016 EFECTOS DE LA REGULACIÓN EN EL PORTAFOLIO DE LAS EMPRESAS RESULTADOS Índice de precios (enero 2010=100) 210 190 170 150 130 110 90 70 50 No regulado COM No regulado INS Regulado COM Regulado INS 13

14 REGULACIÓN DE PRECIOS A LA ENTRADA

15 PUERTA DE ENTRADA • Busca fijar los precios de los medicamentos cuando hacen el proceso de expedición del registro sanitario. • Los precios en función del valor terapéutico de los medicamentos. • Solo aplica para los principios activos nuevos • Se han fijado 6 categorías de valor terapéutico
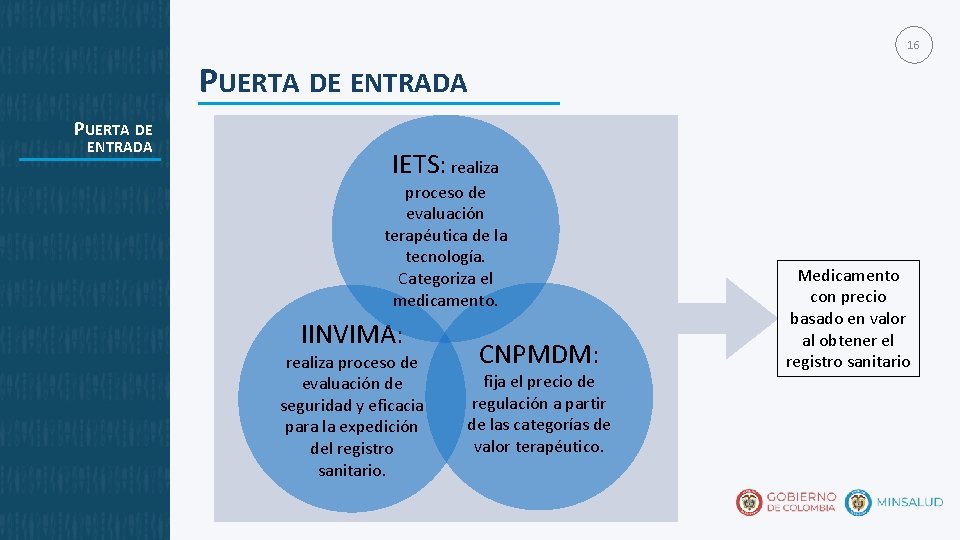
16 PUERTA DE ENTRADA IETS: realiza proceso de evaluación terapéutica de la tecnología. Categoriza el medicamento. IINVIMA: realiza proceso de evaluación de seguridad y eficacia para la expedición del registro sanitario. CNPMDM: fija el precio de regulación a partir de las categorías de valor terapéutico. Medicamento con precio basado en valor al obtener el registro sanitario

17 PUERTA DE ENTRADA Referencia: Decreto 433/2018

MUCHAS GRACIAS POR SU ATENCIÓN Dirección de Medicamentos y Tecnologías en Salud Ministerio de Salud y Protección Social
- Slides: 18