Regorafenib en pacientes con cncer colorrectal metastsico CCRm

Regorafenib en pacientes con cáncer colorrectal metastásico (CCRm) previamente tratados: Resultados obtenidos en 307 pacientes españoles tratados en el estudio abierto fase IIIb CONSIGN Rocío García-Carbonero 1, Carmen Guillén-Ponce 2, Jaime Feliu 3, Beatriz García-Paredes 4, Guillem Argilés 5, Cristina Grávalos 6, Gema Durán-Ogalla 7, Pilar García-Alfonso 8, Mercedes Martínez-Villacampa 9, Joachim Kalmus 10 1 Hospital Universitario 12 de Octubre, Madrid (España) , 2 Hospital Universitario Ramón y Cajal, IRYCIS, Madrid (España) Universitario La Paz, Madrid (España) , 4 Hospital Clínico San Carlos, Madrid (España) , 5 Vall d'Hebrón Instituto de Oncología (VHIO), Barcelona (España), 6 Hospital Universitario Doce de Octubre, Madrid (España), 7 Hospital Universitario Regional y Virgen de la Victoria, Málaga (España), 8 Hospital Universitario Gregorio Marañón, Madrid (España), 9 Institut Català d’Oncologia, ICO-L´Hospitalet, Barcelona (España) , 10 Global Clinical Development Oncology, Ophthalmology & Neurology, Bayer Pharma AG, Berlin (Alemania) 3 Hospital

Antecedentes (I) • Regorafenib es un inhibidor multiquinasa oral que bloquea la actividad de múltiples proteinquinasas implicadas en la angiogénesis, la oncogénesis y el microambiente tumoral 1. • Regorafenib está indicado en el tratamiento de pacientes con CCRm previamente tratados con las terapias disponibles en base a los resultados del estudio fase III CORRECT (NCT 01103323; N=760)2: - Mediana de SG: 6, 4 meses con regorafenib vs. 5. 0 meses con placebo (HR 0, 77 [95% IC 0, 64 – 0, 94]; p one-sided=0, 0052) - Mediana de SLP: 1, 9 meses con regorafenib vs. 1, 7 meses con placebo (HR 0, 49 [95% IC 0, 42 – 0, 58]; p one-sided<0, 0001) - Eventos adversos de grado ≥ 3 emergentes al tratamiento con regorafenib: reacción cutánea mano-pie, fatiga, diarrea, hipertensión y rash/descamación. HR, hazard ratio; IC, intervalo de confianza; SLP, supervivencia libre de progresión; SG, supervivencia global. 1. Wilhelm SM, et al. Int J Cancer 2011; 129: 245– 255; 2. Grothey A, Van Cutsem E, et al. Lancet 2013; 381: 303– 312.

Antecedentes (II) • CONSIGN es un estudio multinacional, abierto, de brazo único, fase IIIb cuyo objetivo fue valorar la seguridad de regorafenib (objetivo primario) y permitir el acceso a regorafenib de pacientes con CCRm previamente a su comercialización (NCT 01538680). También se evaluó la eficacia (SLP)1. - Llevado a cabo entre 2. 872 pacientes de Europa, Norte América, Israel y Australia. - El perfil de seguridad de regorafenib en este estudio fue consistente con el informado en el estudio CORRECT 2. - La SLP estuvo en en rango de la reportada con regorafenib en pacientes con CCRm refractarios al tratamiento 2, 3. Presentamos el análisis del subgrupo de pacientes españoles participantes en el estudio CONSIGN (N = 308 pacientes) SLP, supervivencia libre de progresión 1. Van Cutsem E, et al. ECC 2015, Sept 25– 29, Vienna, Austria. Abst 2139. 2. Grothey A, , et al. Lancet 2013; 381: 303– 12. ; 3. Li J, et al. Lancet Oncol 2015; 16: 619– 29.
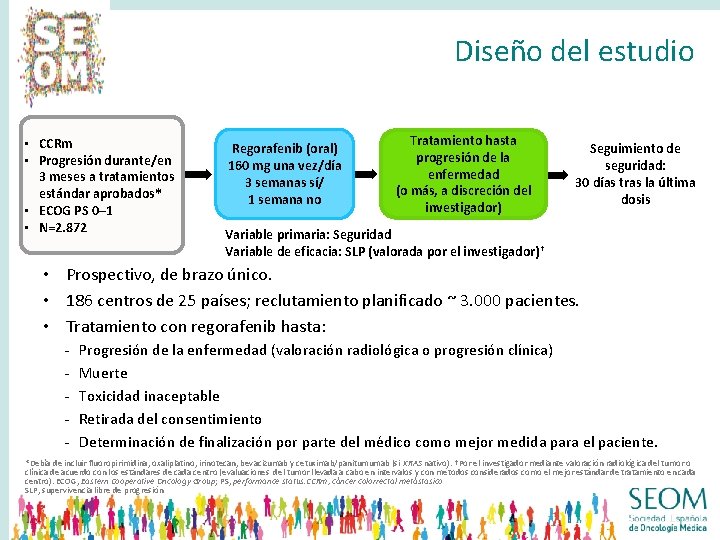
Diseño del estudio • CCRm • Progresión durante/en 3 meses a tratamientos estándar aprobados* • ECOG PS 0– 1 • N=2. 872 Regorafenib (oral) 160 mg una vez/día 3 semanas sí/ 1 semana no Tratamiento hasta progresión de la enfermedad (o más, a discreción del investigador) Seguimiento de seguridad: 30 días tras la última dosis Variable primaria: Seguridad Variable de eficacia: SLP (valorada por el investigador)† • Prospectivo, de brazo único. • 186 centros de 25 países; reclutamiento planificado ~ 3. 000 pacientes. • Tratamiento con regorafenib hasta: - Progresión de la enfermedad (valoración radiológica o progresión clínica) Muerte Toxicidad inaceptable Retirada del consentimiento Determinación de finalización por parte del médico como mejor medida para el paciente. *Debía de incluir fluoropirimidina, oxaliplatino, irinotecan, bevacizumab y cetuximab/panitumumab (si KRAS nativo). †Por el investigador mediante valoración radiológica del tumor o clínica de acuerdo con los estándares de cada centro (evaluaciones del tumor llevada a cabo en intervalos y con métodos considerados como el mejor estándar de tratamiento en cada centro). ECOG, Eastern Cooperative Oncology Group; PS, performance status. CCRm, cáncer colorrectal metástasico SLP, supervivencia libre de progresión
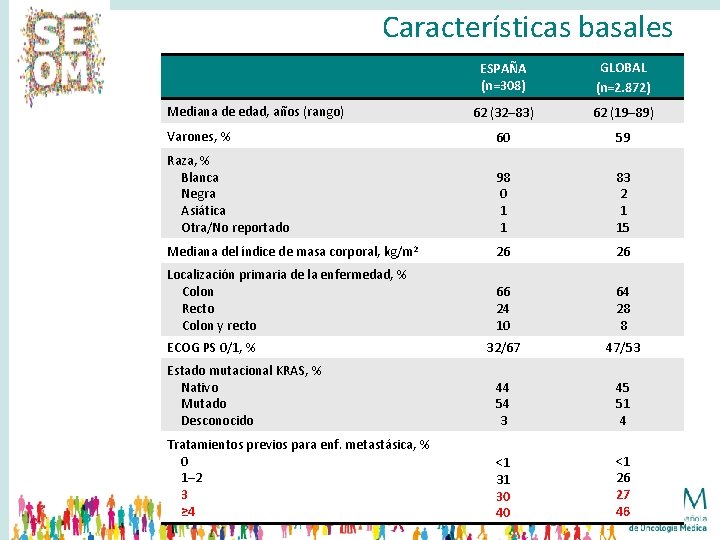
Características basales ESPAÑA (n=308) GLOBAL (n=2. 872) 62 (32– 83) 62 (19– 89) Varones, % 60 59 Raza, % Blanca Negra Asiática Otra/No reportado 98 0 1 1 83 2 1 15 Mediana del índice de masa corporal, kg/m 2 26 26 Localización primaria de la enfermedad, % Colon Recto Colon y recto 66 24 10 64 28 8 32/67 47/53 Estado mutacional KRAS, % Nativo Mutado Desconocido 44 54 3 45 51 4 Tratamientos previos para enf. metastásica, % 0 1– 2 3 ≥ 4 <1 31 30 40 <1 26 27 46 Mediana de edad, años (rango) ECOG PS 0/1, %
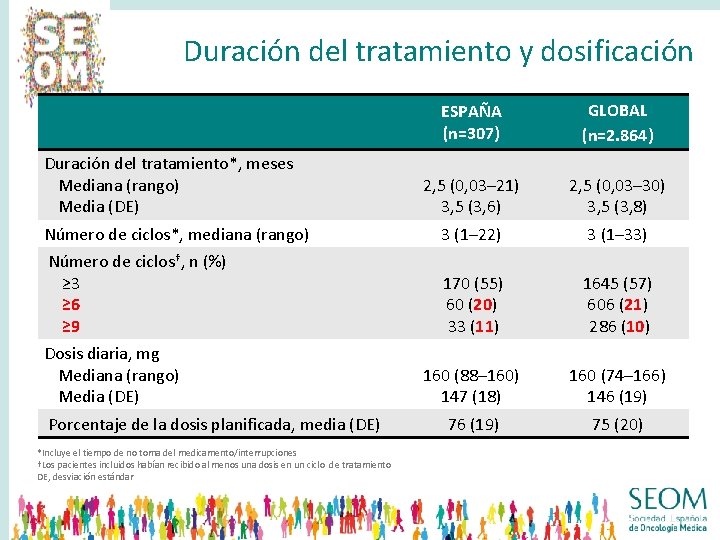
Duración del tratamiento y dosificación ESPAÑA (n=307) GLOBAL (n=2. 864) 2, 5 (0, 03– 21) 3, 5 (3, 6) 2, 5 (0, 03– 30) 3, 5 (3, 8) Número de ciclos*, mediana (rango) 3 (1– 22) 3 (1– 33) Número de ciclos†, n (%) ≥ 3 ≥ 6 ≥ 9 170 (55) 60 (20) 33 (11) 1645 (57) 606 (21) 286 (10) 160 (88– 160) 147 (18) 160 (74– 166) 146 (19) 75 (20) Duración del tratamiento*, meses Mediana (rango) Media (DE) Dosis diaria, mg Mediana (rango) Media (DE) Porcentaje de la dosis planificada, media (DE) *Incluye el tiempo de no toma del medicamento/interrupciones †Los pacientes incluidos habían recibido al menos una dosis en un ciclo de tratamiento DE, desviación estándar
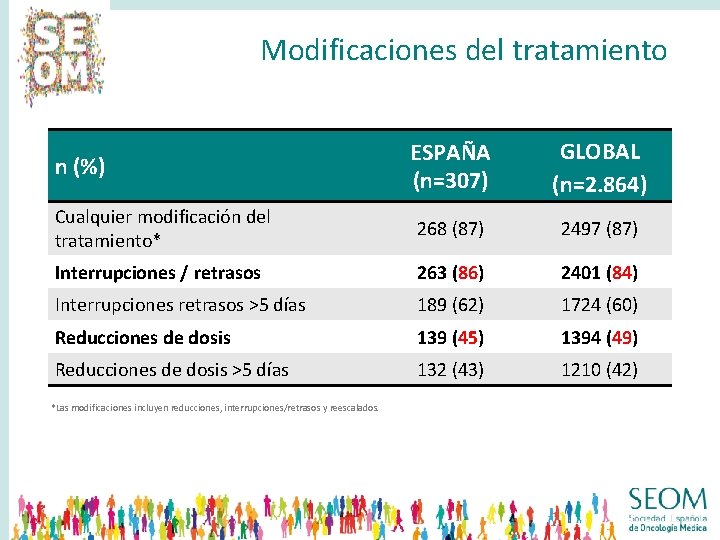
Modificaciones del tratamiento ESPAÑA (n=307) GLOBAL (n=2. 864) Cualquier modificación del tratamiento* 268 (87) 2497 (87) Interrupciones / retrasos 263 (86) 2401 (84) Interrupciones retrasos >5 días 189 (62) 1724 (60) Reducciones de dosis 139 (45) 1394 (49) Reducciones de dosis >5 días 132 (43) 1210 (42) n (%) *Las modificaciones incluyen reducciones, interrupciones/retrasos y reescalados.
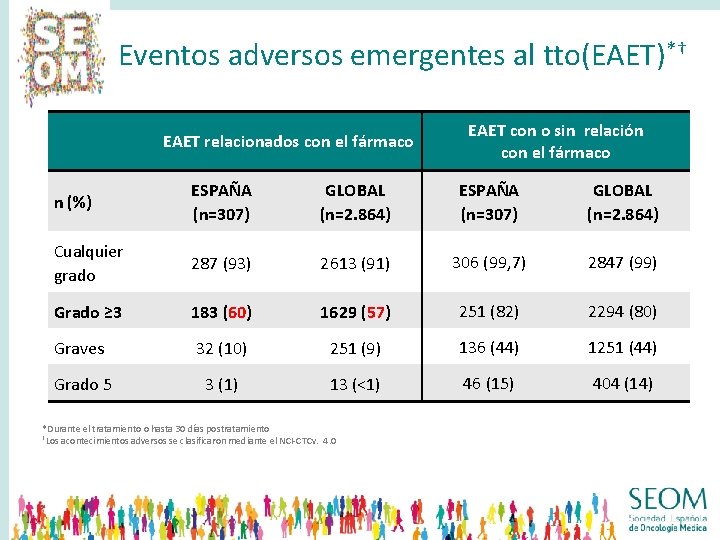
Eventos adversos emergentes al tto(EAET)*† EAET relacionados con el fármaco EAET con o sin relación con el fármaco n (%) ESPAÑA (n=307) GLOBAL (n=2. 864) Cualquier grado 287 (93) 2613 (91) 306 (99, 7) 2847 (99) Grado ≥ 3 183 (60) 1629 (57) 251 (82) 2294 (80) Graves 32 (10) 251 (9) 136 (44) 1251 (44) Grado 5 3 (1) 13 (<1) 46 (15) 404 (14) *Durante el tratamiento o hasta 30 días postratamiento †Los acontecimientos adversos se clasificaron mediante el NCI-CTCv. 4. 0
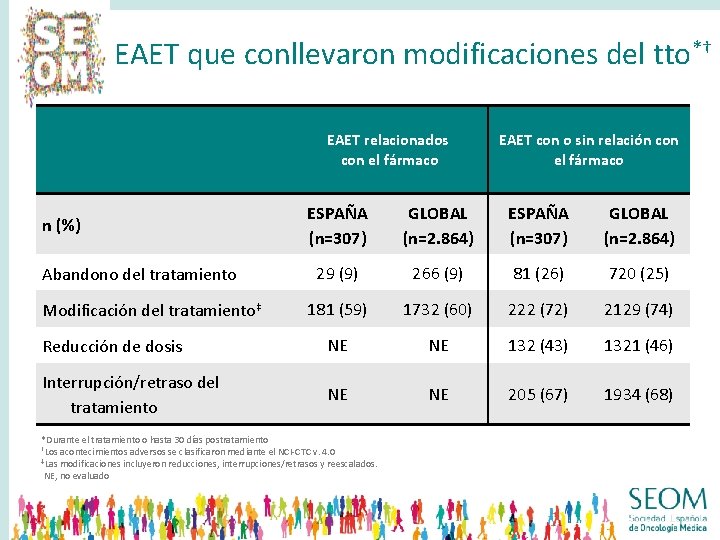
EAET que conllevaron modificaciones del tto*† EAET relacionados con el fármaco EAET con o sin relación con el fármaco ESPAÑA (n=307) GLOBAL (n=2. 864) 29 (9) 266 (9) 81 (26) 720 (25) 181 (59) 1732 (60) 222 (72) 2129 (74) Reducción de dosis NE NE 132 (43) 1321 (46) Interrupción/retraso del tratamiento NE NE 205 (67) 1934 (68) n (%) Abandono del tratamiento Modificación del tratamiento‡ *Durante el tratamiento o hasta 30 días postratamiento †Los acontecimientos adversos se clasificaron mediante el NCI-CTC v. 4. 0 ‡Las modificaciones incluyeron reducciones, interrupciones/retrasos y reescalados. NE, no evaluado

EAET de grado ≥ 3 relacionados con el fármaco presentes en ≥ 5% de los pacientes* ESPAÑA (n=307) GLOBAL (n=2. 864) 183 (60) 1629 (57) Fatiga 55 (18) 376 (13) Hipertensión 50 (16) 435 (15) Reacción cutánea mano-pie 47 (15) 396 (14) Anorexia 17 (6) 68 (2) Hipofosfatemia 16 (5) 149 (5) Diarrea 15 (5) 135 (5) Grado ≥ 3, relacionado con el tratamiento, n (%) *En la cohorte española
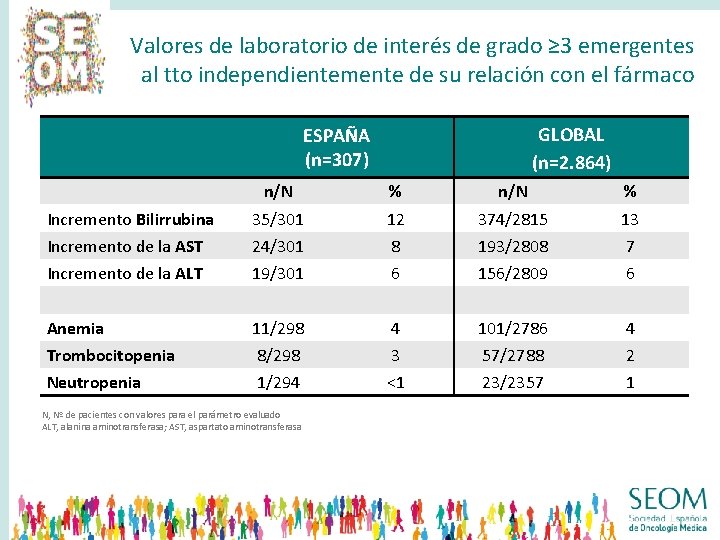
Valores de laboratorio de interés de grado ≥ 3 emergentes al tto independientemente de su relación con el fármaco GLOBAL (n=2. 864) ESPAÑA (n=307) n/N % Incremento Bilirrubina 35/301 12 374/2815 13 Incremento de la AST 24/301 8 193/2808 7 Incremento de la ALT 19/301 6 156/2809 6 Anemia 11/298 4 101/2786 4 Trombocitopenia 8/298 3 57/2788 2 Neutropenia 1/294 <1 23/2357 1 N, Nº de pacientes con valores para el parámetro evaluado ALT, alanina aminotransferasa; AST, aspartato aminotransferasa
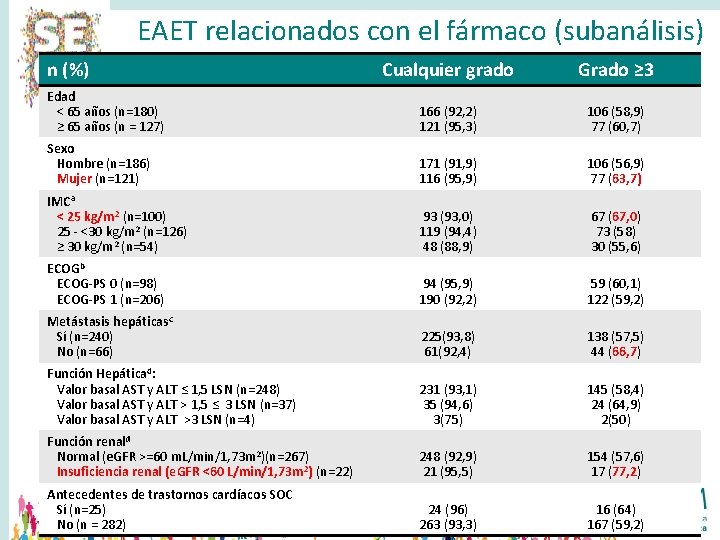
EAET relacionados con el fármaco (subanálisis) n (%) Cualquier grado Grado ≥ 3 Edad < 65 años (n=180) ≥ 65 años (n = 127) 166 (92, 2) 121 (95, 3) 106 (58, 9) 77 (60, 7) Sexo Hombre (n=186) Mujer (n=121) 171 (91, 9) 116 (95, 9) 106 (56, 9) 77 (63, 7) IMCa < 25 kg/m 2 (n=100) 25 - <30 kg/m 2 (n=126) ≥ 30 kg/m 2 (n=54) 93 (93, 0) 119 (94, 4) 48 (88, 9) 67 (67, 0) 73 (58) 30 (55, 6) ECOGb ECOG-PS 0 (n=98) ECOG-PS 1 (n=206) 94 (95, 9) 190 (92, 2) 59 (60, 1) 122 (59, 2) Metástasis hepáticasc Sí (n=240) No (n=66) 225(93, 8) 61(92, 4) 138 (57, 5) 44 (66, 7) Función Hepáticad: Valor basal AST y ALT ≤ 1, 5 LSN (n=248) Valor basal AST y ALT > 1, 5 ≤ 3 LSN (n=37) Valor basal AST y ALT >3 LSN (n=4) 231 (93, 1) 35 (94, 6) 3(75) 145 (58, 4) 24 (64, 9) 2(50) Función renald Normal (e. GFR >=60 m. L/min/1, 73 m 2)(n=267) Insuficiencia renal (e. GFR <60 L/min/1, 73 m 2) (n=22) 248 (92, 9) 21 (95, 5) 154 (57, 6) 17 (77, 2) Antecedentes de trastornos cardíacos SOC Sí (n=25) Perdidos=27; Perdidos=3; Desconocidos=18 No (n = 282) 24 (96) 263 (93, 3) 16 (64) 167 (59, 2) a b c d
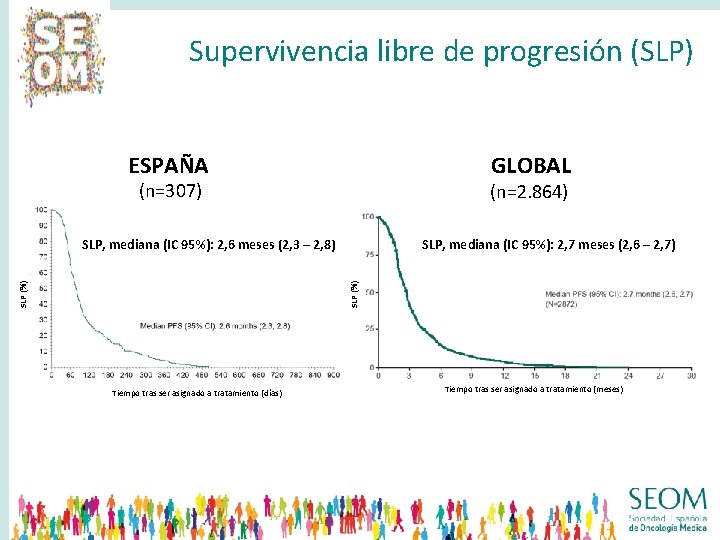
Supervivencia libre de progresión (SLP) ESPAÑA GLOBAL (n=307) (n=2. 864) SLP, mediana (IC 95%): 2, 7 meses (2, 6 – 2, 7) SLP (%) SLP, mediana (IC 95%): 2, 6 meses (2, 3 – 2, 8) Tiempo tras ser asignado a tratamiento (días) CI, confidence interval; PFS, progression-free survival Tiempo tras ser asignado a tratamiento (meses)
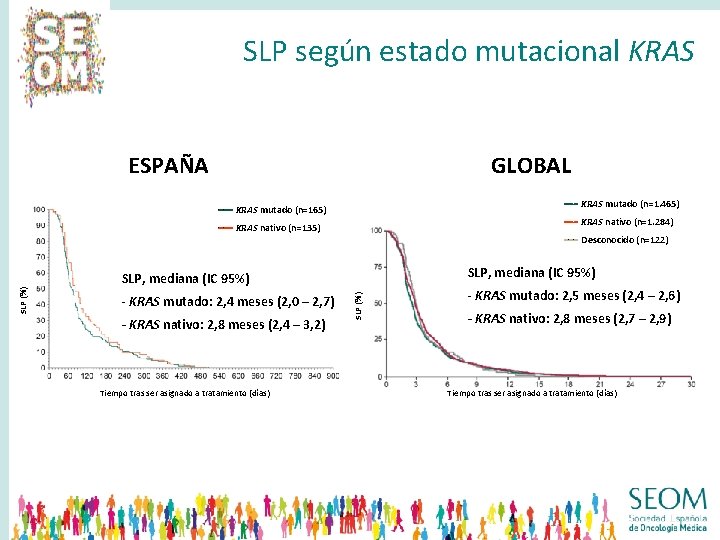
SLP según estado mutacional KRAS ESPAÑA GLOBAL −−− KRAS mutado (n=1. 465) −−− KRAS mutado (n=165) −−− KRAS nativo (n=1. 284) −−− KRAS nativo (n=135) −−− Desconocido (n=122) SLP, mediana (IC 95%) - KRAS mutado: 2, 4 meses (2, 0 – 2, 7) - KRAS nativo: 2, 8 meses (2, 4 – 3, 2) Tiempo tras ser asignado a tratamiento (días) SLP (%) SLP, mediana (IC 95%) - KRAS mutado: 2, 5 meses (2, 4 – 2, 6) - KRAS nativo: 2, 8 meses (2, 7 – 2, 9) Tiempo tras ser asignado a tratamiento (días)

Conclusiones • El perfil de seguridad de regorafenib en la cohorte española del estudio internacional CONSIGN fue, de forma general, consistente con el de la cohorte global. • La SLP en la cohorte española también fue consistente con la de la cohorte gobal y con los resultados de los estudios fase III con regorafenib en pacientes con CCRm 1, 2. • La SLP fue similar en los subgrupos KRAS nativo y mutado. • La alta tasa de reducción de dosis y de interrupción del tratamiento resalta la importancia de la óptima selección del paciente, del manejo de los acontecimientos adversos y de las modificaciones de dosis durante el tratamiento con regorafenib. 1. Grothey A, et al. Lancet 2013; 381: 303– 12; 2. Li J, et al. Lancet Oncol 2015; 16: 619– 29.

Investigadores principales del estudio CONSIGN en España Carles Pericay (Corporació Sanitària Parc Taulí ); Carmen Guillén (Hospital Universitario Ramón y Cajal), Cristina Grávalos (Hospital Universitario 12 de Octubre), Cristina Nadal (Hospital Clínic de Barcelona), Enrique Aranda (Hospital Provincial), Fernando Rivera Herrero (Hospital Universitario Marqués de Valdecilla), Jaime Feliu Batle (Hospital Universitario La Paz), Javier Sastre (Hospital Clínico San Carlos), José Luis Manzano (Institut Català d´Oncologia - Hospital Germans Trias i Pujol), Josep Tabernero (Hospital Vall d’Hebron), Manuel Benavides (Hospital General Universitario Carlos Haya), Manuel Valladares (Complejo Hospitalario Universitario de A Coruña), María José Safont (Hospital General Universitario de Valencia), Mercedes Martínez Villacampa (Institut Català d’Oncologia - Hospital Duran i Reynals), Pilar García Alfonso (Hospital General Universitario Gregorio Marañón), Rocío García-Carbonero (Hospital Universitario Virgen del Rocío) CONSIGN was sponsored by Bayer Health. Care Pharmaceuticals
- Slides: 16