REDUCTION DAMIDES ET DAMIDINES EN SYNTHESE Sabrina CUTRI

REDUCTION D’AMIDES ET D’AMIDINES EN SYNTHESE Sabrina CUTRI Laboratoire Chimie Organique-Prof. Sonnet. EA 3901 -DMAG-INERIS UPJV – Faculté de Pharmacie – Amiens 16/06/2005

PLAN 1. Amides • Hydrogénations • Transferts monoélectroniques – – • Hydrures métalliques – – – 2. Électrochimie Métaux dissous Boranes Borohydrures Aluminohydrures Silanohydrures Comparaison des méthodes Lactames Amidines
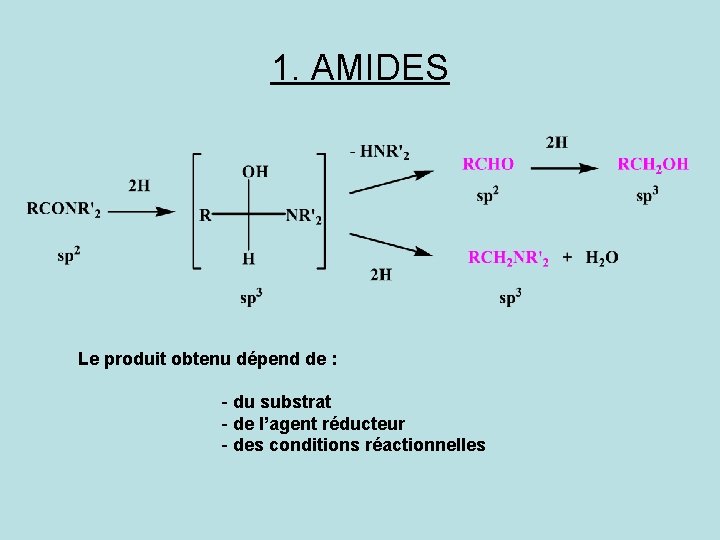
1. AMIDES Le produit obtenu dépend de : - du substrat - de l’agent réducteur - des conditions réactionnelles

HYDROGENATIONS • Conditions plus drastiques que pour les RCOOH et les RCOOR’ • Haute température, Haute pression→ équipements particuliers • Méthode réservée aux « cas désespérés » • Amides tertiaires un « peu » plus facile à réduire (260°C, 15 atm) • N. B. : La résistance des amides à l’hydrogénation peut permettre de différencier des esters et des amides en synthèse • Catalyseurs utilisés : Cu chromate, Ba/Cu chromate, Ni Raney, Cobalt Raney Ru/C Oxyde de rhénium (VII)
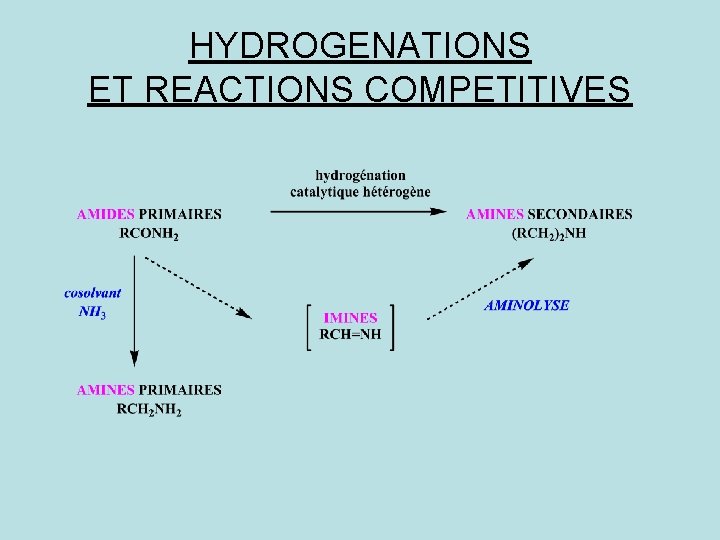
HYDROGENATIONS ET REACTIONS COMPETITIVES
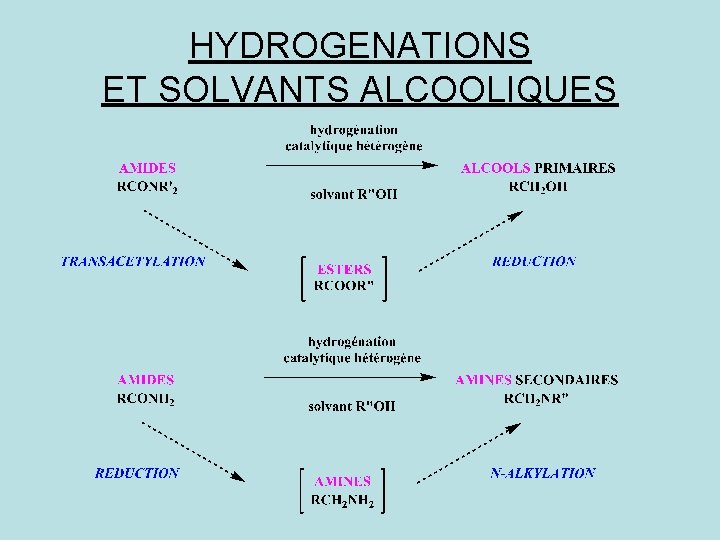
HYDROGENATIONS ET SOLVANTS ALCOOLIQUES
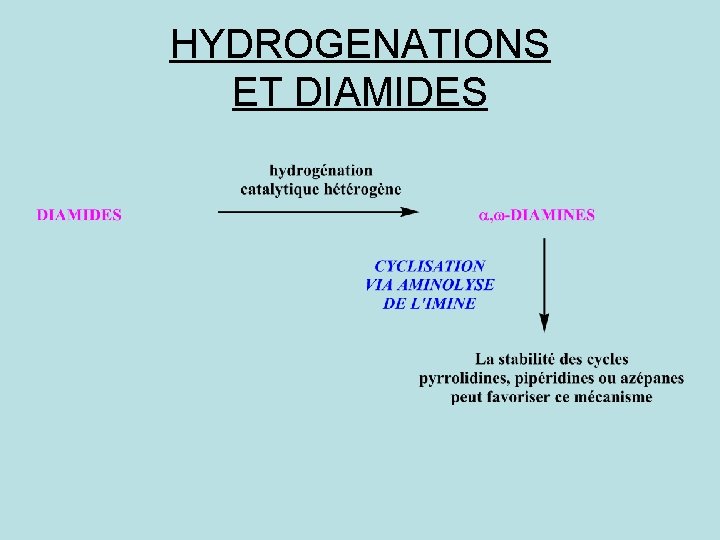
HYDROGENATIONS ET DIAMIDES
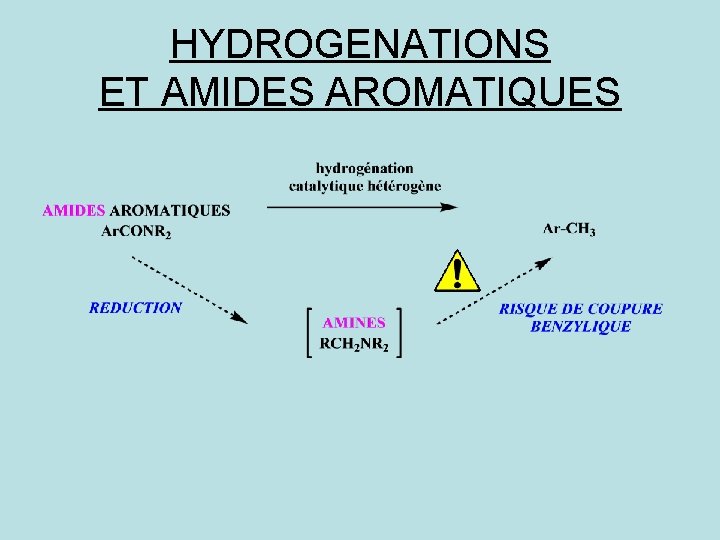
HYDROGENATIONS ET AMIDES AROMATIQUES
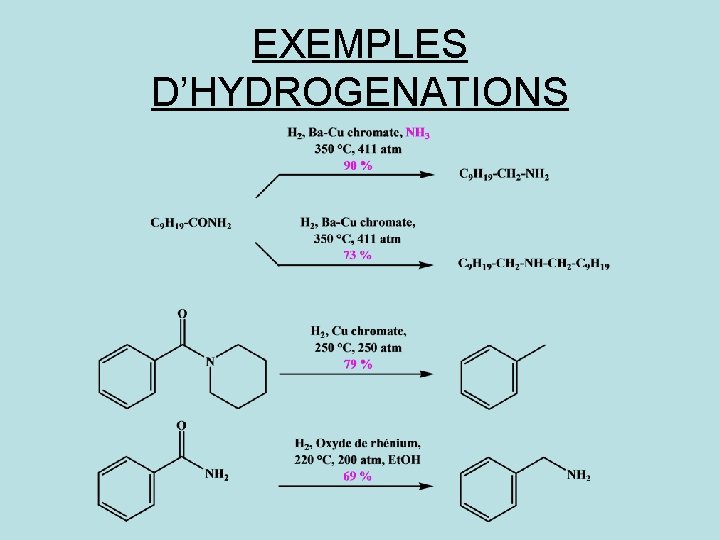
EXEMPLES D’HYDROGENATIONS

ELECTROCHIME : PRINCIPES • L’aldéhyde peut être favoriser en augmentant la temps de vie de la carbinolamine ou en piégeant l’aldéhyde quand il se forme • L’alcool est favorisé par une fragmentation rapide de la carbinolamine suivi d’une réduction à p. H neutre ou basique • L’amine est favorisée avec des cathodes à hydrogène à haute surtension (Pb, Hg, Cd) en milieu très acide : carbinolamine → iminium
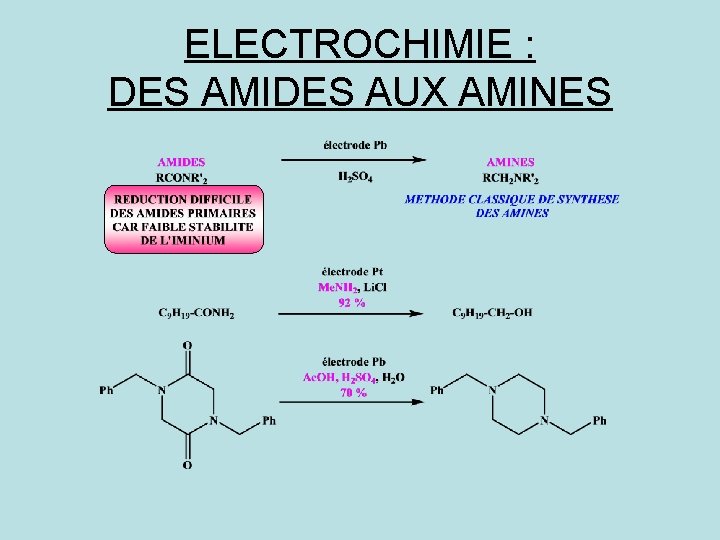
ELECTROCHIMIE : DES AMIDES AUX AMINES

METAUX DISSOUS ET CONDITIONS REACTIONNELLES • Aldéhyde : Li/Me. NH 2, Na/NH 3 en présence d’Et. OH, Ac. OH ou H 2 O • Alcool : métal en excès/NH 3 ou HMPA comme source de protons • Amine : métal, alcool Ce type de réduction fonctionne bien sur des thioamides
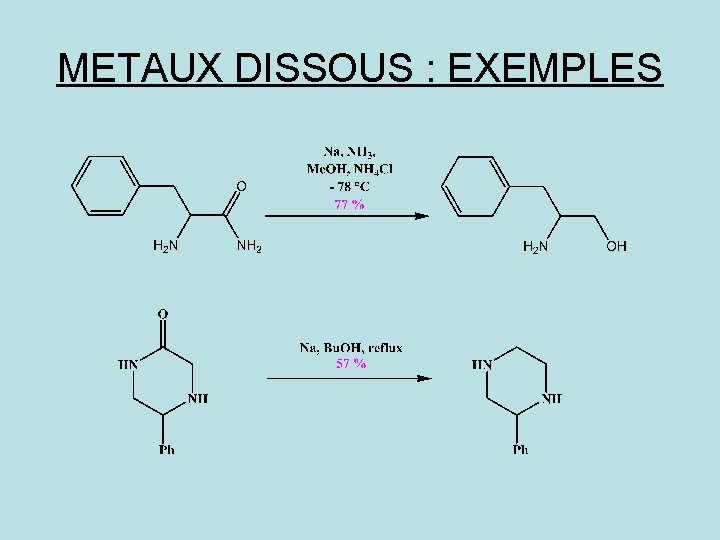
METAUX DISSOUS : EXEMPLES

HYDRURES METALLIQUES • Boranes • Borohydrures • Aluminohydrures • Silanohydrures • Comparaison des méthodes • Lactames

BORANES SIMPLES • Réactifs de choix : BH 3·THF, BH 3·Me 2 S dans l’éther, B 2 H 6 • Tenir compte des problèmes de chimiosélectivité avec les alcènes, les dérivés halogénés, les carbamates, les époxydes, les nitro. . .

ALKYLBORANES • Les alkylboranes réagissent plus lentement. L’encombrement stérique limite la fragmentation de la carbinolamine. • Thexylborane et disiamylborane utilisés pour obtenir des aldéhydes. • Le complexe thexylborane·Ph. NEt 2 est utilisé pour réduire les amides tertiaires en amines. • Globalement ces réactifs sont très peu utilisés.
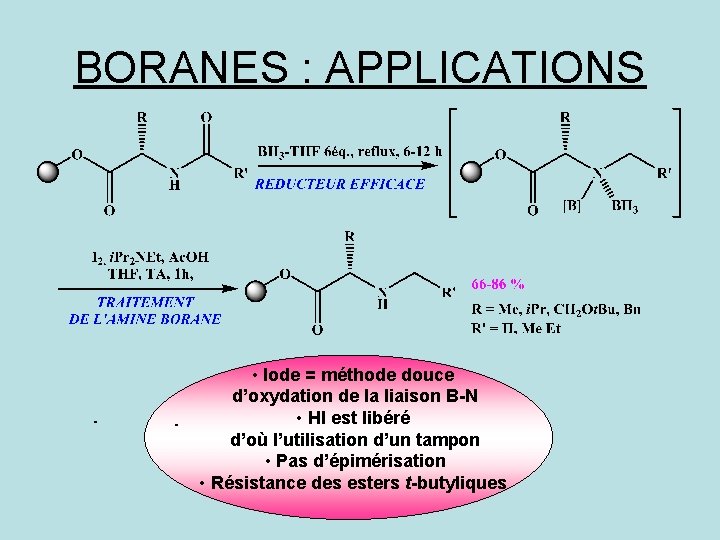
BORANES : APPLICATIONS • Iode = méthode douce d’oxydation de la liaison B-N • HI est libéré d’où l’utilisation d’un tampon • Pas d’épimérisation • Résistance des esters t-butyliques
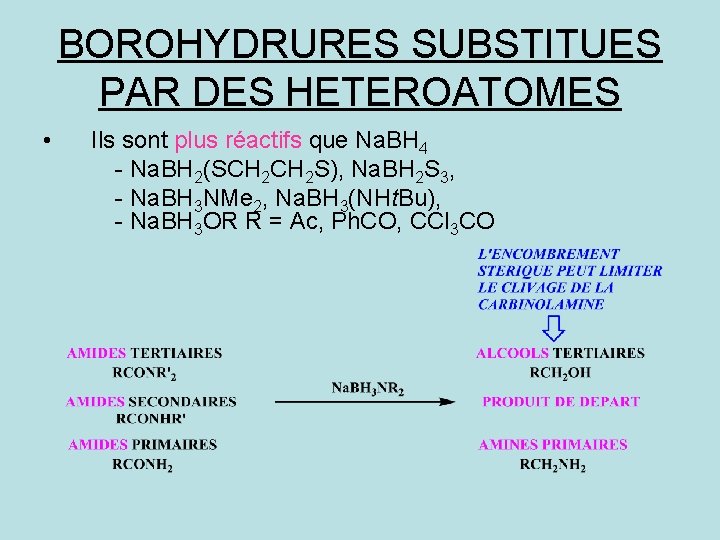
BOROHYDRURES SUBSTITUES PAR DES HETEROATOMES • Ils sont plus réactifs que Na. BH 4 - Na. BH 2(SCH 2 S), Na. BH 2 S 3, - Na. BH 3 NMe 2, Na. BH 3(NHt. Bu), - Na. BH 3 OR R = Ac, Ph. CO, CCl 3 CO
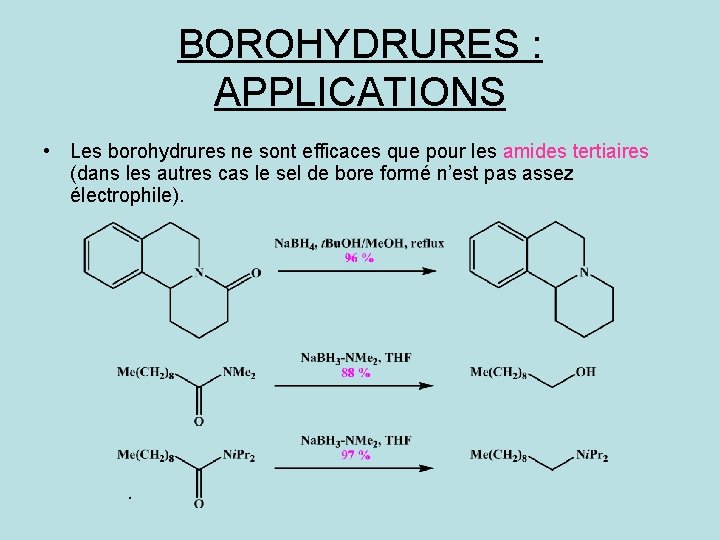
BOROHYDRURES : APPLICATIONS • Les borohydrures ne sont efficaces que pour les amides tertiaires (dans les autres cas le sel de bore formé n’est pas assez électrophile).

BOROHYDRURES • Na. BH 4/ROH, Li. BH 4/éther mauvais réducteur pour les amides, il faut forcer les conditions. • Systèmes utilisés pour obtenir les amines : Na. BH 4, Me. SO 3 H, DMSO Bu 4 NBH 4, CH 2 Cl 2 Na. BH 4 -Ti. Cl 4, DME Na. BH 4 -Co. Cl 2 ou Na. BH 4 -Ni. Cl 2, Me. OH Na. BH 4 -Al. Cl 3 (sauf pour amides Ires) • Systèmes utilisés pour obtenir les alcools : Li. BHEt 3, THF, D

ALUMINOHYDRURES • Systèmes utilisés pour obtenir les amines : Al. H 3, DIBAL-H, Al. H 2 Cl, Li. Al. H 4, Na. Al. H 4… • Et pour les alkoxyaluminohydrures moins réactifs mais souvent plus sélectifs: Li. Al. H(OMe)3, Red-Al, Al 2 H 3(OCH 2 OMe)3, Ca[Al. H 2(Oi. Bu)2]2·THF • v amides IIIR >> v amides IR et IIR • Al. H 3, DIBAL-H utilisés pour les amides insaturés. • Il faut toujours utiliser un excès pour ne pas s’arrêter au stade aldéhyde. • L’obtention de nitriles à partir d’amides primaires est fréquente.
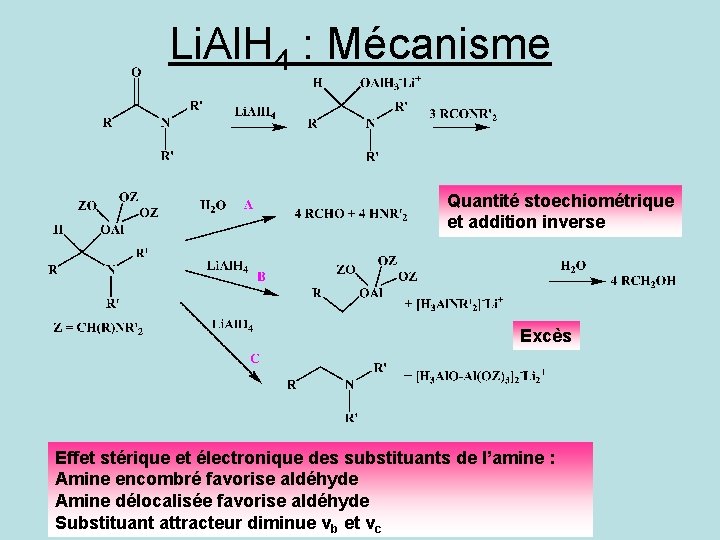
Li. Al. H 4 : Mécanisme Quantité stoechiométrique et addition inverse Excès Effet stérique et électronique des substituants de l’amine : Amine encombré favorise aldéhyde Amine délocalisée favorise aldéhyde Substituant attracteur diminue vb et vc
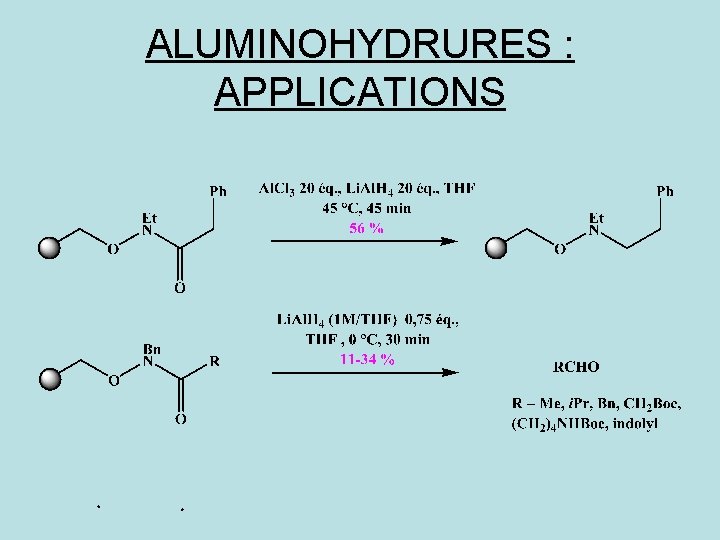
ALUMINOHYDRURES : APPLICATIONS
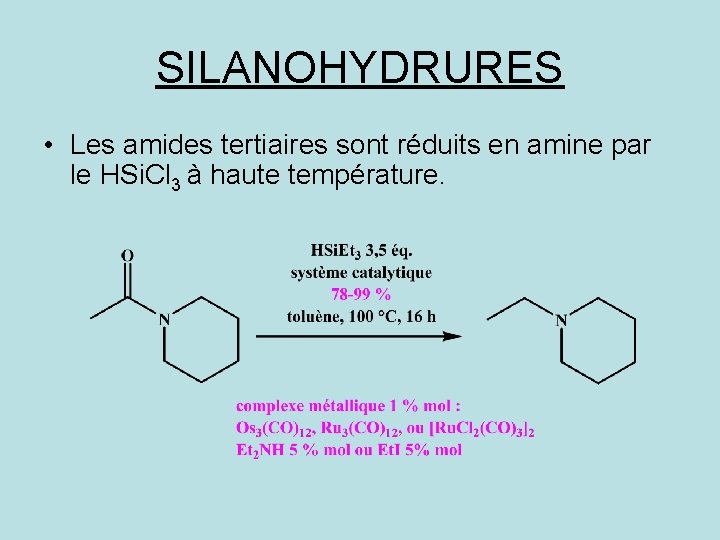
SILANOHYDRURES • Les amides tertiaires sont réduits en amine par le HSi. Cl 3 à haute température.
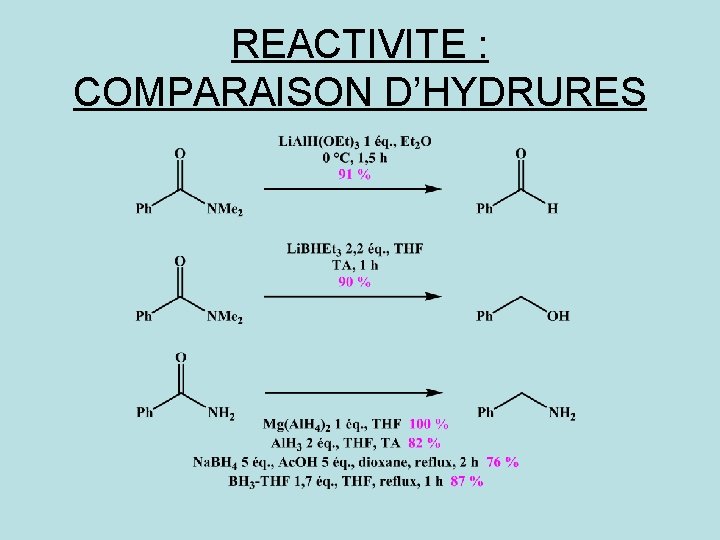
REACTIVITE : COMPARAISON D’HYDRURES
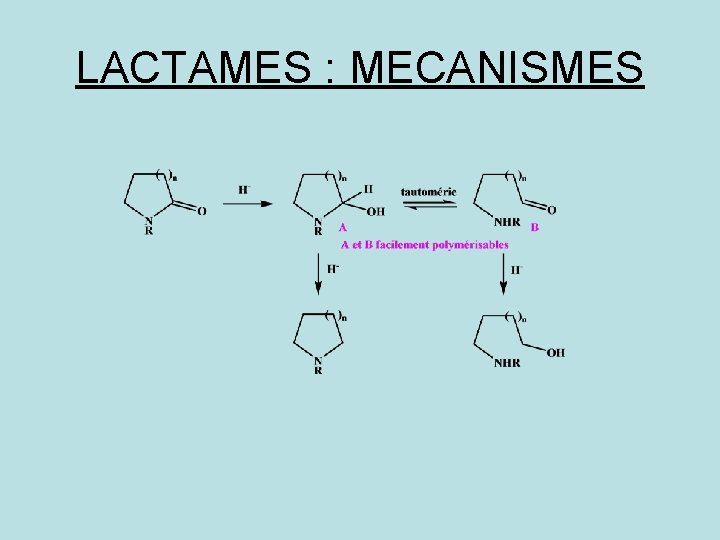
LACTAMES : MECANISMES
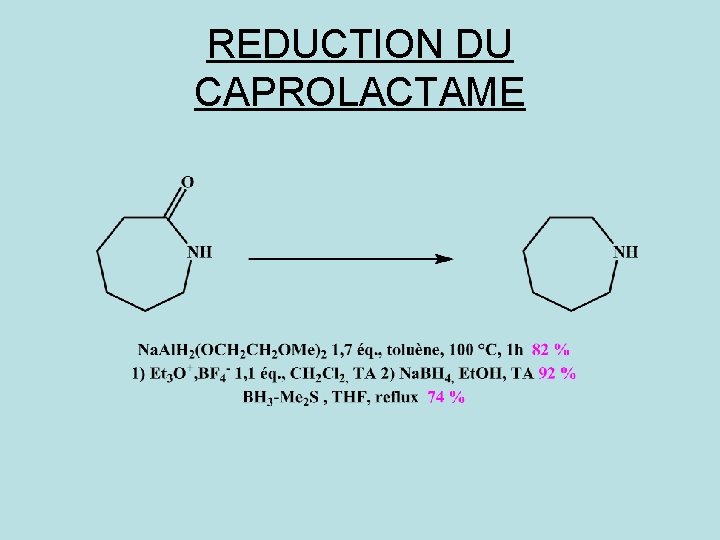
REDUCTION DU CAPROLACTAME
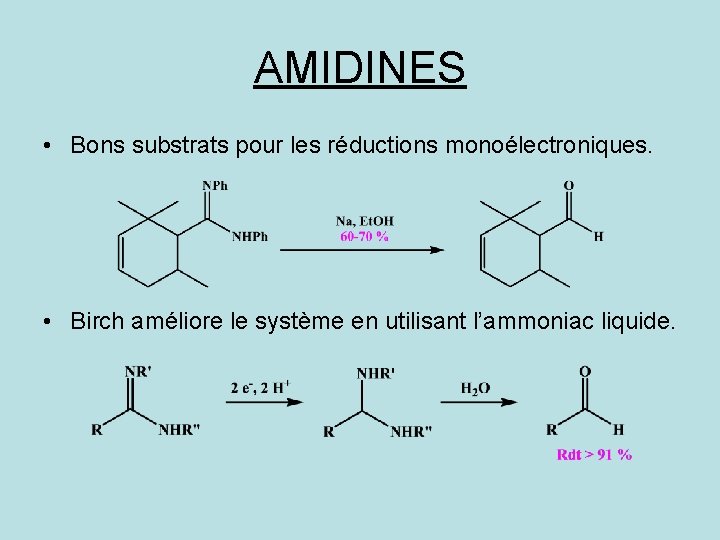
AMIDINES • Bons substrats pour les réductions monoélectroniques. • Birch améliore le système en utilisant l’ammoniac liquide.
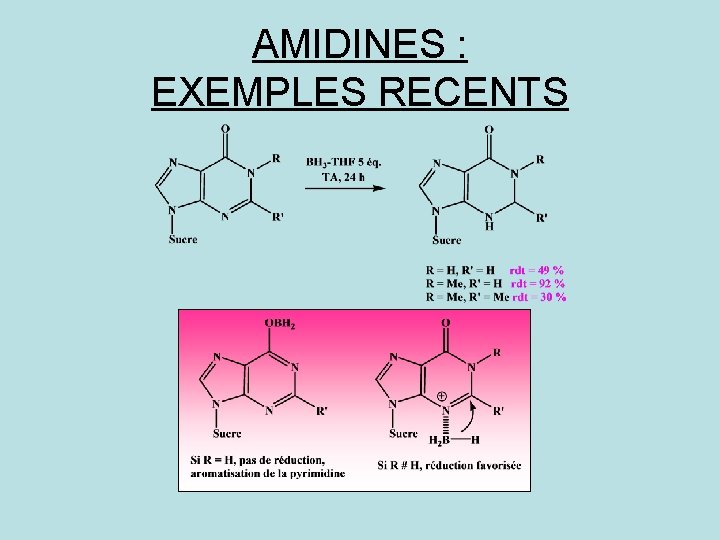
AMIDINES : EXEMPLES RECENTS
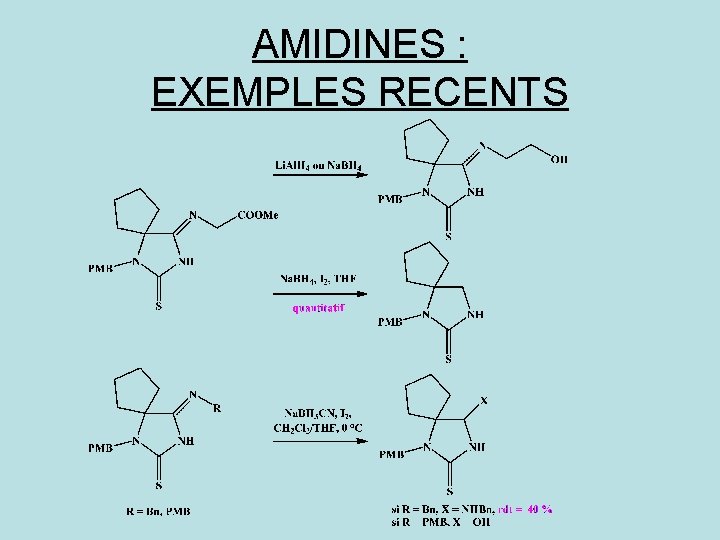
AMIDINES : EXEMPLES RECENTS
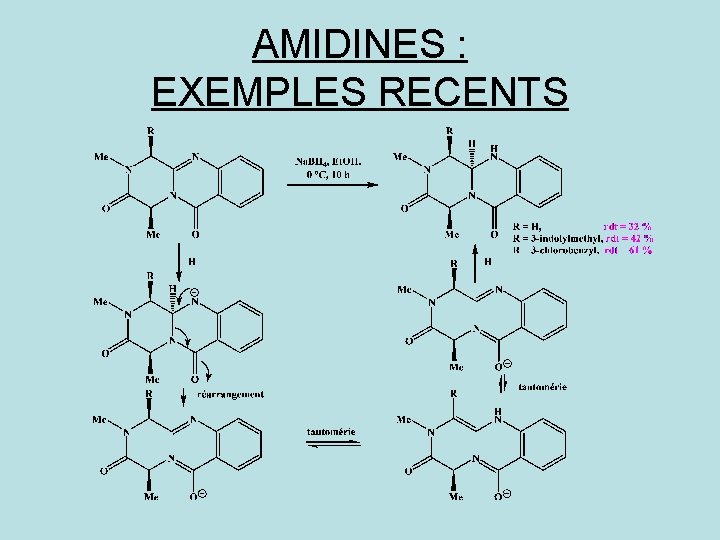
AMIDINES : EXEMPLES RECENTS

BIBLIOGRAPHIE 2. 3. 9. 11. 14. 15. 16. 17. Comprehensive Organic Chemistry, Katritsky, Vol 8, Chapter 1. 7 M. Hudlicky, Reductions in Organic Chemistry, Horwood, Chichester, 1984. T. A. Giudici, A. L. Fluharty, J. Org. Chem. , 1967, 32, 2043. K. Ziegler, K. Schneider, Justus Liebigs Ann. Chem. , 1959, 623, 9. P. Kohn, R. H. Samaritano, L. M. Lerner, J. Am. Chem. Soc. , 1965, 87, 5475. H. C. Brown, P. M. Weissmann, J. Am. Chem. Soc. , 1965, 87, 5614. M. Muraki, T. Mukaiyama, Chem. Lett. , 1974, 1447. P. Kohn, L. M. Lerner, A. Chan, S. D. Ginocchio, C. A. Zitrin, Carbohydr. Res. , 1968, 7, 21. R. E. Ireland, D. A. Evans, D. Glover, G. M. Rubottom, H. Young, J. Org. Chem. , 1969, 34, 3717. H. C. Brown, P. Heim, N. M. Yoon, J. Org. Chem. , 1972, 37, 2942. F. Guibe, P. Four, H. Rivière, J. Chem. Soc. , Chem. Commun. , 1980, 432. L. I. Smith, E. R. Rogier, J. Am. Chem. Soc. , 1951, 73, 4047. F. Weygand, D. Tietjen, Chem. Ber. , 1951, 84, 625. J. W. Jenkins, H. W. Post, J. Org. Chem. , 1950, 15, 556. M. Mouseron, R. Jacquier, M. Mousseron-Canet, R. Zagdoun, Bull. Soc. Chim. Fr. , 1952, 19, 1042. S. Kim, S. S. Kim, Tetrahedron Lett. , 1987, 28, 1913. J. M. Ostresh, C. C. Schoner, V. T. Hamashin, A. Nefzi, J. -P. Meyer, R. A. Houghten, J. Org. Chem. , 1998, 63, 8622. D. G. Hall, C. Laplante, S. Manku, J. Nagendran, J. Org. Chem. , 1999, 64, 698. A. S. Bhanu Prasad, J. V. Bhaskar Kanth, M. Periasamy, Tetrahedron, 1992, 48, 4623. G. Klein, J. M. Ostreh, A. Nefzi, Tetrahedron Lett. , 2003, 44, 2211. S. Kim, Pure Appl. Chem. , 1987, 59, 1005. J. Boyer, C. Brelière, R. J. P. Corriu, A. Kpoton, M. Poitier, G. Royo, J. Organomet. Chem. , 1986, 311, C 39. F. Weygand, G. Eberhardt, Angew. Chem. , 1952, 64, 458. F. Weygand, G. Eberhardt, H. Linden, F. Schäfer, I. Eigen, Angew. Chem. , 1953, 65, 525. V. M. Micovic, M. L. Mihailovic, J. Org. Chem. , 1953, 18, 1190. M. Muraki, T. Mukaiyama, Chem. Lett. , 1975, 215. E. Winterfelt, Synthesis, 1975, 617.

BIBLIOGRAPHIE 18. 20. 22. 23. 28. 29. 30. B. L. . Fox, R. J. Doll, J. Org. Chem. , 1973, 38, 1136. F. Weygand, R. Mitgau, Chem. Ber. , 1955, 88, 301. W. Ried, F. J. Königstein, Angew. Chem. , 1958, 70, 65. M. R. Johnson, B. Rickborn, Org. Synth. , 1971, 51, 11. J. H. Babler, Synth. Commun. , 1982, 12, 839. H. C. Brown, R. F. Mc. Farlin, J. Am. Chem. Soc. , 1958, 80, 5372. P. Coutrot, J. Villieras, J. C. Combret, C. R. Hebd. Seances Acad. Sci. , Ser. C, 1972, 274, 1531. H. A. Staab, H. Bräunling, Justus Liebigs Ann. Chem. , 1962, 654, 119. H. C. Brown, A. Tsukomoto, J. Am. Chem. Soc. , 1961, 83, 2016. H. C. Brown, R. F. Mc. Farlin, J. Am. Chem. Soc. , 1958, 80, 5372. F. Gosselin, J. Van Betsbrugge, M. Hatam, W. D. Lubell, J. Org. Chem. , 1999, 64, 2486. P. Blaney, R. Grigg, Z. Rankovic, M. Thoroghgood, Tetrahedron Lett. , 2000, 41, 6635. J. M. Salvino, M. Mervic, H. J. Mason, T. Kiesow, D. Teager, J. Airey, R. Labaudiniere, J. Org. Chem. , 1999, 64, 1823. H. C. Brown, A. Tsukomoto, J. Am. Chem. Soc. , 1961, 83, 4549. M. Igarashi, T. Fuchikami, Tetrahedron Lett. , 2001, 42, 1945. K. Hirota, H. Sajiki, R. Hattori, Y. Monguchi, G. Tanabe, O. Muraoka, Tetrahedron Lett. , 2002, 43, 653. I. J. Mc. Alpine, R. W. Armstrong, J. Org. Chem. , 1996, 61, 5674. S. Martin-Santamaria, M. Espada, C. Avendano, J. Org. Chem. , 1999, 64, 7233.

CONCLUSION
- Slides: 34