Redoxn reakce Hoen Koroze Redoxn reakce jsou chemick















- Slides: 16

Redoxní reakce Hoření Koroze

Redoxní reakce Ø jsou chemické reakce, při kterých dochází ke změně oxidačních čísel Ø probíhají při nich dva děje současně: 1. Redukce - dochází ke snížení oxidačního čísla, - atom elektrony _ _přijímá ______ 2. Oxidace - dochází ke zvýšení oxidačního čísla, odevzdává - atom elektrony _ _ ______

Redoxní reakce !!! Pamatuj !!! Ø oxidační čísla zapisujeme u každé značky vpravo nahoře Ø u nesloučených prvků (samostatně stojících) je oxidační číslo vždy rovno 0 Ø součet oxidačních čísel ve sloučenině je vždy roven 0 Ø ve sloučeninách má vždy: +I) +I ( H Ø Vodík oxidační číslo Ø Kyslík oxidační číslo -II (O-II) Ø plyny vytváří dvouatomové molekuly H 2 O 2 Cl 2

Redoxní reakce Hoření černého uhlí je vlastně reakce uhlíku s kyslíkem, do ovzduší uniká oxid uhličitý

Redoxní reakce Hoření černého uhlí je vlastně reakce uhlíku s kyslíkem, do ovzduší uniká oxid uhličitý oxidace C + O 2 C O 2 0 0 +IV redukce -II

Redoxní reakce !!! Pamatuj !!! Ø oxidační čísla zapisujeme u každé značky vpravo nahoře Ø u nesloučených prvků (samostatně stojících) je oxidační číslo vždy rovno 0 Ø součet oxidačních čísel ve sloučenině je vždy roven 0 Ø ve sloučeninách má vždy: +I) +I ( H Ø Vodík oxidační číslo Ø Kyslík oxidační číslo -II (O-II) Ø plyny vytváří dvouatomové molekuly H 2 O 2 Cl 2

Redoxní reakce Hoření černého uhlí je vlastně reakce uhlíku s kyslíkem, do ovzduší uniká oxid uhličitý oxidace C + O 2 C O 2 0 0 +IV redukce -II

Redoxní reakce Při korozi dochází ke slučování železa s kyslíkem a vzniká oxid železitý

Redoxní reakce Při korozi dochází ke slučování železa s kyslíkem a vzniká oxid železitý oxidace 4 Fe+3 O 2 2 Fe 2 O 3 0 0 +III redukce -II

Redoxní reakce Zinek reaguje s kyselinou chlorovodíkovou za vzniku vodíku a chloridu zinečnatého

Redoxní reakce Zinek reaguje s kyselinou chlorovodíkovou za vzniku vodíku a chloridu zinečnatého oxidace 0 +I -I Zn +2 HCl redukce 0 +II -I H 2 + Zn. Cl 2

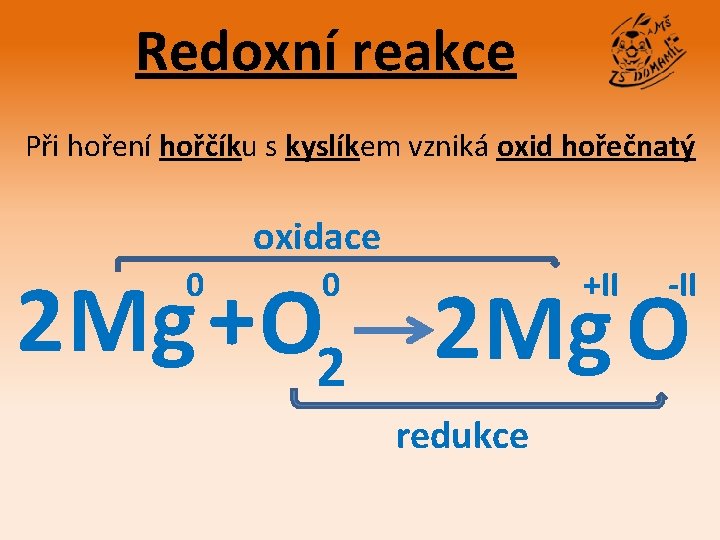
Redoxní reakce Při hoření hořčíku s kyslíkem vzniká oxid hořečnatý

Redoxní reakce Při hoření hořčíku s kyslíkem vzniká oxid hořečnatý oxidace 2 Mg + O 2 2 Mg O 0 0 +II redukce -II

Redoxní reakce Ø Vždy probíhají při nich oba děje současně: 1. Redukce - dochází ke snížení oxidačního čísla, - atom elektrony _ _přijímá ______ 2. Oxidace - dochází ke zvýšení oxidačního čísla, - atom elektrony _odevzdává _______

Redoxní reakce !!! Pamatuj !!! Ø oxidační čísla zapisujeme u každé značky vpravo nahoře Ø u nesloučených prvků (samostatně stojících) je oxidační číslo vždy rovno 0 Ø součet oxidačních čísel ve sloučenině je vždy roven 0 Ø ve sloučeninách má vždy: +I) +I ( H Ø Vodík oxidační číslo Ø Kyslík oxidační číslo -II (O-II) Ø plyny vytváří dvouatomové molekuly H 2 O 2 Cl 2

Redoxní reakce Děkuji za pozornost a hodně zdaru při řešení dalších redoxních reakcí