REDOXN CHEMICK REAKCIE Najprv si zopakujeme ak druhy













- Slides: 15

REDOXNÉ CHEMICKÉ REAKCIE Najprv si zopakujeme, aké druhy chemických reakcií sme sa doteraz učili

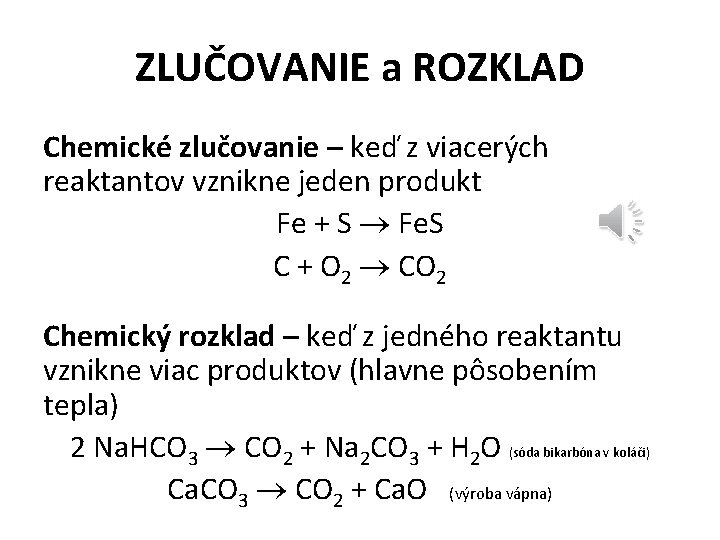
ZLUČOVANIE a ROZKLAD Chemické zlučovanie – keď z viacerých reaktantov vznikne jeden produkt Fe + S Fe. S C + O 2 CO 2 Chemický rozklad – keď z jedného reaktantu vznikne viac produktov (hlavne pôsobením tepla) 2 Na. HCO 3 CO 2 + Na 2 CO 3 + H 2 O (sóda bikarbóna v koláči) Ca. CO 3 CO 2 + Ca. O (výroba vápna)

ENDOTERMICKÉ a EXOTERMICKÉ Endotermická reakcia – taká, ktorá potrebuje teplo, aby prebiehala, sústava sa sama ochladzuje 2 Na. HCO 3 CO 2 + Na 2 CO 3 + H 2 O (sóda bikarbóna v koláči) Ca. CO 3 CO 2 + Ca. O (výroba vápna) Exotermická reakcia – taká, ktorá vydáva teplo, , sústava sa sama ohrieva (horenie, svietenie, výbuch) C + O 2 CO 2

NEUTRALIZÁCIA Neutralizácia je chemická reakcia, pri ktorej reaguje kyselina s hydroxidom. Vzniká soľ a voda. • Na začiatku je kyslá kyselina, zásaditý hydroxid. V reakcii sa to zneutralizuje, takže výsledkom je roztok soli vo vode – voda je neutrálna aj soľ je neutrálna. Na. OH + HCl Na. Cl + H 2 O KOH + HBr KBr + H 2 O Ca(OH)2 + H 2 SO 4 Ca. SO 4 + 2 H 2 O Mg(OH)2 + 2 HNO 3 Mg(NO 3) 2 + 2 H 2 O

Teraz napíšeme každému atómu oxidačné číslo: Na. IO-IIHI + HICl-I Na. ICl-I + HI 2 O-II KIO-IIHI + HIBr-I KIBr-I + HI 2 O-II Ca. II(O-IIHI)2 + HI 2 SVIO 4 -II Ca. IISVIO 4 -II + 2 HI 2 O-II Mg. II(O-IIHI)2 + 2 HINVO 3 -II Mg. II(NVO 3 -II) 2 + 2 HI 2 O-II • Keď porovnáme oxidačné čísla na začiatku a na konci reakcie, vidíme, že sa nemenia. Pri neutralizácii sa nemenia oxidačné čísla atómov.

REDOXNÉ CHEMICKÉ REAKCIE Tu je iný typ reakcie: 2 Na + Cl 2 2 Na. Cl 2 Na 0 + Cl 02 2 Na. ICl-I • Vidíme, že v reakcii sa obom atómom menia oxidačné čísla. Dá sa to zapísať aj takto: Na 0 – e- Na. I Cl 0 + e- Cl-I

Na 0 – e- Na. I • sodík v reakcii stráca elektrón • jeho oxidačné číslo narastie o 1 • hovoríme, že sodík sa oxiduje Cl 0 + e- Cl-I • chlór v reakcii prijíma elektrón od sodíka • jeho oxidačné číslo klesne o 1 (lebo je potom zápornejší) • hovoríme, že chlór sa redukuje

REDOXNÉ CHEMICKÉ REAKCIE • Redoxné chemické reakcie sú také reakcie, pri ktorých si atómy vymieňajú elektróny a potom sa menia oxidačné čísla atómov. Prebieha tam redukcia a oxidácia. (red-ox)

KLINEC V MODREJ SKALICI

KLINEC V MODREJ SKALICI Zápis reakcie: Fe + Cu. SO 4 Cu + Fe. SO 4 S oxid. číslami: Fe 0 + Cu. IISVIO-II 4 Cu 0 + Fe. IISVIO-II 4 Fe 0 – 2 e- Fe. II Železo stráca dva elektróny – oxiduje sa Cu. II + 2 e- Cu 0 Meď prijíma dva elektróny – redukuje sa

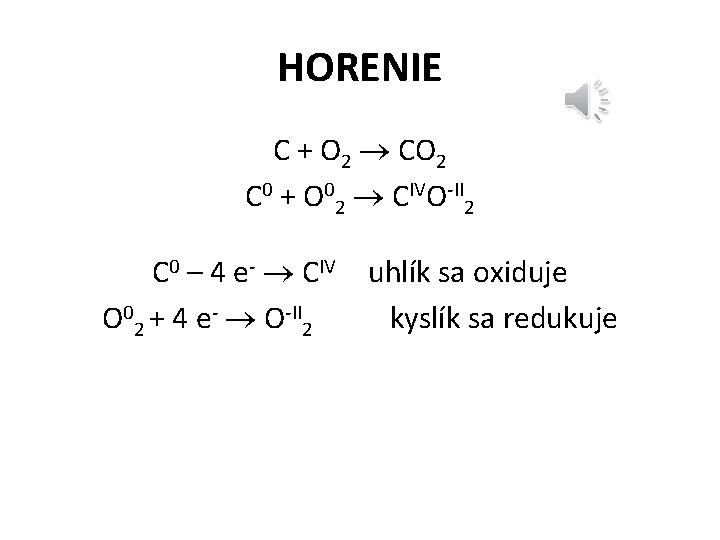
HORENIE C + O 2 CO 2 C 0 + O 02 CIVO-II 2 C 0 – 4 e- CIV uhlík sa oxiduje O 02 + 4 e- O-II 2 kyslík sa redukuje

ELEKTRINA • Keď sa niekde vymieňajú elektróny, prebieha tam elektrický prúd. Preto sú redoxné reakcie podstatou vzniku elektrického prúdu v batériách, akumulátoroch. (pozor nie v elektrárňach, tam sa to vyrába pomocou krútenia elektromagnetu, to je fyzika)

ALKALICKÁ BATÉRIA 2 Mn. O 2 + H 2 O + Zn Mn 2 O 3 + Zn(OH)2 2 Mn. IVO-II 2 + HI 2 O-II + Zn 0 Mn. III 2 O-II 3 + Zn. II(O-IIHI)2 2 Mn. IV + 2 e- Mn. III 2 mangán sa redukuje Zn 0 – 2 e- Zn. II zinok sa oxiduje Kto si chce o batériách niečo pozrieť, tak toto je dobré: https: //youtu. be/yg. Dq. VDZv. A 64

ÚLOHA • Pozrite si padlet o rakete Falcon 9 https: //padlet. com/radvanska_katarina/jlxuleqsd p 1 dkb 6 m • Môžete tam pripojiť ďalšie zaujímavosti, dostanete známku • Zjednodušený vzorec paliva (propellant) je vzorec metánu: CH 4 takéto má oxidačné čísla C-IVHI 4 • Druhé palivo je kyslík

Vašou úlohou je: – napísať mi reakciu, ktorá prebieha v tejto rakete – napísať jej reaktanty a produkty (skúste pátrať na webe) – pomenovať tieto produkty – reakciu správne vyčísliť – napísať oxidačné čísla reaktantov aj produktov – napísať, ktorý atóm sa oxiduje a ktorý redukuje CH 4 + kyslík ? + ? • Napíšte to perom na papier, odfoťte, pošlite do nedele
 Popoluškine šaty
Popoluškine šaty Najprv šaty zelené potom nosí červené
Najprv šaty zelené potom nosí červené Exotermické reakcie
Exotermické reakcie Redoxn's
Redoxn's Beketovova řada kovů příklady
Beketovova řada kovů příklady Redoxné reakcie
Redoxné reakcie Koncovky oxidačných čísel
Koncovky oxidačných čísel Adriana chemick
Adriana chemick Adriana chemick
Adriana chemick Adriana chemick
Adriana chemick Hydroxidy vzorce
Hydroxidy vzorce Adriana chemick
Adriana chemick Chemické zlučovanie
Chemické zlučovanie Pomalé a rýchle chemické reakcie
Pomalé a rýchle chemické reakcie Protolytické reakcie príklady
Protolytické reakcie príklady Protolytické reakcie
Protolytické reakcie