REDOX Wat is redox Redoxchemie zijn processen waarbij
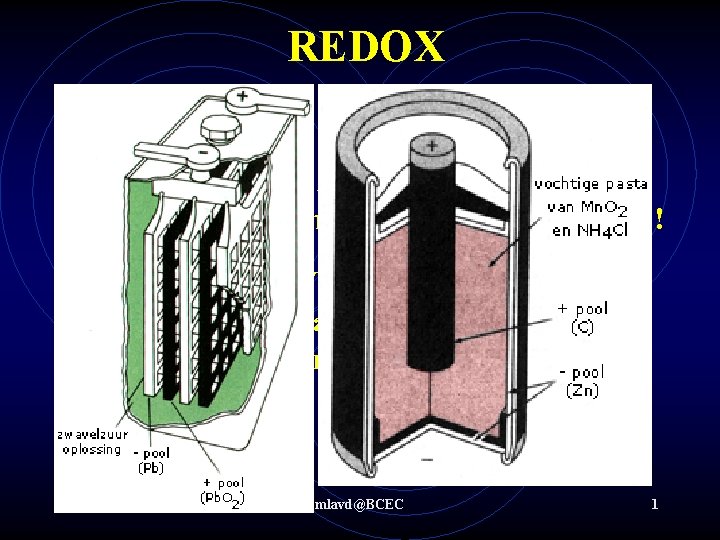
REDOX Wat is redox ? Redox-chemie zijn processen waarbij overdracht van elektronen plaats vindt ! Voorbeelden: Accu’s, batterijen, brandstofcellen, etc mlavd@BCEC 1
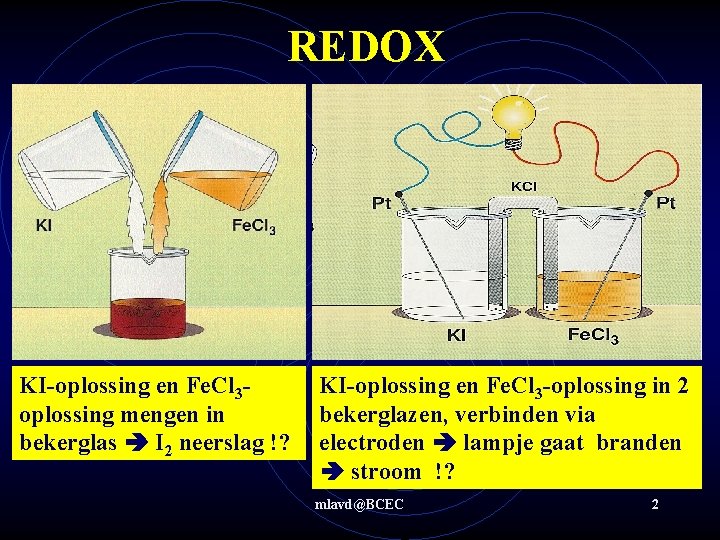
REDOX KI-oplossing en Fe. Cl 3 oplossing mengen in bekerglas I 2 neerslag !? KI-oplossing en Fe. Cl 3 -oplossing in 2 bekerglazen, verbinden via electroden lampje gaat branden stroom !? mlavd@BCEC 2

REDOX 2 I- I 2 (s)+ 2 e- Fe 3+ + e- Fe 2+ 1* 2* + 2 Fe 3+ + 2 I- 2 Fe 2+ + I 2 (s) De elektronen gaan van Inaar Fe 3+ waarbij I 2 en Fe 2+ ontstaan e- e- e-e- mlavd@BCEC 3

REDOX eee- e- 2 I- I 2 (s)+ 2 e- 1* Fe 3+ + e- Fe 2+ 2* + 2 Fe 3+ + 2 I- 2 Fe 2+ + I 2 (s) De elektronen gaan van het ene bekerglas met Idoor de draad en het lampje naar de het bekerglas met Fe 3+. Hierbij ontstaan ook I 2 en Fe 2+ en gaat het lampje branden. mlavd@BCEC 4
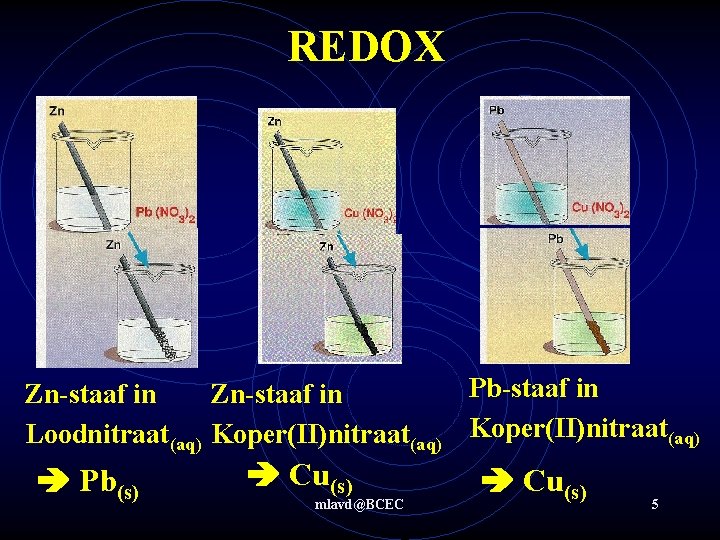
REDOX Pb-staaf in Zn-staaf in Loodnitraat(aq) Koper(II)nitraat(aq) Pb(s) Cu(s) mlavd@BCEC Cu(s) 5

REDOX Redox reacties zijn reacties met elektronen overdracht Element ontstaat of verdwijnt Verbrandingen Alle reacties met ladingsverandering mlavd@BCEC 6
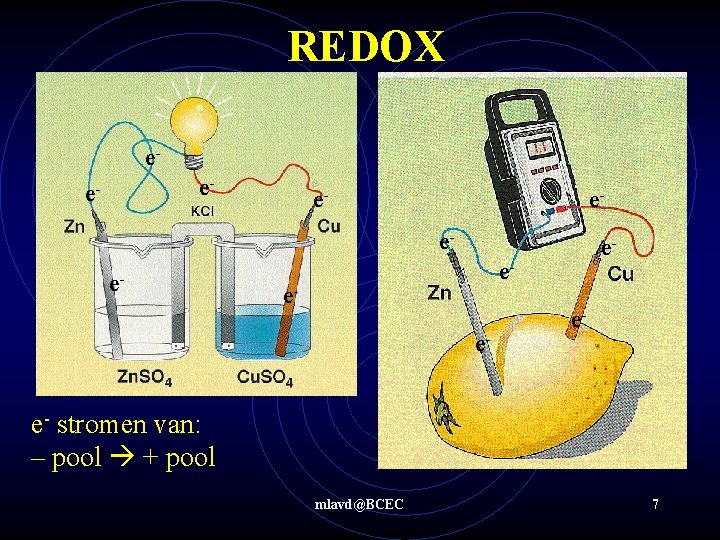
REDOX ee- e- e- stromen van: – pool + pool mlavd@BCEC 7

REDOX Overeenkomsten redox met zuur-base !! Zuur-base Redox Overdracht van H+ Overdracht van e- Sterkste zuren linksboven in Binas tabel 49 Sterkste oxidatoren linksboven in Binas tabel 48 Sterkste basen rechtsonder in Binas tabel 49 Zuursterkte: grootste Kz Basesterkte: grootste Kb Sterkste reductoren rechtsonder in Binas tabel 48 Oxidatorsterkte: hoogste V 0 Reductorsterkte: laagste V 0 mlavd@BCEC 8

REDOX: opstellen reactievergelijkingen Stap 1: zet in een tabel of de aanwezige deeltjes reductoren of oxidatoren zijn. Zet meteen ook de V 0 erbij in de tabel Oxidator Reductor Ox 1 Red 1 Ox 2 Red 2 Stap 2: bepaal de sterkste oxidator (hoogste V 0 en sterkste reductor (laagste V 0). NB: let ook op H 2 O mlavd@BCEC 9

REDOX: opstellen reactievergelijkingen Stap 3: zoek de halfvergelijkingen op in Binas en neem deze over Stap 4: Maak m. b. v. vermenigvuldigingsfactoren het aantal elektronen bij de halfvergelijkingen van de RED en OX. Stap 5: Tel de halfvergelijkingen op tot een totaalvergelijking mlavd@BCEC 10

REDOX: opstellen reactievergelijkingen Stap 6: bepaal het spanningsverschil van de reactie ΔV = V 0 oxidator – V 0 reductor ΔV > 0, 3 V aflopende reactie - 0, 3 V < ΔV < 0, 3 V evenwichtsreactie ΔV < - 0, 3 V reactie verloopt niet mlavd@BCEC 11

REDOX Oefenen met reacties: http: //www. chem. iastate. edu/group/Greenbowe/sections/projectfolder/ flashfiles/redox/home. html mlavd@BCEC 12

Redox: Fe + zoutzuur Bv: mengen van ijzerpoeder met zoutzuur Stap 1+2: OX H+ (0, 0 H 2 O RED V) Fe (-0, 44 V) H 2 O Cl- ΔV = 0 – (-0, 44) = 0, 44 V aflopend Fe HCl H+ + Cl- Stap 3 t/m 6 O: 2 H+ + 2 e- H 2(g) R: Fe 2+ + 2 e. Fe + 2 H+ Fe 2+ + H 2(g) mlavd@BCEC 13

REDOX: opstellen reactievergelijkingen Stap 3: zoek de halfvergelijkingen op in Binas en neem deze over Stap 4: Maak m. b. v. vermenigvuldigingsfactoren het aantal elektronen bij de halfvergelijkingen van de RED en OX. Stap 5: Tel de halfvergelijkingen op tot een totaalvergelijking mlavd@BCEC 14

Redox: koper + waterstofperoxide-oplossing Stap 1+2: OX RED H 2 O 2 (0, 94 V) H 2 O Cu (0, 34 V) H 2 O 2 (0, 68 V) H 2 O Stap 3 t/m 6: Ox: H 2 O 2 + 2 e- 2 OH(0, 94 V) Red: Cu 2+ + 2 e- (0, 34 V) Cu + H 2 O 2 Cu 2+ + 2 OH- (ΔV= 0, 6 V) Cu 2+ + 2 OH- Cu(OH)2 (zie hfst 2) mlavd@BCEC 15

Redox: chloorwater + ijzer(II)chloride-oplossing Stap 1+2: OX RED Cl 2 (1, 36 V) Fe 2+ (-0, 44 V) H 2 O Fe 2+ (0, 77 V) Cl- (1, 36 V) H 2 O Stap 3 t/m 6: Ox: Cl 2 + 2 e- 2 Cl(1, 36 V) 1* Red: Fe 2+ Fe 3+ + e- (0, 77 V) 2* 2 Fe 2+ + Cl 2 2 Fe 3+ + 2 Cl- (ΔV= 0, 59 V) mlavd@BCEC 16

Redox: invloed van omgeving Zoals je ooit wel gemerkt zult hebben of nog zult merken is er een grote invloed van de omgeving op bv de corrosiesnelheid van een stuk metaal - Een stuk metaal roest heel erg langzaam in zuurstofarm zuiver water - Een stuk metaal roest in zuurstofrijk kraanwater - Een stuk metaal roest snel in aangezuurd zuurstofrijk kraanwater mlavd@BCEC 17

Redox: invloed van omgeving - Een stuk metaal roest heel erg langzaam in zuurstofarm zuiver water OX RED H 2 O – 0, 83 V Fe (-0, 44 V) H 2 O ΔV = -0, 39 V < 0, 3 geen reactie mlavd@BCEC 18

Redox: invloed van omgeving - Een stuk metaal roest snel in zuurstofrijk water OX RED O 2/H 2 O (0, 82 V) H 2 O Fe (-0, 44 V) ΔV = 1, 26 V > 0, 3 V aflopende reactie H 2 O O 2 + 2 H 2 O + 4 e- 4 OH- (*1) 0, 82 V Fe 2+ + 2 e(*2) -0, 44 V O 2 + 2 H 2 O + 2 Fe 2 Fe 2+ + 4 OHFe 2+ + 2 OH- Fe(OH)2 mlavd@BCEC 19

Redox: invloed van omgeving - Een stuk metaal roest snel in aangezuurd zuurstofrijk kraanwater Ox Red O 2/H 2 O, H+ (1, 23 V) Fe (-0, 44 V) H 2 O ΔV = 1, 66 V > 0, 3 aflopende reactie Ox : O 2 + 4 H+ + 4 e- 2 H 2 O (1, 23 V) 1* Red: Fe 2+ + 2 e- (-0, 44 V) 2* 2 Fe + O 2 + 4 H+ 2 Fe 3+ + 2 H 2 O (ΔV= 1, 67 V) mlavd@BCEC 20

Redox: invloed van omgeving De omgeving heeft uiteraard ook bij andere stoffen invloed op de reactie !!! Verklaar waarom bij het mengen van ijzerpoeder met kaliumpermanganaat er een mengsel ontstaat van 2 vaste stoffen (waaronder bruinsteen) ontstaat terwijl bij het mengen van ijzerpoeder met een aangezuurd oplossing van kaliumpermanganaat dit niet zal gebeuren maar de oplossing juist helder en kleurloos wordt. mlavd@BCEC 21

Redox: invloed van omgeving Inventarisatie: ijzerpoeder = Fe kaliumpermanganaat = KMn. O 4 = K+ + Mn. O 4 bruinsteen = Mn. O 2 aangezuurd kaliumpermanganaat = K+ + Mn. O 4 - + H+ mlavd@BCEC 22

Redox: invloed van omgeving Stap 1+2: aangezuurd OX RED Mn. O 4 - Fe OX RED Mn. O 4 -/H+ Fe H 2 O mlavd@BCEC H 2 O 23

Redox: invloed van omgeving Stap 3 t/m 6: niet aangezuurd Ox : Mn. O 4 - + 2 H 2 O + 3 e- Mn. O 2 + 4 OH- 2* 3* Red: Fe 2+ + 2 e 2 Mn. O 4 - + 4 H 2 O + 3 Fe 2+ + 2 Mn. O 2 + 8 OHNB vervolgreactie: Fe 2+ + 2 OH- Fe(OH)2 (s) mlavd@BCEC 24

Redox: invloed van omgeving Stap 3 t/m 6: aangezuurd Ox : Mn. O 4 - + 8 H+ + 5 e- Mn 2+ + 4 H 2 O 2* Red: Fe 2+ + 2 e 5* 2 Mn. O 4 - + 16 H+ + 5 Fe 2+ + 2 Mn 2+ + 4 H 2 O mlavd@BCEC 25

Leuk Redox filmpje Thermiet: http: //video. google. com/videoplay? docid=7231843493488769585 Alkali: http: //www. youtube. com/watch? v=Ft 4 E 1 e. CUIt. I&feature=related mlavd@BCEC 26

Zelf opstellen reactievergelijkingen Uiteraard staan niet alle reacties in Binas voor je klaar, je moet ook zelf half- en totaalvergelijkingen op kunnen stellen. Hoe gaat dat zelf opstellen van half- en totaalvergelijkingen ? mlavd@BCEC 27

Zelf opstellen reactievergelijkingen Stap 1: schrijf de formules van de deeltjes op Stap 2: kijk welke (ladings)verandering er op treedt tussen de beginstof en eindstof Stap 3: kijk welk milieu neutraal/basisch wordt meestal H 2 O gebruikt als hulpdeeltje; zuur wordt H+ gebruikt als hulpdeeltje Stap 4: stel a. h. v. de (ladings)verandering en de bekende beginstof en eindstof een halfvergelijking met het juiste aantal e- op. mlavd@BCEC 28

Zelf opstellen reactievergelijkingen Geef de reactievergelijking van de reactie van permanganaat in zuur milieu waarbij o. a. een Mn(II)ion gevormd wordt Stap 1: Mn. O 4 - + Mn 2+ H+ Stap 2/3: er wordt 4*O uit Mn. O 4 - gehaald dus worden er 4 water gemaakt: Mn. O 4 - + H+ Mn 2+ + 4 H 2 O dus zijn er ook 8 H+ nodig Mn. O 4 - + 8 H+ Mn 2+ + 4 H 2 O Stap 4: voor pijl 7+ en na 2+ dus moeten er 5+ weg dus 5 e. Mn. O 4 - + 8 H+ + 5 e- Mn 2+ + 4 H 2 O mlavd@BCEC 29

Zelf opstellen reactievergelijkingen Geef de halfreactie van jodaat in zuur milieu waarbij o. a. jood gevormd wordt Stap 1: 2 IO 3 - + H+ I 2 Stap 2/3: er wordt 6*O uit IO 3 - gehaald 2 IO 3 - + H+ I 2 + 6 H 2 O dus zijn er ook 12 H+ nodig 2 IO 3 - + 12 H+ I 2 + 6 H 2 O Stap 4: voor pijl 10+ en na 0 dus 10+ weg dus 10 e 2 IO 3 - + 12 H+ + 10 e I 2 + 6 H 2 O mlavd@BCEC 30

Zelf opstellen reactievergelijkingen Geef de halfreactie van tin in neutraal milieu waarbij o. a. Tin(IV)oxide gevormd wordt Stap 1: Sn Sn. O 2 Stap 2/3: er wordt 2*O in Sn ‘gedaan’ Sn + 2 H 2 O Sn. O 2 + H+ dus zijn er ook 4 H+ nodig Sn + 2 H 2 O Sn. O 2 + 4 H+ Stap 4: voor pijl 0 en na 4+ dus 4+ teveel dus 4 e- nodig Sn + 2 H 2 O Sn. O 2 + 4 H+ + 4 emlavd@BCEC 31

And now for something completely different (maar ook leuk) http: //www. youtube. com/watch? v=a. A 5 Wggf 7 ft. I&feature=related http: //video. google. nl/videoplay? docid=-7525014357509994289&q=brainiac http: //www. youtube. com/watch? v=Eb 54 ia. Xaqik&feature=related http: //video. google. com/videoplay? docid=-6343218882618828140 http: //video. google. com/videoplay? docid=-8014354858921252855 http: //video. google. com/videoplay? docid=-8666853249964284510&q=type%3 Agpick mlavd@BCEC 32
- Slides: 32