Recenti Sviluppi Metodologici nelle Sperimentazioni cliniche Gli studi







































































- Slides: 79

Recenti Sviluppi Metodologici nelle Sperimentazioni cliniche Gli studi adattativi Paolo Bruzzi Epidemiologia Clinica IRCCS AOU San Martino - IST - Genova

Evoluzione del “pensiero” medico Millenni - Medicina pre scientifica ‘ 700 -’ 900 Medicina Empirica ‘ 40 -50 Randomized Clinical Trial 1985 Evidence Based Medicine >1990 Medicina Molecolare (“Personalizzata? ”)

Approccio Empirico • Pragmatico (Complessita’ risolta dalla statistica) • Primato dell’osservazione (sulla teoria) • Dimostrazione tramite falsificazione (H 0)

Empirical Approach Preclinical work + Clinical observations Clinical rationale

Empirical Approach Preclinical work + Clinical observations Clinical rationale RCT CLINICAL STUDIES INTERPRETATION

RCT -> EBM in Oncologia (& Cardiologia) – Eta’ dell’oro • Protocolli Terapeutici rigidi – Farmaci – Dosi – Cicli – Modificazioni x tossicita’ o progressione • Criteri di selezione generici – Sede (e. g. Stomaco) – Istologia (ADK vs Lymphoma) – Stadio (early vs late)

RCT -> EBM in Oncologia (& Cardiologia) – Eta’ dell’oro Trials enormi su popolazioni eterogenee alla ricerca di effetti modesti

RCT -> EBM in Oncologia (& Cardiologia) – Eta’ dell’oro • Large and Simple Clinical Trials - Revisioni Sistematiche – Meta-analisi • Clinical Guidelines/Raccomandazioni – – Generiche – Non prevista flessibilita’ nella gestione del paziente

Principio Guida: Equita’ • Prospettiva di sanita’ pubblica (es. vaccinazioni) • Piccoli effetti x grosse popolazioni = grandi benefici • Terapie semplici, eguali x tutti (trombolisi, Tamoxifen) • Pazienti non selezionati • Generalizzabilita = Applicabilita’ su larga scala

Rigida separazione delle fasi • Fase I -> MTD -> Aumenti Dose in gruppi successivi di pazienti • Fase II -> Activita’ -> Trial non controllato • Fase III -> Efficacia -> RCT

Trials di Fase III Convenzionali • Criteri di Inclusione -> Fissi x tutto il trial • Terapia -> Protocollo fisso x tutto il trial ’ a t i d i g i R • Statistica -> Piano statistico predefinito nei dettagli • Sample Size -> Prefissato - Enorme

Simile rigidita’ in altre aree di ricerca? • NO! Trial and Error! • Biologia, Ingegneria, Chimica, Fisica I risultati degli esperimenti e le nuove conoscenze (esterne) sono utilizzati per modificarne continuamente la metodologia

Perche’ la flessibilita’ e(ra) poco (o non) tollerata nei Trials di Fase III? • Filosofia Statistica Frequentista – Controllo della false positive rate ( errore alfa) • Scarse possbilita’ di replicare un trial – Se positivo, un altro RCT non etico – Se negativo, replicare troppo costoso • Conoscenza inadeguata della biologia del cancro

Conoscenza indadeguata della biologia del cancro Conseguenze • Farmaci Aspecifici (citotossici) • Pazienti non selezionati (Non-small cell lung c. , Colo-rectal c. , Soft-tissue sarcoma, etc. ) • Grandi trials mirati su effetti moderati/scarsi • Poche possibilita’ di imparare dai risultati precoci

Ultimi 2 decenni Progressi Drammatici delle conoscenze in • Genetica • Biologia Molecolare • Biologia del Cancro (Pathways, Angiogenesi, etc) • Immunologia • Tecniche ed ingegneria molecolare • Farmacologia

Ultimi 2 decenni • Nuovi Pazienti – Sottogruppi Prognostici – Terapie targeted/pazienti con il target – “Responders” – Rarita’

Ultimi 2 decenni • Nuovi Effetti – MTD? – Dose-Risposta? – Tipo di Attivita’? – Risposta? – Associazioni tra farmaci? – Dimensione/Tipo beneficio (median OS? )

Ultimi 5 anni Biologia Molecolare, Genetica, Immunologia, Bionformatica Nuovi farmaci IM M N U R E T O ESottogruppi I P A Molecolari Medicina ‘Personalizzata, «Precision Medicine» Cambiamenti radicali nel modo in cui sono disegnati e analizzati i trials

Nuove metodologie 1. Studi Randomizzati o trials non-controllati? 2. Endpoint Surrogati? 3. Statistica Bayesiana? 4. Disegni adattativi?

Nuove metodologie 1. Studi Randomizzati o trials non-controllati?

GLEEVEC CML -> Large RCT GIST -> Large uncontrolled trial Other rare indications -> Case Series (dermatofibrosarcoma protuberans, plexiform neurofibromas, chordomas)

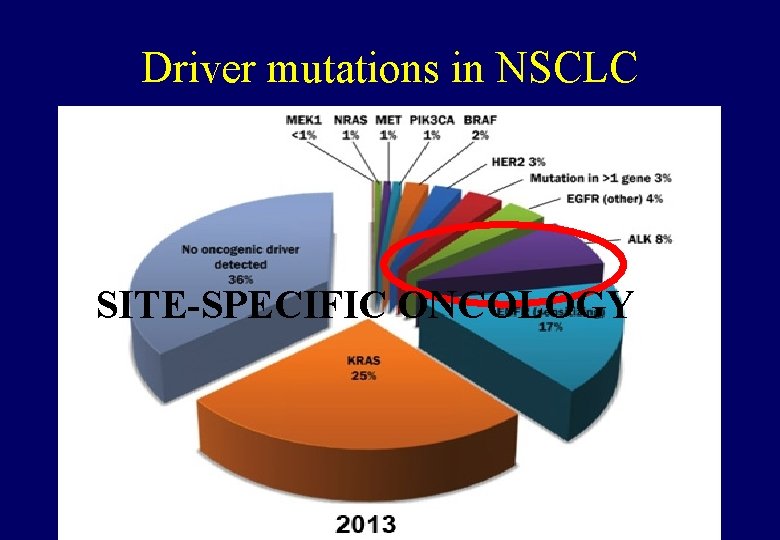
Driver mutations in NSCLC SITE-SPECIFIC ONCOLOGY

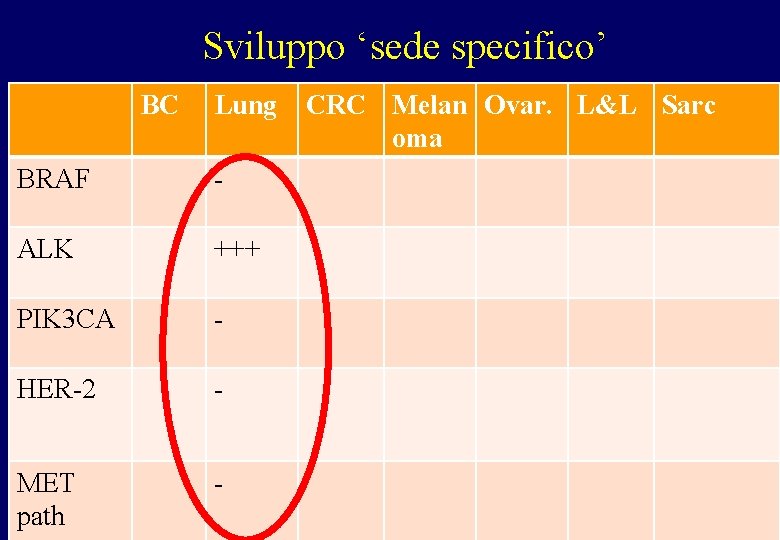
Sviluppo ‘sede specifico’ BC Lung BRAF - ALK +++ PIK 3 CA - HER-2 - MET path - CRC Melan Ovar. L&L Sarc oma

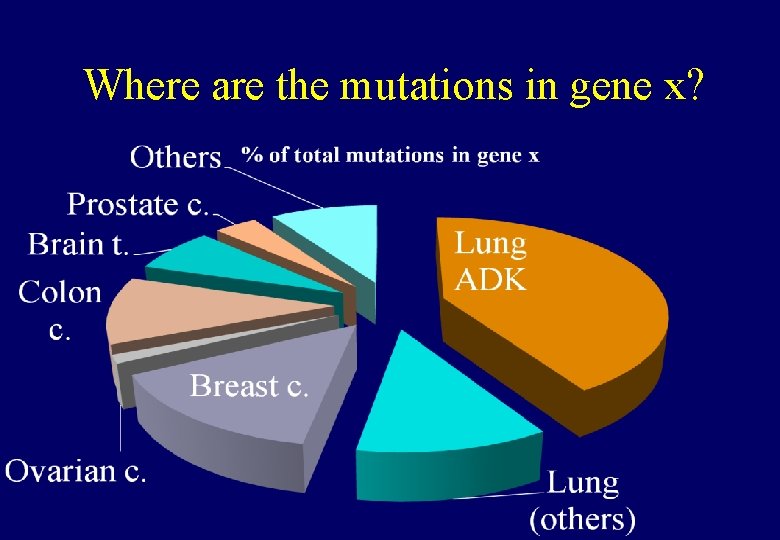
Where are the mutations in gene x?

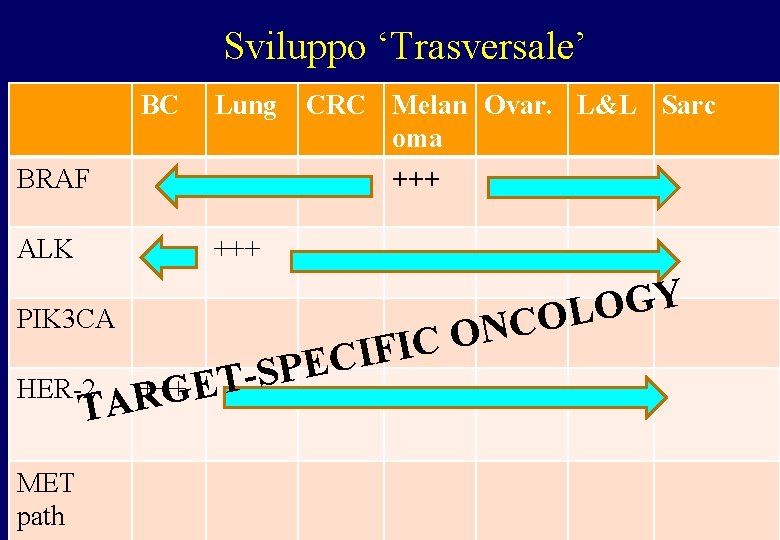
Sviluppo ‘Trasversale’ BC Lung BRAF ALK CRC Melan Ovar. L&L Sarc oma +++ PIK 3 CA C E P S T HER-2 R +++ E G A T N O IFIC MET path Y G O COL

New paths to drug use Large RCT in a frequent cancer with the target Proof of principle – Toxicity Uncontrolled (but formal) trial(s) in other (rare) cancers with the target Off label use in individual cases with the target

New paths to drug use Large RCT in a frequent cancer with the target Proof of principle – Toxicity Accept able? Method ology? Uncontrolled (but formal) trial(s) in other cancers with the target Off label use in individual cases with the target

Nuove metodologie 1. Studi Randomizzati o trials non-controllati? 2. Endpoint Surrogati? 3. Statistica Bayesiana? 4. Disegni adattativi?

Sviluppi Metodologici Bayesian Statistics Surrogate endpoints Adaptive trials

Metodologia Convenzionale Separazione Rigida delle fasi di sviluppo di un farmaco • Fase I -> MTD -> Incrementi di dose in gruppi successivi di pazienti • Fase II -> Attivita’ -> Trials non controllati • Fase III -> Efficacia -> RCT’s

Metodologia Convenzionale All’interno di ogni fase/trial • Un solo obiettivo primario • Un solo endpoint primario, prefissato • Criteri di selezione fissi • Un solo protocollo di trattamento • Dimensioni (sample size) prespecificate: (numero/tipo/tempo delle analisi) • Risultati tenuti segreti: Analisi ad interim

Metodologia Convenzionale • Per finalizzare il disegno degli studi di fase III di un nuovo farmaco sono necessarie informazioni su: – Tossicita’ a vari dosaggi/tempi – Endpoint appropriati di efficacia/surrogati – Attivita’ a vari dosaggi/tempi/Associazioni – Quali pazienti? (sottogruppi) – Tipo ed entita’ del beneficio (delta, sample size) • Quando si avvia il trial spesso le conoscenze sono inadeguate!

Trial Adattativi Metodologia Convenzionale All’interno di ogni fase/trial • Un solo obiettivo primario • Un solo endpoint primario, prefissato • Criteri di selezione fissi • Un solo protocollo di trattamento • Dimensioni (sample size) prespecificate: (numero/tipo/tempo delle analisi) • Risultati tenuti segreti: Analisi ad interim


Adaptive design FDA’s draft guidance for industry on adaptive design clinical trials (http: //www. fda. gov/downloads/Drugs/Guidance. C ompliance. Regulatory. Information/Guidances/U CM 201790. pdf).

NOTA BENE Adaptive trial ≠ Adaptive Licensing

FDA’s Guidance applies to A&WC studies • A&WC “Adequate and well-controlled effectiveness studies intended to provide substantial evidence of effectiveness required by law to support a conclusion that a drug is effective” = Pivotal trials: BOTH PHASE II & III • (Exploratory Studies)?

Adaptive design clinical trial FDA’s Definition: “… a study that includes a prospectively planned opportunity for modification of one or more specified aspects of the study design and hypotheses based on analysis of data (usually interim data) from subjects in the study”

Adaptive design clinical trial • Opportunita’ di cambiamenti • pianificate nel disegno dello studio • sulla base di analisi intermedie di dati raccolti nello studio

Perche’interessano i disegni adattativi? • • Endpoints Precoci - Endpoint Molecolari – Risposte Tossicita’ Sottogruppi Aspetti organizzativi Nel corso del trial, si possono ottenere informazioni (molto) utili per migliorarne vari aspetti

“Seamless Phase II-III Trials”

Approccio Convenzionale Phase I (20 -40 pazienti) A Analisi, Scelta della dose -> Disegno Phase II N Approvazione e Conduzione Phase II (20 -60 pz) l N Analisi, Scelta dei pazienti I -> Disegno Phase III ? Conduzione Phase III -> Analisi (sottogruppi? )

Seamless Phase II-III trials Phase IA (safety) Disegno Phase I-II-III, Adaptive Trial Selezione Dose Selezione Sottogruppi (Cambiamento Endpoint) Interim anal. Tossicita’-> Delta (endpoint Analisi Ripetute e Stopping rules surrogati? )

Seamless Phase II-III trials • Minimizzano il tempo tra fase III (Nessuna interruzione) • Flessibilita’ per studiare altri aspetti cruciali – dose finding – selezione di sottogruppi • I pazienti arruolati in entrambe le fasi sono utilizzati nell’analisi finale

Vantaggi (presunti) • Minor tempo: Un solo trial, non trials successivi • Minore burocrazia: Approvazione Unica • Maggiore flessibilita’: Dose, endpoint, pazienti, • Piu’ efficienza (dati fase II usati in analisi fase III)

I trial convenzionali hanno spesso una componente adattativa 1. Stopping rules basate su analisi intermedie 2. Modificazioni dei criteri di selezione 3. Modificazioni per conservare power studio BEN COMPRESE E ACCETTATE DALLA COMUNITA’ SCIENTIFICA

I trial convenzionali hanno spesso una componente adattativa 1. Stopping rules basate su analisi intermedie - Tossicita’ - Rifiuto dell’ipotesi nulla - Futility

I trial convenzionali hanno spesso una componente adattativa 1. Stopping rules basate su analisi intermedie 2. Modificazioni dei criteri di selezione - Difficolta’ di reclutamento Costi Informazioni da altri studi (es. Tox. in pz specifici) Necessita’ di mantenere la potenza dello studio

I trial convenzionali hanno spesso una componente adattativa 1. Stopping rules basate su analisi intermedie 2. Modificazioni dei criteri di selezione 3. Modificazioni per conservare power studio (es. x bassa Event rate) - Incremento dimensioni studio - Prolungamento durata studio - Cambio endpoint primario?

Less well-understood types of adaptations • Adaptations for Dose Selection Studies. • Adaptive Randomization Based on Relative Treatment Group Responses • Adaptation of Sample Size Based on Interim-Effect Size Estimates • Adaptation of Patient Population Based on Treatment-Effect Estimates • Adaptation for Endpoint Selection Based on Interim Estimate of Treatment Effect • Adaptation of Multiple-Study Design Features in a Single Study • Adaptations in Non-Inferiority Studies

“Concerns” associati con i disegni adattativi 1. Bias dovuto ai test multipli (Risultati falsi positivi) 2. Confusione tra generazione e test di ipotesi 3. Difficolta’ a interpretare i risultati quando si osserva un effetto del trattamento (Sovrastima dell’ effect size) 4. Operational Bias

Critical Factor - Blinded interim analyses - Unblinded interim analyses

Blinded interim analyses • Adaptations of eligibility criteria …. • Adaptations to maintain study power…. …… based on blinded interim analyses of aggregate data. No bias No need to be (but better if) planned in advance

• Adaptations based on unblinded analyses – for stopping early – for dose selection studies – of patient subgroups based on treatment-effect estimates – for end-point selection based on interim estimates of treatment effect Bias if not addressed in study design

Unplanned adaptations based on unblinded analyses • Undermine the statistical validity of the study • Compromise the possibility to interpret its results ALSO IN EXPLORATORY STUDIES

Perche’? Se utilizzo l’evidenza che mi ha portato a modificare il trial nell’analisi finale, confondo la generazione di ipotesi con il test di ipotesi ES. A meta’ studio analisi di 40 sottogruppi: in 1 trovo un effetto significativo del tr. sperimentale Non potrei utilizzare questo dato nell’analisi finale

Requirements of adaptative trials • Adaptations based on unblinded analyses - Planned in advance (study design-protocol-statistical plan-SOPs) - Statistical adjustments - Specialised statistical support

Tecniche statistiche di aggiustamento • Area di ricerca • Complesse • Scopo: Prevenire bias e utilizzare dati learning phase + Confirmatory Phase – Frequentiste: Focalizzate su significativita’ (closure principle, correction for multiplicity) – Bayesiane (maggiore attenzione a effect size)

Nota Bene! Lo studio adattativo è particolarmente indicato quando la numerosità dei pazienti è scarsa La «rarita’» sta diventando il problema dominante dell’oncologia! Non ha piu’ senso parlare di tumori «rari» perche’ la maggior parte delle situazioni cliniche stanno diventando rare

Due quesiti correlati • Nei tumori rari/sottogruppi, e’ necessario condurre studi analoghi a quelli dei tumori frequenti? • Quanta (e quale) evidenza e’ necessaria per introdurre un trattamento nella pratica clinica?

Trials Clinici & EBM nei tumori rari Nei tumori rari/sottogruppi, e’ necessario condurre studi analoghi a quelli dei tumori frequenti? (Per la maggior parte di questi sono reclutabili x studi in Italia <100 casi/anno)

Methodological recommendations for clinical studies in rare cancers ‘alternative ways to conceive study design, analysis of data and combination of results would be exceedingly important. It is possible that some innovative solutions may imply a price to pay in terms of a higher uncertainty. ’

Trials in rare cancers 1. Still randomized? 2. New statistical approaches? 3. Surrogate Endpoints? 4. Adaptive designs ?

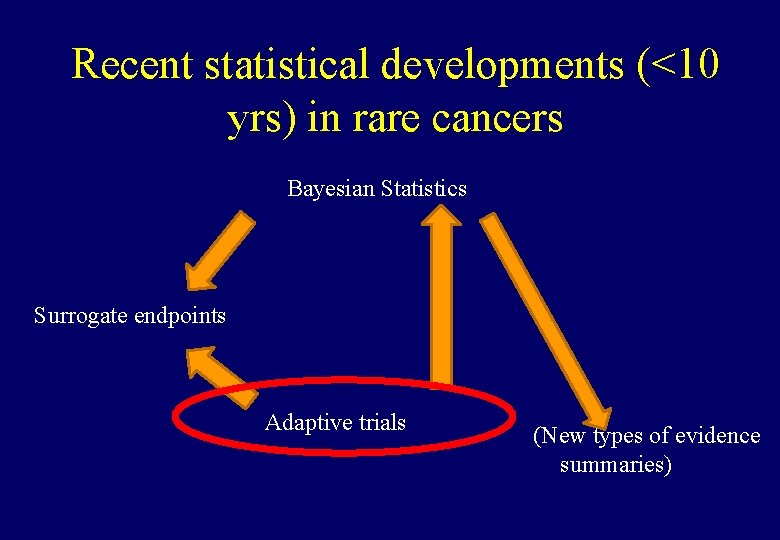
Recent statistical developments (<10 yrs) in rare cancers Bayesian Statistics Surrogate endpoints Adaptive trials (New types of evidence summaries)

Adaptive studies Bayesian Statistics 1. 2. 3. 4. To monitor study results for early stop To use validated surrogate endpoints To select subgroups To extrapolate results across cancers of different sites bearing the same target

New generation of efficacy trials in rare cancers – Uncontrolled efficacy (phase II-III) trials of high quality – Randomized activity (Phase II) trials followed by uncontrolled efficacy trials (with historical controls) – RCT’s with surrogate endpoints – Adaptive, Bayesian, activity/efficacy RCT’s

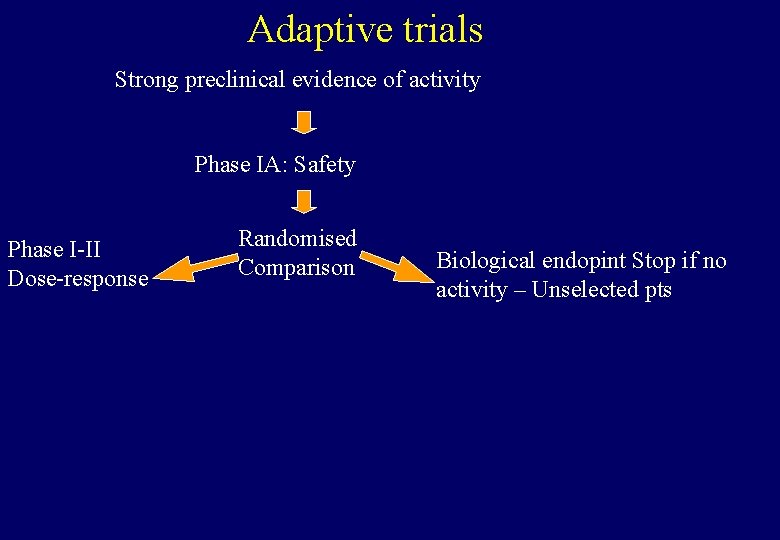
Adaptive trials Strong preclinical evidence of activity Phase IA: Safety – Different doses

Adaptive trials Strong preclinical evidence of activity Phase IA: Safety Phase I-II Dose-response Randomised Comparison Biological endopint Stop if no activity – Unselected pts

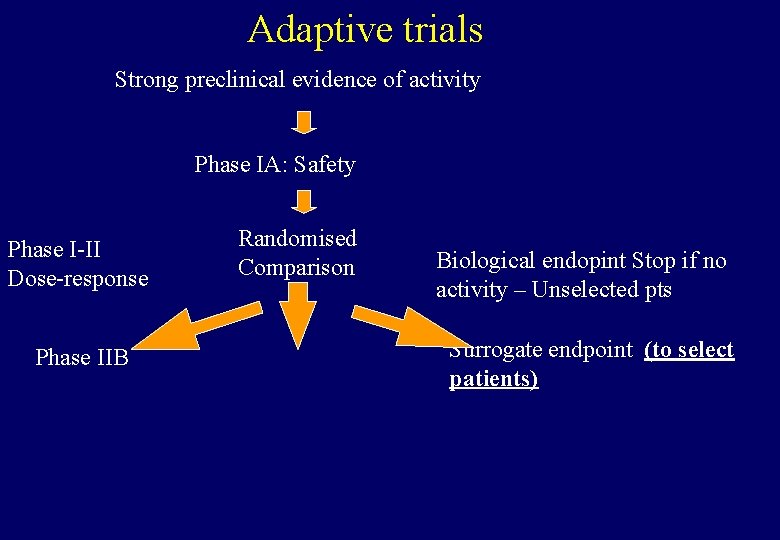
Adaptive trials Strong preclinical evidence of activity Phase IA: Safety Phase I-II Dose-response Phase IIB Randomised Comparison Biological endopint Stop if no activity – Unselected pts Surrogate endpoint (to select patients)

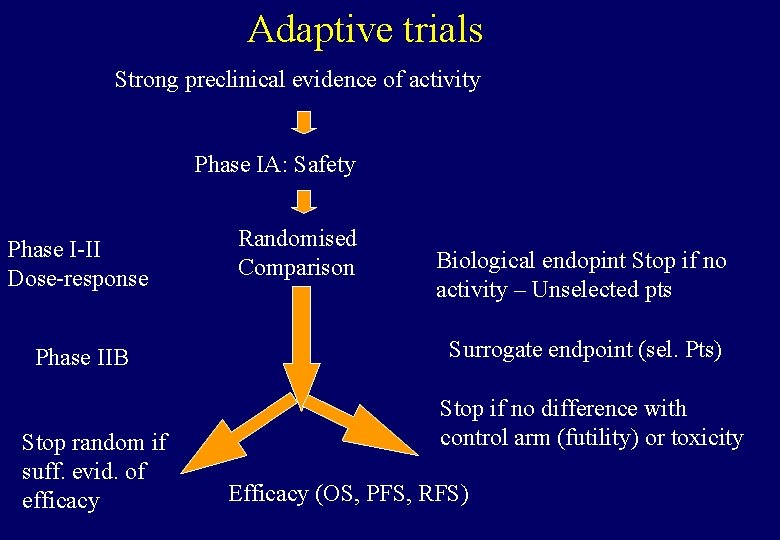
Adaptive trials Strong preclinical evidence of activity Phase IA: Safety Phase I-II Dose-response Phase IIB Stop random if suff. evid. of efficacy Randomised Comparison Biological endopint Stop if no activity – Unselected pts Surrogate endpoint (sel. Pts) Stop if no difference with control arm (futility) or toxicity Efficacy (OS, PFS, RFS)

Adaptive trials Strong preclinical evidence of activity Phase IA: Safety Phase I-II Dose-response Phase IIB Stop random if suff. evid. of efficacy Randomised Comparison Biological endopint Stop if no activity – Unselected pts Surrogate endpoint (sel. Pts) Stop if no difference with control arm (futility) or toxicity No predetermined number of patients

Attenzione La progettazione di nuovi trials con disegni innovativi richiede piu’ cura per. . – Disegno di studio – Piano Statistico – Preparazione del Protocollo – Organizazzione …rispetto ai trials convenzionali

Organizzazione • Documentazione, Comitati Etici, Convenzioni e Contratti • Numero di Centri? • Raccolta, trasporto e analisi materiale x analisi • Raccolta e analisi dati/Rapporti • DMC, SC: Riunioni e Decisioni • Comunicazioni

Studi adattativi Potenziale strumento di grande utilita’ Opportunita’ di rilanciare la ricerca metodologica e statistica Grave carenza di competenze in italia ARMA MOLTO PERICOLOSA

Statistical Significance = Presence of a benefit Statistically Significant Difference = Difference leading to the rejection of H 0 Not necessarily Clinically Relevant


Time to raise the bar in localised prostate cancer. Penson DF. BJU Int. 2013 Aug; 112(3): 278. Raise the bar even higher for primary prevention interventions. Wright JM, Arch Intern Med. 2012 Sep 24; 172(17): 1352 -3 RAISE THE BAR! Applaud the novel intrathecal baclofen trialing method: time to raise the bar! Ruan X, Pain Physician. 2012 Mar-Apr; 15(2): . Time to raise the bar. Cosh J. Nurs Stand. 2012 Jan 11 -17; 26 E gli studi adattativi? Time has come to raise the bar in oncology clinical trials. Dilts DM. JCO 2014 American Society of Clinical Oncology perspective: Raising the bar for clinical trials by defining clinically meaningful outcomes. Ellis LM, JCO 2014

Scopo dei trial adattativi? Ottimizzare il processo di DIMOSTRAZIONE della presenza di un beneficio (qualsiasi)? A discapito della precisione delle VALUTAZIONI di efficacia? - Analisi intermedie (sovrastima efficacia) - Enfasi sul controllo dell’errore di I tipo (P) - Efficacia stimata su casistiche piu’ piccole (sottogruppi) a v i t t e p s ? o e r l P a i r t s u d in

Conclusioni • Gli studi adattativi devono diventare uno strumento al servizio della comunita’ dei pazienti = migliore stima dell’efficacia – Modalita’ di impiego – Personalizzazione delle terapie – Riduzione dei tempi di sviluppo • A questo scopo e’ necessario che Agenzie Regolatorie e Sistemi Sanitari riprendano il governo della ricerca clinica