REAZIONI DI SOSTITUZIONE Uno dei meccanismi di reazione







- Slides: 13

REAZIONI DI SOSTITUZIONE Uno dei meccanismi di reazione più importante è quello di addizione: A–B + C A–B–C Esistono anche altre possibilità che hanno due reattivi A e B di reagire tra loro con un meccanismo diverso. Può verificarsi, ad es. , che A reagisca con C sostituendo B, ossia: A–B + C A–C + B Abbiamo avuto la rottura del legame A – B e la formazione del legame A – C. Chi mette a disposizione gli elettroni per il nuovo legame? Ci sono due possibilità: v Lo stesso C porta con sé elettroni per legarsi ad A al posto di B. Se ciò avviene significa che C ha elettroni disponibili, quindi è un nucleofilo, per cui le reazioni sono dette “Sostituzioni nucleofile” v C non ha elettroni disponibili, e dunque è di tipo elettrofilo, per cui le reazioni sono dette “Sostituzioni elettrofile” C è detto “gruppo entrante” B è detto “gruppo uscente” 1

Naturalmente C per entrare deve essere un nucleofilo migliore di B, la carica in tal caso non scompare: A–B + C A – C + BSe C e B sono paragonabili (come nucleofilicità) si ha l’equilibrio: A–B + C- A–C + B - Se C è un elettrofilo si legherà ad A utilizzando gli elettroni del legame A – B , per cui B viene fuori senza elettroni: A–B + C A–C + B Anche in questo caso, se C e B sono paragonabili (come elettrofilicità) si ha l’equilibrio: A–B + C A–C + B 2

REAZIONI DI SOSTITUZIONI NUCLEOFILE ALIFATICHE Consideriamo un composto del C generico, R – X, in cui R è un raggruppamento di atomi di C ed X un atomo più elettronegativo del C: R = CH 3 – CH 2 e X = Cl Come sappiamo, se X è più elettronegativo del C, il legame C – X è spostato verso X (cioè è polarizzato), e dà origine ad un dipolo: + R X - L’entità della polarizzazione è tanto più grande quanto maggiore è la differenza di elettronegatività tra i due atomi. Supponiamo di introdurre nel sistema un nucleofilo: + R X - + Y- R–Y + X- Un nucleofilo entra ed un nucleofilo esce. 3

Vediamo qual è il possibile meccanismo di reazione. Vi possono essere due casi: 1) Si rompe il legame R – X e si forma il legame R – Y (2 stadi di reazione) 2) Man mano che si rompe il legame R – X si forma il legame R – Y (reazioni concertate o contemporanee) Caso 1) Essendo X più elettronegativo di R, richiamerà a sé gli elettroni: 1° stadio: R–X 2° stadio: R Y- + R + X R–Y Questa reazione viene indicata con il simbolo SN 1 , cioè sostituzione nucleofila mononucleare. Tutto il processo si svolgerà con una certa velocità, che però non è la stessa per entrambi gli stadi. Sappiamo che data V 1 la velocità del 1° stadio e V 2 la velocità del 2° stadio, la V totale sarà data da quella più lenta. 4

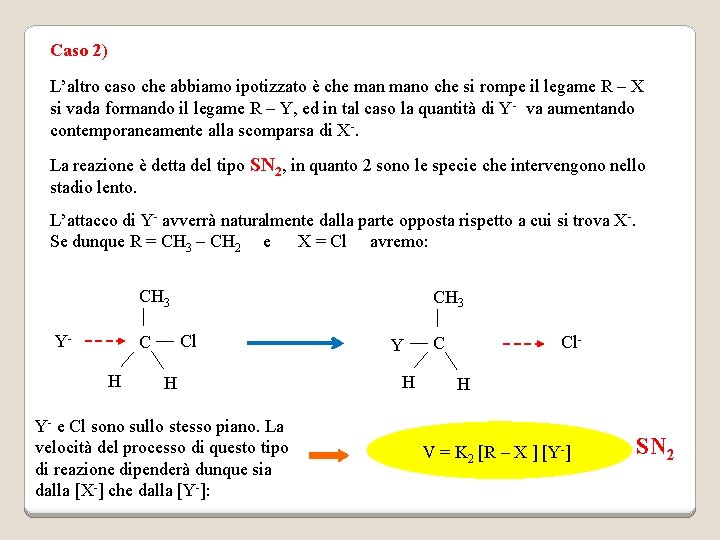
Caso 2) L’altro caso che abbiamo ipotizzato è che mano che si rompe il legame R – X si vada formando il legame R – Y, ed in tal caso la quantità di Y- va aumentando contemporaneamente alla scomparsa di X-. La reazione è detta del tipo SN 2, in quanto 2 sono le specie che intervengono nello stadio lento. L’attacco di Y- avverrà naturalmente dalla parte opposta rispetto a cui si trova X-. Se dunque R = CH 3 – CH 2 e X = Cl avremo: CH 3 Y- Cl C H CH 3 H Y- e Cl sono sullo stesso piano. La velocità del processo di questo tipo di reazione dipenderà dunque sia dalla [X-] che dalla [Y-]: Y H Cl- C H V = K 2 [R – X ] [Y-] SN 2

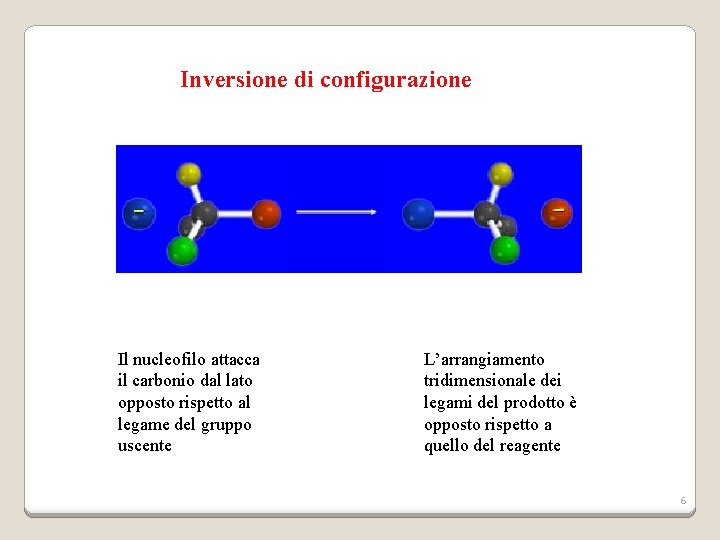
Inversione di configurazione Il nucleofilo attacca il carbonio dal lato opposto rispetto al legame del gruppo uscente L’arrangiamento tridimensionale dei legami del prodotto è opposto rispetto a quello del reagente 6

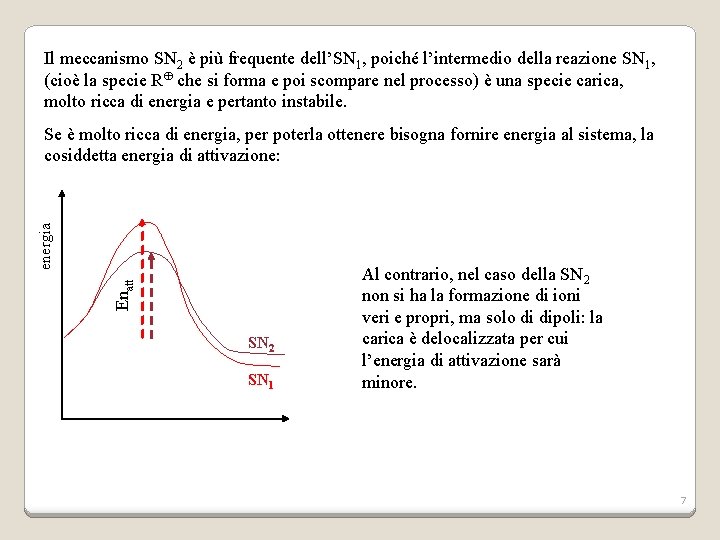
Il meccanismo SN 2 è più frequente dell’SN 1, poiché l’intermedio della reazione SN 1, (cioè la specie R che si forma e poi scompare nel processo) è una specie carica, molto ricca di energia e pertanto instabile. Enatt energia Se è molto ricca di energia, per poterla ottenere bisogna fornire energia al sistema, la cosiddetta energia di attivazione: SN 2 SN 1 Al contrario, nel caso della SN 2 non si ha la formazione di ioni veri e propri, ma solo di dipoli: la carica è delocalizzata per cui l’energia di attivazione sarà minore. 7

ALOGENURI ALCHILICI In generale gli alogenuri alchilici si classificano come: Cl alogenuri primari: CH 3 – CH 2 Cl alogenuri secondari: CH 3 – CH 3 alogenuri terziari: CH 3 – CH – Cl CH 3 8

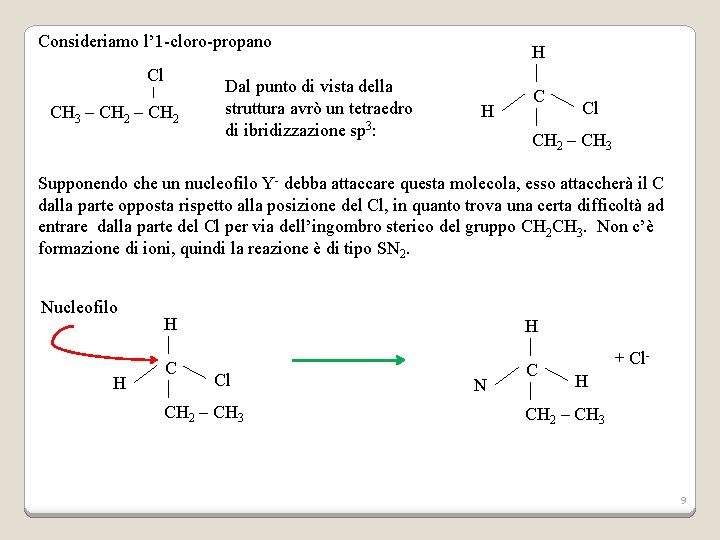
Consideriamo l’ 1 -cloro-propano Cl CH 3 – CH 2 Dal punto di vista della struttura avrò un tetraedro di ibridizzazione sp 3: H H C Cl CH 2 – CH 3 Supponendo che un nucleofilo Y- debba attaccare questa molecola, esso attaccherà il C dalla parte opposta rispetto alla posizione del Cl, in quanto trova una certa difficoltà ad entrare dalla parte del Cl per via dell’ingombro sterico del gruppo CH 2 CH 3. Non c’è formazione di ioni, quindi la reazione è di tipo SN 2. Nucleofilo H H Cl CH 2 – CH 3 N C + Cl. H CH 2 – CH 3 9

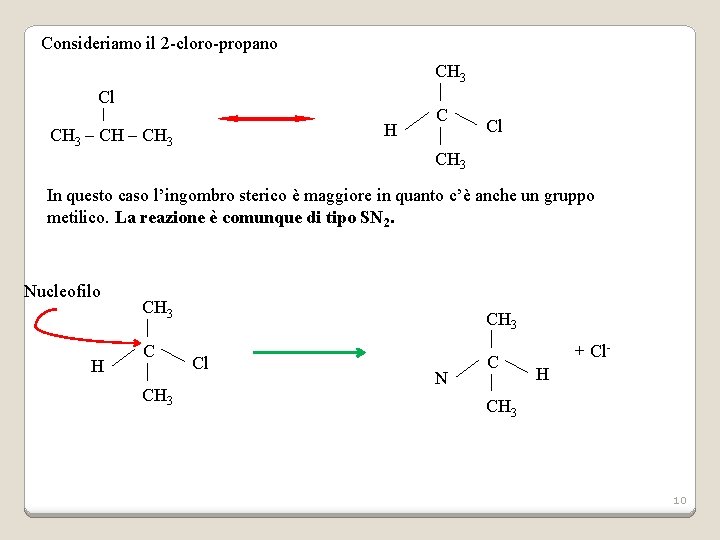
Consideriamo il 2 -cloro-propano CH 3 Cl H CH 3 – CH 3 C Cl CH 3 In questo caso l’ingombro sterico è maggiore in quanto c’è anche un gruppo metilico. La reazione è comunque di tipo SN 2. Nucleofilo H CH 3 Cl N C + Cl. H CH 3 10

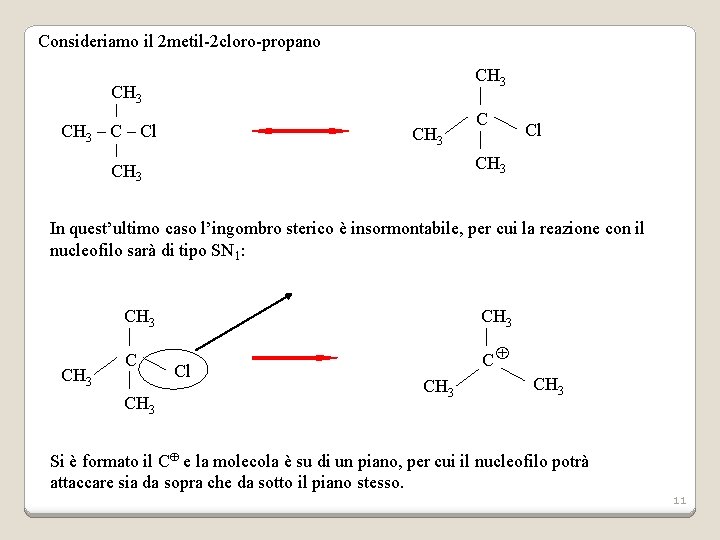
Consideriamo il 2 metil-2 cloro-propano CH 3 – Cl CH 3 C Cl CH 3 In quest’ultimo caso l’ingombro sterico è insormontabile, per cui la reazione con il nucleofilo sarà di tipo SN 1: CH 3 C C CH 3 Cl CH 3 Si è formato il C e la molecola è su di un piano, per cui il nucleofilo potrà attaccare sia da sopra che da sotto il piano stesso. 11

Conclusioni generali: v Le reazioni SN 2 si hanno con tutti gli alogenuri Iari ed anche con i IIari se non c’è un forte ingombro sterico v Le reazioni SN 1 si hanno con gli alogenuri IIIari Importante: Al di là della posizione dell’alogeno (primario, secondario o terziario) è fondamentale valutare l’ingombro sterico dei sostituenti vicini al C cui è legato l’alogeno: se il gruppo presente è molto ingombrante, anche su un alogenuro primario si potrà avere una reazione SN 1 e non la prevedibile SN 2. La velocità di reazione è influenzata dalla natura dell’alogeno, in quanto dipende dall’energia di legame tra il C e l’alogeno stesso: F >> Cl > Br > I Lo ione ioduro reagirà molto più velocemente dei bromuri, e questi dei cloruri, etc. , proprio perché più forte è il legame con il C meno veloce sarà la reazione (è indirettamente correlata all’elettronegatività). 12

RIEPILOGANDO: 1. Le reazioni nucleofile sono reazioni che si verificano in 2 modi diversi a seconda dell’ingombro sterico 2. Le sostituzioni nucleofile sono tanto più difficili quanto più forte è il legame da rompere 3. Le sostituzioni nucleofile si verificano quando il gruppo entrante è un miglior nucleofilo del gruppo uscente 4. Le sostituzioni nucleofile SN 2 sono più favorite rispetto alle SN 1 e si verificano se non c’è un forte ingombro sterico 13