Reaktsioonivrrandeid sademe tekkimine metall sool metallhape Sademe teke






- Slides: 12

Reaktsioonivõrrandeid (sademe tekkimine; metall + sool; metall+hape

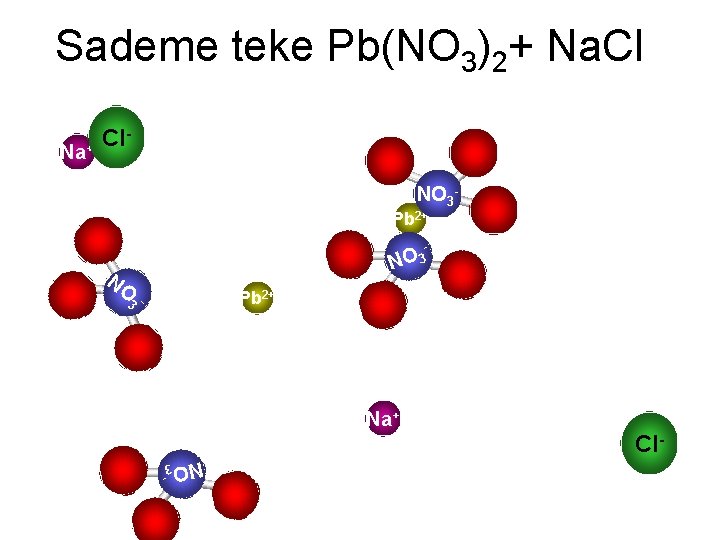
Sademe teke Pb(NO 3)2+ Na. Cl NO 3 - Pb 2+ NO 3 NO Pb 2+ 3 - Na+ Cl. NO 3 - Na+ Cl-

Eelnev reaktsioon võrrandina (tuleb vaadata et oleksid lähteained ja saadused lahustuvustabelist!) Pb(NO 3)2 + 2 Na. Cl→ Pb. Cl 2↓ + 2 Na. NO 3 Pb. Cl 2 läks sademesse, ei olnud enam lahuses vabu ioone!

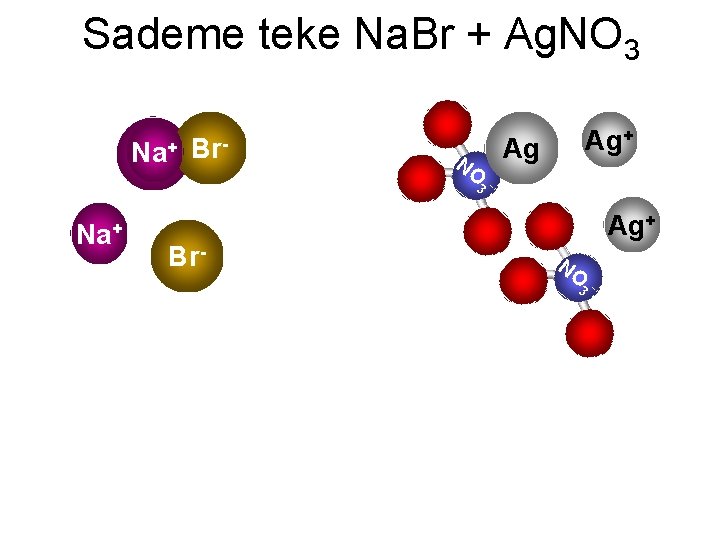
Sademe teke Na. Br + Ag. NO 3 Na+ Na Br- NO Ag+ Ag 3 - Na+ Ag+ Br- NO 3 -

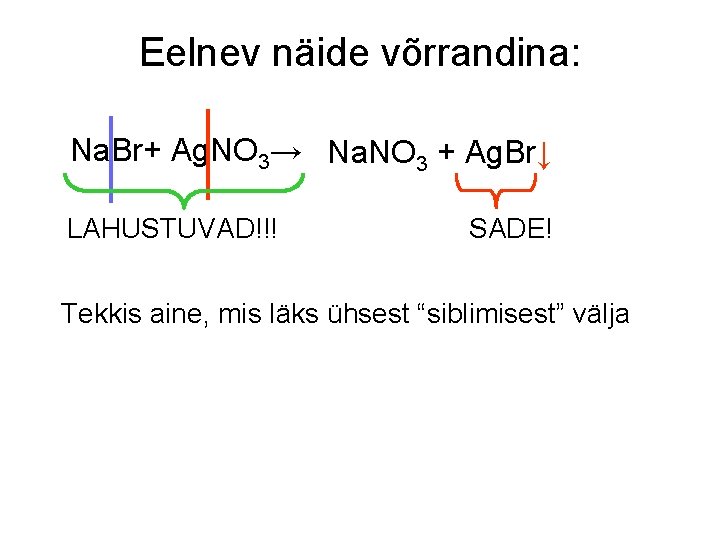
Eelnev näide võrrandina: Na. Br+ Ag. NO 3→ Na. NO 3 + Ag. Br↓ LAHUSTUVAD!!! SADE! Tekkis aine, mis läks ühsest “siblimisest” välja

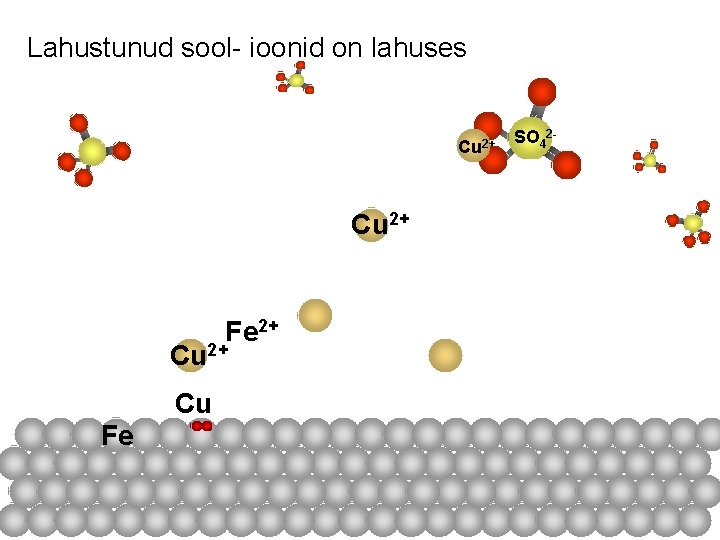
Lahustunud sool- ioonid on lahuses Cu 2+ Fe 2+ Cu Fe SO 42 -

Eelnev reaktsioon võrrandina Fe + Cu. SO 4→ Fe. SO 4 + Cu Raud reageerib vasksulfaadiga. Rauale tekib vase kiht.

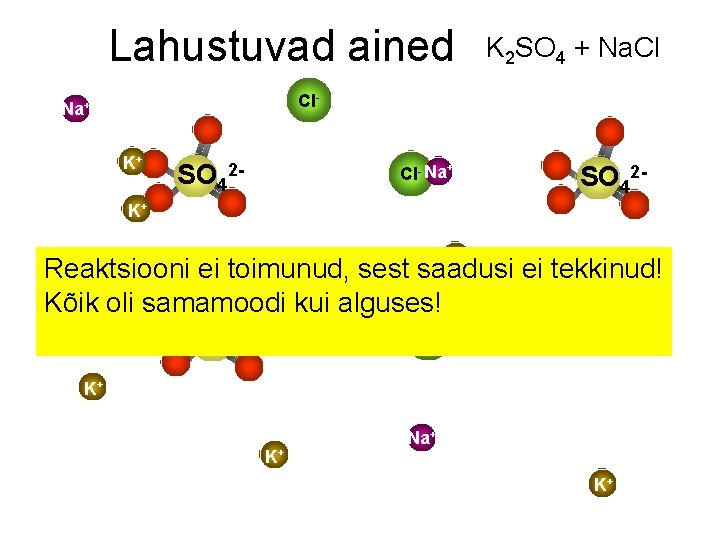
Lahustuvad ained K 2 SO 4 + Na. Cl Cl- Na+ K+ SO 42 - Cl- Na+ SO 42 - K+ K+ Reaktsiooni ei toimunud, sest saadusi ei tekkinud! Kõik oli samamoodi kui alguses! Cl. SO 42 K+ K+ Na+ K+

Eelmise võrrandi näitel, otsusta, kas reaktsioon toimub • Na. Cl + Ba. S→ Ei toimu – ei teki saadusi • Fe. S + Li. Br→ Ei toimu – lähteained ei lahustu • Fe. Cl 2 + Na 2 SO 3→ Fe. SO 3 + 2 Na. Cl • 3 K 2 Si. O 3+ 2 Fe. Cl 3→ Fe. Si. O 3 + 6 KCl • Cu 3(PO 4)2 + Li 2 S→ Ei toimu – lähteained ei lahustu

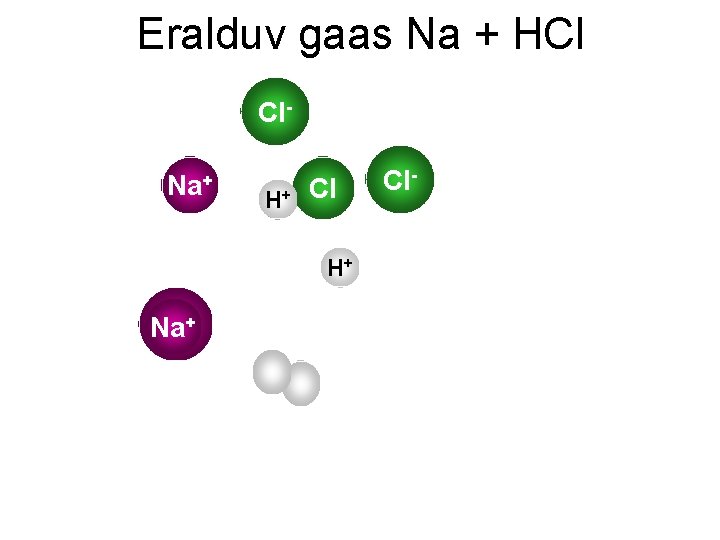
Eralduv gaas Na + HCl Cl. Na+ H H++ Cl H+ Na -Cl

Eelnev reaktsioon võrrandina-jälgi aktiivsusrida! Na +2 HCl→ 2 Na. Cl + H 2 Eraldus gaas (H 2) – ei säilinud võrrand esialgselt. Reageerivatest ainetest puudus vesinik. Eralduv gaas võib olla ka mõni hapetest: HCl, HF, H 2 CO 3 (laguneb H 2 O + CO 2), H 2 S NB! Hape, mis teisega reageerib, peab olema TUGEV! Tugevam tõrjub nõrgema välja! (H 2 SO 4 ja HNO 3 Toimel võib saada vesinikhalogeniide!)

Reaktsioonivõrrandid eelnevalt õpitu põhjal (ära unusta ka aktsiivsusrida!) • • Fe. S + H 2 SO 4→ Fe. SO 4 + H 2 S Cu. SO 4 + H 2 S→ Ei toimu – ei teki saadusi (lendavat gaasi) H 2 SO 4 + 2 K→ K 2 SO 4 + H 2 2 Na + H 2 CO 3→ Na 2 CO 3 + H 2 CO 3 + Cu→ Ei toimu – Cu on liiga nõrk (vaata pingerida!) Fe. CO 3 + H 2 SO 4→ Fe. SO 4 + H 2 O + CO 2 Ag + HNO 3→ Ei toimu – Ag on liiga nõrk (vaata pingerida!)