REAKSI KIMIA Reaksi kimia adalah suatu proses perubahan

REAKSI KIMIA Reaksi kimia adalah suatu proses perubahan materi yang menghasilkan suatu zat baru yang berbeda sifat dengan awal/sebelumnya. Dalam penulisan reaksi kimia, zat-zat disebelah kiri tanda panah merupakan zat yang akan bereaksi atau pereaksi (reactan), tanda panah menunjukkan bereaksi dan zat-zat di sebelah kanan reaksi adalah hasil reaksi (production) Berbagai jenis reaksi kimia, diantaranya a. Reaksi Pembentukan 3 Ca. O + 6 H 2 O + N 2 P 2 O 5 6 CO 2 + 3 H 2 Ca 3(PO 4)2 C 6 H 1206 + 6 O 2 2 NH 3 b. Reaksi Peruraian Ca. CO 3 Ca. O + Ca. Mg(C 03)2 Ca. CO 3 + CO 2 Mg. CO 3

c. Reaksi ion : peruraian suatu zat menjadi ion-ion penyusunnya Na. Cl Na+ + Cl- Fe(OH)3 Fe 3+ + 3 OH- Na 2 SO 4 2 Na+ + SO 42 - d. Reaksi asam-basa Reaksi asam adalah reaksi kimia yang menghasilkan ion hidrogen (H+). HCl H 2 SO 4 H+ 2 H+ + Cl+ SO 42 - Reaksi basa adalah reaksi yang menghasilkan ion hidroksil (OH -). NH 4 OH NH 4+ + OH- KOH K+ + OH-

e. Reaksi oksidasi dan reduksi Reaksi oksidasi adalah reaksi kimia yang melepaskan elektron dan menghasilkan ion bermuatan positif. Ca Ca 2+ + 2 elektron (e) Al Al 3+ + 3 e Reaksi reduksi adalah reaksi kimia yang menerima atau menangkap elektron dan menghasilkan ion bermuatan negatif. Cl + e Cl. S + 2 e S 2 f. Reaksi Eksoterm dan reaksi endoterm Reaksi eksoterm adalah reaksi yang menghasilkan kalor Reaksi endoterm adalah reaksi yang menyerap kalor

Persamaan reaksi kimia Menghubungkan pereaksi (zat-zat yang bereaksi) dengan hasil reaksi dalam bentuk suatu persamaan. Tandah panah ( ) sebagai penghubung (proses). A + B (A dan B peraksi ) C + D ( C dan D hasil reaksi) Persamaan reaksi harus ditulis dengan benar dengan menggunakan rumus molekul dan harus disetarakan.

Penyetaraan reaksi kimia Reaksi dikatakan setara apabila jumlah atom-atom yang terlibat sebagai pereaksi sudah sama dengan jumlah atom-atom dalam hasil reaksi atau jumlah atom-atom dikiri tanda panah sama dengan jumlah atom-atom di kanan tanda panah. Cara-cara penyetaraan reaksi kimia A. Cara Langsung B. Cara Pingpong C. Cara Aljabar D. Cara redoks

Cara Langsung • Carilah unsur yang hanya terdapat dalam satu zat sebelum maupun sesudah reaksi (satu dalam pereaksi dan satu dalam hasil) • Carilah dari antara unsur-unsur tersebut yang mempunyai indeks terbesar, berilah koefisien awal • Hindarilah pecahan; kalau perlu jangan mulai dengan koefisien 1, tetapi 2 atau lebih. Setarakan reaksi berikut : 1. 2 H 2 + 02 2 H 2 O 2. 3 H 2 + N 2 2 NH 3 3. 3 CO 2 + Al 2 O 3 4. 2 KCl. O 3 5. C 3 H 8 Al 2(CO 3)3 3 O 2 + 5 O 2 + 3 CO 2 + 2 KCl 4 H 2 O Cara ini efektif digunakan untuk reaksi-reaksi yang sederhana

Cara Pingpong Contoh: Cara ini pada dasarnya sama dengan cara langsung, tetapi dapat diterapkan pada setiap reaksi, juga yang paling rumit. Untuk mempelajari cara ini mari kita ambil contoh paling sederhana berikut (a sampai dengan f merupakan koefisien yang dicari): a b c Si. O 2 + Ca. F 2 + H 2 SO 4 d e Ca. SO 4 + H 2 O f + Si. F 4 (1)Indeks terbesar terdapat pada Si. F 4 jadi kita mulai pemberian koefisien pada Si. F 4; misalnya f = 1. Langkah-langkah selanjutnya ialah: (2)a. menyamakan jumlah atom Si; maka a = f = 1 b. menyamakan jumlah atom F; maka b = 2 (2 b =4 f = 4) (3)Menyamakan jumlah atom Ca; maka d = b = 2
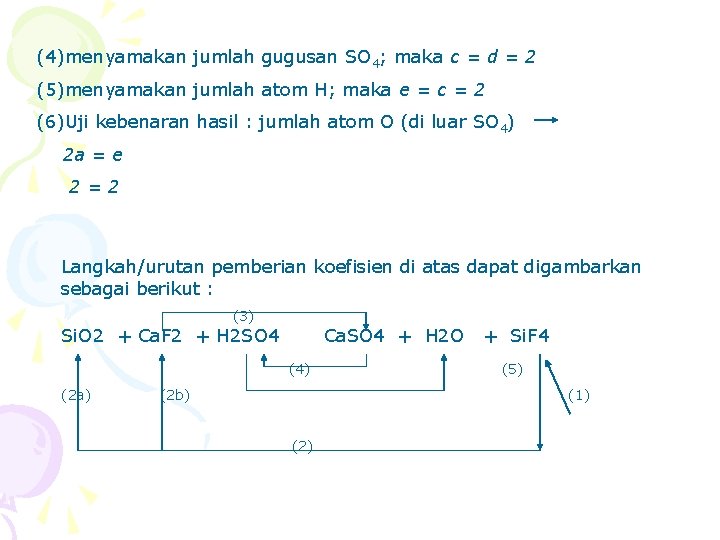
(4)menyamakan jumlah gugusan SO 4; maka c = d = 2 (5)menyamakan jumlah atom H; maka e = c = 2 (6)Uji kebenaran hasil : jumlah atom O (di luar SO 4) 2 a = e 2=2 Langkah/urutan pemberian koefisien di atas dapat digambarkan sebagai berikut : (3) Si. O 2 + Ca. F 2 + H 2 SO 4 Ca. SO 4 + H 2 O (4) (2 a) (2 b) + Si. F 4 (5) (1) (2)
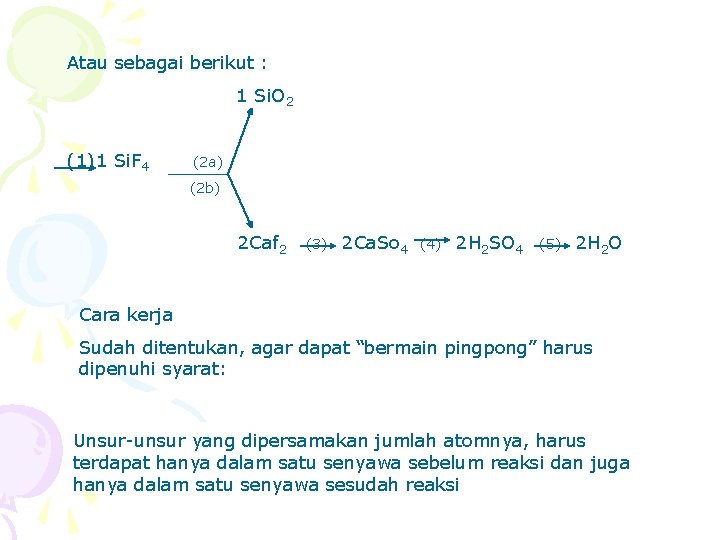
Atau sebagai berikut : 1 Si. O 2 (1)1 Si. F 4 (2 a) (2 b) 2 Caf 2 (3) 2 Ca. So 4 (4) 2 H 2 SO 4 (5) 2 H 2 O Cara kerja Sudah ditentukan, agar dapat “bermain pingpong” harus dipenuhi syarat: Unsur-unsur yang dipersamakan jumlah atomnya, harus terdapat hanya dalam satu senyawa sebelum reaksi dan juga hanya dalam satu senyawa sesudah reaksi

Penerapan secara sistematis cara pingpong ialah: a. Mencari unsur-unsur yang memenuhi syarat di atas. Tandailah unsur-unsur tersebut, mislnya dengan garis di bawahnya, seperti contoh ini: a b c Al 2(SO 4)3 + Na 2 CO 3 + H 2 O 1 d Al(OH)3 2 e f + Na 2 SO 4 + CO 2 3 dalam contoh ini hanya O yang tidak memenuhi syarat (mengapa? ) b. Memberi nilai koefisien kepada senyawa yang bertanda paling banyak dan berindeks paling besar. Di sini Al 2(SO 4)3 dan diberi koefisien 1 (a=1). Tulislah sementara nilai 1 tersebut di bawah senyawa, juga kemudian nilai koefisien yang lain di bawah zat yang bersangkutan

c. Dengan memperhatikan garis/tanda pada Al 2(SO 4)3, carilah senyawa atau senyawa-senyawa yang berisi unsur/unsur-unsur yang sama disisi lain tanda panah, dan berilah koefisien yang benar. Disini senyawa-senyawa tersebut ialah Al(OH)3 (mendapat koefisien 2) dan Na 2 SO 4 (mendapat koefisien 3). Dengan begitu, baik jumlah atom Al maupun gugus SO 4 menjadi sama sebelum dan sesudah reaksi. selanjutnya dari tanda/garis di bawah H, H 2 O dapat diberi koefisien 3 dan di tanda di bawah Na, Na 2 CO 3 dapat diberi koefisien 3 pula. Akhirnya berdasar C, CO 2 memperoleh koefisien 3 dan lengkaplah sudah koefisien reaksi ini : Al 2(SO 4)3 + 3 Na 2 CO 3 + 3 H 2 O 2 Al(OH)3 + 3 Na 2 SO 4 + 3 CO 2 d. Uji kebenaran koefisien: cocokkanlah jumlah atom O (sebab belum dipersamakan). Gugus SO 4 tidak dihitung O nya dan tampak jumlah atom O dengan begitu : 3 x 3+3=2 x 3+3 x 2 12 = 12
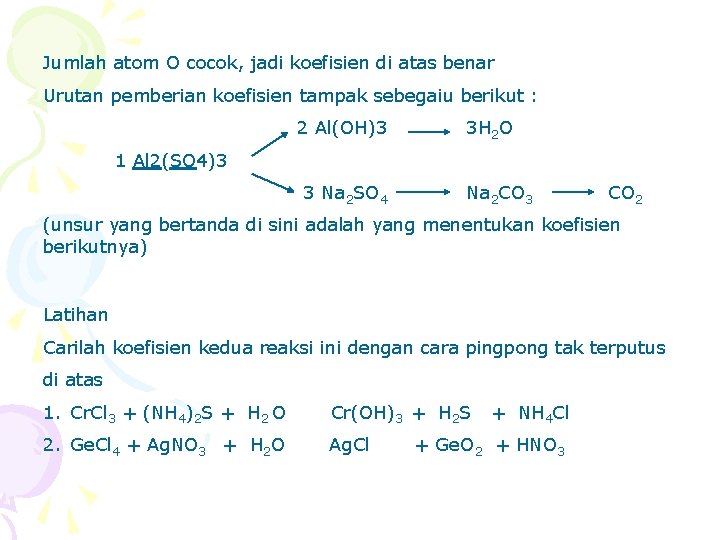
Jumlah atom O cocok, jadi koefisien di atas benar Urutan pemberian koefisien tampak sebegaiu berikut : 2 Al(OH)3 3 H 2 O 1 Al 2(SO 4)3 3 Na 2 SO 4 Na 2 CO 3 CO 2 (unsur yang bertanda di sini adalah yang menentukan koefisien berikutnya) Latihan Carilah koefisien kedua reaksi ini dengan cara pingpong tak terputus di atas 1. Cr. Cl 3 + (NH 4)2 S + H 2 O Cr(OH)3 + H 2 S 2. Ge. Cl 4 + Ag. NO 3 + H 2 O Ag. Cl + NH 4 Cl + Ge. O 2 + HNO 3



- Slides: 15