REACTIVIDAD EN QUIMICA ORGANICA OBJETIVO Conocer la Reactividad

REACTIVIDAD EN QUIMICA ORGANICA

OBJETIVO • Conocer la Reactividad de Moléculas, asociando conceptos que expliquen ese comportamiento.
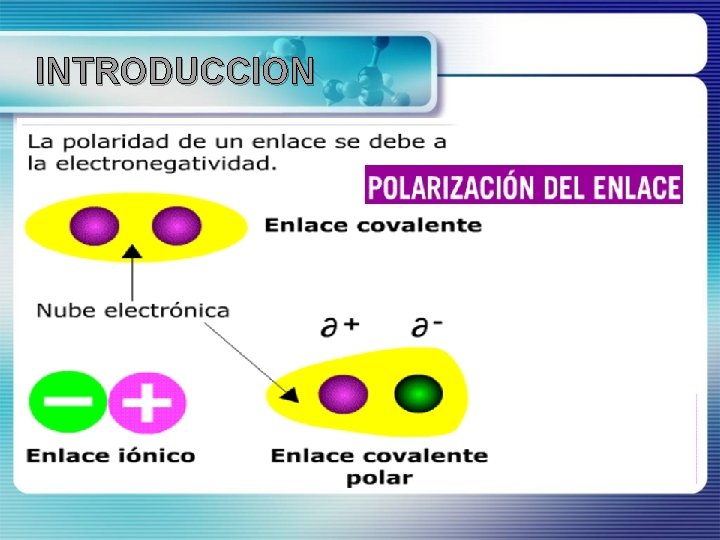
INTRODUCCION

Para entender como ocurren estas • El conocimiento acerca de la reactividad reacciones es necesario tener claro dos de distintas sustancias orgánicas es cosas: importante, ya que se relacionan con n RUPTURA DE ENLACES. procesos bioquímicos, procesos n CLASES DE REACTIVOS. industriales, entre otros.

RUPTURA DE ENLACES A)RUPTURA HOMOLITICA (RADICALARIA) Las reacciones implican una redistribución de los electrones en las • Ocurre en presencia de radiación (de moléculas de los reactivos para UV formar mayor energía) nuevos enlaces. • La ruptura. Esta del enlace rupturacovalente puede seres de forma simétrica (un e- para c/u ) • Especies eléctricamente neutras ØHOMOLITICA. pero muy reactivas conocidas como RADICALES ØHETEROLITICA.
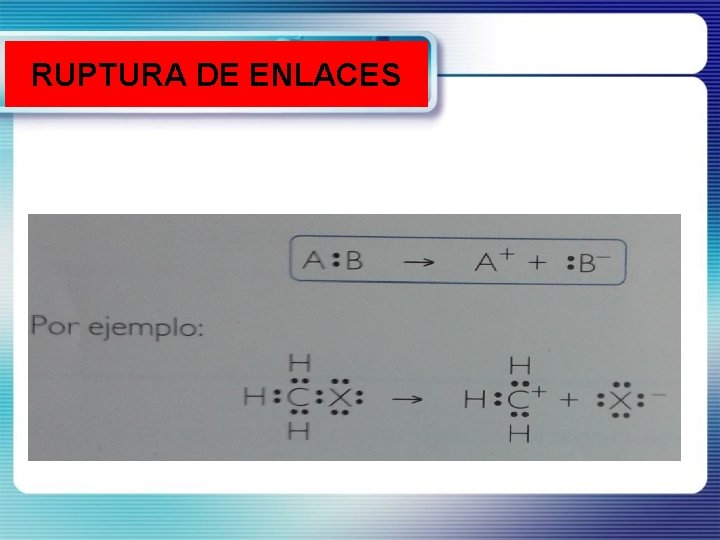
RUPTURA DE ENLACES

En este tipo de ruptura se produce un carbono con las siguientes propiedades: Carbanión R- (conserva e- ) Carbocatión R+ (deficiente de e-)

CLASES DE REACTIVOS En las reacciones orgánicas vamos a tener la intervención de sustancias conocida como: Sustratos. . . molécula reaccionante que es atacada. Reactivo. . es el que ataca al sustrato.
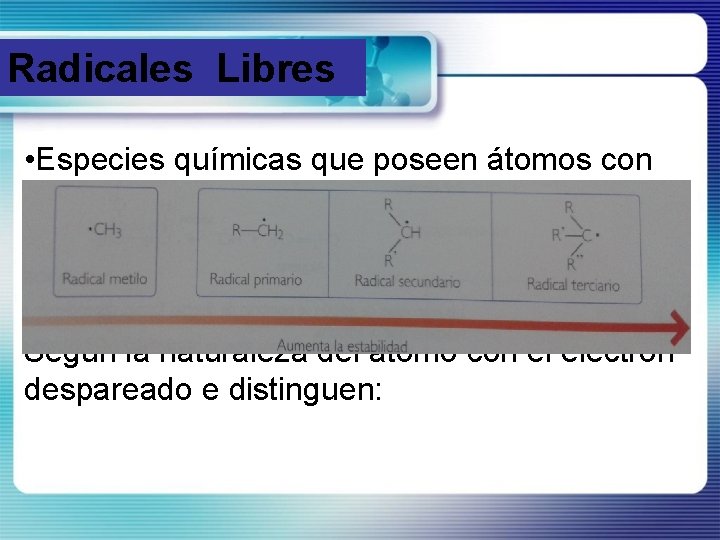
Radicales Libres • Especies químicas que poseen átomos con electrones desapareados. • Se forman por ruptura homolítica. • Altamente reactivos. Según la naturaleza del átomo con el electrón despareado e distinguen:

Reactivos Electrófilos • Atacan dobles o triples enlaces o átomos negativos. (zonas de alta densidad electrónica) • Pueden ser cationes o átomos con orbitales atómicos vacíos. • Tenemos el caso de: H+; NO 2+; carbocationes BF 3 ; Al. Cl 3 ; SO 3

Reactivos Nucleófilos • Actúan sobre átomos de sustratos con deficiencia electrónica o con carga positiva. • Poseen un átomo de gran densidad electrónica. • Suelen ser aniones, moléculas con pares de e(dadores de e -) Tenemos el caso de: (F-, Cl-, Br-); OH-; CN-; R-COOH 2 O; NH 3; R-OH
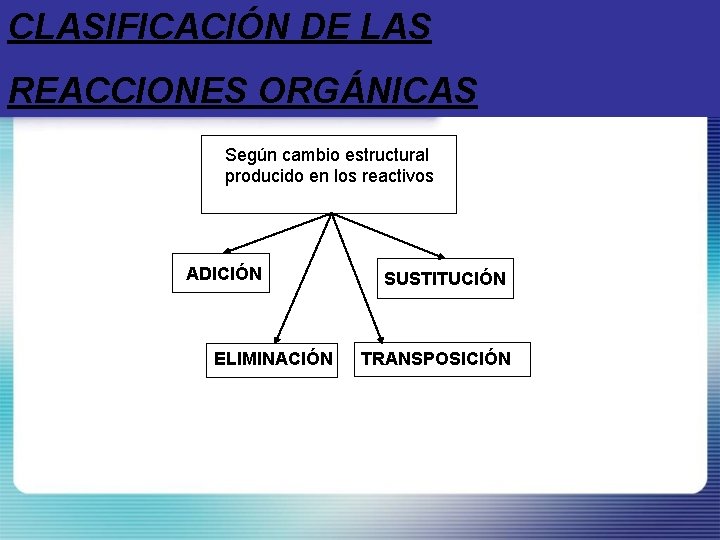
CLASIFICACIÓN DE LAS REACCIONES ORGÁNICAS Según cambio estructural producido en los reactivos ADICIÓN ELIMINACIÓN SUSTITUCIÓN TRANSPOSICIÓN
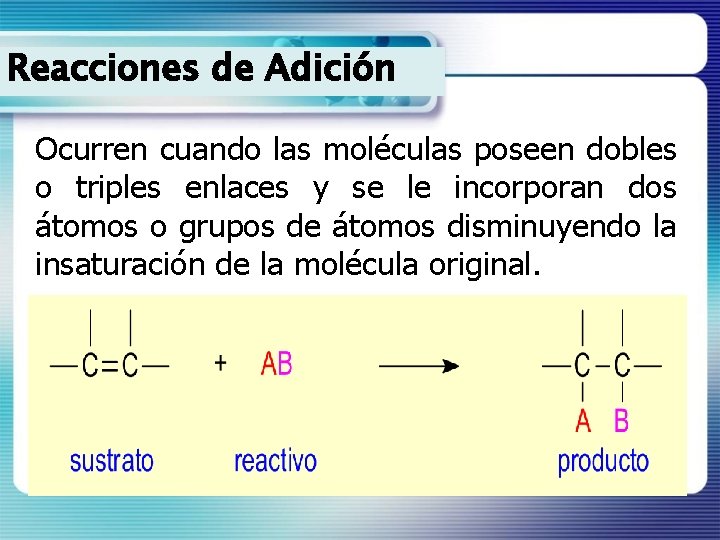
Reacciones de Adición Ocurren cuando las moléculas poseen dobles o triples enlaces y se le incorporan dos átomos o grupos de átomos disminuyendo la insaturación de la molécula original.

Reacciones de Adición Ejemplos:

Reacciones de Sustitución Son aquéllas en las que un átomo o grupo de átomos del sustrato son sustituidos por un átomo o grupo de átomos del reactivo.
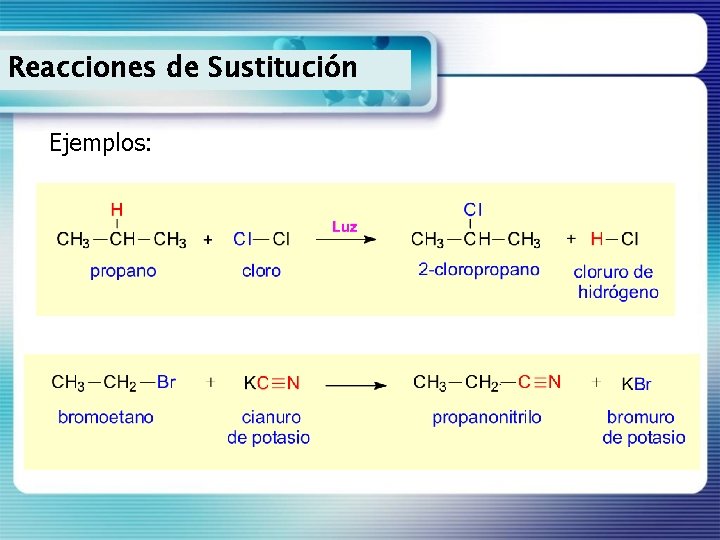
Reacciones de Sustitución Ejemplos:
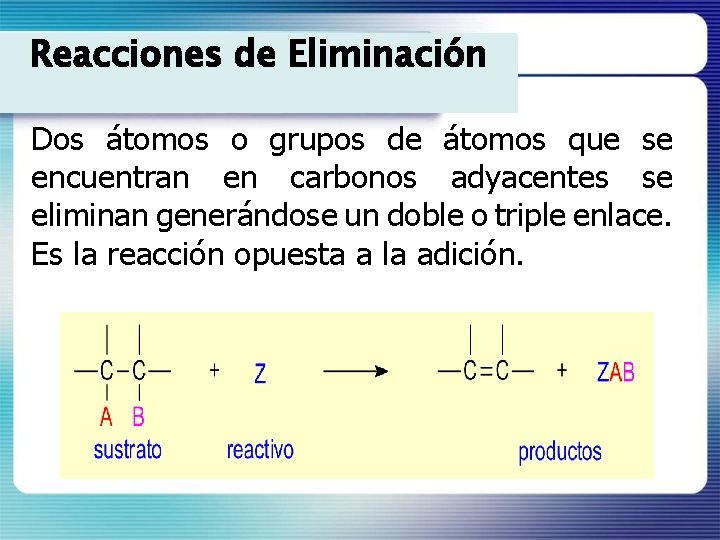
Reacciones de Eliminación Dos átomos o grupos de átomos que se encuentran en carbonos adyacentes se eliminan generándose un doble o triple enlace. Es la reacción opuesta a la adición.

Reacciones de Eliminación Ejemplos:
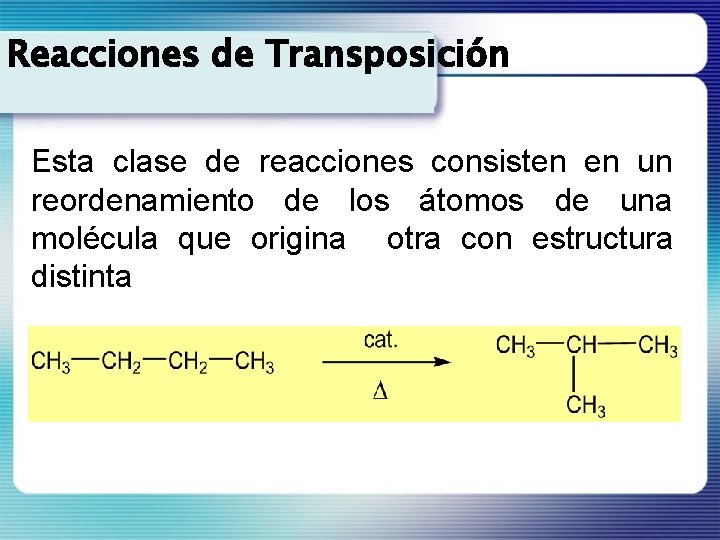
Reacciones de Transposición Esta clase de reacciones consisten en un reordenamiento de los átomos de una molécula que origina otra con estructura distinta
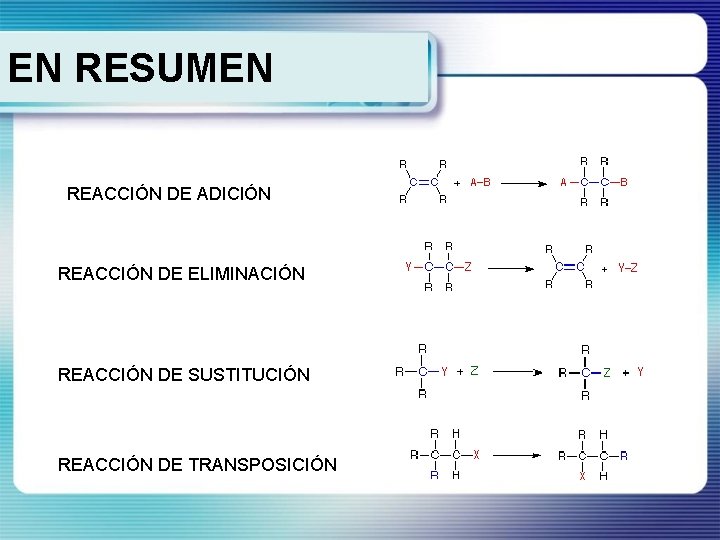
EN RESUMEN REACCIÓN DE ADICIÓN REACCIÓN DE ELIMINACIÓN REACCIÓN DE SUSTITUCIÓN REACCIÓN DE TRANSPOSICIÓN
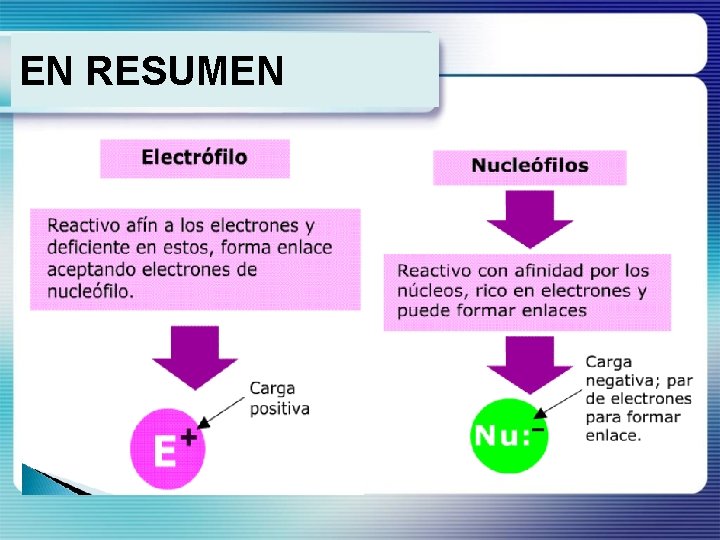
EN RESUMEN

Ejemplos de reactivos nucleófilos y electrófilos. • NUCLEÓFILOS – – – – – R–OH R–O– H 2 O R–NH 2 R – C N R–COO– NH 3 OH– halogenuros: Cl–, Br– • ELECTRÓFILOS – – – – – H+ NO 2+ NO+ BF 3, Al. Cl 3 cationes metálicos: Na+ R 3 C + SO 3 CH 3 Cl, CH 3–CH 2 Cl halógenos: Cl 2 , Br 2

El mecanismos de las reacciones orgánicas debe explicar: Debilitamiento de los enlaces entre los átomos de los reactantes Formación de un complejo activado inestable Aparición de nuevos enlaces entre los átomos que forman los productos Variación de la energía del proceso (la energía necesaria para que se forme el complejo activado es la energía de activación Eact )

2. 2. Sustitución Nucleófila de primer orden SN 1 e) Resumen de SN 1 Sustrato: alquilo terciario > bencílico ~ alquilo secundario > alquilo primario Nucleófilo: no afecta la reacción Grupos salientes: Los buenos grupos salientes (bases débiles) favorecen la reacción Disolvente: Los disolventes polares favorecen la reacción por estabilización del carbocatión. Estereoquímica: racemización

2. 3. Sustitución Nucleófila de segundo orden SN 2 e) Resumen de SN 2 Sustrato: CH 3 ->alquiloprimario> alquilo segundario > alquilo terciario (efecto estérico) Nucleófilo: La reacción se favorece con nucleófilos fuertes y básicos Grupos salientes: Los buenos grupos salientes (bases débiles) favorecen la reacción Disolvente: Los disolventes apróticos polares favorecen la reacción Estereoquímica: 100% inversión de configuración
SN 2 entre CH 3 Br y Cl
- Slides: 27