REACES DOS METAIS Reaces dos metais Os metais





- Slides: 7

REACÇÕES DOS METAIS

Reacções dos metais Os metais podem sofrer corrosão. A corrosão de metais corresponde a oxidação (indesejável), associada, simultaneamente, a uma redução. Quando uma gota de água entra em contacto com um pedaço de ferro, que reacções ocorrem? Que factores favorecem a corrosão dos metais? Todos os metais possuem igual propensão para se oxidarem? Como proteger um metal da corrosão? Poderá a oxidação de um metal ser útil?

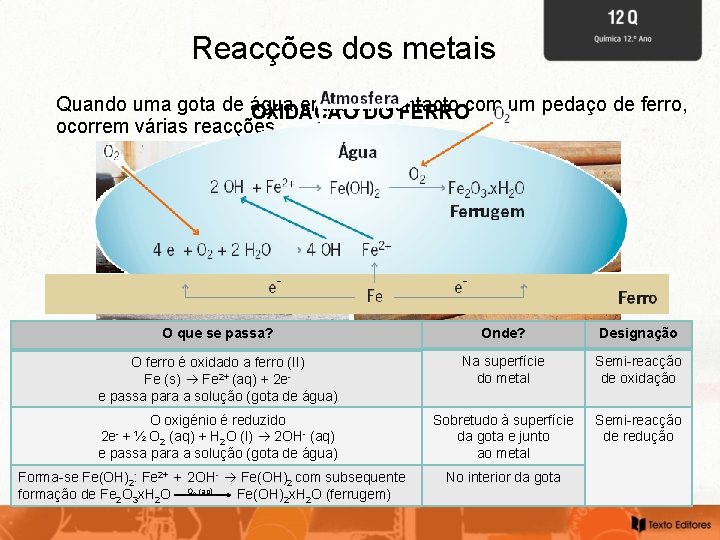
Reacções dos metais Quando uma gota de água entra em OXIDAÇÃO DOcontacto FERROcom um pedaço de ferro, ocorrem várias reacções. O que se passa? Onde? Designação O ferro é oxidado a ferro (II) Fe (s) Fe 2+ (aq) + 2 ee passa para a solução (gota de água) Na superfície do metal Semi-reacção de oxidação O oxigénio é reduzido ½ O 2 (aq) + H 2 O (l) 2 OH- (aq) e passa para a solução (gota de água) Sobretudo à superfície da gota e junto ao metal Semi-reacção de redução 2 e- + Forma-se Fe(OH)2: Fe 2+ + 2 OH- Fe(OH)2 com subsequente formação de Fe 2 O 3 x. H 2 O O (aq) Fe(OH)2 x. H 2 O (ferrugem) 2 No interior da gota

Reacções dos metais Que factores favorecem a corrosão do ferro? Meio ácido. SO 2. Iões.

Reacções dos metais Propensão dos metais para se oxidarem. Reactividade crescente: maior propensão dos metais para se oxidarem, maior poder redutor dos metais. Reactividade crescente: maior propensão dos iões para se reduzirem, maior poder oxidante dos iões.

Reacções dos metais Protecção dos metais contra a corrosão.

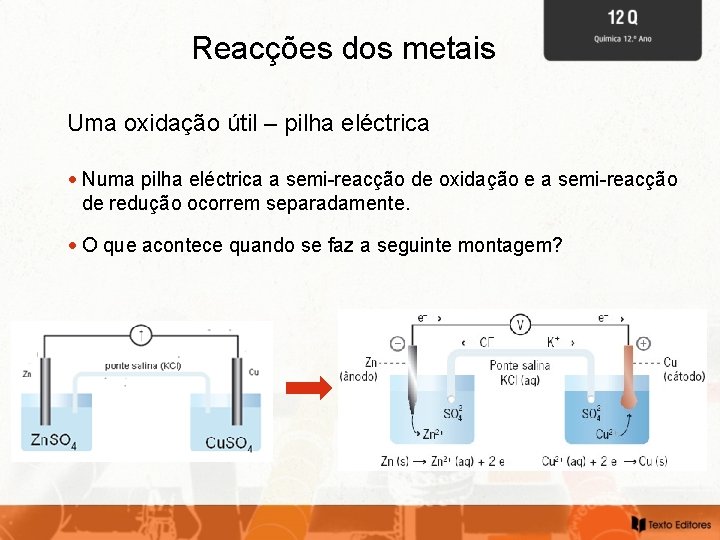
Reacções dos metais Uma oxidação útil – pilha eléctrica Numa pilha eléctrica a semi-reacção de oxidação e a semi-reacção de redução ocorrem separadamente. O que acontece quando se faz a seguinte montagem?