REACCIONES REDOX Mara Jos Pars Gonzlez Mster en








- Slides: 28

REACCIONES REDOX María José París González Máster en formación del profesorado en Física y Química Metodología experimental y aprendizaje de la Física y la Química

ÍNDICE 1. SITUACIÓN 2. CONTENIDO 2. 1. Reacciones redox 2. 2. Ajuste de reacciones redox 2. 3. Introducción a la celda electroquímica 3. RESUMEN. MAPA CONCEPTUAL 4. BIBLIOGRAFÍA

1. Situación BLOQUE 7. Introducción a la electroquimica CONTENIDOS Nivel: 2ºBachilletaro. CRITERIOS DE EVALUACIÓN Según LOE - Reacciones de oxidacion-reduccion. Especies oxidantes y reductoras. Número de oxidacion. – Concepto de potencial de reduccion estandar. Escala de oxidantes y reductores. – Valoraciones redox. Tratamiento experimental. – Aplicaciones y repercusiones de las reacciones de oxidacion reduccion: pilas y baterias electricas. – La electrolisis: importancia industrial y economica. La corrosion de metales y su prevencion. Residuos y reciclaje. Ajustar reacciones de oxidacion-reduccion y aplicarlas a problemas estequiometricos. Saber el significado de potencial estandar de reduccion de un par redox, predecir, de forma cualitativa, el posible proceso entre dos pares redox y conocer algunas de sus aplicaciones como la prevencion de la corrosion, la fabricacion de pilas y la electrolisis. Se trata de saber si, a partir del concepto de numero de oxidacion, se reconocen este tipo de reacciones y se ajustan y aplican a la resolucion de problemas estequiometricos. Tambien si se predice, a traves de las tablas de los potenciales estandar de reduccion de un par redox, la posible evolucion de estos procesos y si se conoce y valora la importancia que, desde el punto de vista economico, tiene la prevencion de la corrosion de metales y las soluciones a los problemas que el uso de las pilas genera. Asimismo, debe valorarse si se conoce el funcionamiento de las celulas electroquimicas y las electroliticas.

2. Contenido 2. 1. Reacciones redox Un tipo muy importante de reacciones son las denominadas de oxidaciónreducción, también llamadas redox o de transferencia de electrones.

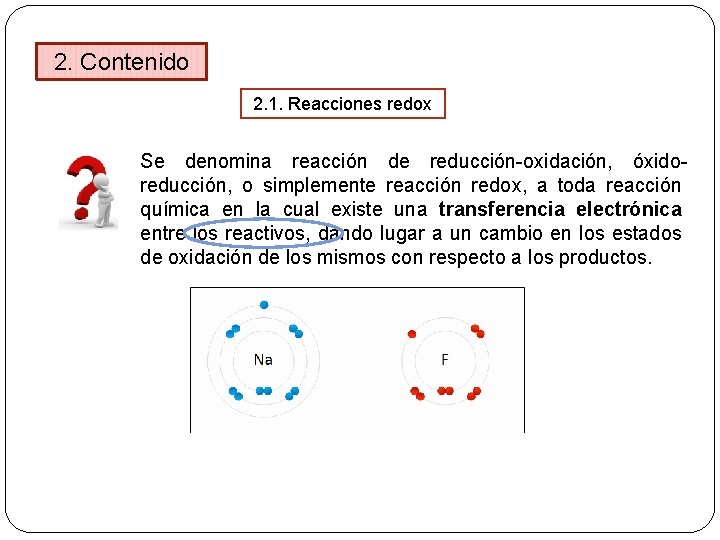
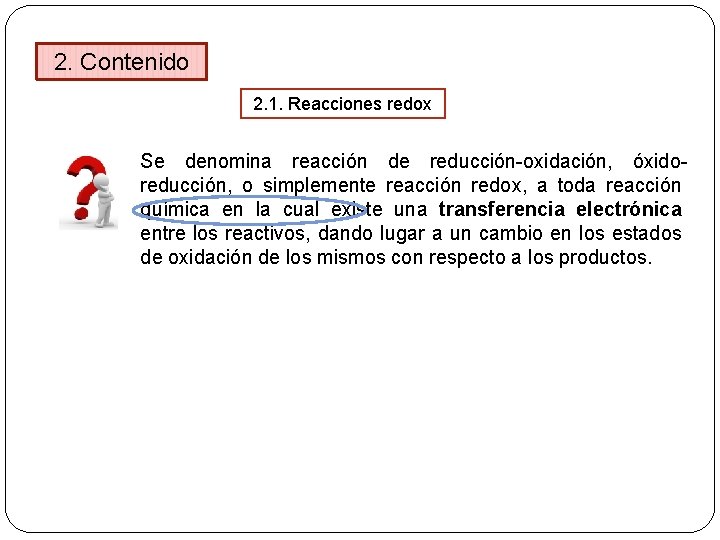
2. Contenido 2. 1. Reacciones redox Se denomina reacción de reducción-oxidación, óxidoreducción, o simplemente reacción redox, a toda reacción química en la cual existe una transferencia electrónica entre los reactivos, dando lugar a un cambio en los estados de oxidación de los mismos con respecto a los productos.

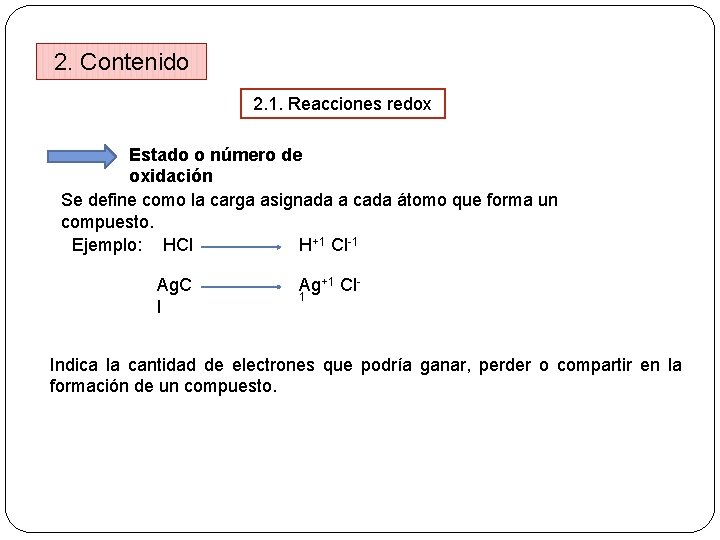
2. Contenido 2. 1. Reacciones redox Estado o número de oxidación Se define como la carga asignada a cada átomo que forma un compuesto. Ejemplo: HCl H+1 Cl-1 Ag. C l Ag+1 Cl 1 Indica la cantidad de electrones que podría ganar, perder o compartir en la formación de un compuesto.

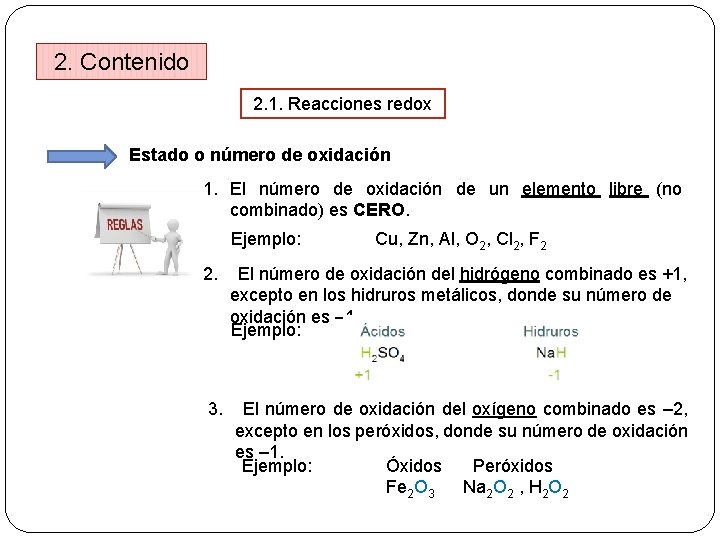
2. Contenido 2. 1. Reacciones redox Estado o número de oxidación 1. El número de oxidación de un elemento libre (no combinado) es CERO. Ejemplo: Cu, Zn, Al, O 2, Cl 2, F 2 2. El número de oxidación del hidrógeno combinado es +1, excepto en los hidruros metálicos, donde su número de oxidación es – 1. Ejemplo: 3. El número de oxidación del oxígeno combinado es – 2, excepto en los peróxidos, donde su número de oxidación es – 1. Óxidos Peróxidos Ejemplo: Fe 2 O 3 Na 2 O 2 , H 2 O 2

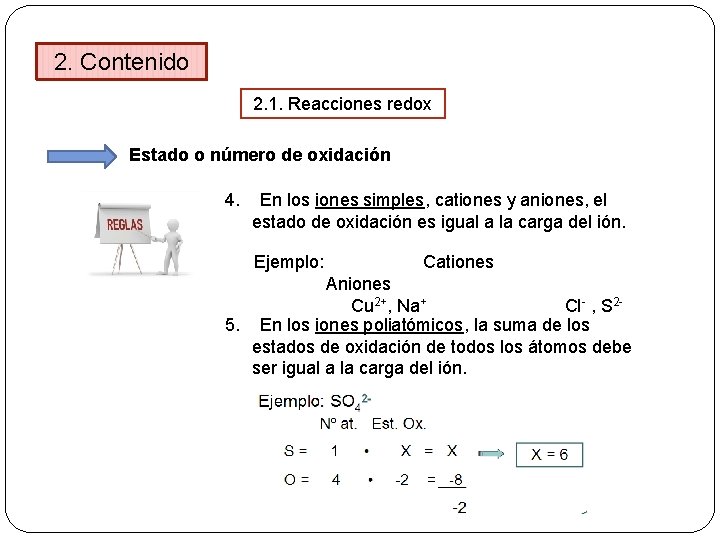
2. Contenido 2. 1. Reacciones redox Estado o número de oxidación 4. En los iones simples, cationes y aniones, el estado de oxidación es igual a la carga del ión. Ejemplo: Cationes Aniones Cu 2+, Na+ Cl- , S 25. En los iones poliatómicos, la suma de los estados de oxidación de todos los átomos debe ser igual a la carga del ión.

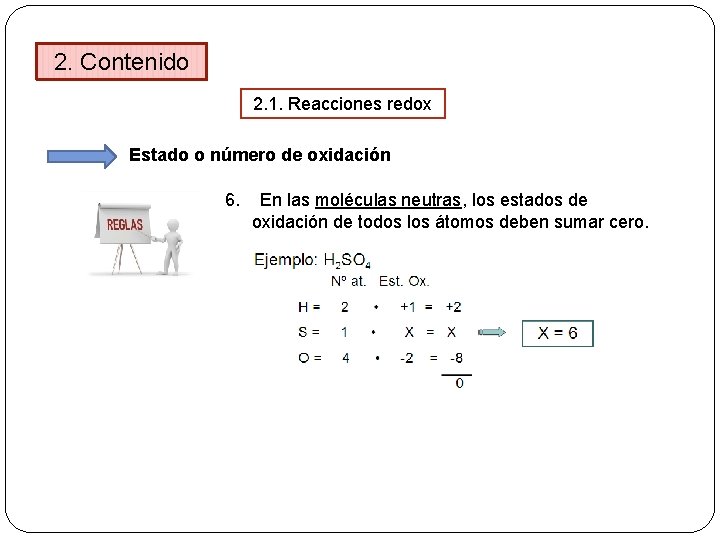
2. Contenido 2. 1. Reacciones redox Estado o número de oxidación 6. En las moléculas neutras, los estados de oxidación de todos los átomos deben sumar cero.

2. Contenido 2. 1. Reacciones redox Estado o número de oxidación Determine el estado de oxidación de : -Cl 2 -De Fe en Fe 2 O 3 -De Na en Na. OH -De P en H 3 PO 3 -De Cl en KCl. O 3 -De Mn en Mn. O 42 -

2. Contenido 2. 1. Reacciones redox Se denomina reacción de reducción-oxidación, óxidoreducción, o simplemente reacción redox, a toda reacción química en la cual existe una transferencia electrónica entre los reactivos, dando lugar a un cambio en los estados de oxidación de los mismos con respecto a los productos.

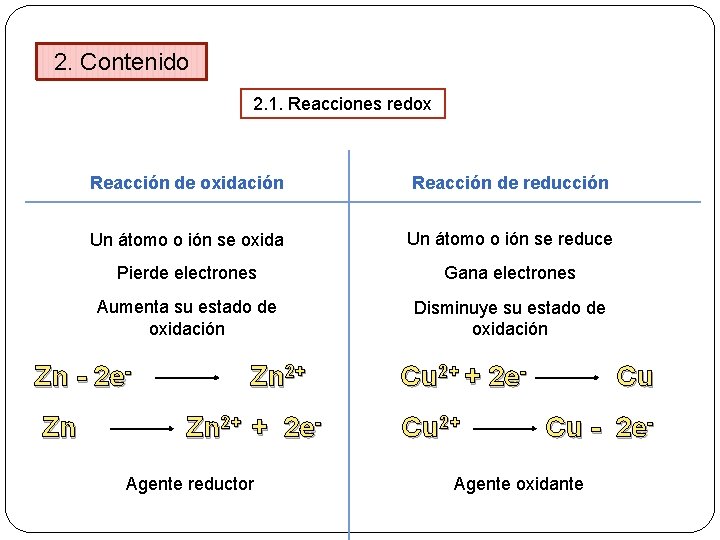
2. Contenido 2. 1. Reacciones redox Reacción de oxidación Reacción de reducción Un átomo o ión se oxida Un átomo o ión se reduce Pierde electrones Gana electrones Aumenta su estado de oxidación Disminuye su estado de oxidación Zn - 2 e. Zn Zn 2+ + 2 e- Agente reductor Cu 2+ + 2 e. Cu 2+ Cu Cu - 2 e- Agente oxidante

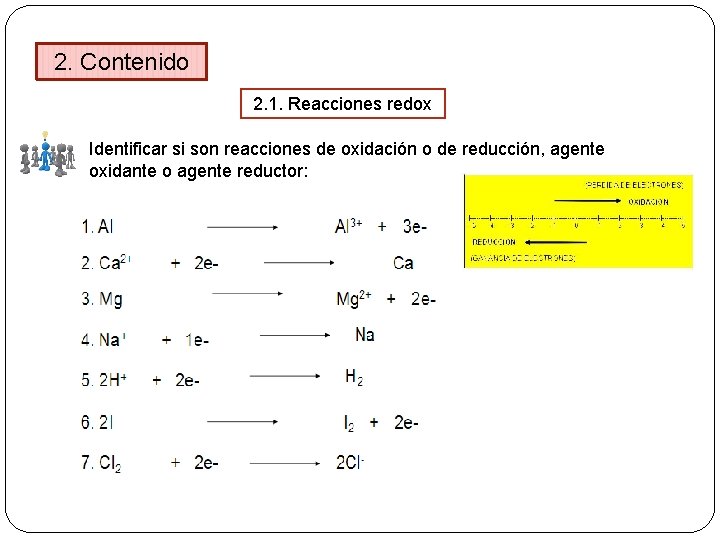
2. Contenido 2. 1. Reacciones redox Identificar si son reacciones de oxidación o de reducción, agente oxidante o agente reductor:

2. Contenido 2. 1. Reacciones redox Se denomina reacción de reducción-oxidación, óxidoreducción, o simplemente reacción redox, a toda reacción química en la cual existe una transferencia electrónica entre los reactivos, dando lugar a un cambio en los estados de oxidación de los mismos con respecto a los productos.

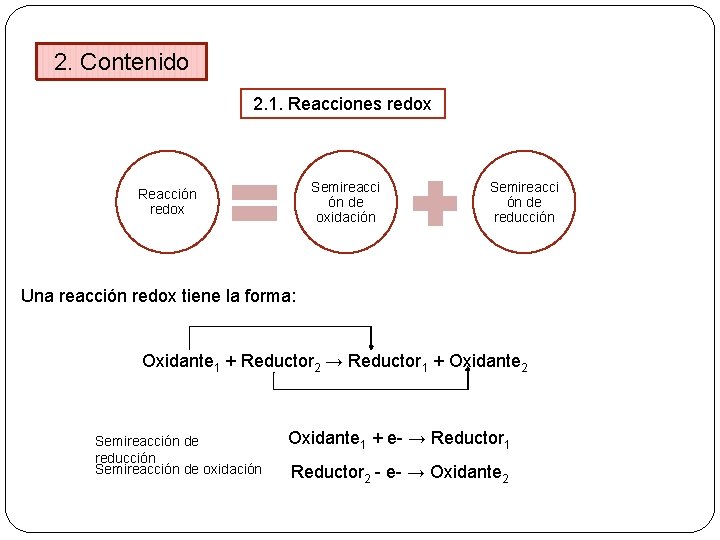
2. Contenido 2. 1. Reacciones redox Semireacci ón de oxidación Reacción redox Semireacci ón de reducción Una reacción redox tiene la forma: Oxidante 1 + Reductor 2 → Reductor 1 + Oxidante 2 Semireacción de reducción Semireacción de oxidación Oxidante 1 + e- → Reductor 1 Reductor 2 - e- → Oxidante 2

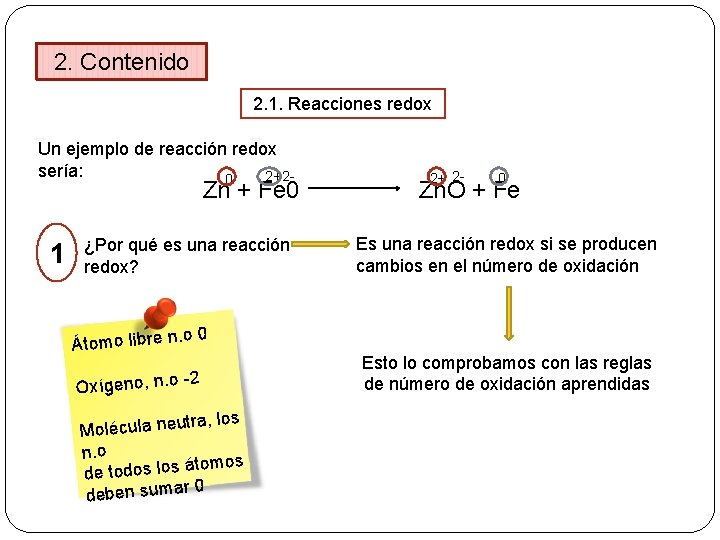
2. Contenido 2. 1. Reacciones redox Un ejemplo de reacción redox sería: 2+ 20 Zn + Fe 0 1 ¿Por qué es una reacción redox? . o 0 Átomo libre n 2 Oxígeno, n. o tra, los u e n la u c lé o M n. o tomos á s o l s o d o t e d 0 deben sumar 2+ 2 - 0 Zn. O + Fe Es una reacción redox si se producen cambios en el número de oxidación Esto lo comprobamos con las reglas de número de oxidación aprendidas

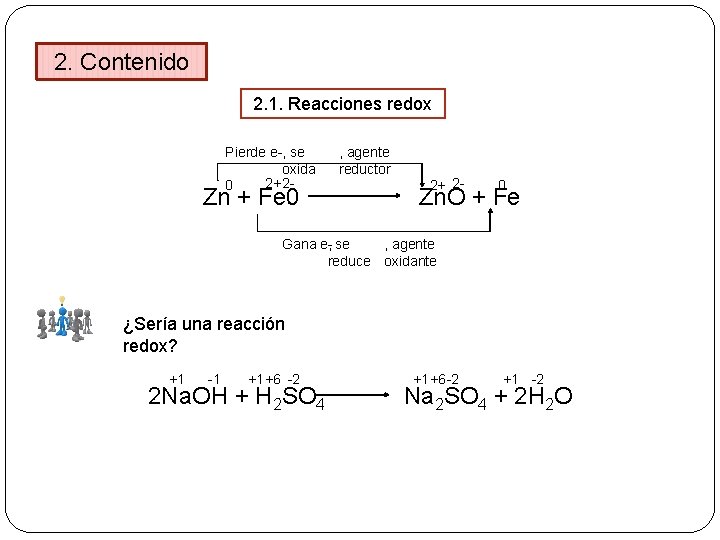
2. Contenido 2. 1. Reacciones redox Pierde e-, se oxida 2+ 20 Zn + Fe 0 , agente reductor 2+ 2 - 0 Zn. O + Fe Gana e-, se , agente reduce oxidante ¿Sería una reacción redox? +1 -1 +1+6 -2 2 Na. OH + H 2 SO 4 +1 +6 -2 +1 -2 Na 2 SO 4 + 2 H 2 O

2. Contenido 2. 2. Ajuste de reacciones redox Al igual que todas las reacciones químicas, las ación id x o e d o r e m Nú ación reacciones redox requieren comprobar el ajuste id x o e d n ió c Reac ión estequiométrico. c c u d e r e d n Reacció edox ¡HAY QUE AJUSTAR SIEMPRE LAS REACCIONES Reacciones r QUÍMICAS! Si recordamos: HCl + Na. OH Na. Cl + H 2 O 2 Mg + O 2 2 Mg. O

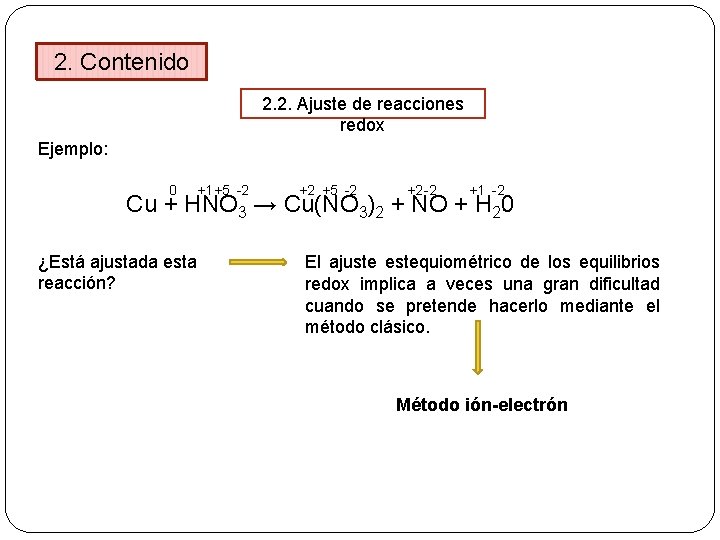
2. Contenido 2. 2. Ajuste de reacciones redox Ejemplo: 0 +1 +5 -2 +2 -2 +1 -2 Cu + HNO 3 → Cu(NO 3)2 + NO + H 20 ¿Está ajustada esta reacción? El ajuste estequiométrico de los equilibrios redox implica a veces una gran dificultad cuando se pretende hacerlo mediante el método clásico. Método ión-electrón

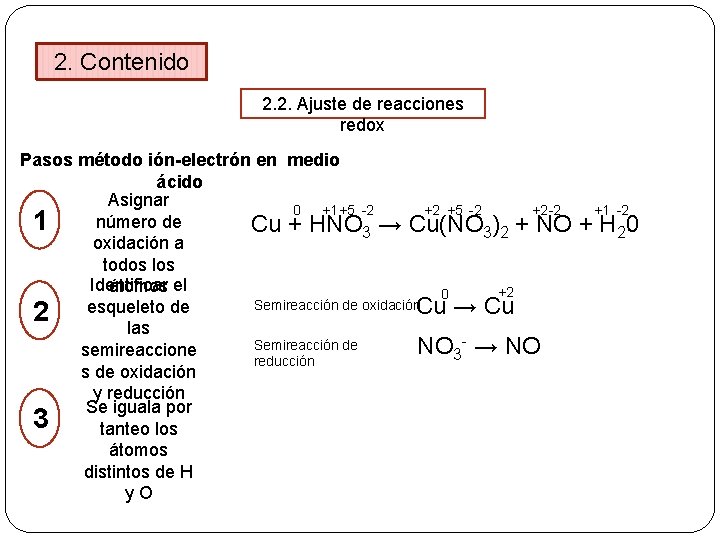
2. Contenido 2. 2. Ajuste de reacciones redox Pasos método ión-electrón en medio ácido Asignar 0 +1 +5 -2 +2 -2 +1 -2 número de 1 Cu + HNO 3 → Cu(NO 3)2 + NO + H 20 oxidación a todos los Identificar el átomos +2 0 Semireacción de oxidación Cu → Cu 2 esqueleto de las Semireacción de NO 3 - → NO semireaccione reducción s de oxidación y reducción Se iguala por 3 tanteo los átomos distintos de H y O

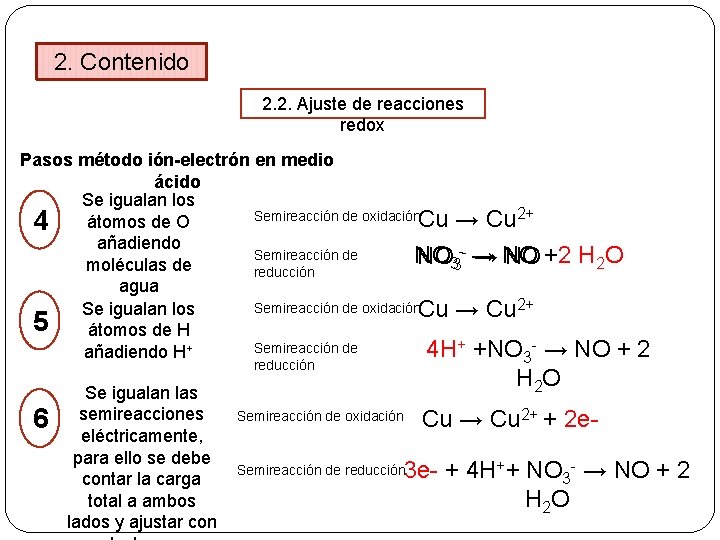
2. Contenido 2. 2. Ajuste de reacciones redox Pasos método ión-electrón en medio ácido Se igualan los Semireacción de oxidación. Cu → Cu 2+ 4 átomos de O añadiendo -- → NO +2 H O Semireacción de NO NO 33 → NO 2 moléculas de reducción agua Semireacción de oxidación. Cu → Cu 2+ Se igualan los 5 átomos de H Semireacción de 4 H+ +NO 3 - → NO + 2 añadiendo H+ reducción 6 Se igualan las semireacciones eléctricamente, para ello se debe contar la carga total a ambos lados y ajustar con H 2 O Semireacción de oxidación Cu → Cu 2+ + 2 e- 3 e- + 4 H++ NO 3 - → NO + 2 H 2 O Semireacción de reducción

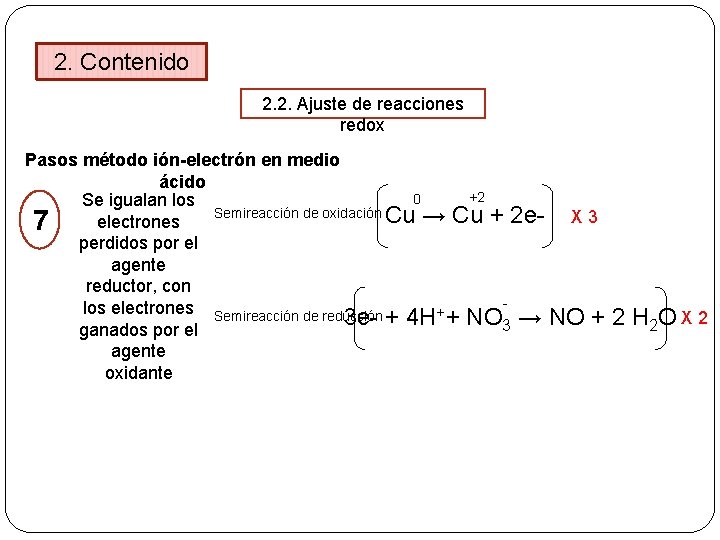
2. Contenido 2. 2. Ajuste de reacciones redox Pasos método ión-electrón en medio ácido +2 0 Se igualan los Semireacción de oxidación Cu → Cu + 2 e. X 3 electrones 7 perdidos por el agente reductor, con los electrones Semireacción de reducción + 3 e- + 4 H + NO 3 → NO + 2 H 2 O X 2 ganados por el agente oxidante

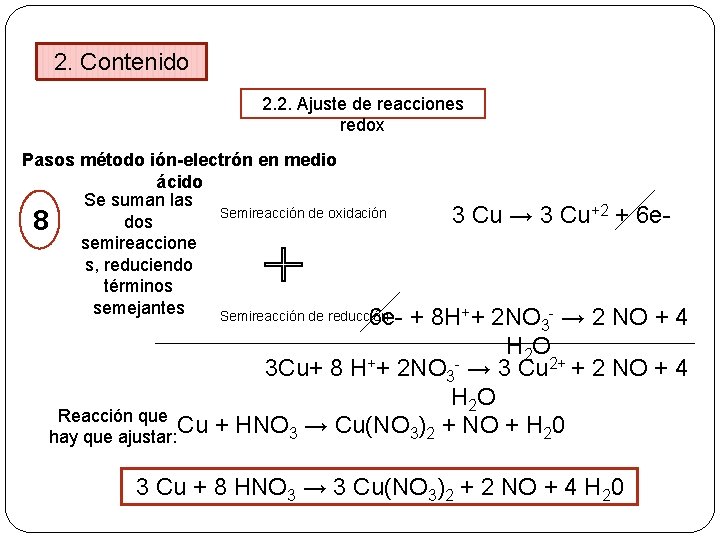
2. Contenido 2. 2. Ajuste de reacciones redox Pasos método ión-electrón en medio ácido Se suman las Semireacción de oxidación dos 8 semireaccione s, reduciendo términos semejantes Semireacción de reducción 3 Cu → 3 Cu+2 + 6 e- + 8 H++ 2 NO 3 - → 2 NO + 4 H 2 O 3 Cu+ 8 H++ 2 NO 3 - → 3 Cu 2+ + 2 NO + 4 H 2 O Reacción que Cu + HNO 3 → Cu(NO 3)2 + NO + H 20 hay que ajustar: 3 Cu + 8 HNO 3 → 3 Cu(NO 3)2 + 2 NO + 4 H 20

2. Contenido 2. 2. Ajuste de reacciones redox Podemos tener reacciones tanto en medio ácido como en básico. Método ión-electrón Todos los pasos son iguales excepto cuando se tiene que igualar el oxígeno y el hidrógeno a ambos lados. Medio ácido 4 5 Se igualan los átomos de O añadiendo moléculas de agua Se igualan los átomos de H añadiendo H+ Medio básico 4 5 Se igualan los átomos de O añadiendo 2 iones OH- por cada oxígeno Se igualan los átomos de H añadiendo H 2 O

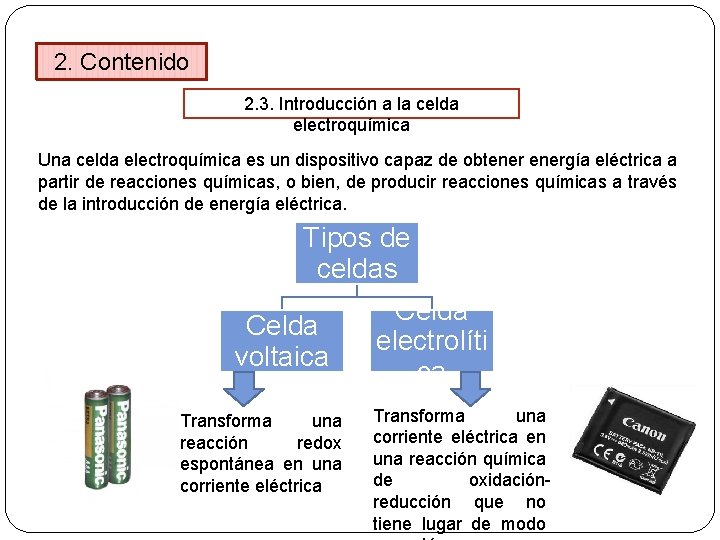
2. Contenido 2. 3. Introducción a la celda electroquímica Una celda electroquímica es un dispositivo capaz de obtenergía eléctrica a partir de reacciones químicas, o bien, de producir reacciones químicas a través de la introducción de energía eléctrica. Tipos de celdas Celda voltaica Transforma una reacción redox espontánea en una corriente eléctrica Celda electrolíti ca Transforma una corriente eléctrica en una reacción química de oxidaciónreducción que no tiene lugar de modo

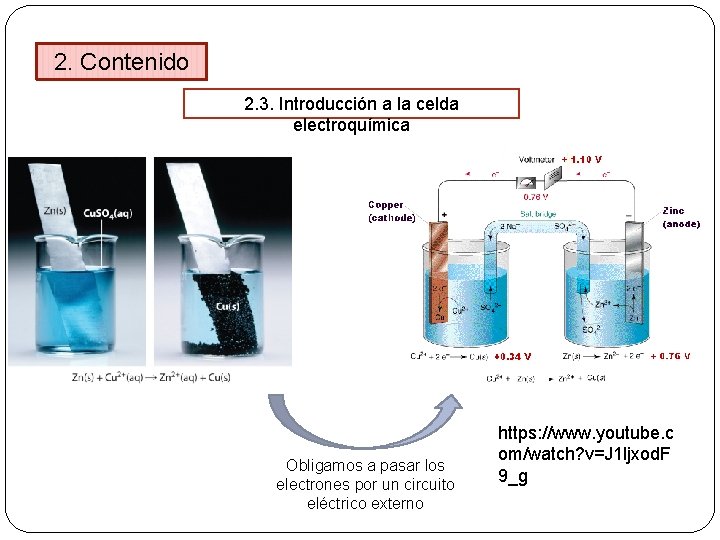
2. Contenido 2. 3. Introducción a la celda electroquímica Obligamos a pasar los electrones por un circuito eléctrico externo https: //www. youtube. c om/watch? v=J 1 ljxod. F 9_g

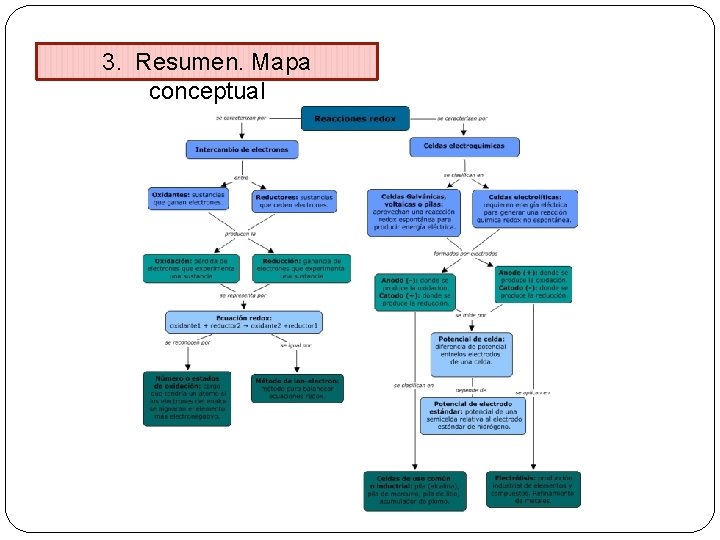
3. Resumen. Mapa conceptual

4. Bibliografía http: //c-h-emistry. wdfiles. com/localfiles/help%3 Atema 3/tema 3 conocimientosprevios. pdf http: //www. iesdmjac. educa. aragon. es/departamentos/fq/asignaturas/quimica 2 bac /materialdeaula/QUI 2 BAC%20 Tema%206%20 Reacciones%20 redox%20 y%20 el ectroquimica/QUI 2 BAC_Tema_6_Reacciones_redox_y_electroquimica__Resum en. pdf http: //www. fisicanet. com. ar/quimica/redox/ap 01_redox. php Simulador de celda electroquímica: http: //www. aularagon. org/files/espa/Bachillerato/Segundo/Quimica/U 6_arch ivos_Quimica/galvan 5. swf