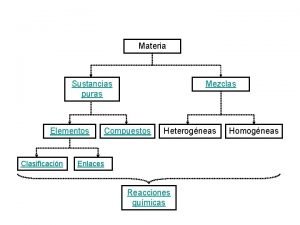
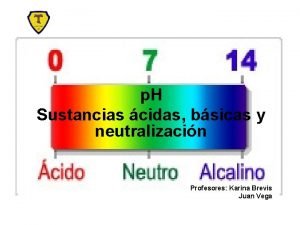
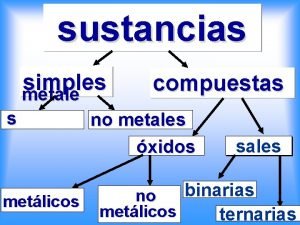
REACCIONES QUMICAS SUSTANCIAS PURAS Cambios fsicos Cambios Qumicos

REACCIONES QUÍMICAS
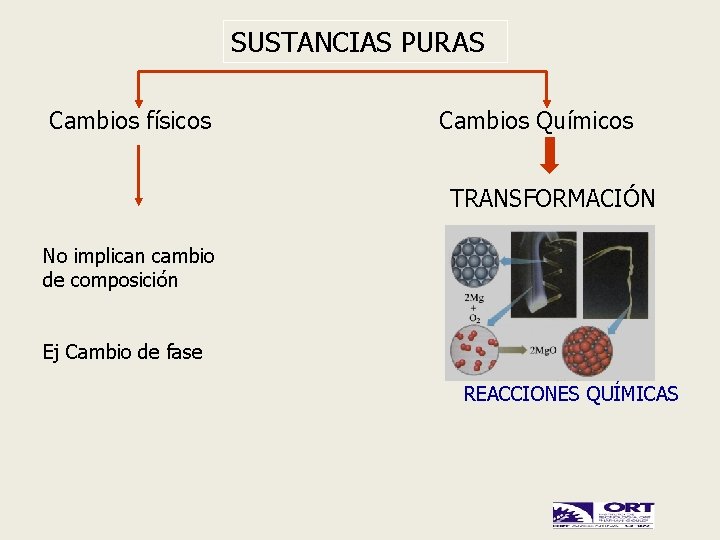
SUSTANCIAS PURAS Cambios físicos Cambios Químicos TRANSFORMACIÓN No implican cambio de composición Ej Cambio de fase REACCIONES QUÍMICAS

CAMBIO FÍSICO Y CAMBIO QUÍMICO. • CAMBIO FÍSICO: es aquél que tiene lugar sin transformación de materia. Cuando se conserva la sustancia original. – Ejemplos: cualquiera de los cambios de estado y también patear una pelota, romper una hoja de papel. En todos los casos, encontraremos que hasta podría cambiar la forma, como cuando rompemos el papel, pero la sustancia se conserva, seguimos teniendo papel. • CAMBIO QUÍMICO: es aquél que tiene lugar con transformación de materia. Cuando no se conserva la sustancia original. – Ejemplos: cuando quemamos un papel, cuando respiramos, y en cualquier reacción química. En todos los casos, encontraremos que las sustancias originales han cambiado, puesto que en estos fenómenos es imposible conservarlas.

¿Cómo nos damos cuenta que se produce una reacción química? Cuando al poner en contacto dos o más sustancias: • Se forma un precipitado • Se desprenden gases • Cambia de color • Se desprende o absorbe energía (calor) • Se percibe un “olor”, etcétera

Una reacción química es un proceso en el cual una o mas sustancias al interaccionar forman otras, como consecuencia de la ruptura de algunos enlaces y la formación de otros nuevos. En la reacción: H 2 + I 2 — 2 HI Reactivos Productos Se rompen 1 enlace H—H y 1 enlace I —I y se forman 2 enlaces H—I
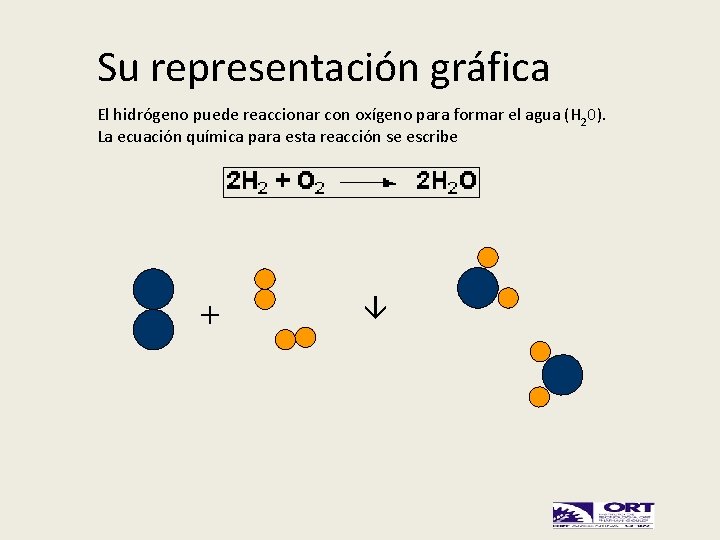
Su representación gráfica El hidrógeno puede reaccionar con oxígeno para formar el agua (H 20). La ecuación química para esta reacción se escribe +

¿qué es una reacción química? • Una reacción química consiste en la “ruptura de enlaces químicos” entre los átomos de los reactivos y la “formación de nuevos enlaces” que originan nuevas sustancias químicas, con liberación o absorción de energía. • En toda reacción química la masa se conserva, es decir permanece constante OJO! Cambios de estado NO son reacciones químicas.

Ejemplos de reacciones químicas https: //www. alonsoformula. com/FQESO/2_4__reacciones_qu%C 3 %ADmicas. htm

Teoría de las Reacciones Químicas Teoría de las colisiones. Estado de transición Una reacción química supone la ruptura de ciertos enlaces de las moléculas de reactivos y la formación de otros nuevos, para dar lugar a las moléculas de productos. Ejemplo: Formación de cloruro de sodio Cuando se introduce un trozo de sodio caliente en el interior de un frasco que contiene gas cloro, se produce una violenta reacción en la que se forma una sustancia nueva, el cloruro de sodio. Esta reacción se puede expresar así:

2 Na + Cl 2 2 Na Cl

Teoría de las Reacciones Químicas Teoría de las colisiones. Estado de transición Todas las reacciones químicas pasan por un estado de transición de máxima energía, denominado complejo activado (complejo de transición) que es un agregado constituido por las moléculas reaccionantes y en el que algunos de los enlaces primitivos se han relajado (o incluso roto) y se han empezado a formar nuevos enlaces. Es un estado intermedio, de transición, en una reacción química que posee gran energía, tiene acumulada toda la energía cinética de las moléculas reaccionantes y por ello es muy inestable y se descompone inmediatamente originando los productos de reacción. Ejemplo: Formación de cloruro de hidrógeno https: //www. youtube. com/watch? v=68 x. SPY 9 GDUU https: //www. youtube. com/watch? v=-RQIf. Eef. Azg
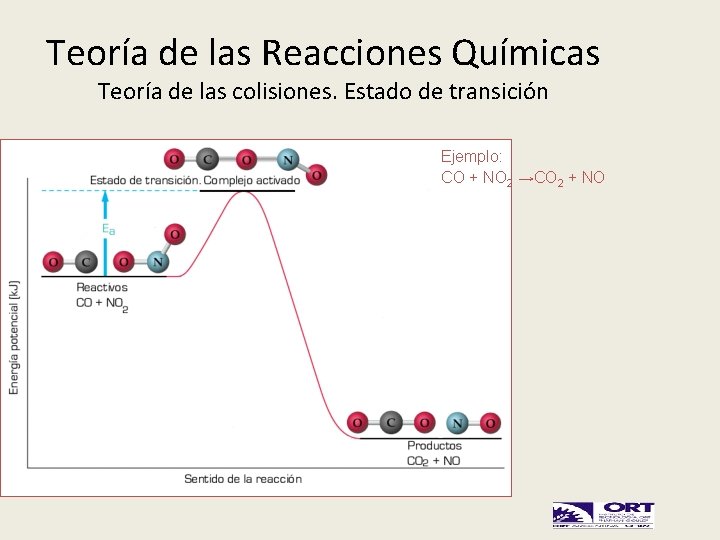
Teoría de las Reacciones Químicas Teoría de las colisiones. Estado de transición Ejemplo: CO + NO 2 →CO 2 + NO

Teoría de las Reacciones Químicas Teoría de las colisiones. Estado de transición

Teoría de las Reacciones Químicas Teoría de las colisiones. Estado de transición

Energía en las Reacciones Químicas EXOTÉRMICA ENDOTÉRMICA Al calentar la termita se produce una reacción fuertemente exotérmica. El aluminio reacciona con óxido de hierro (III), produciendo una lluvia de chispas de hierro fundido. La reacción entre sulfocianuro amónico e hidróxido de bario octahidratado es una reacción endotérmica. Absorbe una cantidad de calor del exterior del recipiente que produce la congelación del vapor de agua del aire. En una reacción exotérmica, la energía se pierde en forma de calor, la cantidad de calor perdida depende de la cantidad de reactivos disponible. En una reacción endotérmica, la energía se absorbe en forma de calor.
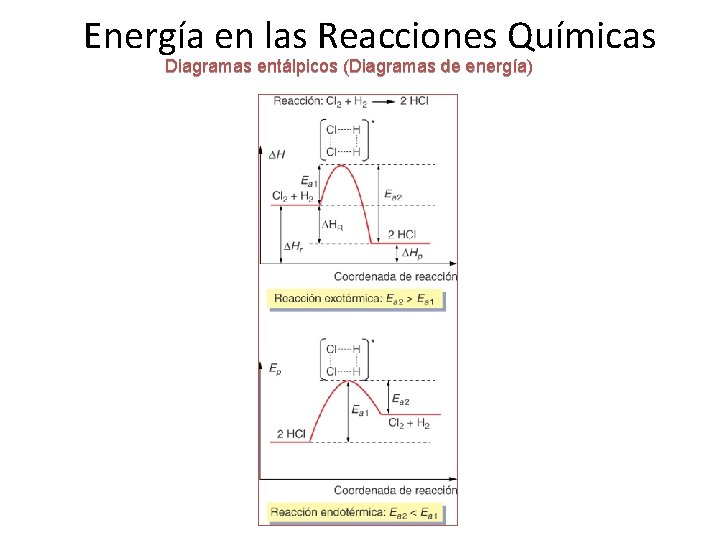
Energía en las Reacciones Químicas Diagramas entálpicos (Diagramas de energía)

Reacciones termoquímicas: Las reacciones químicas siempre se ven acompañadas por cambios de energía; esta puede presentarse en forma de calor. Cuando las reacciones liberan calor, son llamadas exotérmicas y cuando lo absorben de su alrededor, endotérmicas.

Quimioluminiscencia Algunas reacciones químicas exoenergéticas emiten en energía en forma de radiación luminosa.

Clases de Reacciones Químicas Reacciones de síntesis: Consiste en la unión de dos o más sustancias sencillas para formar una más compleja. Reacciones de descomposición: Este tipo de reacción es inversa a la síntesis; una sustancia compleja, se descompone en 2 o más sustancias sencillas
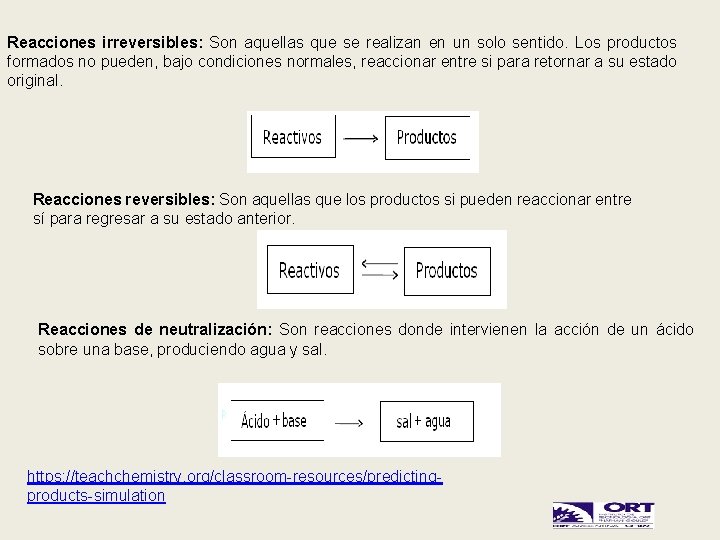
Reacciones irreversibles: Son aquellas que se realizan en un solo sentido. Los productos formados no pueden, bajo condiciones normales, reaccionar entre si para retornar a su estado original. Reacciones reversibles: Son aquellas que los productos si pueden reaccionar entre sí para regresar a su estado anterior. Reacciones de neutralización: Son reacciones donde intervienen la acción de un ácido sobre una base, produciendo agua y sal. https: //teachchemistry. org/classroom-resources/predictingproducts-simulation

• Procesos en los que cambia la naturaleza de una o más sustancias (Reactivos), formándose otras nuevas (Productos). Ecuación Química Reactivos Productos

Las R. Q tienen un sentido o dirección. Según ésto pueden ser: Irreversibles: La flecha apunta hacia la derecha. C (s) + O 2 (g) CO 2 (g) Reversibles: La flecha apunta en los dos sentidos. Los productos formados reaccionan regenerando las sustancias originales. H 2 (g) + CO 2 (g) H 2 O (g) + CO (g)

Símbolos usados en una ecuación química: • + se usa entre dos fórmulas para indicar la presencia de varios reactivos o de varios productos. • se llama “flecha de reacción” y separa los reactivos de los productos. Indica que la combinación de los reactivos “produce”.

Símbolos usados en una ecuación química: • la flecha hacia arriba indica que se desprende un gas. • (s) indica que la sustancia se encuentra en estado sólido. • (l) indica que la sustancia se encuentra en estado líquido. • (g) indica que la sustancia se encuentra en estado gaseoso. Ò la flecha con una “Ǿ” o la palabra calor encima indica que la reacción requiere energía térmica para llevarse a cabo. • Cualquier “signo” que se ponga encima de la flecha, nos indica que se requiere de este para que la reacción ocurra. • (aq) indica que el reactivo o el producto se encuentra en solución acuosa.

Ejemplo: Combustión de la nafta • ¿En qué se transforma la nafta una vez es consumida? . • ¿Cuáles son los reactivos y los productos de dicha combustión? . • ¿La masa de dichos productos? , ¿Es igual a la masa de los reactivos? .

La ecuación química permite establecer relaciones cuantitativas entre reactivos y productos y debe estar BALANCEADA, IGUALADA O EQUILIBRADA. Para esto se anteponen coeficientes numéricos a elementos o compuestos, para igualar el número de átomos de cada elemento en ambos miembros. Muchas ecuaciones químicas se balancean por simple inspección, usando el método de tanteo (prueba y error).

Ajuste de reacciones. Formación del agua. • • A los números que hemos añadido para ajustar la ecuación se les llama coeficientes estequiométricos. 2 H 2 + O 2 2 H 2 O nº de átomos en la molécula. coeficiente estequiométrico(nº de moléculas) • “ las ecuaciones químicas son las representaciones simbólicas de las reacciones reales. En ellas, el número de átomos de cada elemento es el mismo en las sustancias iniciales y en las finales. ”

Ejemplo de reacción química: Por cada molécula de oxígeno que reacciona son necesarias dos de hidrógeno para formar 2 moléculas de agua. Esto se expresa mediante la ecuación química: O 2(g) + 2 H 2(g) 2 H 2 O (g)

Balance de ecuaciones 1) Escribir la ecuación no igualada con símbolos y/o fórmulas correctas de reactivos y productos. 2) Igualar la ecuación ajustando los coeficientes que preceden las fórmulas y/o símbolos. Ej) C 2 H 4 + 3 O 2 2 CO 2 + 2 H 2 O 2 átomos de C 4 átomos de H 6 átomos de O

METODO ALGEBRAICO 1) Se anteponen letras frente a cada elemento o compuesto. 2) Se plantea una ecuación matemática para cada elemento. 3) Se asigna un valor “arbitrario“ a una de las variables 4) Se despeja el resto de las variables 5) Si esto último no es posible se deducen otras ecuaciones a partir de las ya planteadas 6) El conjunto final de resultados debe contener sólo números enteros lo más pequeños posibles.
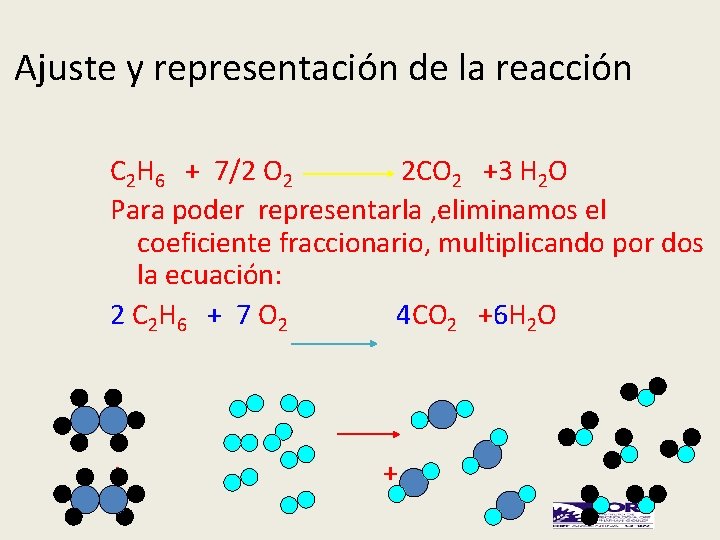
Ajuste y representación de la reacción C 2 H 6 + 7/2 O 2 2 CO 2 +3 H 2 O Para poder representarla , eliminamos el coeficiente fraccionario, multiplicando por dos la ecuación: 2 C 2 H 6 + 7 O 2 4 CO 2 +6 H 2 O + +

Relación en moles Los coeficientes estequiométricos informan sobre el número de moles de cada elemento y de cada compuesto que intervienen en la reacción. 2 CO + O 2 2 moléculas de CO 1 molécula de O 2 20 moléculas de CO 10 molécula de O 2 2 · 6, 02 · 1023 moléculas de CO 2 moles de CO 6, 02 · 1023 moléculas de O 2 1 mol de O 2 2 CO 2 2 moléculas de CO 2 20 moléculas de CO 2 2 · 6, 02 · 1023 moléculas de CO 2 2 moles de CO 2 Los coeficientes estequiométricos de una ecuación química ajustada informan de la proporción entre moles de reactivos y productos

Escala en moles. • Ejemplo: CH 4 +2 O 2 CO 2 + 2 H 2 O 1 molécula de CH 4 generan 2 moléculas de H 2 O 6. 023 1023 moléculas de CH 4 generan 2 x 6. 023 1023 moléculas de H 2 O. 1 mol de CH 4 genera 2 moles de H 2 O

Relación en masas A partir de las masas atómicas de los elementos que intervienen en la reacción, se puede establecer la relación entre las masas de los reactivos y de los productos N 2 + 3 H 2 2 NH 3 Conociendo las masas atómicas (H = 1, 01 u y N = 14, 01 u), se determinan las masas moleculares: H 2 = 2, 02 u; N 2 = 28, 02 u; NH 3 = 17, 04 u 1 mol de N 2 28, 02 g de N 2 3 moles de H 2 3 · 2, 02 = 6, 06 g de H 2 2 moles de NH 3 2 x 17, 04 = 34, 08 g de NH 3 Los coeficientes estequiométricos de una ecuación química ajustada informan de la proporción entre gramos de reactivos y productos
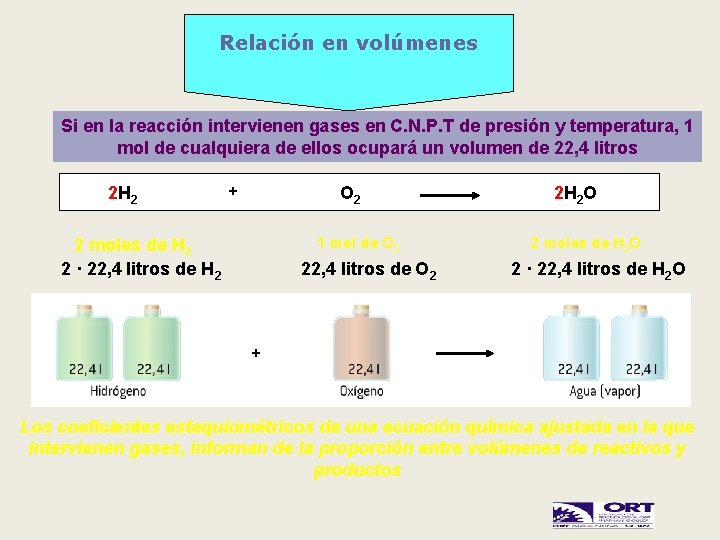
Relación en volúmenes Si en la reacción intervienen gases en C. N. P. T de presión y temperatura, 1 mol de cualquiera de ellos ocupará un volumen de 22, 4 litros 2 H 2 + O 2 1 mol de O 2 2 moles de H 2 2 · 22, 4 litros de H 2 22, 4 litros de O 2 2 H 2 O 2 moles de H 2 O 2 · 22, 4 litros de H 2 O + Los coeficientes estequiométricos de una ecuación química ajustada en la que intervienen gases, informan de la proporción entre volúmenes de reactivos y productos

Es común incluir el estado físico de la sustancia: Cu (s) cobre en fase sólida; H 2 O (l) agua líquida H 2 (g) hidrógeno gaseoso 2 Li (s) + 2 átomos H 2 (g) 1 molécula 2 moles de átomos 1 mol de moléculas 13. 8 g 2 x(6. 02 x 1023) átomos 2. 0 g 6. 02 x 1023 moléculas 22. 4 L (C. N. T. P) 2 Li. H (s) 2 moléculas 2 moles de moléculas 15. 8 g 2 x(6. 02 x 1023) moléculas

Cálculos estequiométricos. En una reacción química las proporciones se cumplen molécula a molécula , átomo a átomo y mol a mol. 2 Fe + O 2 2 Fe. O 2 moles de hierro , y un mol de oxígeno dan 2 moles de oxido de Fe.

CÁLCULOS ESTEQUIOMÉTRICOS. CÁLCULOS CON MASAS Conocida la masa de un reactivo o de un producto, pueden calcularse el resto de las masas que intervienen en la reacción Ejemplo: En la descomposición del clorato de potasio se obtiene cloruro de potasio y oxígeno. A partir de 5 gr KCl. O 3 , calcular a)¿Cuántos gramos de oxígeno se obtienen, 2 KCl. O 3 2 KCl 2 moles de KCl. O 3 2 moles de KCl 3 mol de O 2 74, 45 x 2 = 148, 9 g de KCl 122, 45 g x 2 = 244, 9 g de KCl. O 3 3 O 2 + 96 g de O 2 Suma masa de los reactivos = suma masa de los productos a) = 148, 9 + 96 1000 g de KCl. O 3 244, 9 g de KCl. O 3 96 g O 2 = 5 g de KCl. O 3 X g O 2 ü X g de O 2 X = 5 · 96 244, 9 = 244, 9 1, 96 g de O 2

Ej) El cloruro de potasio (KCl) se produce a partir de clorato de potasio (KCl. O 3) según la reacción no balanceada: KCl. O 3 (s) KCl (s) + O 2 (g) Si se descomponen totalmente 5 g de KCl. O 3 calcule: a) Cuántos gramos de oxígeno se obtienen b) masa de KCl formados c) número de moles de KCl. O 3 descompuestos. d) número de moles de KCl formados. e) moles de O 2 formados f) volumen (en L) de O 2 obtenidos en C. N. P. T g) volumen (en L) de O 2 a 748 mm Hg y 37ºC h) moléculas de KCl formadas i) átomos presentes en el O 2 formado

Ej) ¿Qué masa de hidróxido de sodio se requiere para producir 250 g de sulfato de sodio de acuerdo a la reacción no balanceada? H 2 SO 4 + 2 Na. OH Na 2 SO 4 + 2 H 2 O ácido sulfúrico hidróxido de sodio sulfato de sodio agua Ej) ¿Qué masa de carbono reacciona con 500 g de óxido de manganeso (IV) según la reacción no balanceada? . Mn. O 2 + 2 C Mn + 2 CO

Ejercicio de aplicación: En la obtención de agua: • H 2 (g) + O 2 (g) H 2 O(l) • Se tienen 4. 5 g de hidrógeno • ¿Qué cantidad* de oxígeno se requiere para que reaccione todo el hidrógeno? • ¿Qué cantidad* de agua se obtendra? *cantidad de sustancia(mol) y en gramos.

Ejercicio de aplicación • ¿Cuánto gas se desprenderá si pongo a reaccionar 1. 3 moles de bicarbonato de sodio con 3. 5 m. L de vinagre (5% en volumen), en condiciones de laboratorio (20°C y 586 mm. Hg)?

Ejercicios adicionales • http: //www. eis. uva. es/~qgintro/genera. php? tema=4&ejer=2

Actividades interactivas http: //concurso. cnice. mec. es/cnice 2005/35_las_reacciones_quimicas/curso /index. html http: //concurso. cnice. mec. es/cnice 2005/35_las_reacciones_quimicas/curso /lrq_rq. html
- Slides: 44