REACCIONES QUMICAS Es cuando las sustancias sufren cambios

REACCIONES QUÍMICAS: Es cuando las sustancias sufren cambios. Aquí se consumen una o más sustancias y se forman otras.
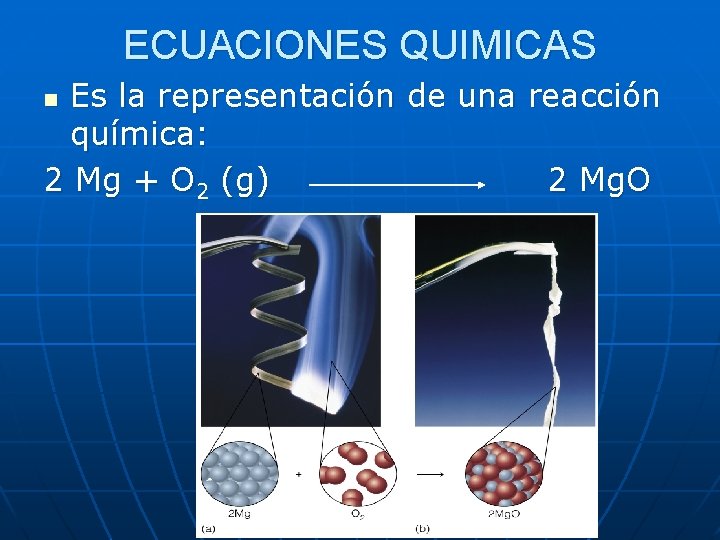
ECUACIONES QUIMICAS Es la representación de una reacción química: 2 Mg + O 2 (g) 2 Mg. O n

ECUACIONES QUIMICAS

n n n Los reactivos o materiales de partida: lado izquierdo Los productos: lado derecho Los productos y reactivos están separados por una flecha que significa “ produce”

SÍMBOLOS ESPECIALES:
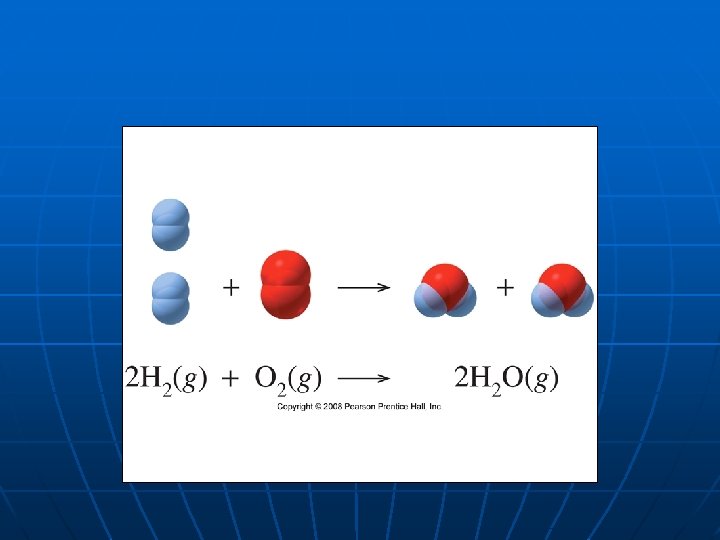

BALANCEO DE ECUACIONES QUÍMICAS: n n n La masa total (átomos) de reactivos debe ser igual a la masa total (átomos) de productos. Ley de conservación de la MASA: no se crean, ni se destruyen átomos y tampoco se crea o se destruye masa. Una ecuación química no está completa si no está balanceada

PROCEDIMIENTO: Primero se escriben la ecuación química no balanceada con las fórmulas correctas de los reactivos y productos n Por tanteo: 1. Metales 2. No metales 3. Hidrógenos 4. Oxígeno n
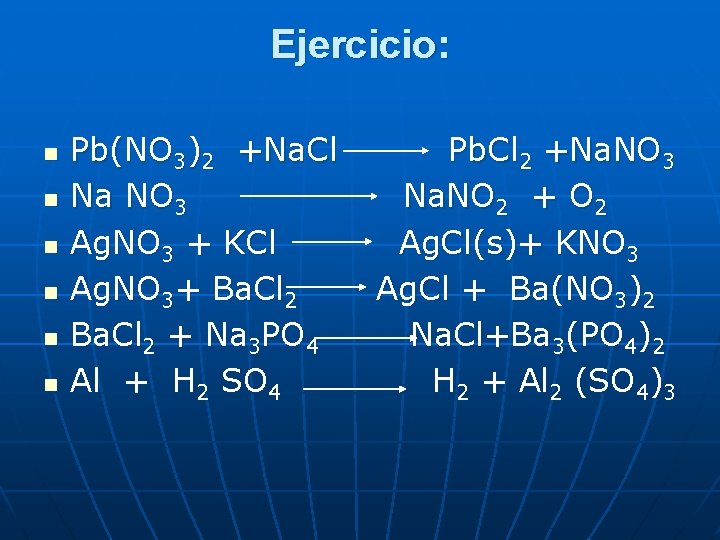
Ejercicio: n n n Pb(NO 3)2 +Na. Cl Na NO 3 Ag. NO 3 + KCl Ag. NO 3+ Ba. Cl 2 + Na 3 PO 4 Al + H 2 SO 4 Pb. Cl 2 +Na. NO 3 Na. NO 2 + O 2 Ag. Cl(s)+ KNO 3 Ag. Cl + Ba(NO 3)2 Na. Cl+Ba 3(PO 4)2 H 2 + Al 2 (SO 4)3

CLASIFICACION DE LAS REACCIONES: REACCIONES DE COMBINACIÓN (SÍNTESIS): n Cuando dos elementos o compuestos se combinan para formar un producto nuevo n A + B AB

REACCION DE ANÁLISIS O DESCOMPOSICIÓN: n Cuando un compuesto AB se descompone en dos o más sustancias sencillas. n AB A + B

REACCIONES DE SUSTITUCIÓN SIMPLE O DE SIMPLE DESPLAZA-MIENTO: n n Cuando un elemento reemplaza a otro elemento dentro de un compuesto A + BC AC + B METAL
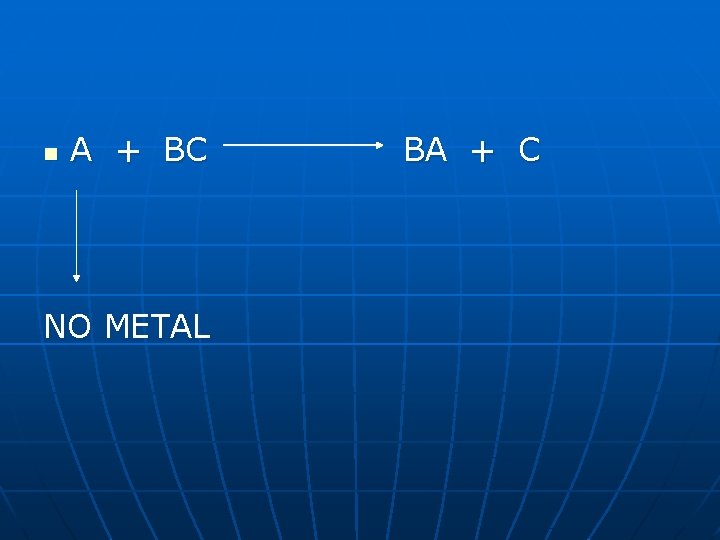
n A + BC NO METAL BA + C
REACCIONES DE DOBLE DESPLAZAMIENTO O METATESIS: n n Cuando los compuestos intercambian parejas entre sí para producir dos compuestos diferentes AB + CD AD + CB • Neutralización: n H + + OH- H 2 O + sal

REACCION EXOTÉRMICA: n Es una reacción en la cual se libera energía calorífica CH 4 + 2 O 2 (g) CO 2 +2 H 2 O + 90 KJ (g) (L)

REACCION ENDOTERMICA: n Es una reacción que absorbe o toma energía calorífica 2 H 2 O + 566 KJ 2 H 2 (g) + O 2(g)

Ejercicio: Clasifica las reacciones de acuerdo a su categoría: 1. Ag. NO 3 + Ba Cl 2 Ag. Cl + Ba(NO 3)2 2. Ca + O 2 Ca. O 3. Al + Ni SO 4 Ni + Al 2 (SO 4)3 4. Na NO 3 Na. NO 2 + O 2 (g) 5. HCl + Na. OH H 2 O + Na. Cl

ESTADOS DE OXIDACIÓN: n Son números que se asignan a los elementos para indicar su estado (o estados) de combinación que pueden asumir. Indican la habilidad de un elemento para formar compuestos.
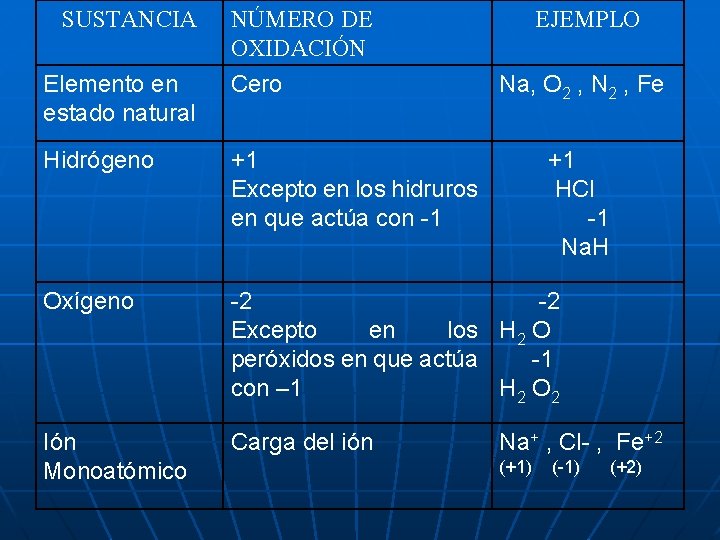
SUSTANCIA NÚMERO DE OXIDACIÓN EJEMPLO Elemento en estado natural Cero Na, O 2 , N 2 , Fe Hidrógeno +1 Excepto en los hidruros en que actúa con -1 Oxígeno -2 -2 Excepto en los H 2 O peróxidos en que actúa -1 con – 1 H 2 O 2 Ión Monoatómico Carga del ión +1 HCl -1 Na. H Na+ , Cl- , Fe+2 (+1) (-1) (+2)

SUSTANCIA NÚMERO DE OXIDACIÓN EJEMPLO Dos elementos combinados El menos electronegativo con número de oxidación positivo y el más electronegativo con número de oxidación negativo +1 -1 HCl Ión Poliatómico La suma algebraica de los números de oxidación es igual a la carga del ión NO 3 – 1 -6 = -1 +5 -2 N O 3 Compuesto La suma algebraica de los H 2 SO 4 números de oxidación debe ser cero Na 2 O

n n n EJERCICIO: Calcule el número de oxidación del Br en el HBr Calcule el número de oxidación del Ca en el Ca. O Calcule el número de oxidación del manganeso en el KMn. O 4 Calcule el número de oxidación del azufre en el SO 4 -2 Calcule el número de oxidación del carbono en el Na 2 CO 3 Calcule el número de oxidación del Fe en el Fe. SO 4
- Slides: 21