REACCIONES CIDO BASE Caractersticas Generales de los cidos

REACCIONES ÁCIDO - BASE

Características Generales de los Ácidos • En soluciones diluidas tienen sabor agrio (ácido) • Liberan hidrógeno molecular (H 2) al reaccionar con metales como Al, Zn y Mg – X representa cualquier elemento- • Zn + 2 HX Zn. X 2 + H 2 • Cambian de color a sustancias indicadoras de p. H – como lo vimos en el experimento- • Cuando reaccionan con carbonatos (CO 3 -2) y bicarbonatos (HCO 3 -) desprenden CO 2 (g) • Cuando reaccionan con una Base, forman SAL y AGUA • En solución acuosa conducen la electricidad (son electrolitos) • Valor de p. H menor a 7

Características Generales de las Bases • En soluciones diluidas tienen sabor amargo • Cuando reaccionan con un Ácido, forman SAL y AGUA • Cambian de color a sustancias indicadoras de p. H – como • Muchas bases son causticas (queman tejidos orgánicos) • Disuelven grasas de la piel • Al tacto son jabonosas • Valor de p. H Mayor a 7
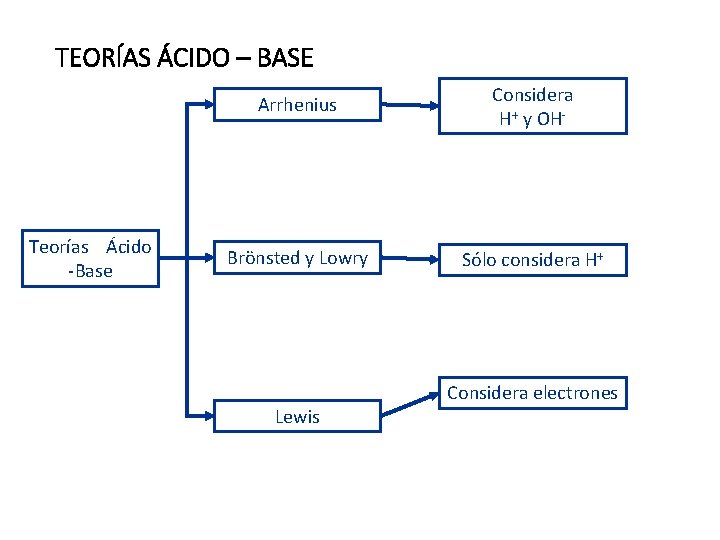
TEORÍAS ÁCIDO – BASE Arrhenius Teorías Ácido -Base Brönsted y Lowry Lewis Considera H+ y OH- Sólo considera H+ Considera electrones
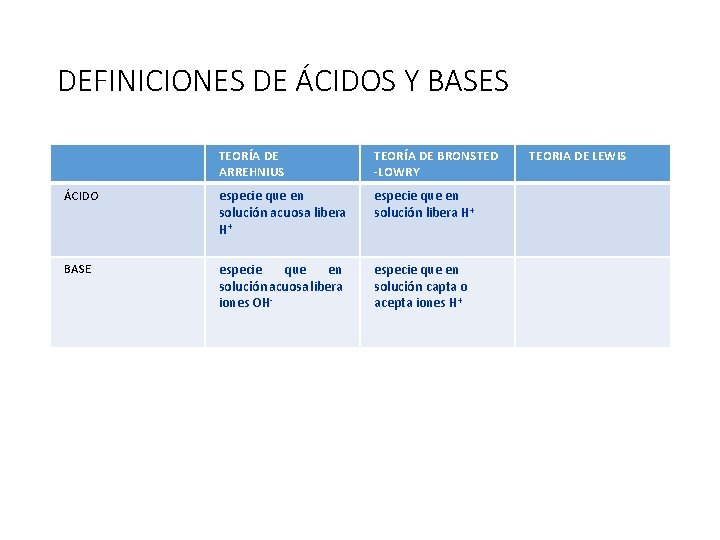
DEFINICIONES DE ÁCIDOS Y BASES TEORÍA DE ARREHNIUS TEORÍA DE BRONSTED -LOWRY ÁCIDO especie que en solución acuosa libera H+ especie que en solución libera H+ BASE especie que en solución acuosa libera iones OH- especie que en solución capta o acepta iones H+ TEORIA DE LEWIS

TEORÍA DE S. ARRHENIUS § Ácido: especie que en solución acuosa libera H+ HBr(ac) H+(ac) + Br-(ac) § Base: especie que en solución acuosa libera iones OHNa. OH(ac) Na+(ac) + OH-(ac) § Un ácido al reaccionar con una base, forman una sal y agua: HCl + Na. OH Na. Cl + H 2 O

TEORÍA DE BRÖNSTED Y LOWRY § Ácido: especie que en solución libera H+ HNO 3 H+ + NO 3 - § Base: especie que en solución capta o acepta iones H+ HSO 3 - + H+ H 2 SO 3 En esta teoría sólo se consideran los protones (H+) y no se limita al solvente agua, es decir, puede ser considerado cualquier solvente

Ejercicios de Práctica: § Identifique, de acuerdo a las teorías ya revisadas, si las siguientes especies son ácidos o bases 1. Solvente agua: HNO 2 H+ + NO 2 - 2. Solvente agua: H 3 PO 4 3 H+ + PO 4 -3 3. Solvente agua: Ca(OH)2 Ca+2 + 2 OH- 4. Solvente etanol: HCOOH H+ + HCOO- 5. Solvente etanol: NH 3 + H+ NH 4+

RESPUESTAS § Identifique, de acuerdo a las teorías ya revisadas, si las siguientes especies son ácidos o bases Arrhenius Brönsted y Lowry 1. Solvente agua: HNO 2 H+ + NO 2 - ÁCIDO 2. Solvente agua: H 3 PO 4 3 H+ + PO 4 -3 ÁCIDO 3. Solvente agua: Ca(OH)2 Ca+2 + 2 OH- BASE NO APLICA 4. Solvente etanol: HCOOH H+ + HCOO- NO APLICA ÁCIDO 5. Solvente etanol: NH 3 + H+ NH 4+ NO APLICA BASE

Pares Conjugados de Ácidos y Bases ÁCIDO H+ + BASE Par Conjugado § Un ácido y una base se consideran conjugados, cuando su estructura química difiere sólo en un H+ HF H+ + F- § HF es el ácido y F- es su base conjugada § F- es la base y HF es su ácido conjugado § NO ES CORRECTO DECIR: HF es el ácido conjugado y F- la base conjugada. El término conjugado sólo se ocupa al final de la frase
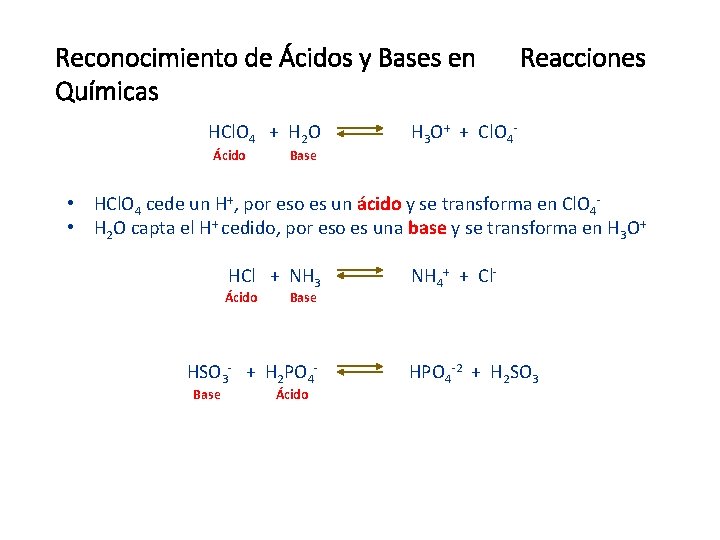
Reconocimiento de Ácidos y Bases en Químicas Reacciones HCl. O 4 + H 2 O H 3 O+ + Cl. O 4Ácido Base • HCl. O 4 cede un H+, por eso es un ácido y se transforma en Cl. O 4 • H 2 O capta el H+ cedido, por eso es una base y se transforma en H 3 O+ HCl + NH 3 NH 4+ + Cl- Ácido Base HSO 3 - + H 2 PO 4 - HPO 4 -2 + H 2 SO 3 Base Ácido
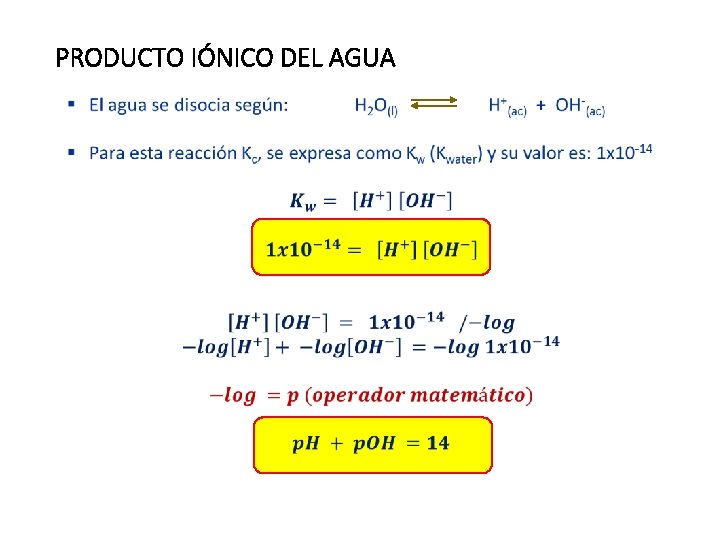
PRODUCTO IÓNICO DEL AGUA
![Ejercicios de Práctica: § Calcule la [H+] o [OH-] según corresponda: a) [H+] = Ejercicios de Práctica: § Calcule la [H+] o [OH-] según corresponda: a) [H+] =](http://slidetodoc.com/presentation_image/25d78d21f163759744b221702104e009/image-13.jpg)
Ejercicios de Práctica: § Calcule la [H+] o [OH-] según corresponda: a) [H+] = 1 x 10 -5 [OH-] = 1 x 10 -9 b) [H+] = 1 x 10 -12 [OH-] = 1 x 10 -2 c) [H+] = 1 x 10 -11 [OH-] = 1 x 10 -3 d) [H+] = 1 x 10 -6 [OH-] = 1 x 10 -8 § Calcule la p. H o p. OH según corresponda: a) p. H = 10 p. OH = 4 b) p. H = 1 p. OH = 13 c) p. OH = 14 p. H = 0
![ESCALA DE p. H neutro [H+] = [OH-] p. H ácido [H+] > [OH-] ESCALA DE p. H neutro [H+] = [OH-] p. H ácido [H+] > [OH-]](http://slidetodoc.com/presentation_image/25d78d21f163759744b221702104e009/image-14.jpg)
ESCALA DE p. H neutro [H+] = [OH-] p. H ácido [H+] > [OH-] p. H básico o alcalino [H+] < [OH-] p. H = -log [H+] y p. OH = -log [OH-] § Se tiene que: [H+] = 1 x 10 -p. H [OH-] = 1 x 10 -p. OH § • • Así entonces: [H+] = 0, 001 = 1 x 10 -3 [H+] = 0, 00001 = 1 x 10 -5 [OH-] = 0, 01 = 1 x 10 -2 [OH-] = 0, 1 = 1 x 10 -1 p. H = 3 p. H = 5 p. OH = 2 p. OH = 11 p. OH = 9 p. H = 12 p. H = 13
- Slides: 14