re Biyosensr Yapm ve Uygulamas Sorumlu retim yesi

Üre Biyosensörü Yapımı ve Uygulaması Sorumlu Öğretim Üyesi : Prof. Dr. İbrahim Işıldak Sorumlu Öğretim Elemanları : Arş. Gör. Rıdvan Yıldırım Grup 4 Halime Mıh A. Delal Tüy Sedef Kaptan Seda Acar Merve Mumay İstanbul, 2013 Elif Ebru Altunsoy İrem Eldemir Işıl Aslan Hatice Oruçoğlu İnas Özcan

İçerik § Biyosensörler § Üre Biyosensörü § Deneyin Amacı § Deneyin Yapılışı § Metod § Üre Biyosensörü Düzeneği § Grafik / Denklem / Hesaplamalar § Sonuçlar § Tartışma ve Yorum § Kaynaklar İstanbul, 2013

Biyosensörler § Biyosensörler biyolojik tepkimelerde hedef analitleri denetlemek için kullanılan küçük algılayıcı cihazlardır. § Transducer (çevirici) ve reseptör kısmından oluşur. § Reseptör kısmın etkileştiği hedef moleküllere ise ‘Analit’ denir. İstanbul, 2013

Biyosensörler § Reseptör kısmında immobilize edilmiş ligandlar bulunabilir. § Ligandlar ve analitler arasında bir etkileşim meydana gelir. İstanbul, 2013
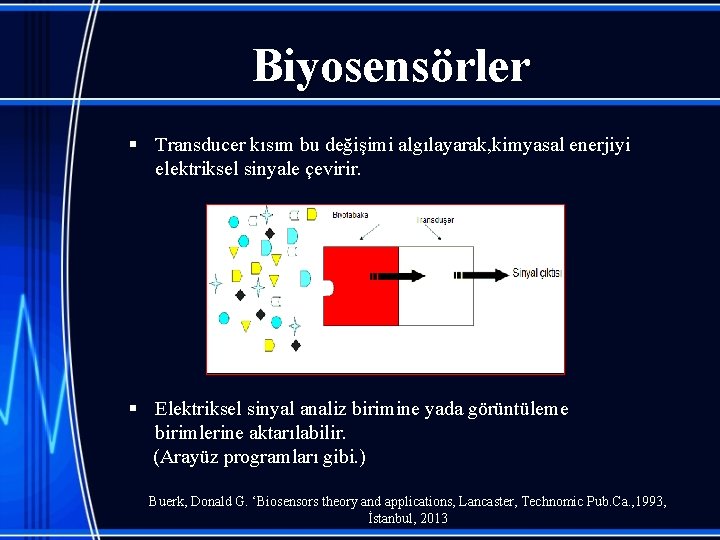
Biyosensörler § Transducer kısım bu değişimi algılayarak, kimyasal enerjiyi elektriksel sinyale çevirir. § Elektriksel sinyal analiz birimine yada görüntüleme birimlerine aktarılabilir. (Arayüz programları gibi. ) Buerk, Donald G. ‘Biosensors theory and applications, Lancaster, Technomic Pub. Ca. , 1993, İstanbul, 2013

Biyosensörlerin Uygulama Alanları • Klinik diyagnostik, biyomedikal sektör • • Proses kontrolü: Biyoreaktör kontrol ve analitiği, Gıda üretim ve analizi • • Tarla tarımı, bağ– bahçe tarımı ve veterinerlik • • Bakteriyal ve viral diyagnostik • • İlaç analizi • • Endüstriyel atık su kontrolü • • Çevre koruma ve kirlilik kontrolü • • Maden işletmelerinde toksik gaz analizleri • • Askeri uygulamalar “Biyosensörler” http: //tr. scribd. com/doc/8604698/BYOSENSORLER<alındı: 29. 04. 2013 İstanbul, 2013

İdeal bir biyosensörün sahip olması gereken özellikler • • • Seçicilik Kullanım Ömrü Kalibrasyon Gereksinmesi Tekrarlanabilirlik Stabilite Yüksek Duyarlılık Yeterli Düzeyde Tayin Sınırı Geniş Ölçüm Aralığı Hızlı Cevap Zamanı Hızlı Geriye Dönme Zamanı Basitlik ve Ucuzluk Küçültülebilirlik ve Sterilize edilebilirlik İstanbul, 2013

Biyosensörler BİYOSENSÖR GRUBU KAPSADIĞI ANALİZ ALANI Enzim sensörleri Küçük moleküllü organik ve anorganik maddeler( ilaçlar, gida maddeleri, vitaminler, antibiyotikler. . ) Mikrobiyal sensörler Enzim sensörlerin kapsadığı alanlar +BOD, Toksisite, Mutajenite DNA – Sensörleri Virusler, patojen mikroorganizmalar Immuno Sensörler Virusler, patojen mikroorganizmalar + ksenobiyotikler web. iyte. edu. tr/biotech/BTEC 585_Biosensors_Syllabus_YENI. pdf<alındı: 29. 04. 2013 İstanbul, 2013

Biyosensörler İmmobilizasyon ; § Biyoaktif bileşenler reseptör yüzeyine hapsedilirken farklı immobilizasyon yöntemlerinden yararlanılabilir. § Biyoaktif bileşen, sensör olarak da adlandırabileceğimiz temel iletici sistem üzerine; Ø Ø Fiziksel olarak tutturulabilir, Jel içinde veya polimer matrikste tutuklanabilir, Elektrot yüzeyinde biriktirilebilir, Çapraz bağlanarak immobilize edilebilir. İstanbul, 2013

Üre Biyosensörü § Çözeltilerdeki üre konsantrasyonu tayininde kullanılan sensörlerdir. § Potansiyometrik ölçüm esasına dayanır. § Çözeltiye daldırılan iki elektrod arasındaki potansiyel farkının ölçülmesine dayalı konsantrasyon tayini yapılır. İstanbul, 2013

Üre Biyosensörü § Potansiyometri ölçümünde kullanılan Nernst Eşitliği şu şekildedir: E = E 0 – 2. 303 (RT/n. F) log a. H+ Burada; R = Gaz Sabiti, 8, 314 atm. L/K-1 mol-1 T = Kelvin n = Transfer Edilen Elektronlar F = Faraday Sabit. i, 96500 kulon İstanbul, 2013

Üre Biyosensörü § Burada analitin potansiyometrisi ölçülerek Nernst denkleminde yerine konulur. E = E 0 – 2. 303 (RT/n. F) log a. H+ § Daha sonra grafiğe aktarılarak miktarını veya konsantrasyonunu bilmediğimiz çözeltinin konsantrasyonu bulunabilir. O. Çubuk, Bütünüyle Katı-Hal Mikro Enzim Sensorler Ve Uygulamaları, Doktora Tezi, Samsun, 2007 İstanbul, 2013

Deneyin Amacı § Katı hal kontakt PVC-NH 2 membranlı p. H’a duyarlı bir üreaz biyosensörü yapmak, § Bu biyosensörün bir uygulamasını gerçekleştirmektir. İstanbul, 2013

Deneyin Yapılışı Çözelti ve Kimyasallar Solüsyon-1 0. 25 g glutaraldehit (% 2. 5’lik glutaraldehit) 9. 25 m. L su Solüsyon-2 10 m. L 0. 05 M fosfat tamponu (0. 05 M fosfat tamponu p. H 7) 90 m. L su Solüsyon-3 1 mg Üreaz (Üreaz çözeltisi) 20 µl 0. 05 M fosfat tamponu (p. H 7) Solüsyon-4 0. 1 , 0. 001 , 0. 00001 M üre çözeltileri İstanbul, 2013

Metod Üre Biyosensörü hazırlanması ; § Katı hal kontakt PVC-NH 2 membranlı p. H’a duyarlı elektrod üreaz enzim çözeltisine daldırıldı. § % 2. 5’lik glutaraldehit çözeltisine daldırılarak 15 -20 dk beklenildi. § Soğuk su ile yıkama yapıldı. § Bir daha üreaz çözeltisine daldırılıp çıkarılır, çapraz bağlanma için 15 saat +4°C de bekletildi. bağlanma için 15 saat +4 İstanbul, 2013

Metod Üre Biyosensörü hazırlanması ; § Elektrod 0. 05 M fosfat tamponu ile yıkanır. § Tampon çözeltisi içerisinde +4°C de saklanır. İstanbul, 2013

Metod Üre Biyosensörü için kalibrasyon eğrileri şu şekilde edilir ; § Biyosensör ve referans elektrod, potansiyometreye bağlanarak uçları örneğe daldırılır. § Değer okunarak kaydedilir, her örnek için tekrarlandı. § Değerler tabloya aktarılarak ölçülen değerlerin ortalaması alınarak potansiyele karşı üre konsantrasyonu grafiği çizildi. İstanbul, 2013

Metod Ø Bunların dışında örnek üre çözeltisinin bilinmeyen konsantrasyonunun belirlenmesi işlemi gerçekleştirildi Bu işlem ; 1. Elektrotlar çözeltiye daldırılıp potansiyel okundu, 2. Çıkartılan kalibrasyon eğrisi kullanılarak bu çözeltinin konsantrasyonu belirlendi. § Aynı işlem p. H elektrot kullanılarak ta yapıldı ve buradan p. H’ a karşı üre konsantrasyonu grafiği çizildi. İstanbul, 2013

Üre Biyosensörü Düzeneği, Deney Koşulları ve Güvenlik Kaygısı • Deneyde kullanılacak kimyasal maddelerin verebilecekleri zarar karşı eldiven kullanılmalı ve önlük giyilmelidir. • Farklı konsantrasyonlardaki çözeltilerden ölçüm yapılırken çözeltilerin dökülmemesine dikkat edilmelidir. • Deneyde kullanılan elektrotlar hassas ölçüm yaptığından çözeltiler deney düzeneğine dikkatli ve düzgün bir biçimde yerleştirilmelidir. İstanbul, 2013
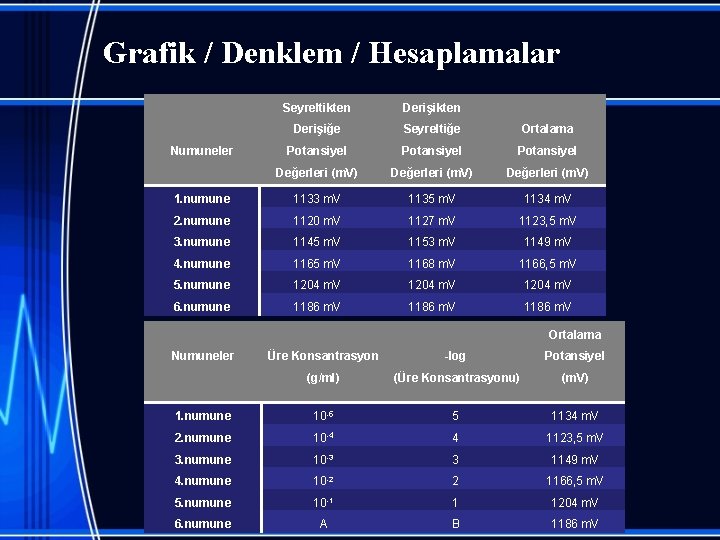
Grafik / Denklem / Hesaplamalar Seyreltikten Derişikten Derişiğe Seyreltiğe Ortalama Numuneler Potansiyel Değerleri (m. V) 1. numune 1133 m. V 1135 m. V 1134 m. V 2. numune 1120 m. V 1127 m. V 1123, 5 m. V 3. numune 1145 m. V 1153 m. V 1149 m. V 4. numune 1165 m. V 1168 m. V 1166, 5 m. V 5. numune 1204 m. V 6. numune 1186 m. V Ortalama Numuneler Üre Konsantrasyon -log Potansiyel (g/ml) (Üre Konsantrasyonu) (m. V) 1. numune 10 -5 5 1134 m. V 2. numune 10 -4 4 1123, 5 m. V 3. numune 10 -3 3 1149 m. V 4. numune 10 -2 2 1166, 5 m. V 5. numune 10 -1 1 1204 m. V 6. numune A B 1186 m. V
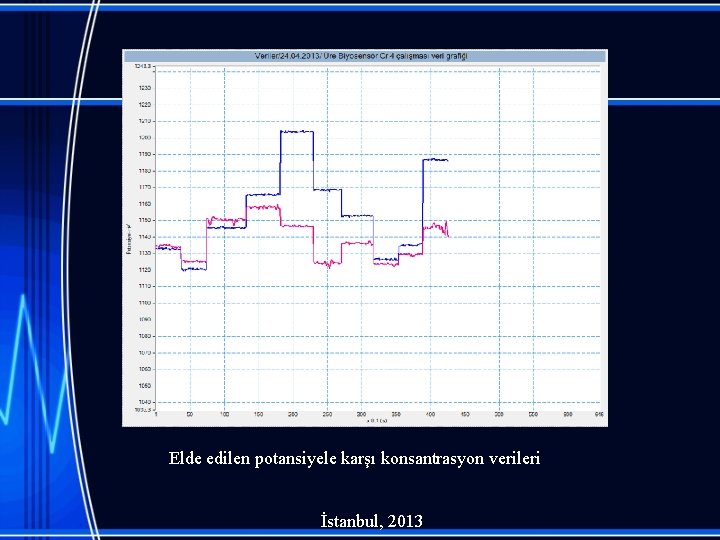
Elde edilen potansiyele karşı konsantrasyon verileri İstanbul, 2013
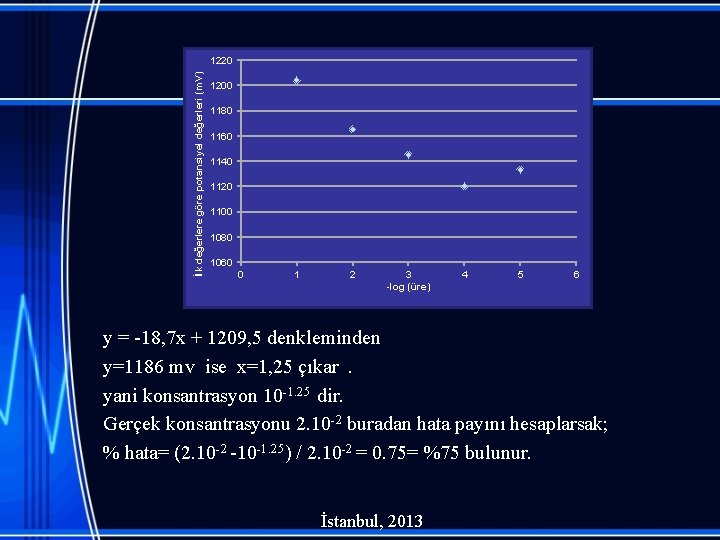
İlk değerlere göre potansiyel değerleri (m. V) 1220 1200 1180 1160 1140 1120 1100 1080 1060 0 1 2 3 -log (üre) 4 5 6 y = -18, 7 x + 1209, 5 denkleminden y=1186 mv ise x=1, 25 çıkar . yani konsantrasyon 10 -1. 25 dir. Gerçek konsantrasyonu 2. 10 -2 buradan hata payını hesaplarsak; % hata= (2. 10 -2 -10 -1. 25) / 2. 10 -2 = 0. 75= %75 bulunur. İstanbul, 2013
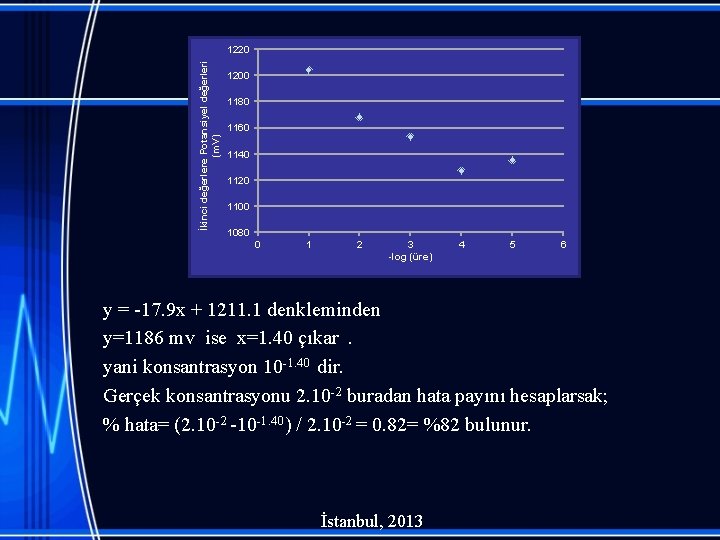
İkinci değerlere Potansiyel değerleri (m. V) 1220 1200 1180 1160 1140 1120 1100 1080 0 1 2 3 -log (üre) 4 5 6 y = -17. 9 x + 1211. 1 denkleminden y=1186 mv ise x=1. 40 çıkar . yani konsantrasyon 10 -1. 40 dir. Gerçek konsantrasyonu 2. 10 -2 buradan hata payını hesaplarsak; % hata= (2. 10 -2 -10 -1. 40) / 2. 10 -2 = 0. 82= %82 bulunur. İstanbul, 2013
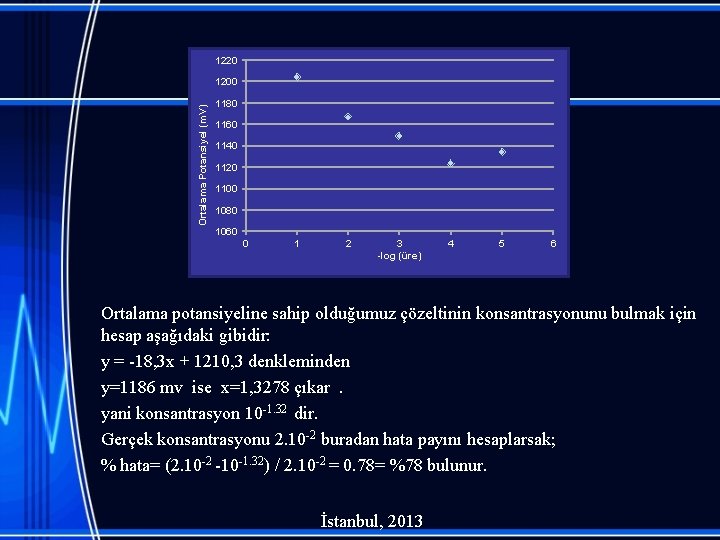
1220 Ortalama Potansiyel (m. V) 1200 1180 1160 1140 1120 1100 1080 1060 0 1 2 3 -log (üre) 4 5 6 Ortalama potansiyeline sahip olduğumuz çözeltinin konsantrasyonunu bulmak için hesap aşağıdaki gibidir: y = -18, 3 x + 1210, 3 denkleminden y=1186 mv ise x=1, 3278 çıkar . yani konsantrasyon 10 -1. 32 dir. Gerçek konsantrasyonu 2. 10 -2 buradan hata payını hesaplarsak; % hata= (2. 10 -2 -10 -1. 32) / 2. 10 -2 = 0. 78= %78 bulunur. İstanbul, 2013

Sonuçlar Deneyde yapılan katı-hal kontakt PVC-NH 2 membranlı p. H’a duyarlı üreaz biyosensörü ile 4 farklı konsantrasyonlardaki çözeltilerin potansiyellerinin ölçümü gerçekleştirildi. Potansiyeller ile konsantrasyonlar arasındaki ilişkinin iyi bir şekilde belirlenebilmesi için seyreltikten derişiğe, derişikten seyreltiğe olmak üzere 2 kez ölçüm yapıldı. Bu değerlerin ortalaması kullanılarak kalibrasyon eğrisi çizildi. Bu kalibrasyon eğrisi dikkate alınarak konsantrasyonu bilinmeyen çözeltilerin konsantrasyon değerleri hesaplandı. Bu ölçümler ve hesaplamalar sonucunda konsantrasyon ile potansiyel değerler arasında ters orantı olduğu görüldü. İstanbul, 2013

Tartışma ve Yorum Potansiyometrik yöntemler, bir çözeltiye daldırılan iki elektrot arasındaki gerilim farkının ölçülmesi ilkesine dayanır. Elektrotlar ve elektrotların daldırıldığı çözelti bir elektrokimyasal hücre oluşturur. Elektrotlar arasındaki gerilim farkı bir p. H/m. V metre kullanılarak ölçülür. Elektrotlardan biri karşılaştırma elektrotu olup bu elektrodun yarı hücre gerilimi sabittir. Çalışma elektrodu olarak tanımlanan ikinci elektrodun yarı hücre gerilimi ise çözeltideki türlerin aktiflikleriyle değişir. Yarı hücre gerilimleri, gerilimi sıfır olan standart hidrojen elektroduna (SHE) göre ölçülür ve tablolarda da bu değerle belirtilir. Potansiyometride bir elektrotun potansiyeli içine daldırıldığı çözeltide bulunan, iyon veya iyonların aktivitelerine bağlıdır. Bu iyon veya iyonlar elektrot elementinin tuzlarından gelebileceği gibi, elektrot elementiyle ilgisi olmayan başka bir elementin tuzlarından da gelebilir. Potansiyometri bu temel üzerine kurulmuştur. İstanbul, 2013

Tartışma ve Yorum Referens elektrot potansiyeli, daldırıldığı çözeltiden etkilenmez. Potansiyeli sıcaklık değişmediği sürece sabit kalır (sıcaklık yükselmesi potansiyelin düşmesine neden olur). İndikatör elektrot daldırıldığı çözeltide bulunan elektroaktif iyonun konsantrasyonuna bağlı olarak bir potansiyel gösterir. Bu özellik Nernst denklemiyle gösterilir. a. A + b. B + ne- -----> c. C + d. D E = E 0 – (RT/n. F). ln[(C)c. (D)d / (A)a. (B)b] E = Hücre potansiyeli E 0 = Standart hücre potansiyeli (birim değişimde ve 1 atm basınçtaki hücre potansiyeli) n = Transfer edilen elektron sayısı R = Gaz sabiti 8. 314 J / K. mol T = Mutlak sıcaklık 298 K F = Faraday sabiti 96500 coulomb Sabitler yerine konulursa; E=E 0 -0, 059/n. log a. H+ [10] eşitliği elde edilir. Elde edilen veriler yerlerine yerleştirilerek denklemde kalibrasyon eğrisi oluşturulur. Kalibrasyon eğrisinden koralesyon katsayısı belirlenir. Belirlenen değer ne kadar bire yakın ise yaptığımız deneyin doğruluğu o kadar artar. İstanbul, 2013

Tartışma ve Yorum Deney verilerimize göre çizilen kalibrasyon eğrisinin kolerasyon katsayısının tam olarak 1 çıkmamasının birçok sebebi olabilir. Bu sebeplerin bazıları laboratuvar ortamından kaynaklanmaktadır. Deney ortamının temiz olup olmaması, hazırlanan çözeltilerin saklanması sırasında sıcaklık değerlerinin optimum seviyede olup olmaması ortam kaynaklı hatalardan bazılarıdır. Değerlerin hatalı çıkmasındaki bir diğer sebep de kullanılan elektrotun eskimesi yani hassaslığını ve spesifikliğini kaybetmesi olabilir. Her elektrotun bir kullanım süresi vardır. Bu süre dolduğunda elektrot hatalı değerler vermeye başlar. Böyle durumlarda elektrotun yenilenmesi gerekir. Deneyde okuduğumuz değerlerin hatalı çıkmasının bazı nedenleri de deney esnasında yapılan bireysel kaynaklı hatalar olduğu söylenebilir. İstanbul, 2013

Tartışma ve Yorum Bu bireysel hatalardan biri ölçüm sırasında elektrotun çözeltilere hızlı daldırılmasıyla elektrot yüzeyinde oluşan hava kabarcıkları olabilir. Böylece elektrot potansiyel değerini hatalı okuyabilir. Bir başka bireysel hata da elektrotun çözelti içine daldırıldığı yüksekliklerin farklı olması olabilir. Bu da hatalı okumalara neden olabilir. Başka bir hata da elektrotun çözeltiden çıkarıldıktan sonra iyi temizlenmemesi olabilir. Okuma sırası seyreltik çözeltiden derişik çözeltiye doğru olduğu zaman bu olay fazla sıkıntı yaratmaz fakat derişik çözeltiden seyreltik çözeltiye olduğu zaman elektrot uçlarının çok iyi temizlenmesi gerekmektedir. Çünkü önceki çözeltiden elektrot ucunda kalan bir madde okumanın hatalı olmasına neden olabilir. İstanbul, 2013
![KAYNAKLAR [1] Buerk, Donald G. ‘Biosensors theory and applications, Lancaster, Technomic Pub. Ca. , KAYNAKLAR [1] Buerk, Donald G. ‘Biosensors theory and applications, Lancaster, Technomic Pub. Ca. ,](http://slidetodoc.com/presentation_image/09cae44227d84ab663135d434b3c3bd9/image-30.jpg)
KAYNAKLAR [1] Buerk, Donald G. ‘Biosensors theory and applications, Lancaster, Technomic Pub. Ca. , 1993 [2] “Biyosensörler” http: //tr. scribd. com/doc/8604698/BYOSENSORLER<alındı: 29. 04. 2013> [3] Yar. Doç. M. F. Abasıyanık, E. Şakalar, M. Şenel, “Biyosensörlere Genel Bir Bakış Ve Biyosavunmada Kullanılan Biyosensörler”, Fatih Üniversitesi, Genetik Ve Biyomühendislik Bölümü <alındı: 29. 04. 2013> [4] “Biyosensör” http: //pharm. ege. edu. tr/pp/ozsozs/biosensor. pdf <alındı: 29. 04. 2013> [5]web. iyte. edu. tr/biotech/BTEC 585_Biosensors_Syllabus_YENI. pdf<alındı: 29. 04. 2013 [6] O. Çubuk, Bütünüyle Katı-Hal Mikro Enzim Sensorler Ve Uygulamaları, Doktora Tezi, Samsun, 2007 [7] Msc. Fateme Frootan, Kompozit Ph Elektrodu, 2012 [8] A. Baran Teke, Farklı Yöntemlerle Üreaz Enzim Çiftinin İmmobilizasyonu Ve Sistemik Kan Üre Düzeyini Düşürebilme Olanaklarının Araştırılması, 2008 [9] “Potansiyometrik Yöntemler” web. itu. edu. tr/~ozcanm/kim/Sunuelektro. pps <alındı: 29. 04. 2013> [10] “Potansiyometri” http: //www. wikiturk. net/Madde/36437/potansiyometri <alındı: 29. 04. 2013> İstanbul, 2013

İstanbul, 2013
- Slides: 31