rda energii baterie akumulatory superkondensatory Zygmunt Kubiak Instytut

Źródła energii baterie, akumulatory, superkondensatory Zygmunt Kubiak Instytut Informatyki Politechnika Poznańska Źródła: Elektronika praktyczna, Elektronik i inne

Źródła energii Elektrochemiczne źródła energii elektrycznej Ogniwa elektryczne (łączone w zespoły – baterie) Akumulatory - źródła zasilania wielokrotnego ładowania Oznaczenia baterii wg IEC (technologia wykonania) (brak) - ogniwo cynkowo-grafitowe (anoda – cynk; katoda – tlenek manganu (IV)/grafit; elektrolit – chlorek amonu lub cynku) A – ogniwo cynkowo powietrzne (anoda - cynk; katoda – tlen/węgiel; elektrolit – chlorek amonu lub cynku) B - ogniwo litowo-węglowe (anoda - lit; katoda - monofluorek węgla; elektrolit organiczny); napięcie nominalne 3 V C - ogniwo litowo-manganowe (anoda - lit; katoda- tlenek manganu(IV); elektrolit organiczny); napięcie nominalne 3 V E - ogniwo litowo-tionylowe (anoda - lit; katoda - chlorek tionylu); elektrolit niewodny nieorganiczny) 04 -2017 Zygmunt Kubiak 2

Źródła energii Oznaczenia baterii wg IEC (technologia wykonania) F - ogniwo litowo-żelazowe (poza normą) H - ogniwo niklowo-metalowo-wodorkowe ładowalne (poza normą) ; (akumulator Ni. MH); napięcie nominalne 1, 2 V K - ogniwo niklowo-kadmowe ładowalne (poza normą) ; (akumulator Ni-CD); napięcie nominalne 1, 2 V L - ogniwo alkaliczno-braunsztynowe (anoda - cynk; katoda tlenek manganu(IV); elektrolit - wodorotlenek metalu alkalicznego) M – (obecnie) ogniwo litowe ładowalne P - ogniwo alkaliczno-powietrzne (anoda - cynk; katoda tlen/węgiel; elektrolit - wodorotlenek metalu alkalicznego); napięcie nominalne 1, 4 V S - ogniwo srebrowo-cynkowe (anoda - cynk; katoda - tlenek srebra(I) lub tlenek srebra(II); elektrolit - wodorotlenek potasu) Z - ogniwo niklowo-manganowe (Ni-Mn) 04 -2017 Zygmunt Kubiak 3

Źródła energii Baterie Ogniwo Leclanchego – najtańsze, popularne ogniwa galwaniczne Ogniwo galwaniczne jednorazowe; anoda – pojemnik cynkowy (Zn); katoda – sproszkowany tlenek manganu (IV) (Mn. O 2); elektrolit – chlorek amonu (NH 4 Cl - salmiak) Napięcie nominalne 1, 5 V Dla urządzeń o małym i średnim poborze prądu (100 – 300 m. A) 1 - metalowe wieczko (+) 2 - grafitowy pręt (dodatnia elektroda) 3 - cynkowy pojemnik (ujemna elektroda) 4 - tlenek manganu(IV) 5 - pasta chlorku amonu (elektrolit) 6 - metalowe denko (-) 04 -2017 Zygmunt Kubiak 4
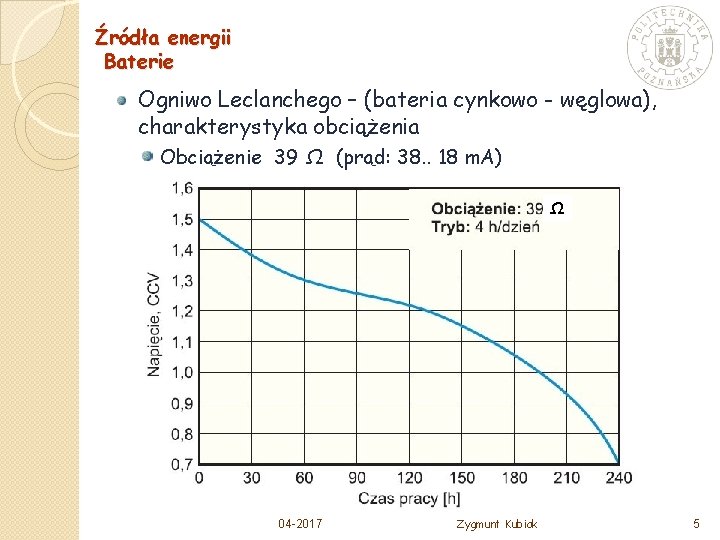
Źródła energii Baterie Ogniwo Leclanchego – (bateria cynkowo - węglowa), charakterystyka obciążenia Obciążenie 39 Ω (prąd: 38. . 18 m. A) Ω 04 -2017 Zygmunt Kubiak 5
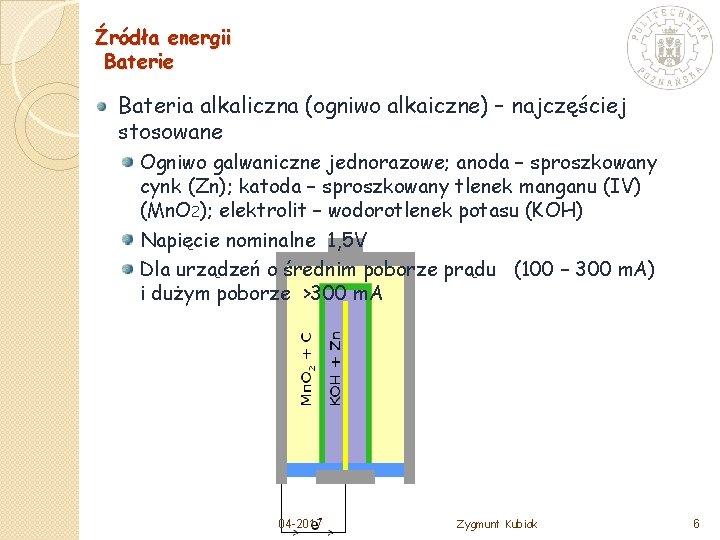
Źródła energii Baterie Bateria alkaliczna (ogniwo alkaiczne) – najczęściej stosowane Ogniwo galwaniczne jednorazowe; anoda – sproszkowany cynk (Zn); katoda – sproszkowany tlenek manganu (IV) (Mn. O 2); elektrolit – wodorotlenek potasu (KOH) Napięcie nominalne 1, 5 V Dla urządzeń o średnim poborze prądu (100 – 300 m. A) i dużym poborze >300 m. A 04 -2017 Zygmunt Kubiak 6
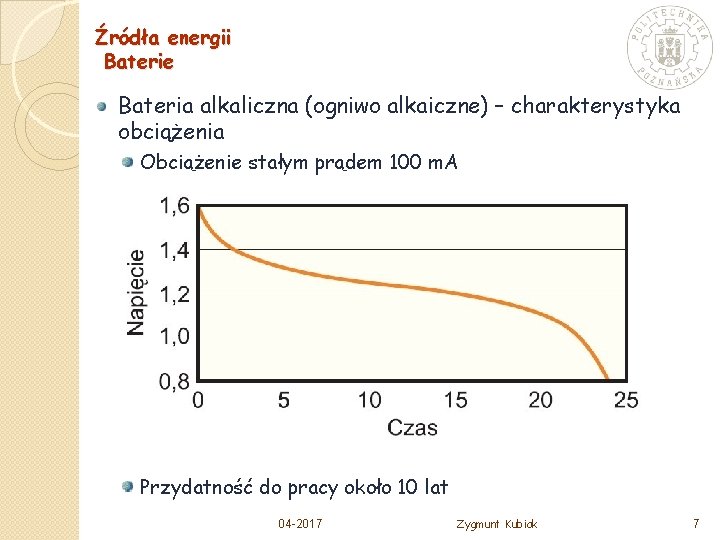
Źródła energii Baterie Bateria alkaliczna (ogniwo alkaiczne) – charakterystyka obciążenia Obciążenie stałym prądem 100 m. A Przydatność do pracy około 10 lat 04 -2017 Zygmunt Kubiak 7
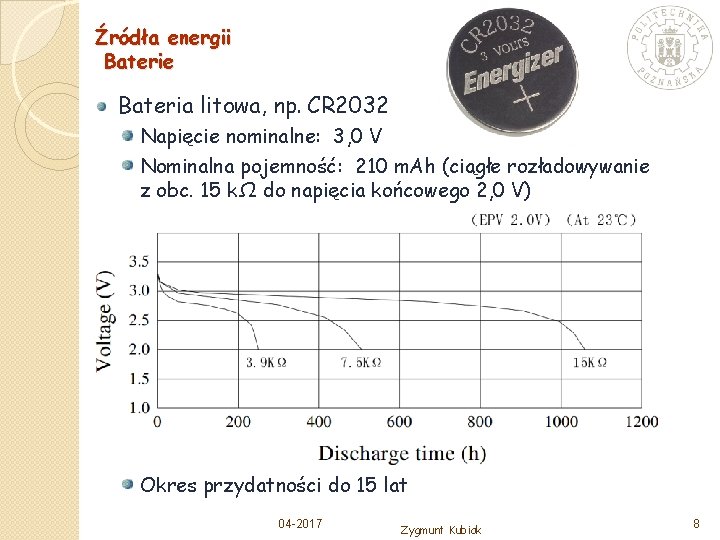
Źródła energii Baterie Bateria litowa, np. CR 2032 Napięcie nominalne: 3, 0 V Nominalna pojemność: 210 m. Ah (ciągłe rozładowywanie z obc. 15 kΩ do napięcia końcowego 2, 0 V) Okres przydatności do 15 lat 04 -2017 Zygmunt Kubiak 8
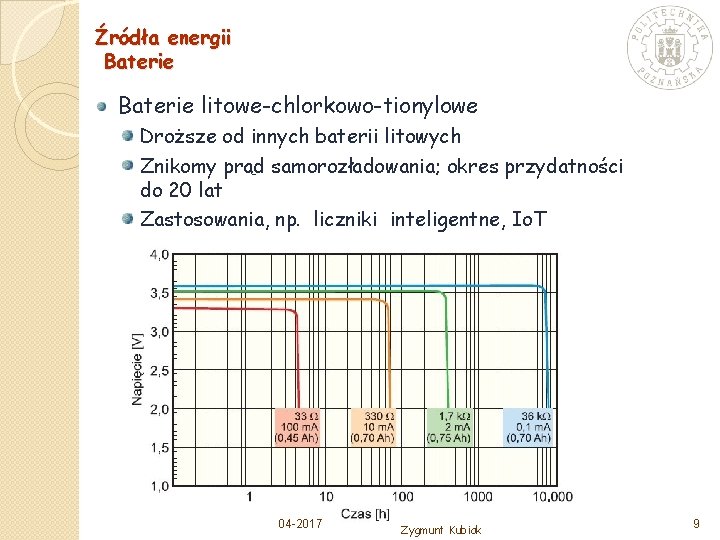
Źródła energii Baterie litowe-chlorkowo-tionylowe Droższe od innych baterii litowych Znikomy prąd samorozładowania; okres przydatności do 20 lat Zastosowania, np. liczniki inteligentne, Io. T 04 -2017 Zygmunt Kubiak 9
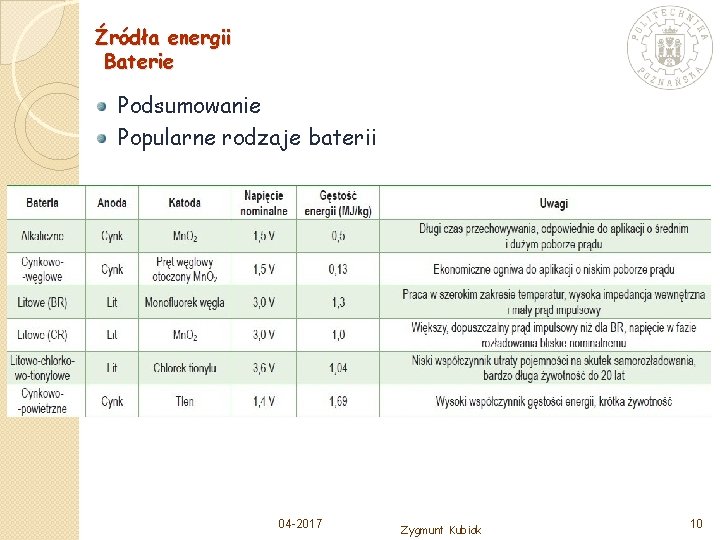
Źródła energii Baterie Podsumowanie Popularne rodzaje baterii 04 -2017 Zygmunt Kubiak 10

Źródła energii Akumulatory kwasowe i zasadowe Akumulatory kwasowo-ołowiowe (1859 r. ) Akumulatory niklowo-żelazowe (1901 r. )– były stosowane w kolejnictwie, górnictwie Akumulatory niklowo-kadmowe (Ni. Cd); anoda – kadm gąbczasty; katoda – oksowodorek niklu(III)(Ni. OOH); elektrolit – wodorotlenek potasu (KOH); napięcie nominalne 1, 2 V; odporne na przeładowanie i całkowite rozładowanie; duże prądy ładowania i rozładowania; wada – efekt pamięci, trujący kadm – ograniczenie w EU Akumulatory wodorkowe (niklowo-metalowo-wodorkowe) (Ni. MH) 1991 r. ; większa gęstość energii niż dla Ni. Cd Akumulatory niklowe – duże prądy samorozładowania Akumulatory niklowe – mogą pracować buforowo z małym prądem podładowania około 0, 01 C (10 m. A/1 Ah) 04 -2017 Zygmunt Kubiak 11
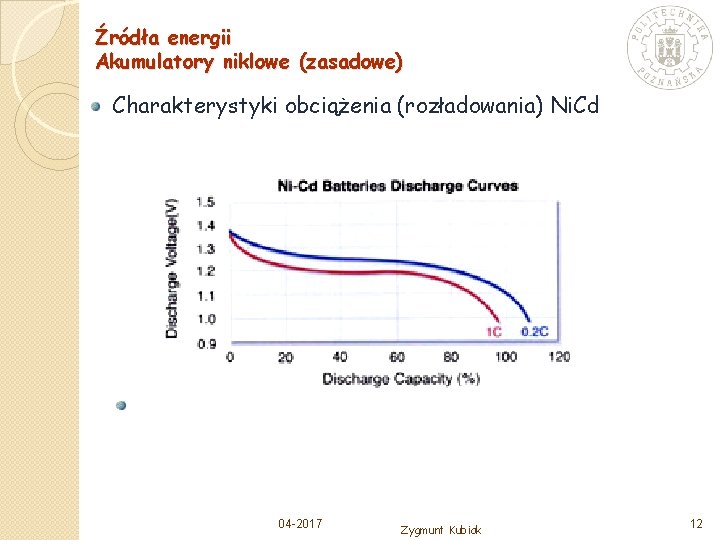
Źródła energii Akumulatory niklowe (zasadowe) Charakterystyki obciążenia (rozładowania) Ni. Cd 04 -2017 Zygmunt Kubiak 12
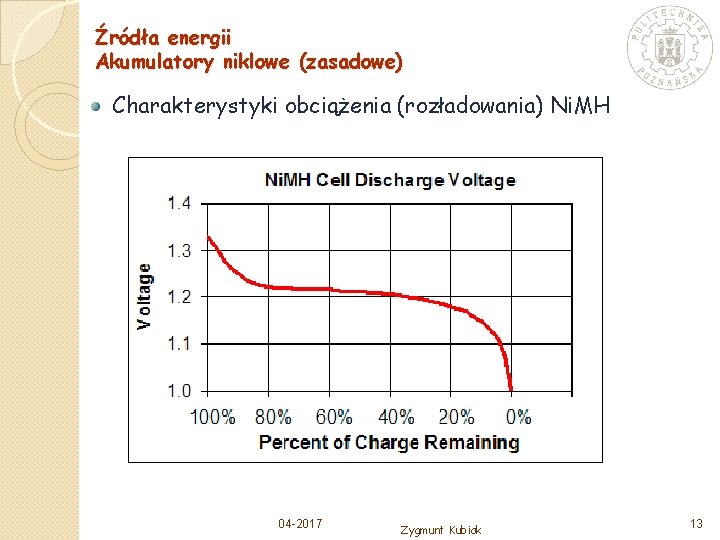
Źródła energii Akumulatory niklowe (zasadowe) Charakterystyki obciążenia (rozładowania) Ni. MH 04 -2017 Zygmunt Kubiak 13
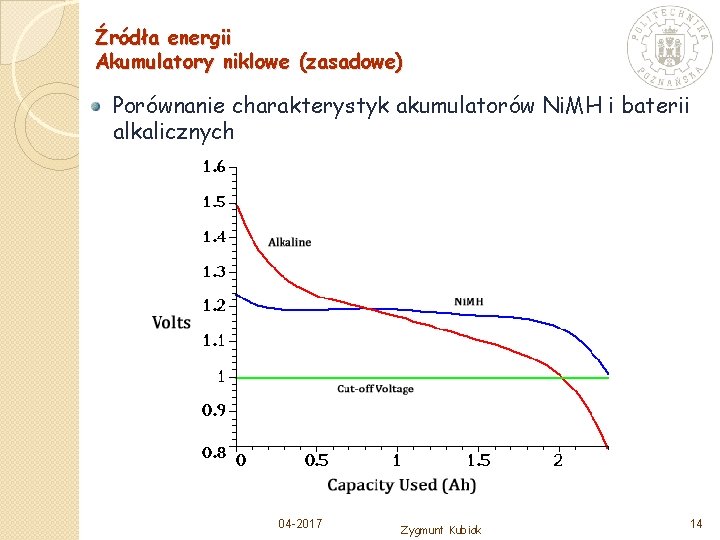
Źródła energii Akumulatory niklowe (zasadowe) Porównanie charakterystyk akumulatorów Ni. MH i baterii alkalicznych 04 -2017 Zygmunt Kubiak 14
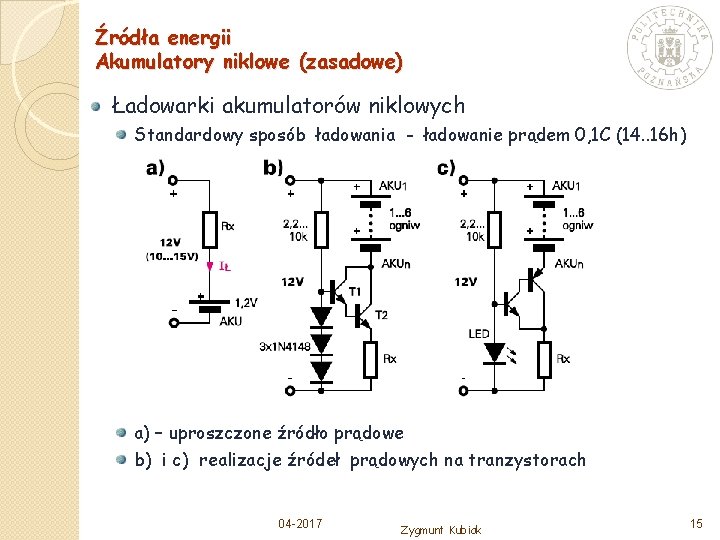
Źródła energii Akumulatory niklowe (zasadowe) Ładowarki akumulatorów niklowych Standardowy sposób ładowania - ładowanie prądem 0, 1 C (14. . 16 h) a) – uproszczone źródło prądowe b) i c) realizacje źródeł prądowych na tranzystorach 04 -2017 Zygmunt Kubiak 15
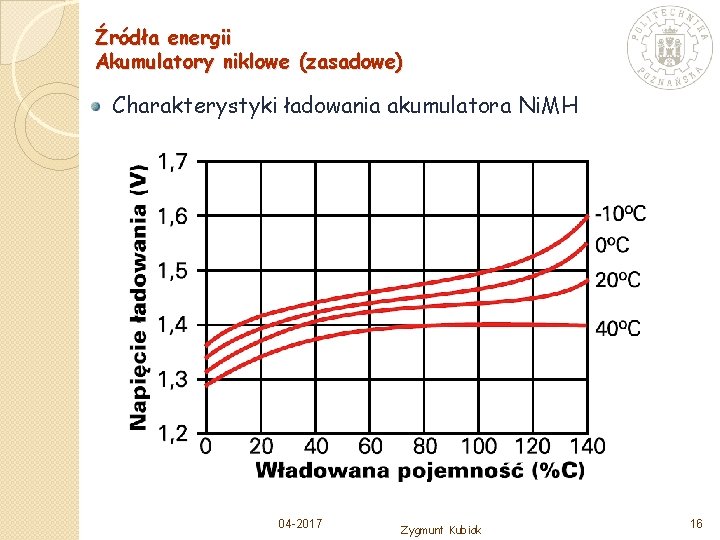
Źródła energii Akumulatory niklowe (zasadowe) Charakterystyki ładowania akumulatora Ni. MH 04 -2017 Zygmunt Kubiak 16
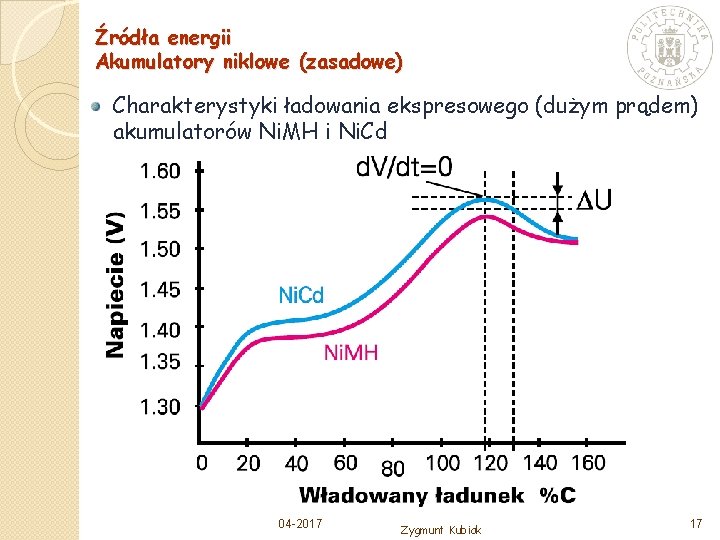
Źródła energii Akumulatory niklowe (zasadowe) Charakterystyki ładowania ekspresowego (dużym prądem) akumulatorów Ni. MH i Ni. Cd 04 -2017 Zygmunt Kubiak 17
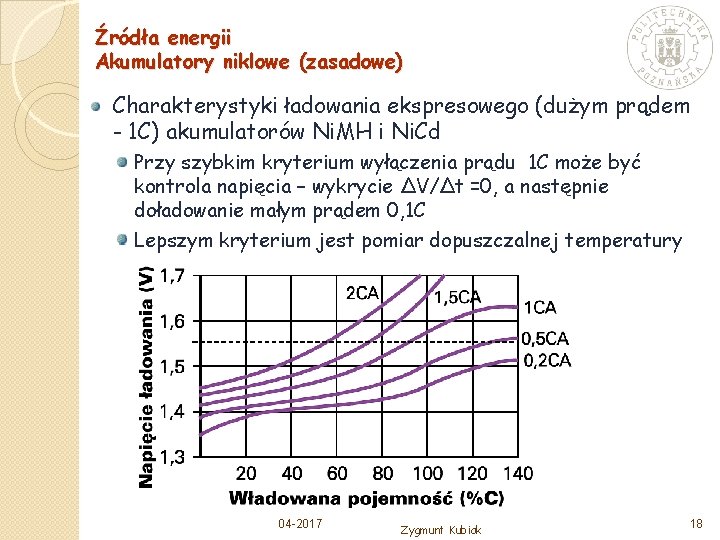
Źródła energii Akumulatory niklowe (zasadowe) Charakterystyki ładowania ekspresowego (dużym prądem - 1 C) akumulatorów Ni. MH i Ni. Cd Przy szybkim kryterium wyłączenia prądu 1 C może być kontrola napięcia – wykrycie ΔV/Δt =0, a następnie doładowanie małym prądem 0, 1 C Lepszym kryterium jest pomiar dopuszczalnej temperatury 04 -2017 Zygmunt Kubiak 18

Źródła energii Akumulatory litowe Opracowano w 1991 r. Akumulatory litowo-jonowe Li-ion (Li-jon) Akumulatory litowo-polimerowe Li-po (Li-poly) Akumulatory litowo-żelazowo-fosfatowymi Li. Fe. PO 4 (Li. Fe. PO 4) Napięcie nominalne >3 V Największa gęstość energii Brak efektu pamięciowego Niewielkie samorozładowanie Niebezpieczne przeładowanie - grozi POŻAREM Pobór prądu większego o dopuszczalnego – grozi POŻAREM Szkodliwe nadmierne rozładowanie (rozładowanie poniżej 2, 5 V/celę) – nieodwracalna utrata pojemności 04 -2017 Zygmunt Kubiak 19
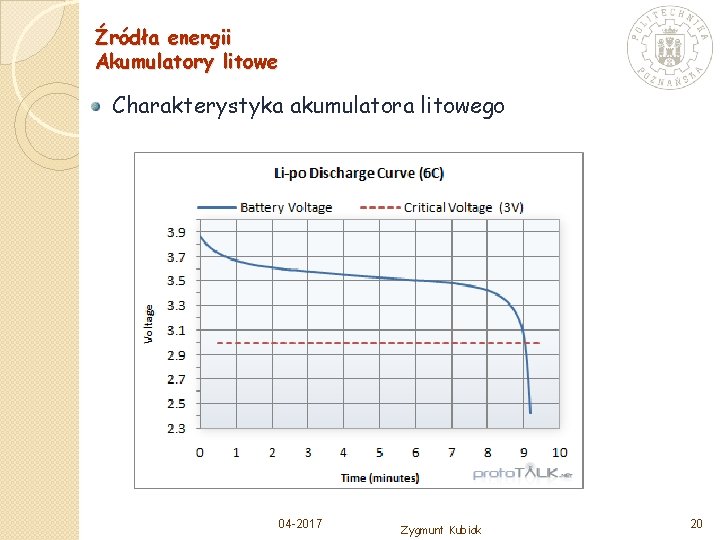
Źródła energii Akumulatory litowe Charakterystyka akumulatora litowego 04 -2017 Zygmunt Kubiak 20
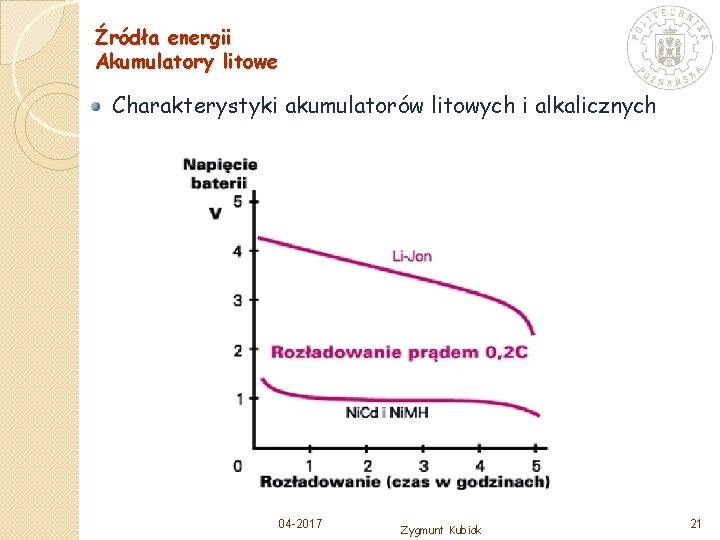
Źródła energii Akumulatory litowe Charakterystyki akumulatorów litowych i alkalicznych 04 -2017 Zygmunt Kubiak 21
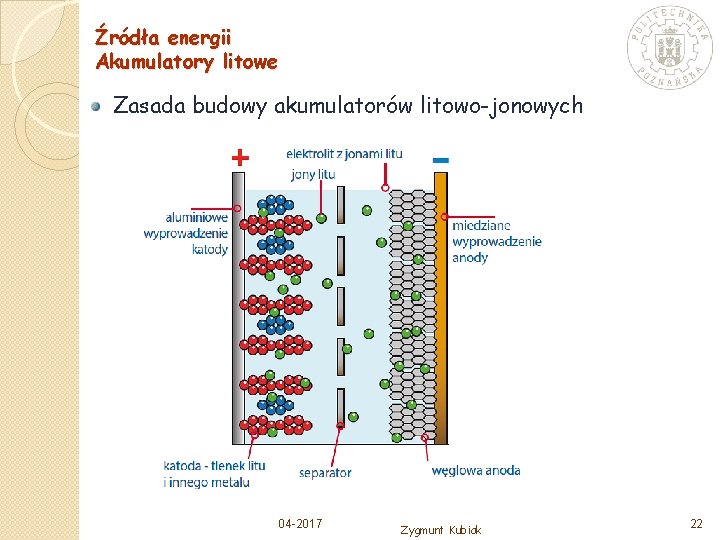
Źródła energii Akumulatory litowe Zasada budowy akumulatorów litowo-jonowych 04 -2017 Zygmunt Kubiak 22
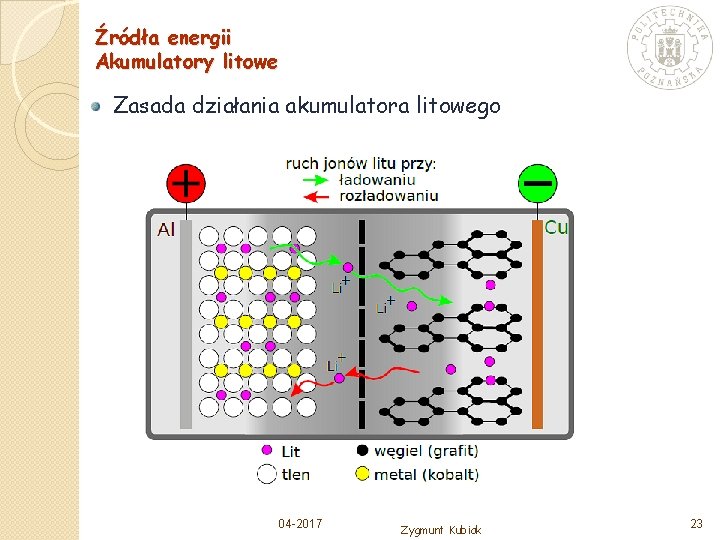
Źródła energii Akumulatory litowe Zasada działania akumulatora litowego 04 -2017 Zygmunt Kubiak 23

Źródła energii Akumulatory litowe Zasada działania akumulatora litowego Podczas ładowania dodatnie jony litu przechodzą z katody do węglowej anody, gdzie łączą się z atomami węgla w specyficzną warstwową strukturę opisywaną wzorem chemicznym Li. C 6. Podczas rozładowania jony litu wracają z anody do katody. Pierwsze akumulatory (Sony 1991 r. ) budowane były na bazie Li. Co. O 2 (LCO) – do 200 Wh/kg - ale wysokie ceny kobaltu Tańszym rozwiązaniem okazały się akumulatory Li. Mn 2 O 4 (LMO) nazywane są manganowymi albo spinelowymi ; wada – gęstość o połowę mniejsza od kobaltowych Znaleziono rozwiązania kompromisowe: Li. Mn. Co. O 2 (LMC) i Li. Ni. Mn. Co. O 2 (NMC) Inne rozwiązania: Li. Fe. PO 4 (LFP) Nowe rozwiązania: wykorzystanie glinu (NCA – Li. Ni. Co. Al. O 2), tytan (LTO – Li 4 Ti 5 O 12) czy siarki (LIS – Li 2 S 8) – zaletą jest duża gęstość energii do 500 Wh/kg 04 -2017 Zygmunt Kubiak 24

Źródła energii Akumulatory litowe Rozwiązania w akumulatorach litowych W akumulatorach litowych stosowano i nadal stosuje się ciekłe elektrolity zawierające różne bardziej i mniej bezpieczne substancje z litem Istotnym wynalazkiem było zastąpienie ciekłych elektrolitów stałym w postaci przewodzących polimerów, zawierających sole litu - akumulatory litowo-polimerowe (oznaczenia Li. Po, Li. Po lub LIP) Akumulatory polimerowe to też akumulatory litowo-jonowe 04 -2017 Zygmunt Kubiak 25

Źródła energii Akumulatory litowe Ładowanie akumulatorów litowych Akumulatory litowe najpierw należy ładować prądem 0, 2 C. . 0, 3 C a po uzyskaniu odpowiedniej wartości napięcia, należy utrzymać stałe napięcie zasilania Dla akumulatorów Li-Ion i Li-Po o napięciu nominalnym 3, 7 V napięcie ładowania wynosi 4, 2 V ± 50 m. V Dla akumulatorów Li. Fe. PO 4 o napięciu nominalnym 3, 2 V napięcie ładowania wynosi 3, 6 V + 3, 65 V (dokładne wartości w karcie katalogowej) Długotrwałe utrzymywanie końcowego napięcia ładowania (4, 2 V) powoduje zmniejszenie trwałości akumulatora 04 -2017 Zygmunt Kubiak 26
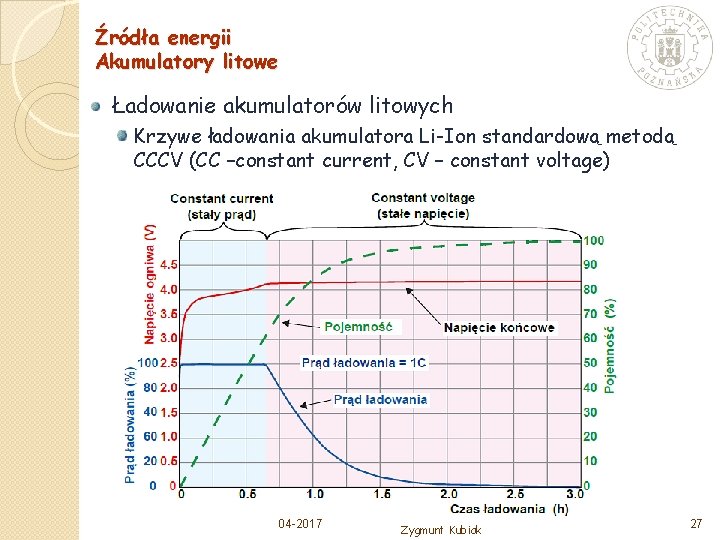
Źródła energii Akumulatory litowe Ładowanie akumulatorów litowych Krzywe ładowania akumulatora Li-Ion standardową metodą CCCV (CC –constant current, CV – constant voltage) 04 -2017 Zygmunt Kubiak 27
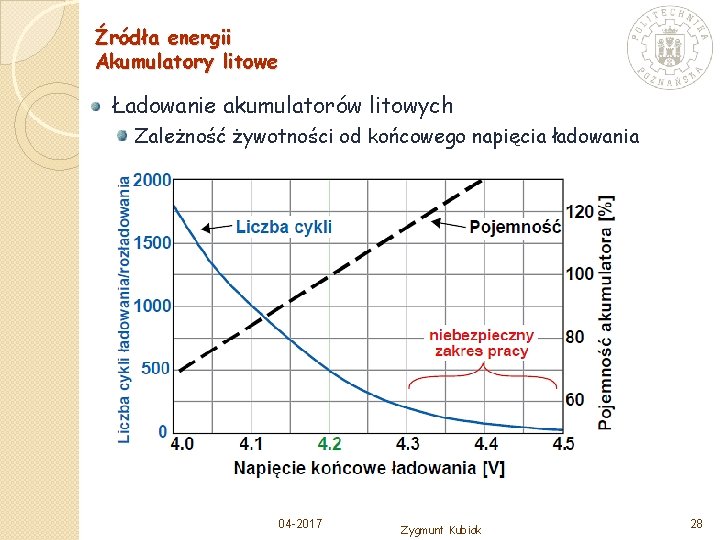
Źródła energii Akumulatory litowe Ładowanie akumulatorów litowych Zależność żywotności od końcowego napięcia ładowania 04 -2017 Zygmunt Kubiak 28
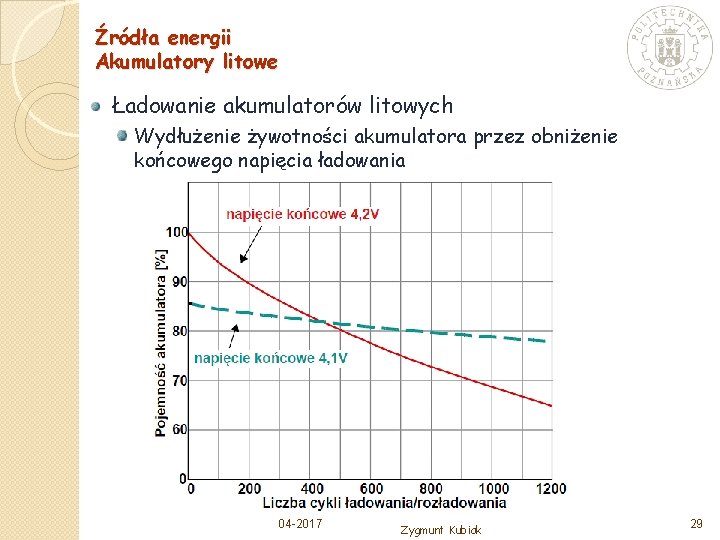
Źródła energii Akumulatory litowe Ładowanie akumulatorów litowych Wydłużenie żywotności akumulatora przez obniżenie końcowego napięcia ładowania 04 -2017 Zygmunt Kubiak 29
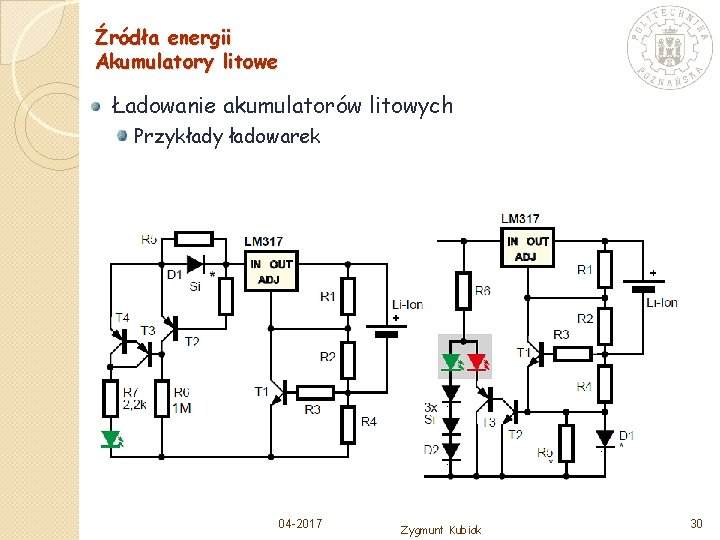
Źródła energii Akumulatory litowe Ładowanie akumulatorów litowych Przykłady ładowarek 04 -2017 Zygmunt Kubiak 30
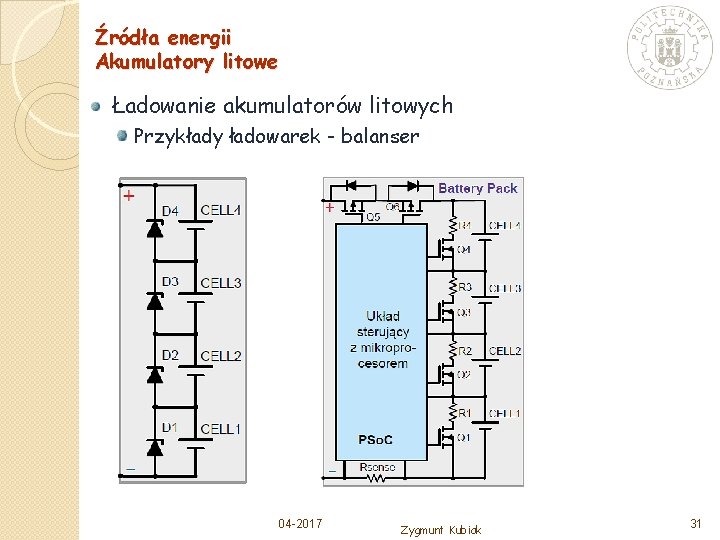
Źródła energii Akumulatory litowe Ładowanie akumulatorów litowych Przykłady ładowarek - balanser 04 -2017 Zygmunt Kubiak 31
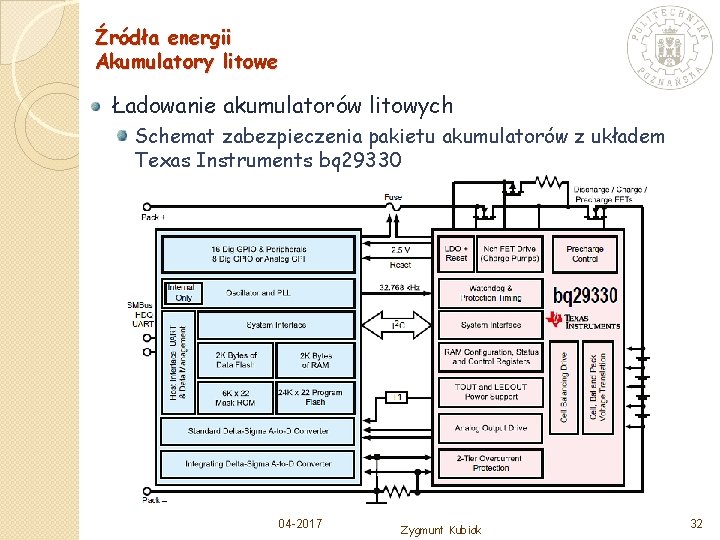
Źródła energii Akumulatory litowe Ładowanie akumulatorów litowych Schemat zabezpieczenia pakietu akumulatorów z układem Texas Instruments bq 29330 04 -2017 Zygmunt Kubiak 32

Źródła energii Nowe rozwiązania 04 -2017 Zygmunt Kubiak 33

Źródła energii Nowe rozwiązania Aktualnie najpopularniejsze są trzy typy akumulatorów Kwasowo-ołowiowe (pojazdy) Niklowe Ni. MH Litowe W najlepszych współczesnych akumulatorach litowych osiąga się gęstość energii na poziomie 200 Wh/kg 04 -2017 Zygmunt Kubiak 34
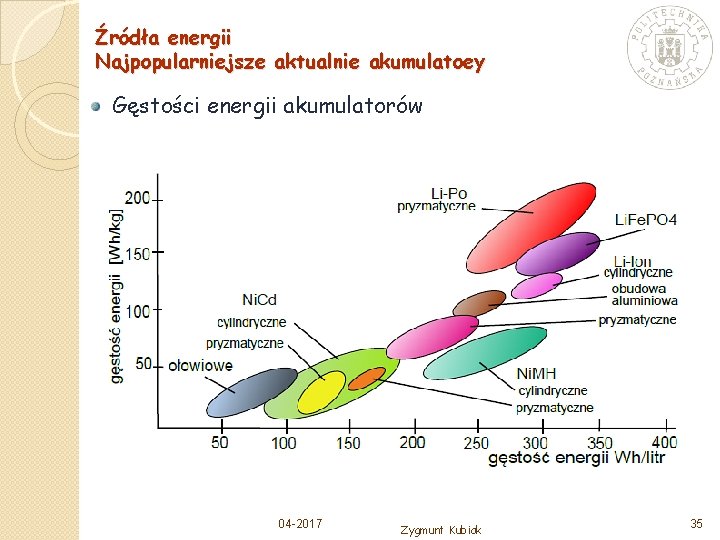
Źródła energii Najpopularniejsze aktualnie akumulatoey Gęstości energii akumulatorów 04 -2017 Zygmunt Kubiak 35

Źródła energii Nowe rozwiązania Akumulatory alkaliczne manganowe (RAM Rechargeable Alkaline Manganese) to odmiana jednorazowych ogniw alkalicznych (1, 5 V) Możliwość ładowania kilkanaście do kilkudziesięciu razy Małe samorozładowanie Znaczna rezystancja wewnętrzna Akumulatory cynkowo-powietrzne (Zn-Air) Duża gęstość energii – oczekiwana ponad 400 Wh/kg W trakcie badań: aluminiowo-powietrzne, litowo-powietrzne - teoretyczne wartości gęstości 11140 Wh/kg Akumulatory niklowo-litowe (Ni-Li) – łączą zalety akumulatorów niklowych i litowo jonowych – oczekiwana gęstość energii ponad 900 Wh/kg 04 -2017 Zygmunt Kubiak 36

Źródła energii Nowe rozwiązania Akumulatory sodowo-jonowe (Na-Ion) – spodziewana gęstość energii ok. 400 Wh/kg; opatentowano potasowojonowe (K-Ion) Obiecujące litowo-siarkowe (Li. S) o teoretycznej gęstości energii do 2600 Wh/kg Badania nad wykorzystaniem sodu – akumulatory sodowosiarkowe (sód stopiony z siarką) - temperatura pracy 300. . 350°C – wykorzystanie w energetyce –potężne pojemności Akumulatory sodowo-niklowe (Na-Ni. Cl 2) – temperatura pracy 245°C – zastosowania jw. Akumulatory wanadowe (przepływowe) – ładowanie klasyczne lub „tankowanie” polegające na wymianie elektrolitu na „naładowany” – niska gęstość energii 20. . 25 Wh/kg (niższa niż w akumulatorach kwasowych)- jw. 04 -2017 Zygmunt Kubiak 37
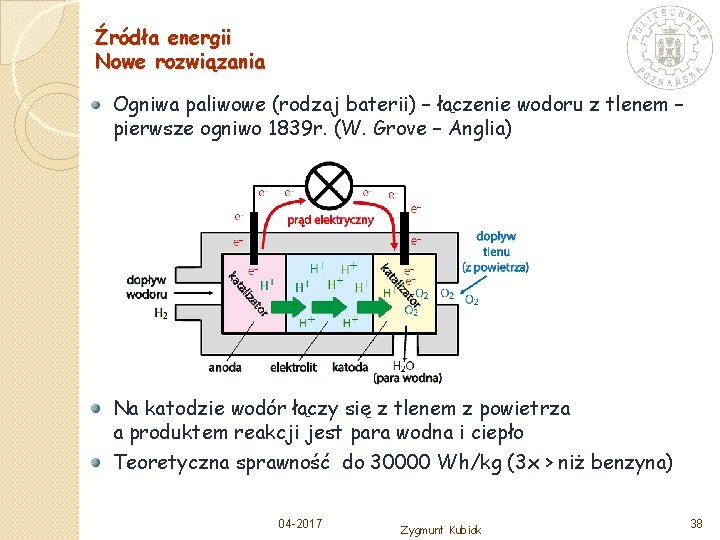
Źródła energii Nowe rozwiązania Ogniwa paliwowe (rodzaj baterii) – łączenie wodoru z tlenem – pierwsze ogniwo 1839 r. (W. Grove – Anglia) Na katodzie wodór łączy się z tlenem z powietrza a produktem reakcji jest para wodna i ciepło Teoretyczna sprawność do 30000 Wh/kg (3 x > niż benzyna) 04 -2017 Zygmunt Kubiak 38
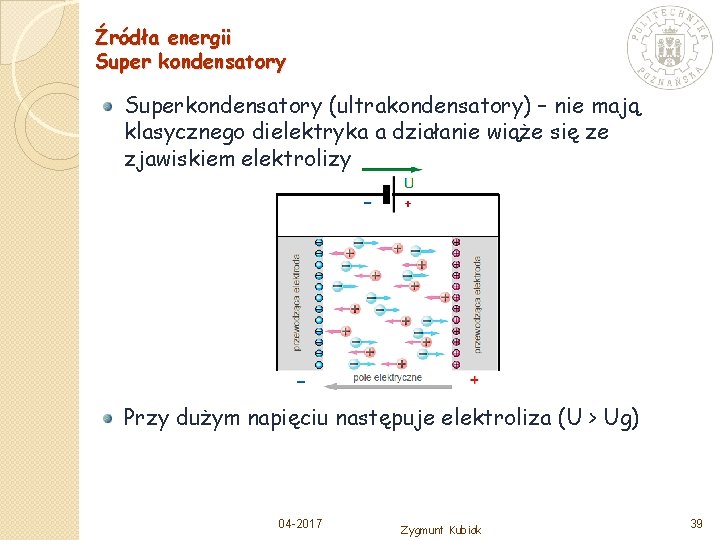
Źródła energii Super kondensatory Superkondensatory (ultrakondensatory) – nie mają klasycznego dielektryka a działanie wiąże się ze zjawiskiem elektrolizy Przy dużym napięciu następuje elektroliza (U > Ug) 04 -2017 Zygmunt Kubiak 39
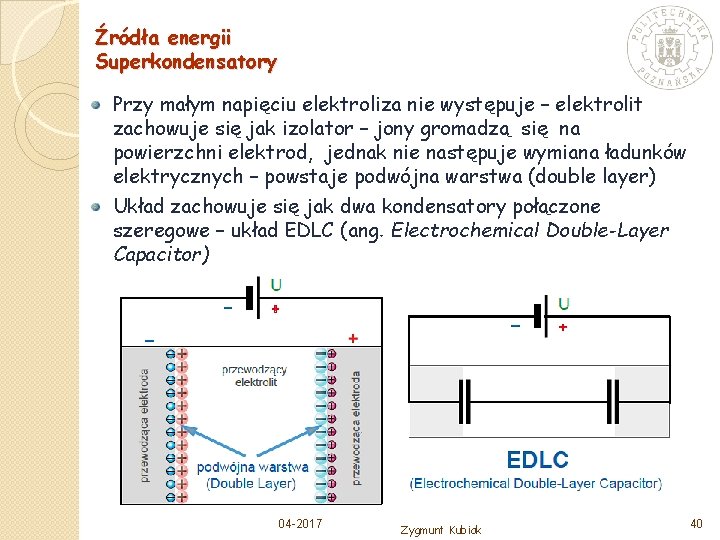
Źródła energii Superkondensatory Przy małym napięciu elektroliza nie występuje – elektrolit zachowuje się jak izolator – jony gromadzą się na powierzchni elektrod, jednak nie następuje wymiana ładunków elektrycznych – powstaje podwójna warstwa (double layer) Układ zachowuje się jak dwa kondensatory połączone szeregowe – układ EDLC (ang. Electrochemical Double-Layer Capacitor) 04 -2017 Zygmunt Kubiak 40
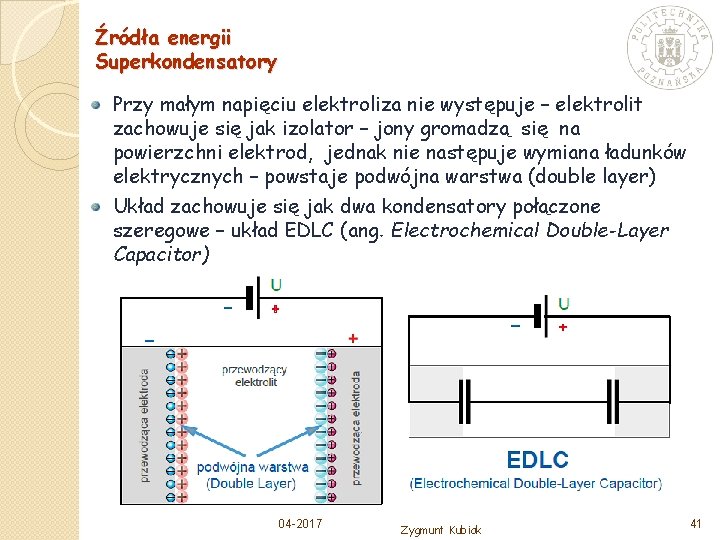
Źródła energii Superkondensatory Przy małym napięciu elektroliza nie występuje – elektrolit zachowuje się jak izolator – jony gromadzą się na powierzchni elektrod, jednak nie następuje wymiana ładunków elektrycznych – powstaje podwójna warstwa (double layer) Układ zachowuje się jak dwa kondensatory połączone szeregowe – układ EDLC (ang. Electrochemical Double-Layer Capacitor) 04 -2017 Zygmunt Kubiak 41

Źródła energii Superkondensatory W akumulatorach podczas ładowania, energia elektryczna zamieniana jest w energię chemiczną (energię wiązań chemicznych) a podczas rozładowania energia chemiczna zamienia się w energię elektryczną Praca akumulatora zwiazana jest z chemicznymi reakcjami redukcji (reduction) i utleniania (oxidation), stąd bierze się skrót redox W superkondensatorach EDCL nie zachodzą żadne reakcje chemiczne Pseudokondensatory (kondensatory redox , kondensatory faradajowskie) do magazynowania energii wykorzystują reakcje chemiczne 04 -2017 Zygmunt Kubiak 42
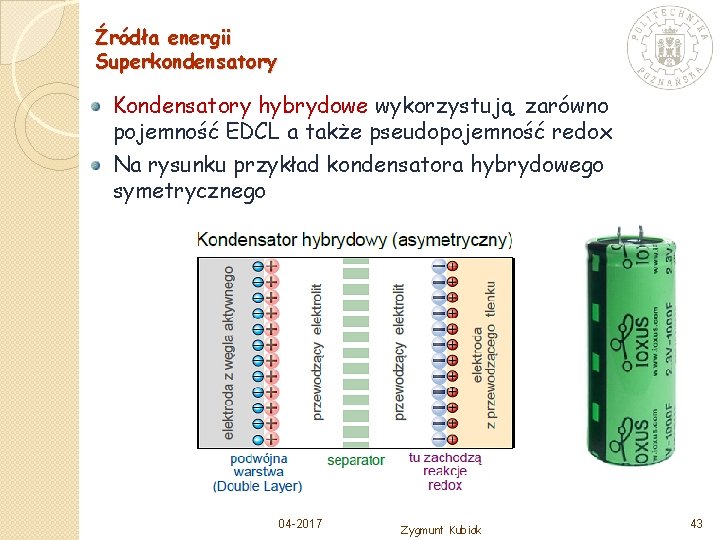
Źródła energii Superkondensatory Kondensatory hybrydowe wykorzystują zarówno pojemność EDCL a także pseudopojemność redox Na rysunku przykład kondensatora hybrydowego symetrycznego 04 -2017 Zygmunt Kubiak 43
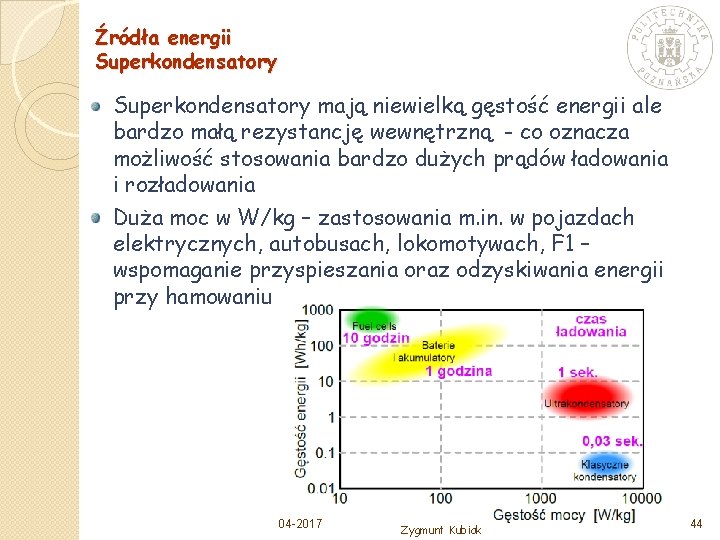
Źródła energii Superkondensatory mają niewielką gęstość energii ale bardzo małą rezystancję wewnętrzną - co oznacza możliwość stosowania bardzo dużych prądów ładowania i rozładowania Duża moc w W/kg – zastosowania m. in. w pojazdach elektrycznych, autobusach, lokomotywach, F 1 – wspomaganie przyspieszania oraz odzyskiwania energii przy hamowaniu 04 -2017 Zygmunt Kubiak 44
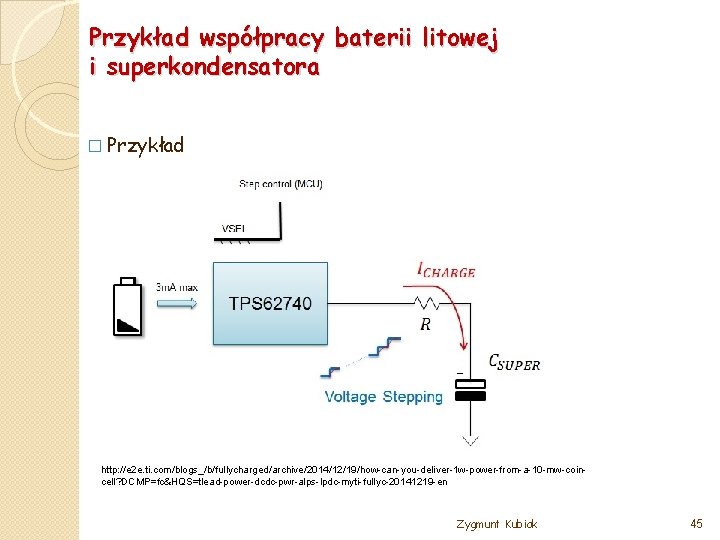
Przykład współpracy baterii litowej i superkondensatora � Przykład http: //e 2 e. ti. com/blogs_/b/fullycharged/archive/2014/12/19/how-can-you-deliver-1 w-power-from-a-10 -mw-coincell? DCMP=fc&HQS=tlead-power-dcdc-pwr-alps-lpdc-myti-fullyc-20141219 -en Zygmunt Kubiak 45

Przykład współpracy baterii litowej i superkondensatora � Bateria litowa Li. SOCl 2 charakteryzuje się długą żywotnością – 15 lat i więcej � Ma bardzo wysoką wydajność energetyczna (Wh /kg), ale nie jest w stanie dostarczyć prądu o wartości większej niż np. . 20 m. A � Źle znoszą pracę przy wyższych prądach � Na poprzednim slajdzie schemat blokowy przedstawia sprawdzoną koncepcję rozwiązania powyższego problemu zasilania z użyciem układu TPS 62740 i superkondensatora co znacznie przedłuża życie baterii � Kondensator ładowany jest z baterii niskim (kontrolowanym) prądem a sam może dostarczyć dużego prądu obciążenia Zygmunt Kubiak 46

Przykład współpracy baterii litowej i superkondensatora �W przykładowej aplikacji dla potrzeb węzła w. M-Bus przyjęto założenia: � Napięcie baterii = 3, 6 V � Prąd maksymalny baterii = 3 m. A � Czas transmisji = 200 ms � Moc transmisji = 1000 m. W Aby dostarczyć energii do transmisji wybrano kondensator 0, 47 F (mu. Rata EDLC typu DMF 3 Z 5 R 5 H 474 M 3 DTA 0) ładowany tylko do 2, 7 V (trwałość ponad 15 lat) Uzyskano sprawność powyżej 90% Zygmunt Kubiak 47
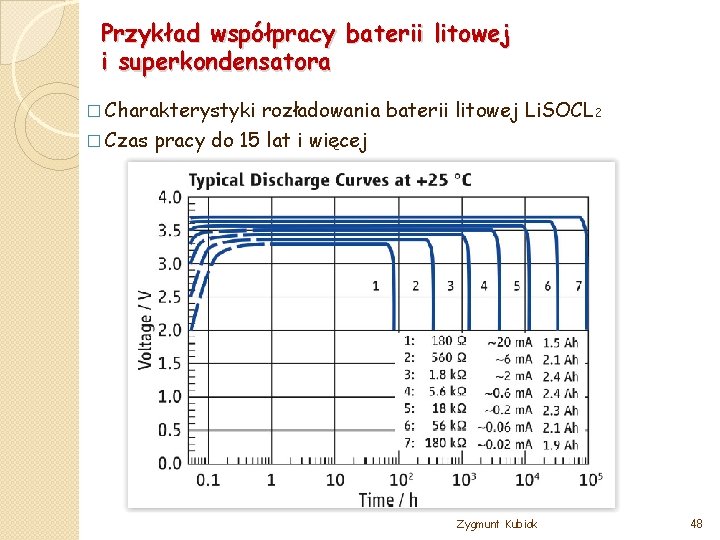
Przykład współpracy baterii litowej i superkondensatora � Charakterystyki rozładowania baterii litowej Li. SOCL 2 � Czas pracy do 15 lat i więcej Zygmunt Kubiak 48
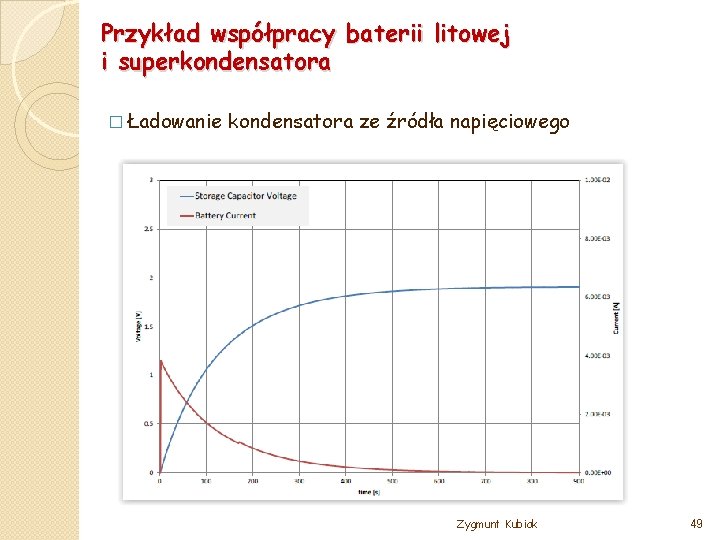
Przykład współpracy baterii litowej i superkondensatora � Ładowanie kondensatora ze źródła napięciowego Zygmunt Kubiak 49
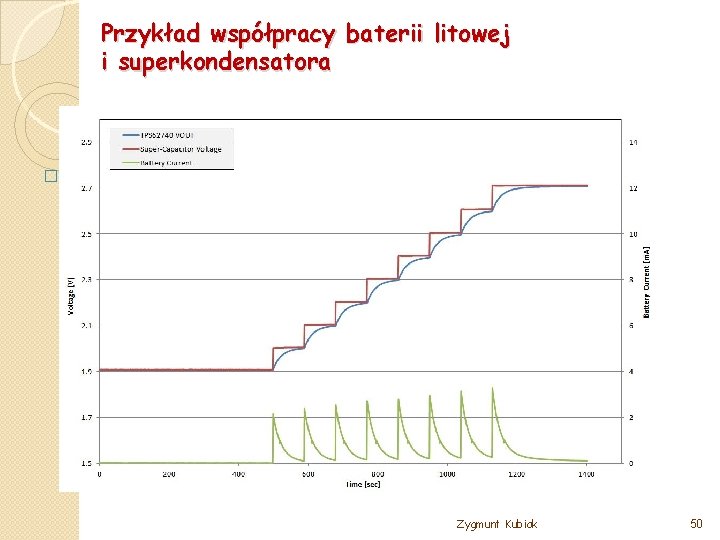
Przykład współpracy baterii litowej i superkondensatora � Zygmunt Kubiak 50
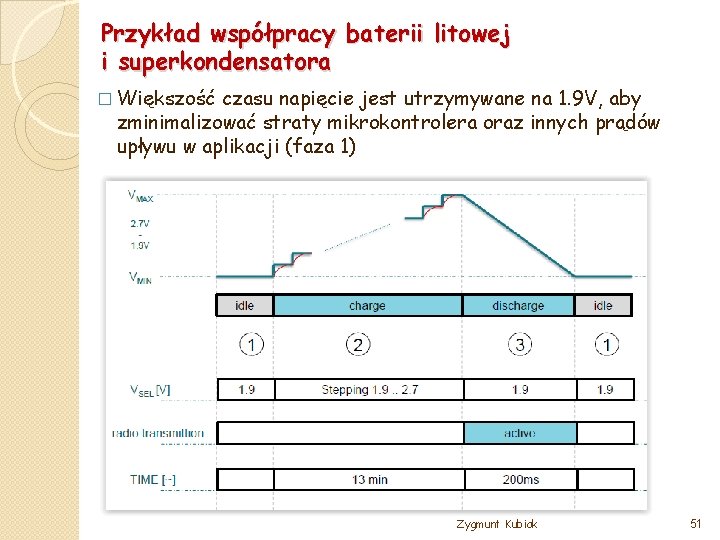
Przykład współpracy baterii litowej i superkondensatora � Większość czasu napięcie jest utrzymywane na 1. 9 V, aby zminimalizować straty mikrokontrolera oraz innych prądów upływu w aplikacji (faza 1) Zygmunt Kubiak 51
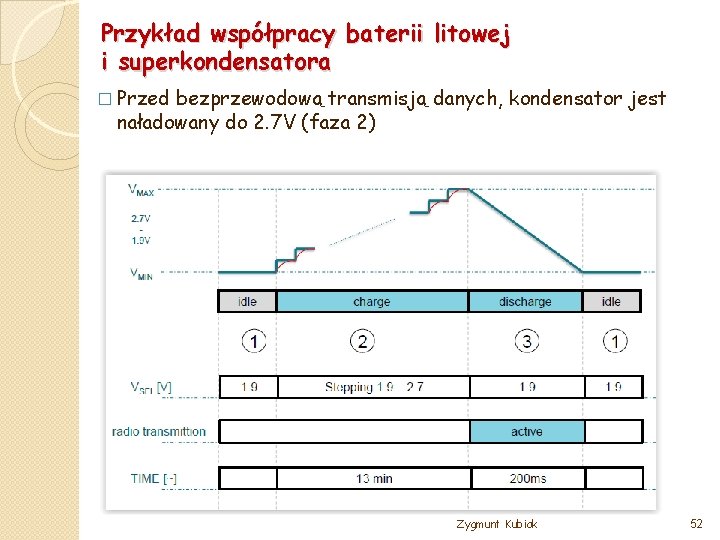
Przykład współpracy baterii litowej i superkondensatora � Przed bezprzewodową transmisją danych, kondensator jest naładowany do 2. 7 V (faza 2) Zygmunt Kubiak 52
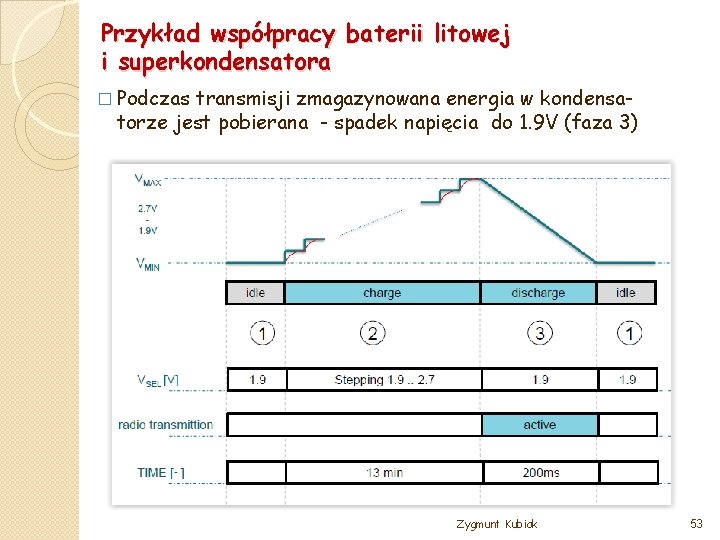
Przykład współpracy baterii litowej i superkondensatora � Podczas transmisji zmagazynowana energia w kondensatorze jest pobierana - spadek napięcia do 1. 9 V (faza 3) Zygmunt Kubiak 53

Dziękuję Zygmunt Kubiak 54 04201 7
- Slides: 54