Rcstpusok Ismtls 1 Nevezd meg a halmazllapot vltozsokat














- Slides: 20

Rácstípusok

Ismétlés 1. Nevezd meg a halmazállapot változásokat, amelyeket a nyilak jelölnek! olvadás szilárd→folyadék: ………………. fagyás folyadék→szilárd: …………………. . szublimáció szilárd→gáz: ……………. lecsapódás gáz→szilárd: …………… párolgás (forrás) folyadék→gáz: …………. . lecsapódás gáz→folyadék: …………. .

2. Csoportosítsd a felsorolt jellemzőket! c; f; g; h Folyadék: ……………. . a; e; g Gáz: …………… b; d; e Szilárd anyag: ……………… a. térfogat állandó, alakjuk változó b. a legnagyobb belső rendezettség jellemzi c. a rendelkezésre álló teret kitöltik d. a részecskék nem tudnak elmozdulni, csak rezeghetnek e. a részecskék közötti taszítás miatt nem lehet összenyomni őket f. az Avogadro törvény az ilyen halmazállapotú anyagokra vonatkozik g. a diffúzió jelensége jellemző rájuk h. könnyen összenyomhatók

4. Jellemezzük a molekularácsos kristályokat!

5. Jellemezzük az ionrácsos kristályokat!

Kristályrácstípusok A kristály rácspontjaiban található anyagi részecskék és a közöttük működő erők típusa szerint négyféle rácstípust különböztetünk meg: molekularács ionrács fémrács atomrács ……………. . ; ……………. ; ………….

Fémrácsos kristályok A rácspontokon pozitív. . ……. . töltésű fématomtörzsek vannak, amelyeket a hozzájuk fémes kötés) közösen tartozó delokalizált …. . ………. . elektronok tartanak össze. (………. A fémes kötés tehát nem irányított, a közös elektronok a rácspontok között viszonylag szabadon mozognak. Ennek következménye: a fémek elektromos áram – és hővezetése …………………… elsődleges ……………… primer (……………. . , vezetők) A fémrács delokalizált elektronjai bármilyen hullámhosszú sugárzással átlátszatlanok és általában ……………. szürke gerjeszthetők, ezért a fémek ………………. színűek réz és az ………. ). arany (kivétel: . …… elsőrendű kémiai kötés, melynek kötési energiája …. …. . , nagy így a A fémes kötés …. . . …. ……. . szilárd (kivétel: ………. . …). higany fémek halmazállapota szobahőmérsékleten: …. . …….

A fizikai tulajdonságok: - a fématomok méretétől; - a közöttük működő erők nagyságától; - az illeszkedés szorosságától függ. 3 típust különböztetünk meg: a. lapon középpontos (lapcentrált) kockarács b. térben középpontos (tércentrált) kockarács c. hatszöges (hexagonális) rács

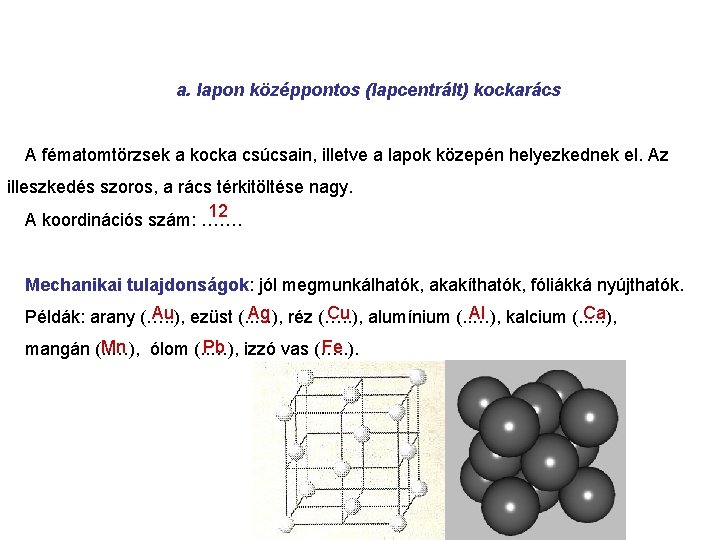
a. lapon középpontos (lapcentrált) kockarács A fématomtörzsek a kocka csúcsain, illetve a lapok közepén helyezkednek el. Az illeszkedés szoros, a rács térkitöltése nagy. 12 A koordinációs szám: ……. Mechanikai tulajdonságok: jól megmunkálhatók, akakíthatók, fóliákká nyújthatók. Au ezüst (. . …), Ag réz (…. . ), Cu alumínium (. . …), Al kalcium (. . …), Ca Példák: arany (…. . ), Mn ólom (. . …), Pb izzó vas (…. . ). Fe mangán (. . …),

b. térben középpontos (tércentrált) kockarács A fématomtörzsek a kocka csúcsain, illetve a középpontjában helyezkednek el. Az illeszkedés nem szoros, a rács térkitöltése kicsi. 8 A koordinációs szám: ……. Mechanikai tulajdonságok: rossz mechanikai tulajdonsággal rendelkeznek. Vagy Li …. . , Na …. . ), K vagy nagyon kemények, ridegek: vas nagyon lágyak, mint az alkálifémek (…. . , (…. . ), Fe króm (…. . ), Cr urán (. . …), Uwolfram (. . …), W vanádium (. . …). V


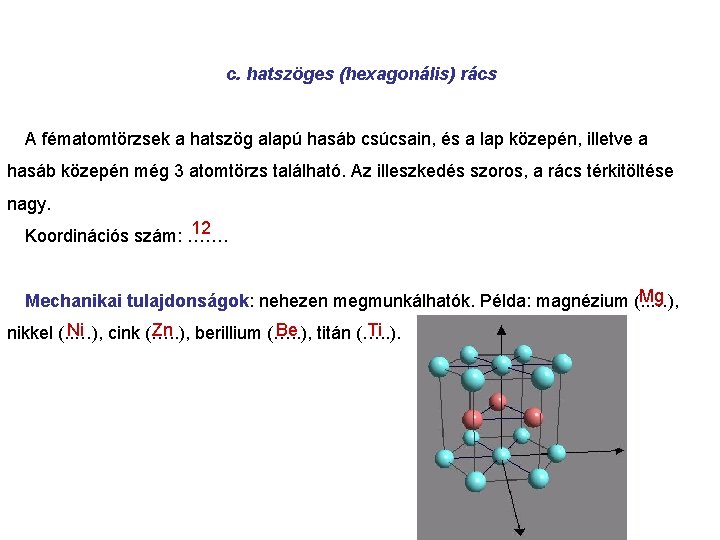
c. hatszöges (hexagonális) rács A fématomtörzsek a hatszög alapú hasáb csúcsain, és a lap közepén, illetve a hasáb közepén még 3 atomtörzs található. Az illeszkedés szoros, a rács térkitöltése nagy. 12 Koordinációs szám: ……. Mg Mechanikai tulajdonságok: nehezen megmunkálhatók. Példa: magnézium (. . …), Ni cink (…. . ), Zn berillium (…. . ), Be titán (…. . ). Ti nikkel (. . …),

Sűrűség A fémek sűrűsége tág határok között változik, általában annak a fémnek a sűrűsége nagyobb, amelynek nagyobb az atomtömege. Sűrűségük alapján két nagy csoportba oszthatjuk őket: könnyűfémek 5 g/cm 3 -nél kisebb (pl: ………) Na; Al - ………………. …. . , sűrűségük …. nehézfémek 5 g/cm 3 -nél nagyobb (pl: Fe; Cu; Pb - …………………. . . , sűrűségük …. ……. . …. …) A fémek egymás olvadékaiban jól oldódnak, a fémelegyek olvadékának ötvözet megszilárdulásával keletkező anyag az …………. .

Atomrácsos kristályok atomokhelyezkednek el; amelyeket meghatározott számú, A rácspontokon ……… irányított, kovalens ………. . kötés kapcsol össze. Az atomrácsos kristályok az erős kovalens ………… nem vezetik. kötések következtében kemények, a hőt és az elektromos áramot ……. magas oldószerük nincs. Olvadáspontjuk ………,

négy másik kapcsolódik, Példák: gyémánt, amelyben minden szénatomhoz ……. σ 109, 5 …. . -kötéssel. A tetraéderes, térhálós atomrácsban a kötésszög (………˚), és a kötéshossz azonos ………… (0, 154 nm) is minden irányban ……………. . Az erős kovalens kötések miatt a legkeményebb természetes anyag, olvadáspontja is nagyon magas (kb. 3500˚C). A szilícium, a germánium, a bór, mint kémiai elemek, illetve egyes vegyületek is kristályosodnak ilyen rácsba: kvarc (Si. O 2), cink-szulfid vagy szfalerit (……. ), szilícium -karbid (Si. C). Zn. S

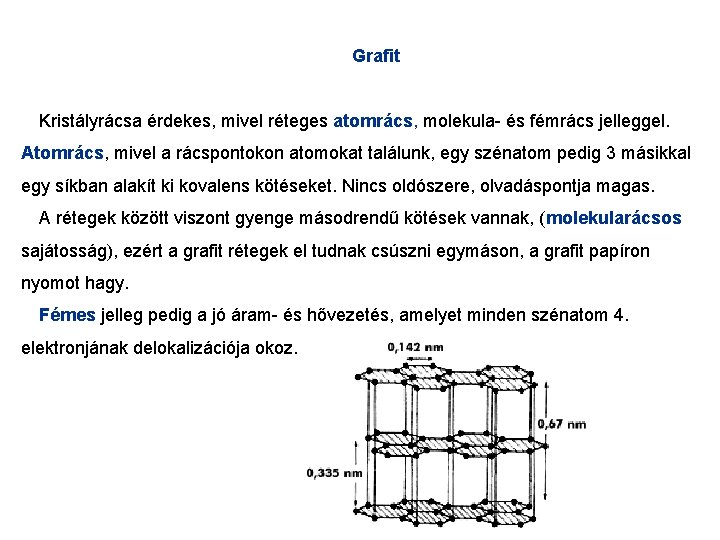
Grafit Kristályrácsa érdekes, mivel réteges atomrács, molekula- és fémrács jelleggel. Atomrács, mivel a rácspontokon atomokat találunk, egy szénatom pedig 3 másikkal egy síkban alakít ki kovalens kötéseket. Nincs oldószere, olvadáspontja magas. A rétegek között viszont gyenge másodrendű kötések vannak, (molekularácsos sajátosság), ezért a grafit rétegek el tudnak csúszni egymáson, a grafit papíron nyomot hagy. Fémes jelleg pedig a jó áram- és hővezetés, amelyet minden szénatom 4. elektronjának delokalizációja okoz.

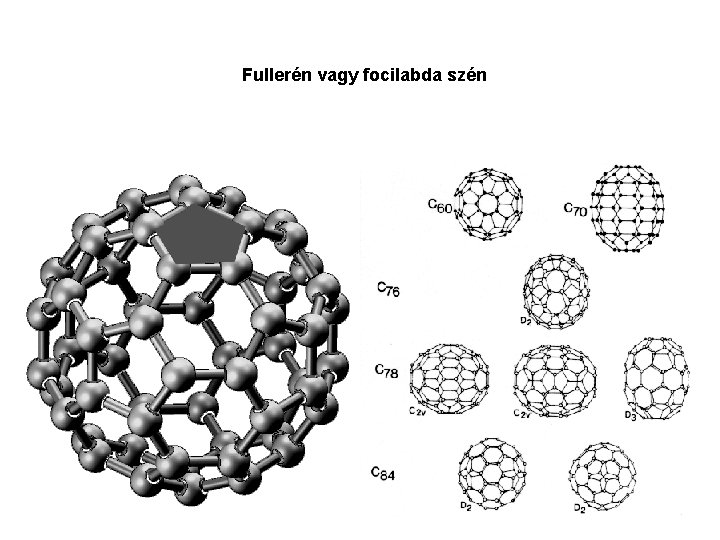
Fullerén vagy focilabda szén

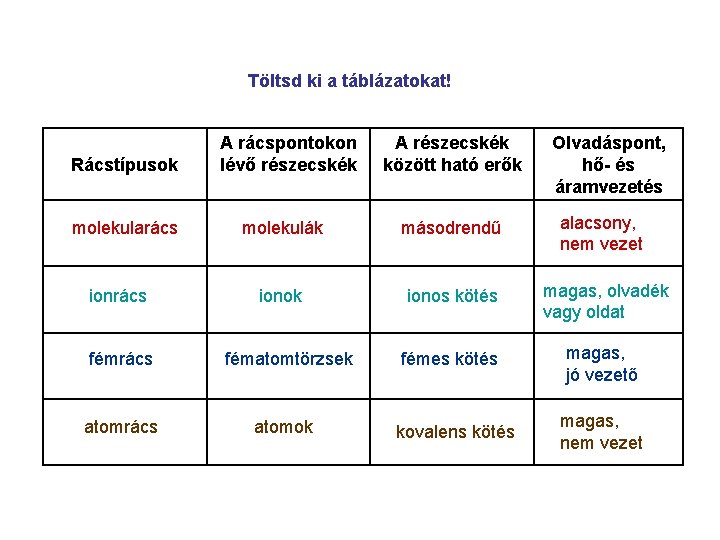
Töltsd ki a táblázatokat! Rácstípusok molekularács ionrács fémrács atomrács A rácspontokon lévő részecskék A részecskék között ható erők Olvadáspont, hő- és áramvezetés molekulák másodrendű alacsony, nem vezet ionok ionos kötés magas, olvadék vagy oldat fémes kötés magas, jó vezető kovalens kötés magas, nem vezet fématomtörzsek atomok

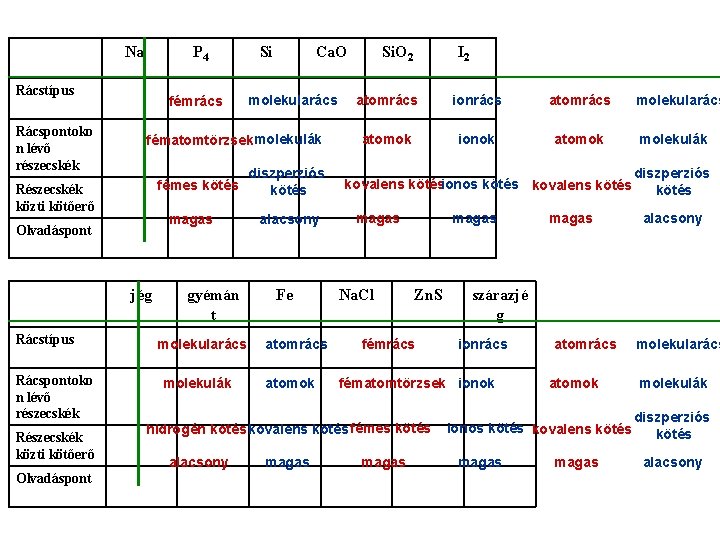
Na P 4 Rácstípus Rácspontoko n lévő részecskék fémrács fémes kötés magas Olvadáspont jég Rácspontoko n lévő részecskék Részecskék közti kötőerő Olvadáspont Ca. O molekularács fématomtörzsek molekulák Részecskék közti kötőerő Rácstípus Si gyémán t molekularács molekulák diszperziós kötés alacsony Fe atomrács atomok Si. O 2 I 2 atomrács ionrács atomok ionok atomok kovalens kötésionos kötés kovalens kötés magas Na. Cl magas Zn. S fémrács alacsony magas molekulák diszperziós kötés alacsony szárazjé g ionrács fématomtörzsek ionok hidrogén kötés kovalens kötés fémes kötés magas molekularács atomok ionos kötés kovalens kötés magas molekularács molekulák diszperziós kötés alacsony

Fehér Badics Nikoletta Balatonalmádi, 2008. 01. 24.