ramforrsok Elsdleges cella ramot termel kmiai anyagokbl melyek

Áramforrások Elsődleges cella: áramot termel kémiai anyagokból, melyek a cellába vannak bezárva. Ha a reakció elérte az egyensúlyt, kimerül. Nem tölthető. Másodlagos cella: Használat előtt fel kell tölteni. Használat előtt van a rendszer egyensúlyban. Újratölthető. Tüzelőanyagcella: Elsődleges cella. A reagenseket a cellán kívülről adagolják.

Elektrokémia A Leclanché-féle szárazelem + 1866 záróréteg burkolat légtér NH 4 Cl + Zn. Cl 2 C + Mn. O 2 Zn membrán grafit _ Hasonlóan működik az alkáli-szárazelem: Georges Leclanché (1839 1882)

Áramforrások Szárazelem Leclanché Anód: Zn(s) Zn 2+(aq) + 2 NH 4+(aq) + OH–(aq) Katód: 2 Mn. O 2(s) + 2 NH 4+(aq) + 2 e- Zn 2+(aq) + 2 e→ [Zn(NH 3)2]2+(aq) + 2 H 2 O Mn 2 O 3(s) + 2 NH 3(aq)+ H 2 O(l) 1, 5 V → 0, 8 V nedves NH 4 Cl és Zn. Cl 2 paszta keményítőben (elektrolit)
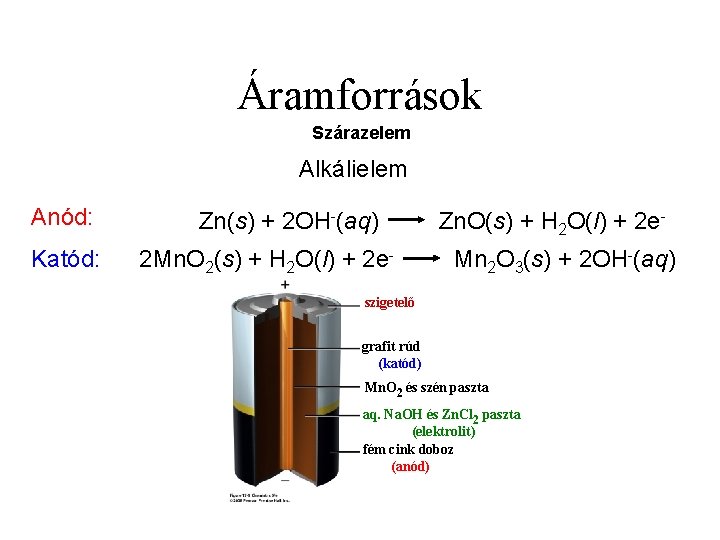
Áramforrások Szárazelem Alkálielem Anód: Katód: Zn(s) + 2 OH-(aq) 2 Mn. O 2(s) + H 2 O(l) + 2 e- Zn. O(s) + H 2 O(l) + 2 e. Mn 2 O 3(s) + 2 OH-(aq) szigetelő grafit rúd (katód) Mn. O 2 és szén paszta aq. Na. OH és Zn. Cl 2 paszta (elektrolit) fém cink doboz (anód)
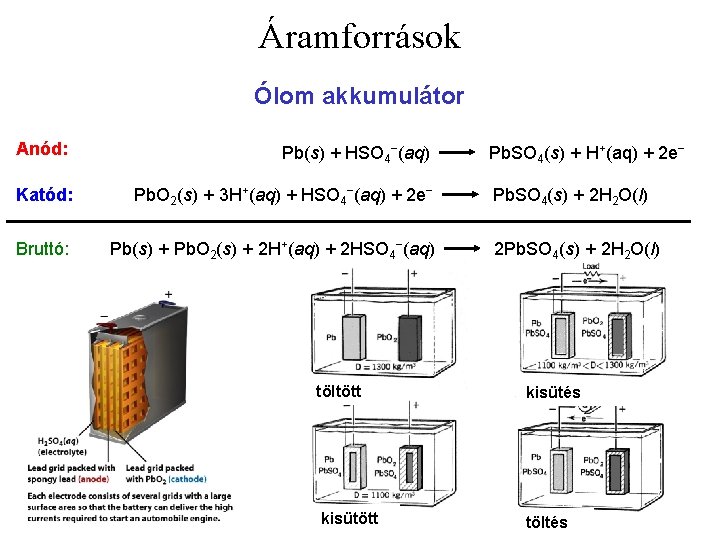
Áramforrások Ólom akkumulátor Anód: Pb(s) + HSO 4−(aq) Katód: Pb. O 2(s) + 3 H+(aq) + HSO 4−(aq) + 2 e− Bruttó: Pb(s) + Pb. O 2(s) + 2 H+(aq) + 2 HSO 4−(aq) Pb. SO 4(s) + H+(aq) + 2 e− Pb. SO 4(s) + 2 H 2 O(l) 2 Pb. SO 4(s) + 2 H 2 O(l) töltött kisütés kisütött töltés
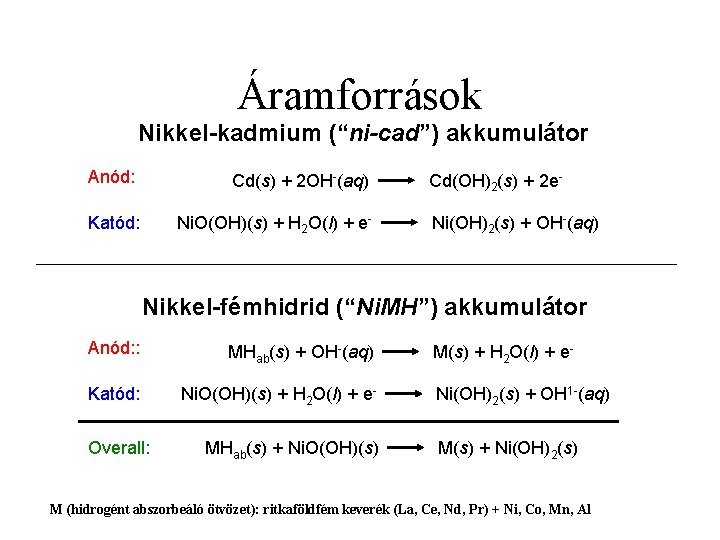
Áramforrások Nikkel-kadmium (“ni-cad”) akkumulátor Anód: Cd(s) + 2 OH-(aq) Katód: Ni. O(OH)(s) + H 2 O(l) + e- Cd(OH)2(s) + 2 e. Ni(OH)2(s) + OH-(aq) Nikkel-fémhidrid (“Ni. MH”) akkumulátor Anód: : MHab(s) + OH-(aq) Katód: Ni. O(OH)(s) + H 2 O(l) + e- Overall: MHab(s) + Ni. O(OH)(s) M(s) + H 2 O(l) + e. Ni(OH)2(s) + OH 1 -(aq) M(s) + Ni(OH)2(s) M (hidrogént abszorbeáló ötvözet): ritkaföldfém keverék (La, Ce, Nd, Pr) + Ni, Co, Mn, Al
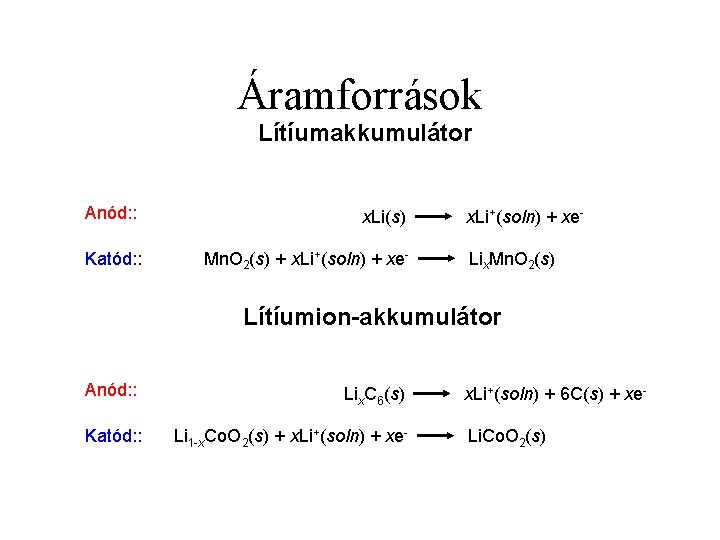
Áramforrások Lítíumakkumulátor Anód: : x. Li(s) Katód: : Mn. O 2(s) + x. Li+(soln) + xe- x. Li+(soln) + xe. Lix. Mn. O 2(s) Lítíumion-akkumulátor Anód: : Lix. C 6(s) Katód: : Li 1 -x. Co. O 2(s) + x. Li+(soln) + xe- x. Li+(soln) + 6 C(s) + xe. Li. Co. O 2(s)
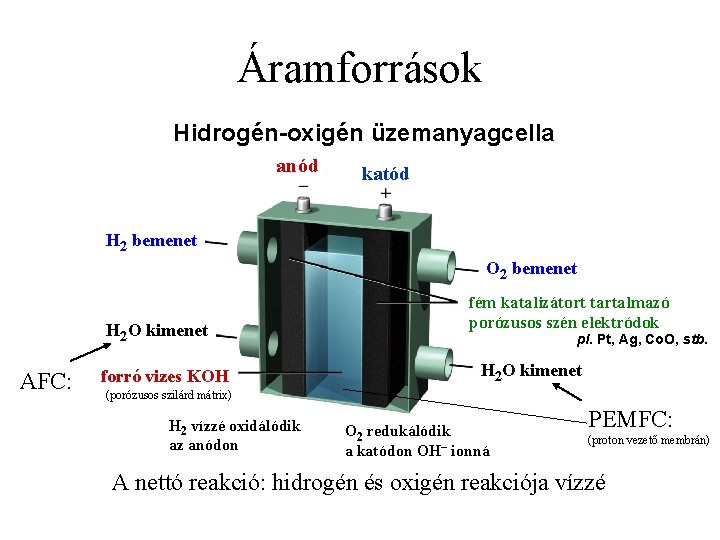
Áramforrások Hidrogén-oxigén üzemanyagcella anód katód H 2 bemenet O 2 bemenet H 2 O kimenet AFC: forró vizes KOH fém katalizátort tartalmazó porózusos szén elektródok pl. Pt, Ag, Co. O, stb. H 2 O kimenet (porózusos szilárd mátrix) H 2 vízzé oxidálódik az anódon O 2 redukálódik a katódon OH– ionná PEMFC: (proton vezető membrán) A nettó reakció: hidrogén és oxigén reakciója vízzé
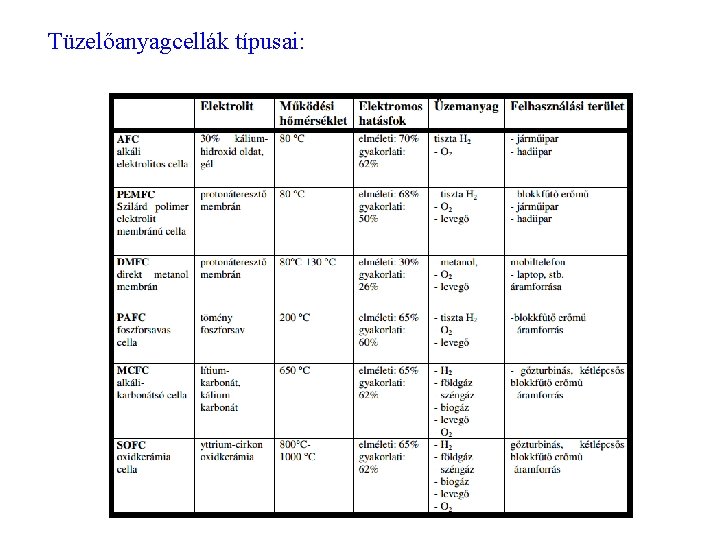
Tüzelőanyagcellák típusai:

Elektrolízis Ha a cellán áramot bocsátanak át, egy különben magától le nem játszódó reakció is megvalósítható. Elektrolízis során a külső feszültségforrás elektronokat juttat az anódról a katódra. A galváncellához képest megfordul az elektródok polaritása.

Elektrokémia Elektrolízis – áram hatására lejátszódó kémiai változás bomlásfeszültség – legkisebb olyan feszültség, amellyel tartós elektrolízis megvalósítható, ha nincs túlfeszültség, akkor e K -e A

Elektrolízis A lehetséges félreakciókból összeállítható cellareakciók mind negatív Eocell-t adnak. Az a reakció várható, amelyiknek a cellapotenciálja a legkisebb negatív érték. Sok esetben a cellapotenciálnál nagyobb feszültségre van szükség, hogy a reakció ténylegesen meginduljon. Túlfeszültségnek nevezik ezt az elektród anyagától és az elektródreakciótól függő extra feszültséget. EOS

Elektrolízis Bomlásfeszültség az a legkisebb olyan feszültség az anód és a katód között egy elektrolizáló cellában, mellyel folyamatos elektrolízis valósítható meg. Termodinamikailag: elektródpotenciálok közötti különbség εkatód − εanód Gyakran az elektrolízishez szükséges feszültség meghaladja a termodinamikai értéket. A túlfeszültség az a potenciálkülönbség, ami a termodinamikailag meghatározott érték és azon potenciál között van, melynél az elektrolízis már kísérletileg megvalósítható.
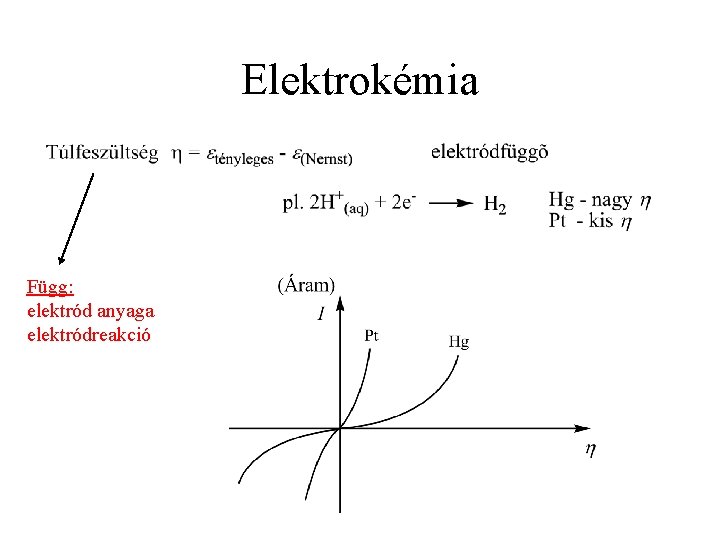
Elektrokémia Függ: elektród anyaga elektródreakció
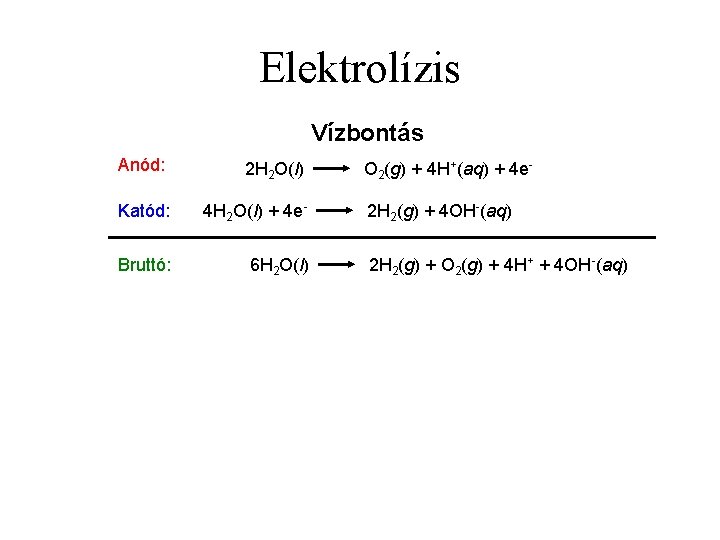
Elektrolízis Vízbontás Anód: 2 H 2 O(l) Katód: 4 H 2 O(l) + 4 e- Bruttó: 6 H 2 O(l) O 2(g) + 4 H+(aq) + 4 e 2 H 2(g) + 4 OH-(aq) 2 H 2(g) + O 2(g) + 4 H+ + 4 OH-(aq)
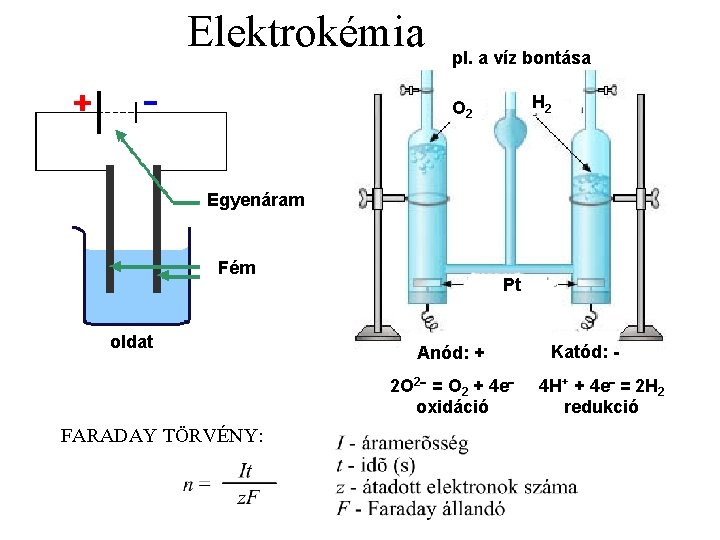
Elektrokémia pl. a víz bontása H 2 O 2 Egyenáram Fém oldat Pt Anód: + 2 O 2 = O 2 + 4 e oxidáció FARADAY TÖRVÉNY: Katód: 4 H+ + 4 e = 2 H 2 redukció
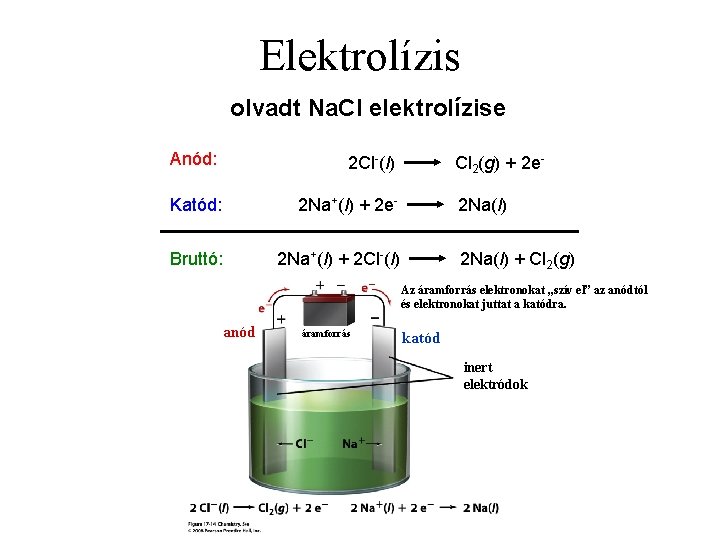
Elektrolízis olvadt Na. Cl elektrolízise Anód: 2 Cl-(l) Katód: 2 Na+(l) + 2 e- Bruttó: 2 Na+(l) + 2 Cl-(l) Cl 2(g) + 2 e 2 Na(l) + Cl 2(g) Az áramforrás elektronokat „szív el” az anódtól és elektronokat juttat a katódra. anód áramforrás katód inert elektródok
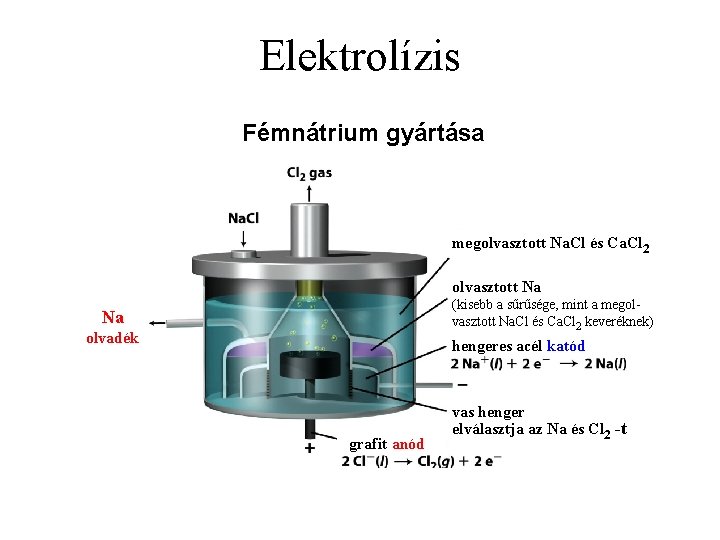
Elektrolízis Fémnátrium gyártása megolvasztott Na. Cl és Ca. Cl 2 olvasztott Na (kisebb a sűrűsége, mint a megolvasztott Na. Cl és Ca. Cl 2 keveréknek) Na olvadék hengeres acél katód grafit anód vas henger elválasztja az Na és Cl 2 -t

Elektrolízis Vizes Na. Cl elektrolízise Anód: : 2 Cl-(aq) Katód: 2 H 2 O(l) + 2 e- Bruttó: 2 Cl-(l) + 2 H 2 O(l) Cl 2(g) + 2 e. H 2(g) + 2 OH-(aq) Cl 2(g) + H 2(g) + 2 OH-(aq)
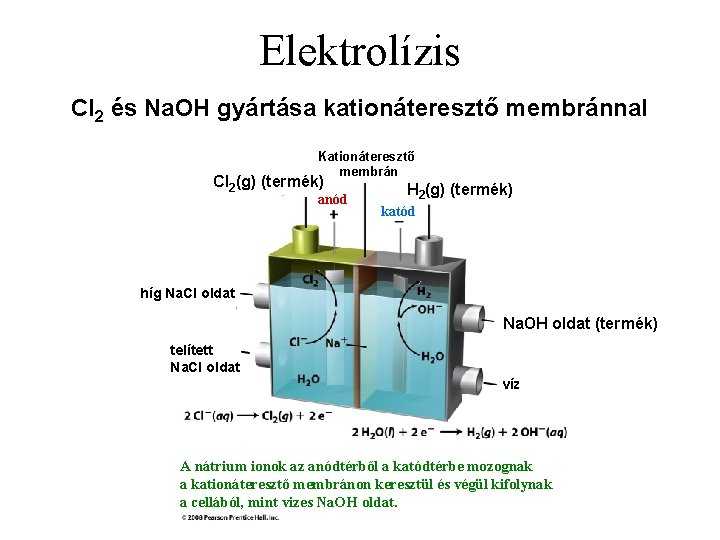
Elektrolízis Cl 2 és Na. OH gyártása kationáteresztő membránnal Kationáteresztő membrán Cl 2(g) (termék) anód H 2(g) (termék) katód híg Na. Cl oldat Na. OH oldat (termék) telített Na. Cl oldat víz A nátrium ionok az anódtérből a katódtérbe mozognak a kationáteresztő membránon keresztül és végül kifolynak a cellából, mint vizes Na. OH oldat.
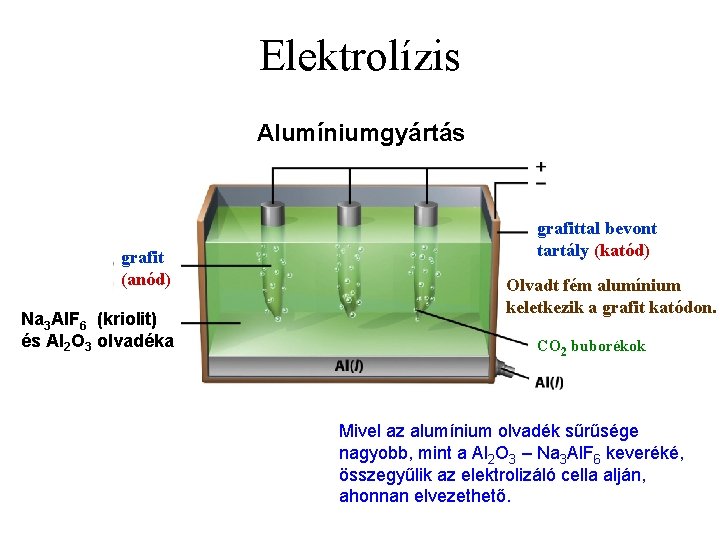
Elektrolízis Alumíniumgyártás grafit (anód) Na 3 Al. F 6 (kriolit) és Al 2 O 3 olvadéka grafittal bevont tartály (katód) Olvadt fém alumínium keletkezik a grafit katódon. CO 2 buborékok Mivel az alumínium olvadék sűrűsége nagyobb, mint a Al 2 O 3 – Na 3 Al. F 6 keveréké, összegyűlik az elektrolizáló cella alján, ahonnan elvezethető.

Faraday törvényei --- Az elektrolízis során az elektródon levált anyag tömege egyenesen arányos az elektródon áthaladt elektromos töltéssel. --- Egy adott töltésmennyiség esetén az elektródon levált elemi anyag tömege egyenesen arányos az elem atomtömegének és az elektrolízis során bekövetkezett oxidációfok változásnak a hányadosával. Összefoglalva az állandó-áramú elektrolízisre: n = moláris mennyisége a levált anyagnak t = idő (amíg az állandó áramerősséget alkalmaztuk) I = áramerősség z = az ion által átadott elektronok száma F = Faraday állandó (96485 C mol− 1)

Elektrolízis A reakcióban résztvevő anyagok tömege függ: moláris tömeg, áthaladó töltés, reagáló elektronok száma A töltés mértékegysége a coulomb (C), egy elektron töltése – 1. 6022 × 10– 19 C, 1 mol töltése a Faraday-állandó. Az áramerősség mértékegysége az amper (A). EOS
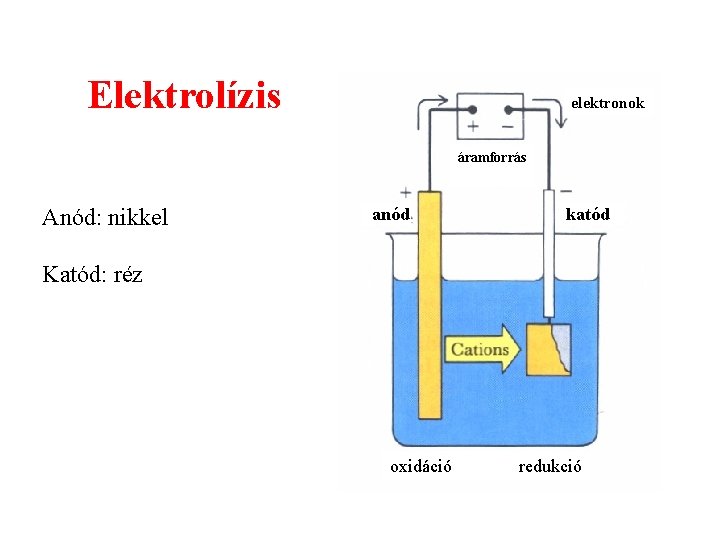
Elektrolízis elektronok áramforrás Anód: nikkel anód katód Katód: réz oxidáció redukció
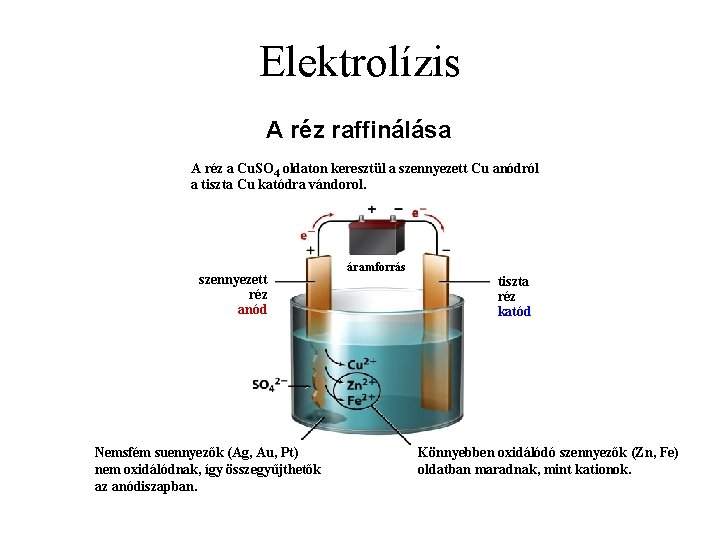
Elektrolízis A réz raffinálása A réz a Cu. SO 4 oldaton keresztül a szennyezett Cu anódról a tiszta Cu katódra vándorol. szennyezett réz anód Nemsfém suennyezők (Ag, Au, Pt) nem oxidálódnak, így összegyűjthetők az anódiszapban. áramforrás tiszta réz katód Könnyebben oxidálódó szennyezők (Zn, Fe) oldatban maradnak, mint kationok.
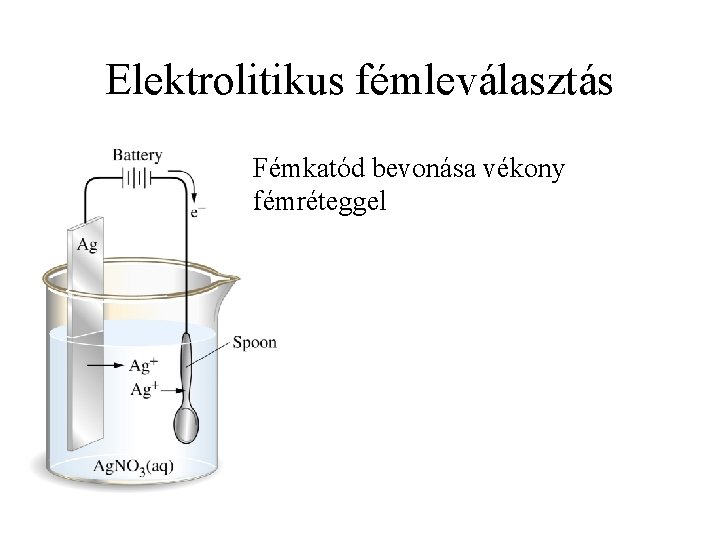
Elektrolitikus fémleválasztás Fémkatód bevonása vékony fémréteggel

vizes oldatát 1 óráig elektrolizálva az anódon 30 °C hőmérsékleten 217 cm 3 101, 3 k. Pa nyomású klórgáz fejlődik. Az anódfolyamatnál az áramkihasználás 100%-nak tekinthető. Mekkora az elektrolízis hatásfoka, ha a katódon ugyanennyi idő alatt 0, 45 g Cu válik le ? (Cu relatív atomtömege: 63, 5) Réz(II)-klorid = 81, 2 % Mekkora áramerősséggel elektrolizáltunk ? = 0, 47 A

2. Zh 2019. december 5. (csütörtök), az előadás helyén és időpontjában. északi tömb családnév: A – M családnév: N – Z 0. 83 Eötvös terem -1. 85 Harmónia terem --------------------------------
- Slides: 28