Ramanovsk spektroskopia a zobrazovanie Pavol Miskovsky Katedra biofyziky

Ramanovská spektroskopia a zobrazovanie Pavol Miskovsky Katedra biofyziky Universita P. J. Safárika, Košice & Medzinárodne laserové centrum Bratislava

Spectroscopy: A way to understand unravel the identity, structure and dynamics of molecules and materials
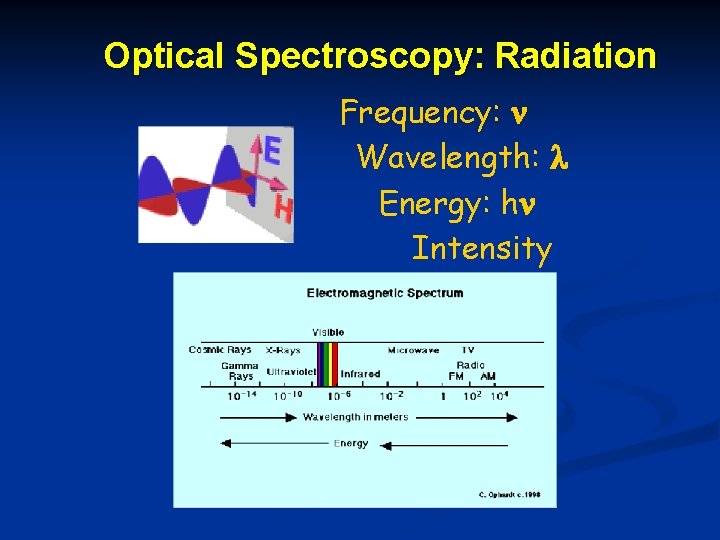
Optical Spectroscopy: Radiation Frequency: Wavelength: Energy: h Intensity
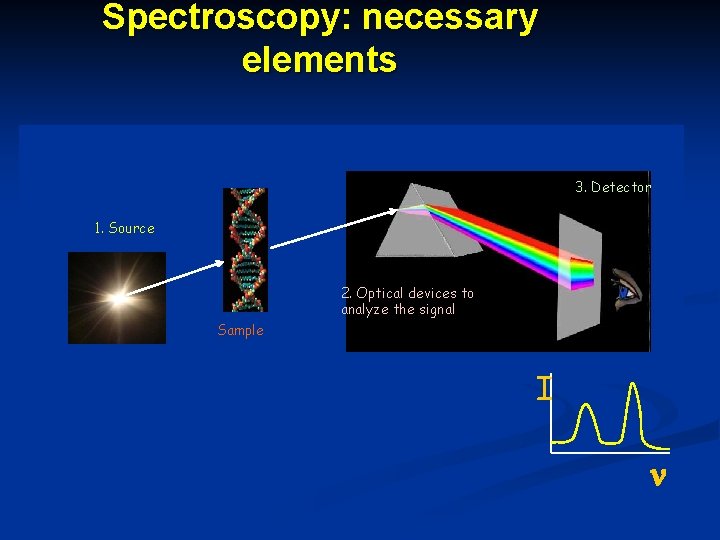
Spectroscopy: necessary elements 3. Detector 1. Source 2. Optical devices to analyze the signal Sample I

Different Sources to compose the message or excitation radiation Atkins & de Paula 2002

OPTICAL Vibrational Spectroscopy: IR Absorption and Raman
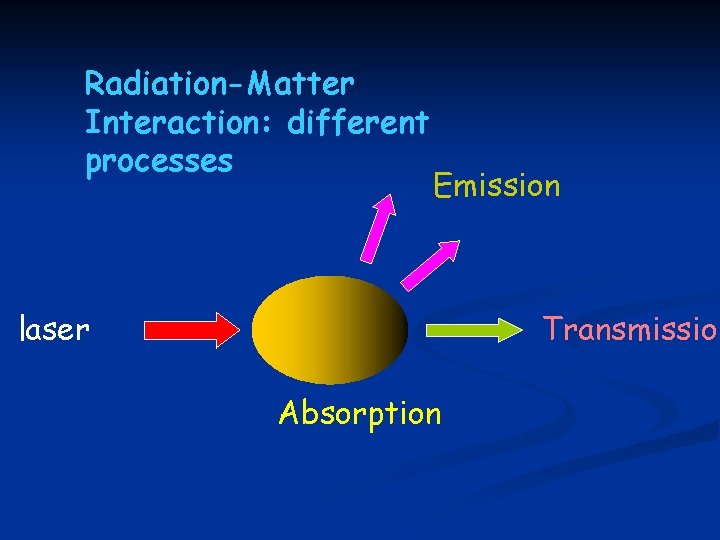
Radiation-Matter Interaction: different processes Emission laser Transmission Absorption
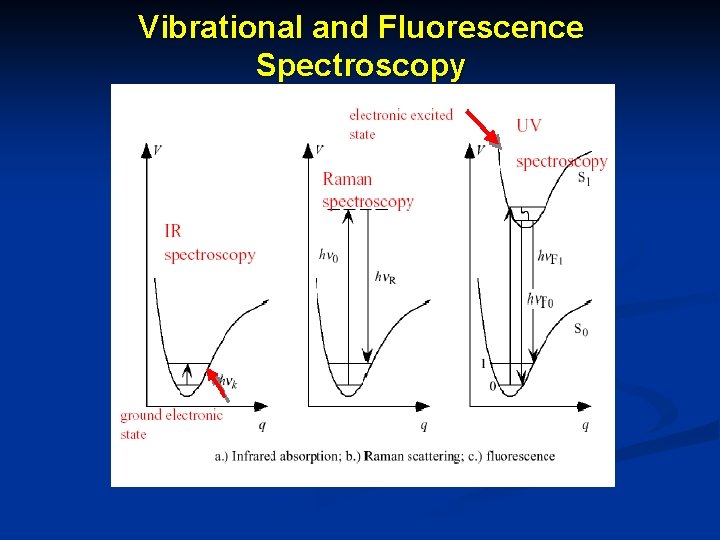
Vibrational and Fluorescence Spectroscopy

Scattering

Why the sky is blue during the day while it is red during the sunset? Light Scattering
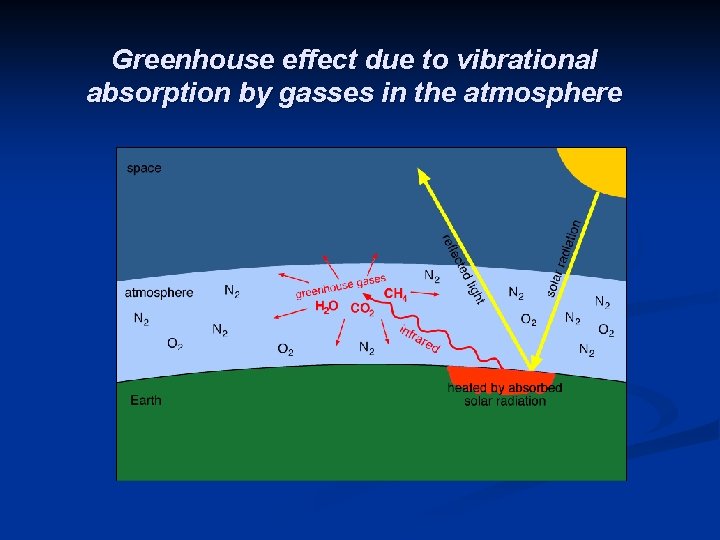
Greenhouse effect due to vibrational absorption by gasses in the atmosphere
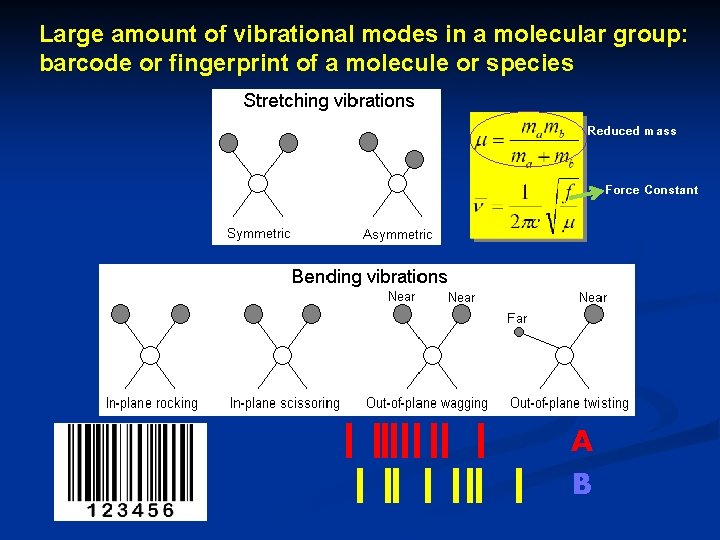
Large amount of vibrational modes in a molecular group: barcode or fingerprint of a molecule or species Reduced mass Force Constant A B
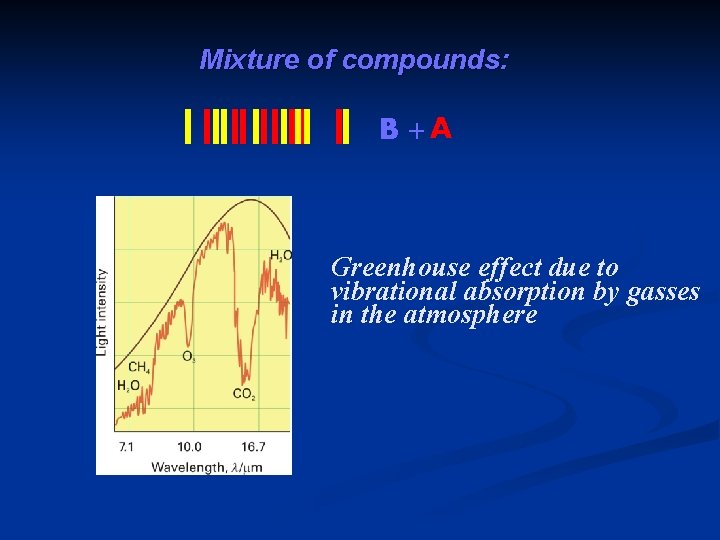
Mixture of compounds: B +A Greenhouse effect due to vibrational absorption by gasses in the atmosphere
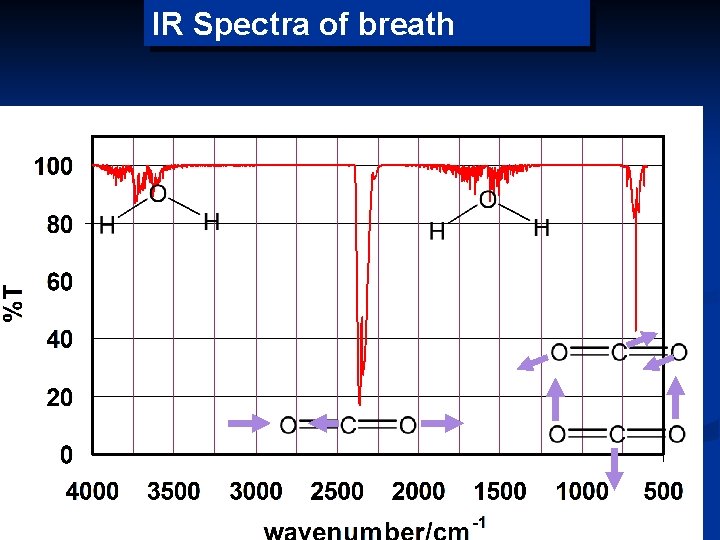
IR Spectra of breath

Selection Rules in Vibrational Spectroscopy IR Raman Ø Symmetric Streching Ø Asymmetric stretching Ø Bending
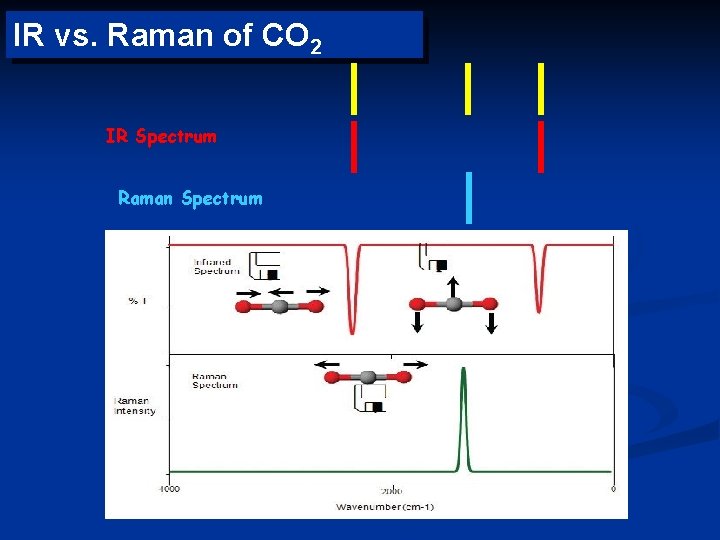
IR vs. Raman of CO 2 IR Spectrum Raman Spectrum

Position of bands Bond C-H C-D C-O C-Cl /cm-1 3000 2200 1100 700 Bond C O C=O C-O /cm-1 2143 1715 1100

Interpretation of Vibrational Spectra The most useful regions to take into account: <1000 cm-1: Large Vibrations of the molecule. Fingerprint Area 1000 -1800 cm-1: Characteristic Fonctional groups 2700 -3100 cm-1: C-H stretching vibrations 3200 -3700 cm-1: OH et NH stretching vibrations.

1. Základy teórie Ramanovej spektroskopie 2. Základne metódy Ramanovej spektroskopie i. Nerezonančná (klasická) RS ii. Rezonančná RS iii. Povrchovo zosilnená RS (SERS) iv. Koherentná anti-stokesovská RS 3. Ramanovské zobrazovanie i. Zobrazovanie na úrovni molekúl ii. Zobrazovanie na úrovni buniek iii. Zobrazovanie na úrovni tkanív
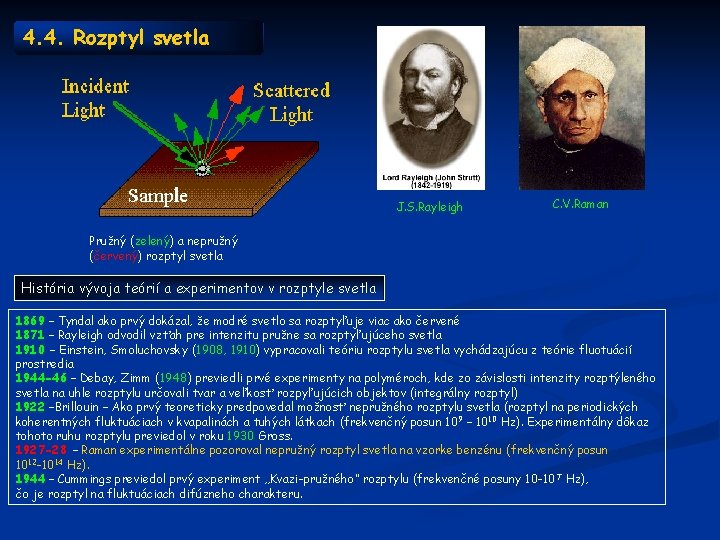
4. 4. Rozptyl svetla J. S. Rayleigh C. V. Raman Pružný (zelený) a nepružný (červený) rozptyl svetla História vývoja teórií a experimentov v rozptyle svetla 1869 – Tyndal ako prvý dokázal, že modré svetlo sa rozptyľuje viac ako červené 1871 – Rayleigh odvodil vzťah pre intenzitu pružne sa rozptyľujúceho svetla 1910 – Einstein, Smoluchovsky (1908, 1910) vypracovali teóriu rozptylu svetla vychádzajúcu z teórie fluotuácií prostredia 1944 -46 – Debay, Zimm (1948) previedli prvé experimenty na polyméroch, kde zo závislosti intenzity rozptýleného svetla na uhle rozptylu určovali tvar a veľkosť rozpyľujúcich objektov (integrálny rozptyl) 1922 –Brillouin – Ako prvý teoreticky predpovedal možnosť nepružného rozptylu svetla (rozptyl na periodických koherentných fluktuáciach v kvapalinách a tuhých látkach (frekvenčný posun 109 – 1010 Hz). Experimentálny dôkaz tohoto ruhu rozptylu previedol v roku 1930 Gross. 1927 -28 – Raman experimentálne pozoroval nepružný rozptyl svetla na vzorke benzénu (frekvenčný posun 1012 -1014 Hz). 1944 – Cummings previedol prvý experiment „Kvazi-pružného“ rozptylu (frekvenčné posuny 10 -10 7 Hz), čo je rozptyl na fluktuáciach difúzneho charakteru.

Sir Chandrasekahra V. Raman: Nobelovská prednáška 1930 „ the effect of inelastic scattering of light by molecules is likely to give rise to a vast new field of spectroscopy“
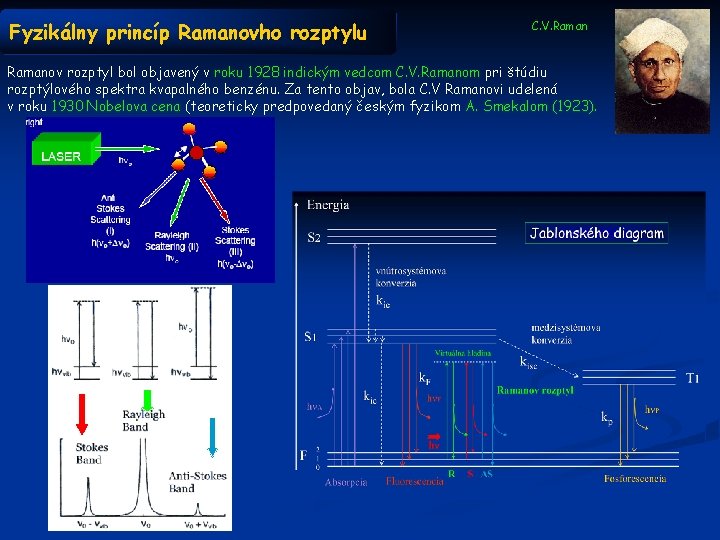
Fyzikálny princíp Ramanovho rozptylu C. V. Ramanov rozptyl bol objavený v roku 1928 indickým vedcom C. V. Ramanom pri štúdiu rozptýlového spektra kvapalného benzénu. Za tento objav, bola C. V Ramanovi udelená v roku 1930 Nobelova cena (teoreticky predpovedaný českým fyzikom A. Smekalom (1923).
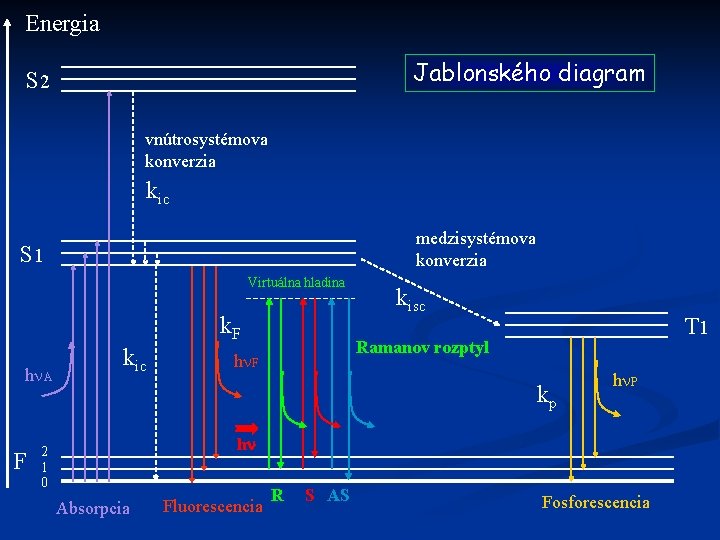
Energia Jablonského diagram S 2 vnútrosystémova konverzia kic medzisystémova konverzia S 1 Virtuálna hladina k. F h A F kic kisc T 1 Ramanov rozptyl h F kp h P h 2 1 0 Absorpcia Fluorescencia R S AS Fosforescencia
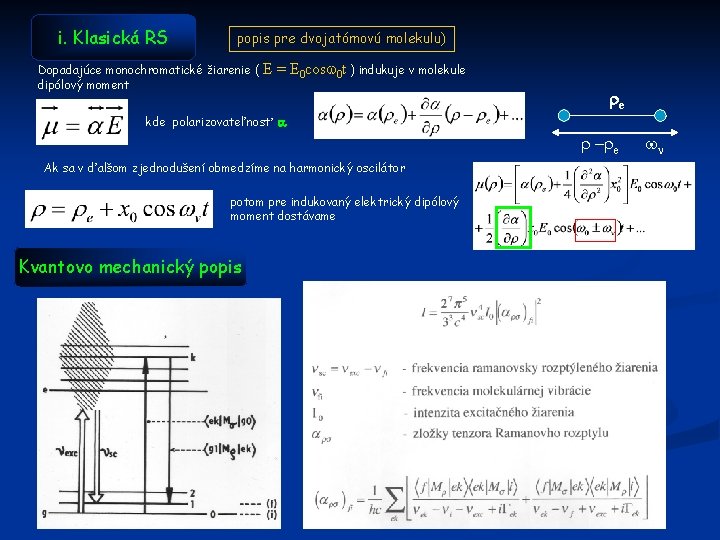
i. Klasická RS popis pre dvojatómovú molekulu) Dopadajúce monochromatické žiarenie ( dipólový moment E = E 0 cosw 0 t ) indukuje v molekule re kde polarizovateľnosť a r –re Ak sa v ďalšom zjednodušení obmedzíme na harmonický oscilátor potom pre indukovaný elektrický dipólový moment dostávame Kvantovo mechanický popis w

Základna schéma aparatúry a vlastnosti RS Vlastnosti RS • Oblasť frekvenčných posuvov 1012 – 1014 Hz (pre vibračné stavy molekúl) • Slabá intenzita IRS/Io ~ 10 -7 – 10 -11 • RS je nekoherentný • Doba trvania: dej okamžitý bez zotrvačnosti
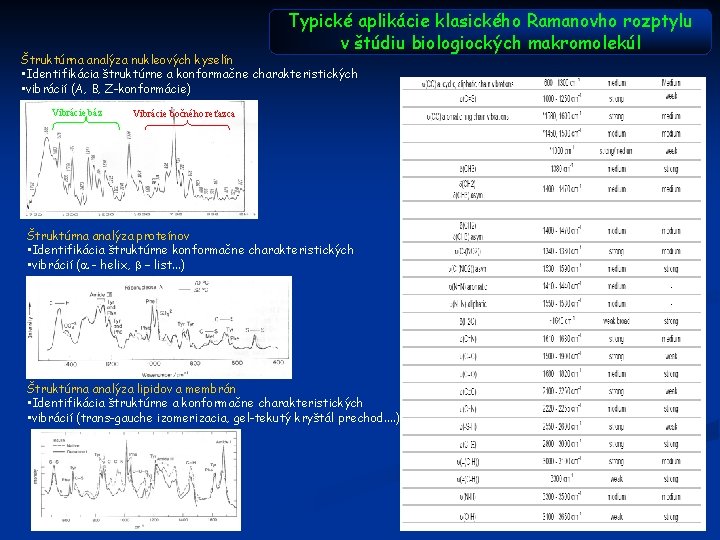
Typické aplikácie klasického Ramanovho rozptylu v štúdiu biologiockých makromolekúl Štruktúrna analýza nukleových kyselín • Identifikácia štruktúrne a konformačne charakteristických • vibrácií (A, B, Z-konformácie) Vibrácie báz Vibrácie bočného reťazca Štruktúrna analýza proteínov • Identifikácia štruktúrne konformačne charakteristických • vibrácií (a - helix, b – list. . . ) Štruktúrna analýza lipidov a membrán • Identifikácia štruktúrne a konformačne charakteristických • vibrácií (trans-gauche izomerizacia, gel-tekutý kryštál prechod. . )
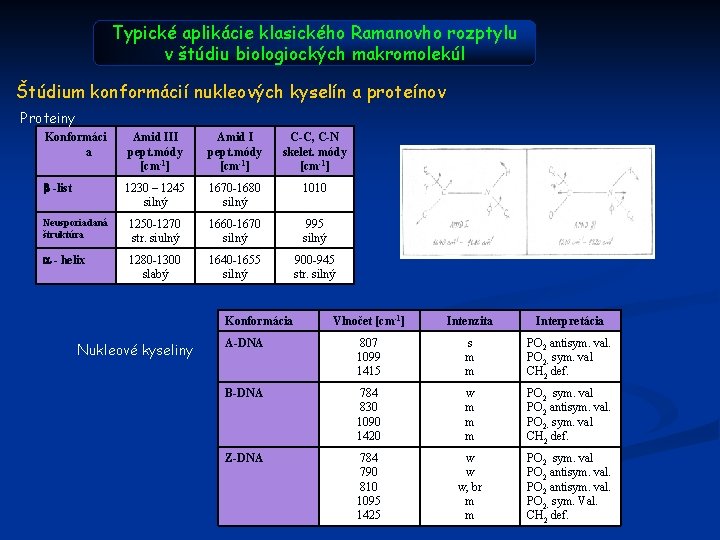
Typické aplikácie klasického Ramanovho rozptylu v štúdiu biologiockých makromolekúl Štúdium konformácií nukleových kyselín a proteínov Proteiny Konformáci a Amid III pept. módy [cm-1] Amid I pept. módy [cm-1] C-C, C-N skelet. módy [cm-1] b -list 1230 – 1245 silný 1670 -1680 silný 1010 Neusporiadaná štruktúra 1250 -1270 str. siulný 1660 -1670 silný 995 silný a - helix 1280 -1300 slabý 1640 -1655 silný 900 -945 str. silný Konformácia Nukleové kyseliny Vlnočet [cm-1] Intenzita Interpretácia A-DNA 807 1099 1415 s m m PO 2 antisym. val. PO 2 - sym. val CH 2 def. B-DNA 784 830 1090 1420 w m m m PO 2 sym. val PO 2 antisym. val. PO 2 - sym. val CH 2 def. Z-DNA 784 790 810 1095 1425 w w w, br m m PO 2 sym. val PO 2 antisym. val. PO 2 - sym. Val. CH 2 def.
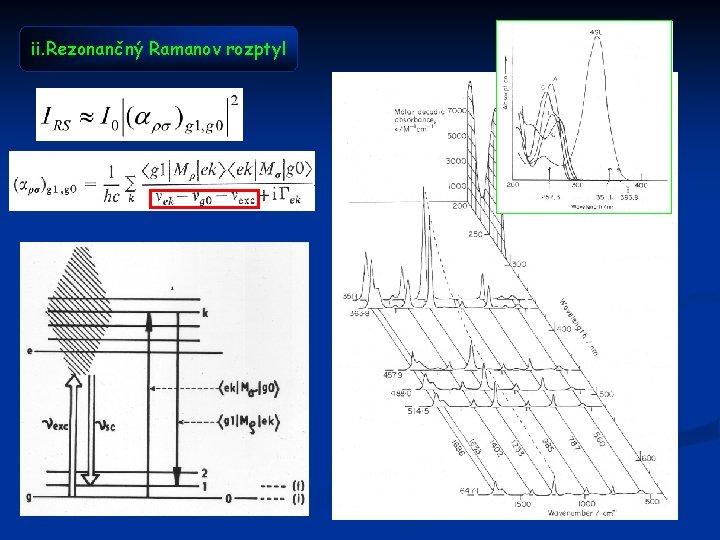
ii. Rezonančný Ramanov rozptyl
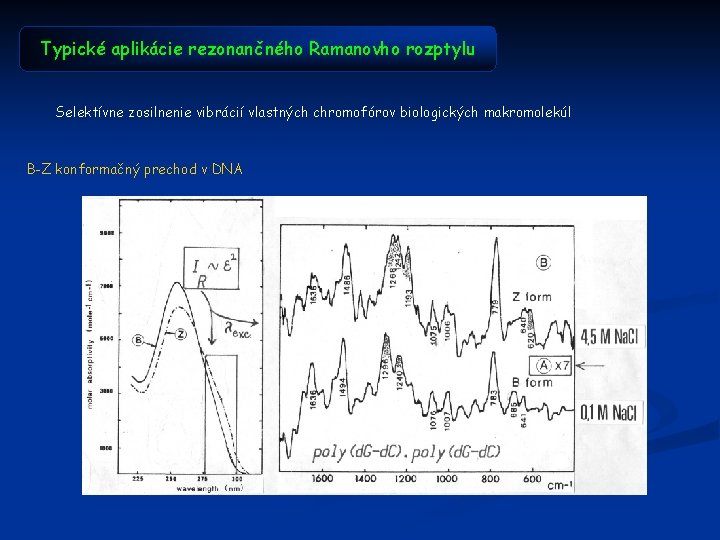
Typické aplikácie rezonančného Ramanovho rozptylu Selektívne zosilnenie vibrácií vlastných chromofórov biologických makromolekúl B-Z konformačný prechod v DNA
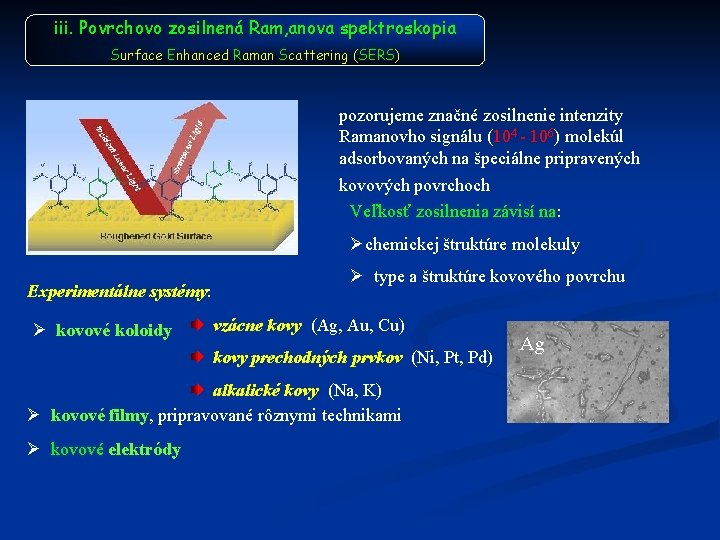
iii. Povrchovo zosilnená Ram, anova spektroskopia Surface Enhanced Raman Scattering (SERS) pozorujeme značné zosilnenie intenzity Ramanovho signálu (104 - 106) molekúl adsorbovaných na špeciálne pripravených kovových povrchoch Veľkosť zosilnenia závisí na: Øchemickej štruktúre molekuly Experimentálne systémy: Ø kovové koloidy Ø type a štruktúre kovového povrchu vzácne kovy (Ag, Au, Cu) kovy prechodných prvkov (Ni, Pt, Pd) alkalické kovy (Na, K) Ø kovové filmy, pripravované rôznymi technikami Ø kovové elektródy Ag
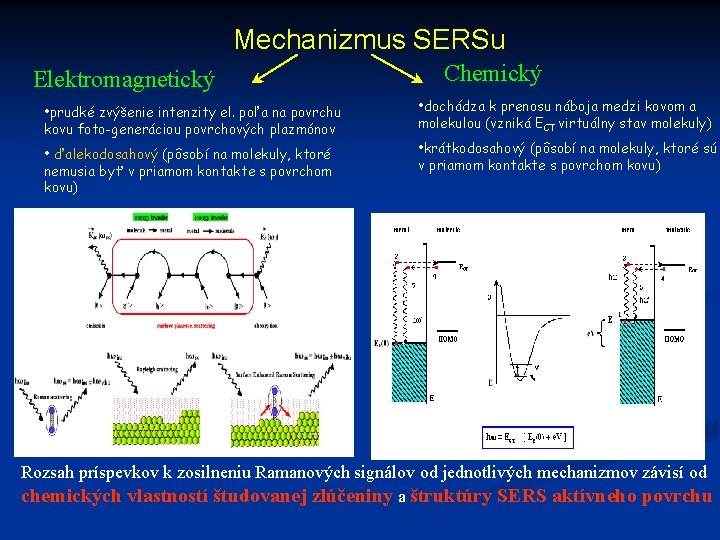
Mechanizmus SERSu Elektromagnetický • prudké zvýšenie intenzity el. poľa na povrchu kovu foto-generáciou povrchových plazmónov • ďalekodosahový (pôsobí na molekuly, ktoré nemusia byť v priamom kontakte s povrchom kovu) Chemický • dochádza k prenosu náboja medzi kovom a molekulou (vzniká ECT virtuálny stav molekuly) • krátkodosahový (pôsobí na molekuly, ktoré sú v priamom kontakte s povrchom kovu) Rozsah príspevkov k zosilneniu Ramanových signálov od jednotlivých mechanizmov závisí od chemických vlastností študovanej zlúčeniny a štruktúry SERS aktívneho povrchu
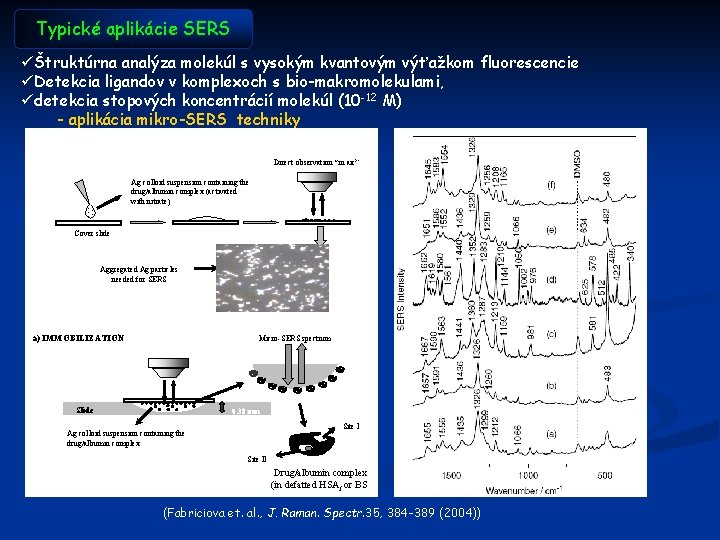
Typické aplikácie SERS üŠtruktúrna analýza molekúl s vysokým kvantovým výťažkom fluorescencie üDetekcia ligandov v komplexoch s bio-makromolekulami, üdetekcia stopových koncentrácií molekúl (10 -12 M) - aplikácia mikro-SERS techniky Direct observation “in air” Ag colloid suspension containing the drug/albumin complex (activated with nitrate) Cover slide Aggregated Ag particles needed for SERS a) IMMOBILIZATION Micro-SERS spectrum Slide 0. 38 mm Site I Ag colloid suspension containing the drug/albumin complex Site II Drug/albumin complex (in defatted HSAf or BS (Fabriciova et. al. , J. Raman. Spectr. 35, 384 -389 (2004))

iv. Coherent Anti-Stokes Raman Scattering (CARS) • polarizácia prostredia spôsobená interakciou s poľom svetelnej vlny je obecne daná vzťahom P = PL + PNL tenzor elekt. susceptibility Ø žiarenie s nízkou intenzitou (E ~ <10, 103> V. m-1) interaguje s prostredím (odraz, absorbcia, rozptyl. . . ) ale nemení jej makroskopické vlatnosti a mikroskopickú štruktúru - takéto pole je slabé a môže vyvolať len lineárnu polarizáciu Ø Ø v silných poliach (E ~ <105, 108> V. m-1) sa menia vlastnosti atómov a molekúl ako aj makroskopické vlastnosti prostredia v silných poliach sa okrem lineárnej polarizácie objavuje aj nelineárna polarizácia vznik nových nelineárnych optických javov üviacfotónova absorpcia ü generácia vyšších harmonických frekvencií (nw) ü zmiešavanie frekvencií (w 1+w 2 - w 3+-. . wn)

Zmiešavanie frekvencií laserového žiarenia Ø na nelineárnu látku bez centra symetrie dopadajú dve elmag. vlny s frekvenciami w 1 a w 2 a vlnovými vektormi k 1 a k 2 Ø polarizácia druhého rádu bude Ø prvýkrát dostávame zmiešavanie vĺn kde Ø Ak máme elmag pole 2. dopadajúcej vlny, potom sa v polarizácii 2. rádu objavý výraz , v ktorom = 1. . w 1 = w 2 = 2. . w 1 ≠ w 2 Ak na nelineárnu látku dopadajú dve elmag. vlny s frekvenciami w 1 a w 2 a vlnovými vektormi k 1 a k 2 potom v látke vzniká nová vlna s frekvenciou w 3 = w 1 ± w 2 - frekvenčný synchroizmus k 3 = k 1 ± k 2 - priestorový synchroizmus

Generácia druhej harmonickej P = PL + PNL P(r, t) = P(1) + P(2) + P(3) +. . . + P(n) P(2) môžeme vyjadriť: Pi(2) (r, t) = cijk. Ej(r, t). Ek(r, t) E(r, t) = E(0). cos(k. r - wt) Statická polarizácia nezávislá na frekvencii Ø v nelineárnom prostredí, kde je cijk ≠ 0 a pri vysokej intenzite žiarenia vzniká statická polarizácia a polarizácia časovo závislá s 2 w, ktorú sprevádza vznik novej elmag. vlny v prostredí s frekvenciou 2 w = Generácia druhej harmonickej Ø Intenzita takto generovanej vlny, ktorá vzniká v nelineárnom prostredí o hrúbke d polarizácia závislá na čase s frekvenciou 2 w 2 w, k 2 kw d priestorový synchroizmus
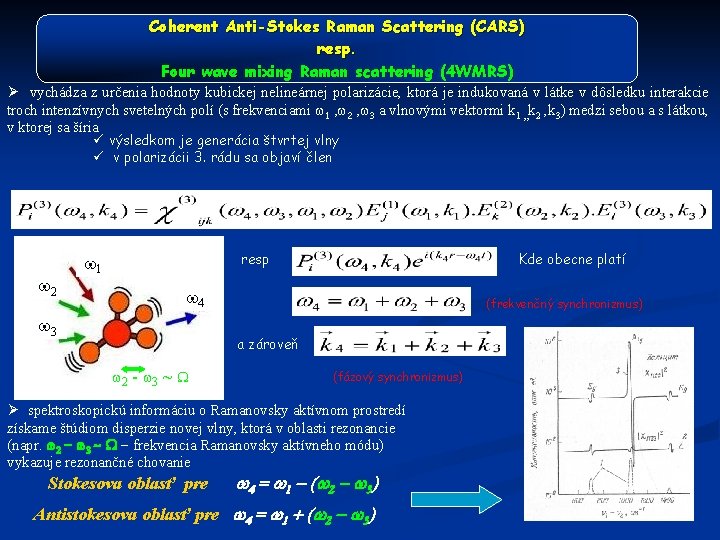
Coherent Anti-Stokes Raman Scattering (CARS) resp. Four wave mixing Raman scattering (4 WMRS) Ø vychádza z určenia hodnoty kubickej nelineárnej polarizácie, ktorá je indukovaná v látke v dôsledku interakcie troch intenzívnych svetelných polí (s frekvenciami w 1 , w 2 , w 3 a vlnovými vektormi k 1 , , k 2 , k 3) medzi sebou a s látkou, v ktorej sa šíria ü výsledkom je generácia štvrtej vlny ü v polarizácii 3. rádu sa objaví člen w 2 resp w 1 Kde obecne platí w 4 w 3 (frekvenčný synchronizmus) a zároveň w 2 - w 3 ~ W (fázový synchronizmus) Ø spektroskopickú informáciu o Ramanovsky aktívnom prostredí získame štúdiom disperzie novej vlny, ktorá v oblasti rezonancie (napr. w 2 - w 3 ~ W - frekvencia Ramanovsky aktívneho módu) vykazuje rezonančné chovanie Stokesova oblasť pre w 4 = w 1 - (w 2 - w 3) Antistokesova oblasť pre w 4 = w 1 + (w 2 - w 3)

Praktická realizácia experimentu CARS Ø obecný výraz pre kubickú nelineárnu polarizáciu prostredia interagujúceho s troma intenzívnymi monochromatickými vlnami ak označíme Potom ramanovsky aktívny vibračný mód je w 1 - w 3 ~ W na chaoticky molekulový pohyb sa nakladajú regulárne vynútené vibrácie, ktorých fázy sú v rôznych molekulách určené fázami svetelného poľa – sfázovanie molekulových vibrácií Ø spektroskopickú informáciu získame štúdiom disperzie as vlny w. AS = w 1+ (w 1 -w 3)=2 w 1 – w 3 Intenzita CARS Dk = k. AS - 2 k 1 + k 3 = 0 k. AS = 2 k 1 – k 3 fázový synchroizmus k. AS a k 3 -k 3 2 k 1

Coherent Anti-Stokes Raman Scattering (CARS) Výhody CARS: Ø priestorové smerovanie – splnenie podmienky fázového synchroizmu umožňuje priestorové oddelenie signálu w. AS od signálu frekvencií w 1 , w 3 Ø signál o frekvencii w. AS leží mimo oblasť luminiscencie, umožňuje sledovať RS farbív Ø intenzita signálu – signál CARS v bielkovinách a nukleových kyselinách je pri medzných intenzitách budenia o rád až dva vyžší ako signál RS Ø priestorové vymedzenie pozorovanej vzorky v mieste priesečníkov dvoch lúčov je možné prevádzať merania v 3 D objektoch (separované časti veľkých buniek) Problémy CARS: Ø nerezonančné pozadie, ktoré je možné potlačiť napr. nasledujúcimi metódami: - polarizačná filtrácia CARS - metóda vynútenej RS (nevhodná pre bio vzorky) - polarizačná modulačná spektroskopia (RIKES) - časovo rozlíšený CARS Ø dosiahnutie fázovej zhody – uhol a medzi k 1 a k 3 nie je ľubovoľný k. AS a k 3 -k 3 k. AS = 2 k 1 – k 3 2 k 1
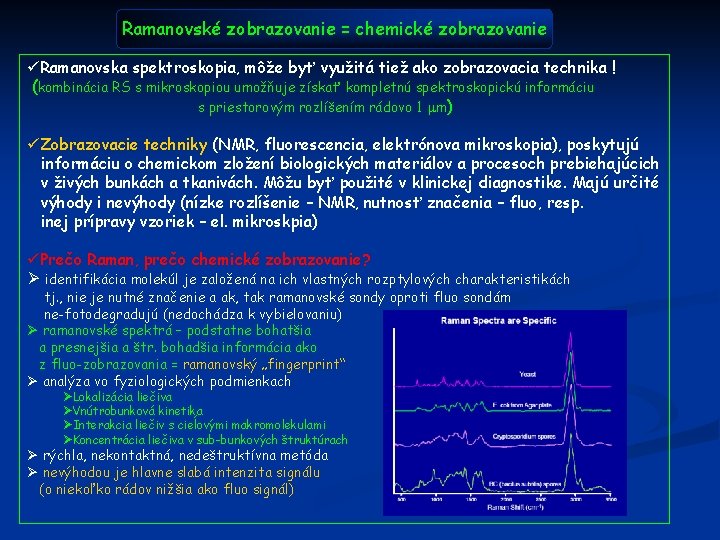
Ramanovské zobrazovanie = chemické zobrazovanie üRamanovska spektroskopia, môže byť využitá tiež ako zobrazovacia technika ! (kombinácia RS s mikroskopiou umožňuje získať kompletnú spektroskopickú informáciu s priestorovým rozlíšením rádovo 1 mm) üZobrazovacie techniky (NMR, fluorescencia, elektrónova mikroskopia), poskytujú informáciu o chemickom zložení biologických materiálov a procesoch prebiehajúcich v živých bunkách a tkanivách. Môžu byť použité v klinickej diagnostike. Majú určité výhody i nevýhody (nízke rozlíšenie – NMR, nutnosť značenia – fluo, resp. inej prípravy vzoriek – el. mikroskpia) üPrečo Raman, prečo chemické zobrazovanie? Ø identifikácia molekúl je založená na ich vlastných rozptylových charakteristikách tj. , nie je nutné značenie a ak, tak ramanovské sondy oproti fluo sondám ne-fotodegradujú (nedochádza k vybielovaniu) Ø ramanovské spektrá – podstatne bohatšia a presnejšia a štr. bohadšia informácia ako z fluo-zobrazovania = ramanovský „fingerprint“ Ø analýza vo fyziologických podmienkach ØLokalizácia liečiva ØVnútrobunková kinetika ØInterakcia liečiv s cieĺovými makromolekulami ØKoncentrácia liečiva v sub-bunkových štruktúrach Ø rýchla, nekontaktná, nedeštruktívna metóda Ø nevýhodou je hlavne slabá intenzita signálu (o niekoľko rádov nižšia ako fluo signál)
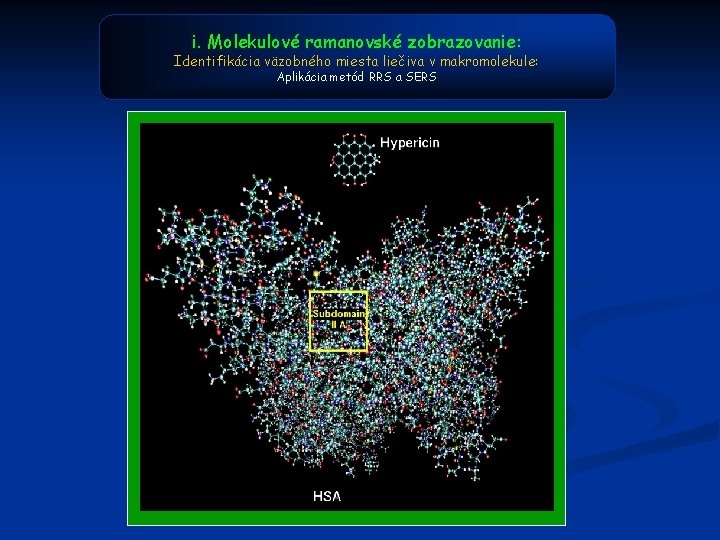
i. Molekulové ramanovské zobrazovanie: Identifikácia väzobného miesta liečiva v makromolekule: Aplikácia metód RRS a SERS
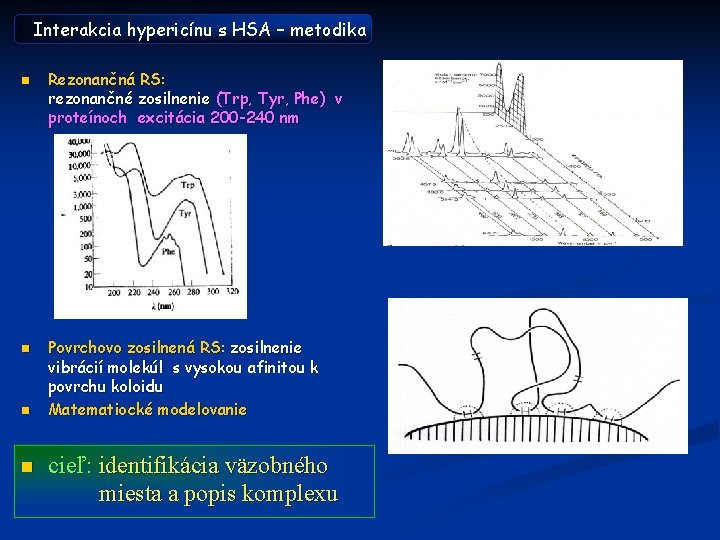
Interakcia hypericínu s HSA – metodika n n Rezonančná RS: rezonančné zosilnenie (Trp, Tyr, Phe) v proteínoch excitácia 200 -240 nm Povrchovo zosilnená RS: zosilnenie vibrácií molekúl s vysokou afinitou k povrchu koloidu Matematiocké modelovanie cieľ: identifikácia väzobného miesta a popis komplexu
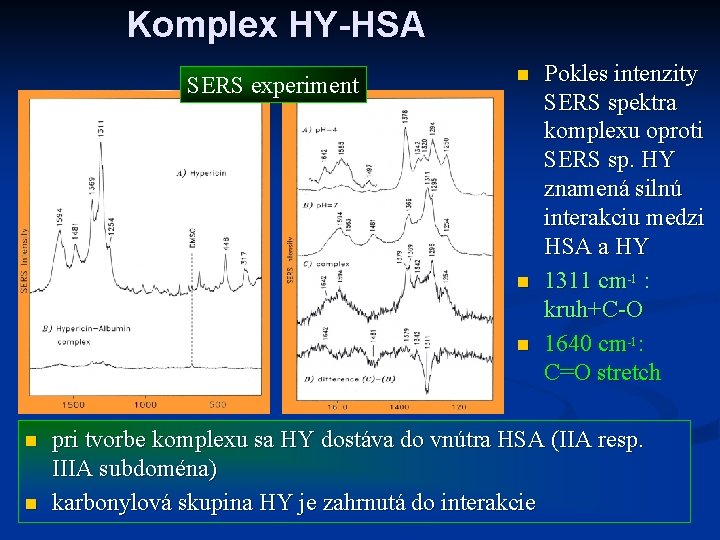
Komplex HY-HSA SERS experiment n n n Pokles intenzity SERS spektra komplexu oproti SERS sp. HY znamená silnú interakciu medzi HSA a HY 1311 cm-1 : kruh+C-O 1640 cm-1: C=O stretch pri tvorbe komplexu sa HY dostáva do vnútra HSA (IIA resp. IIIA subdoména) karbonylová skupina HY je zahrnutá do interakcie
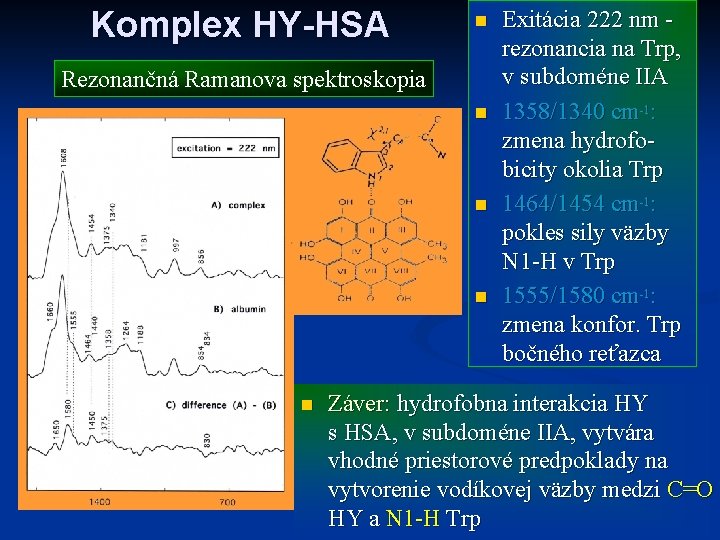
Komplex HY-HSA n Rezonančná Ramanova spektroskopia n n Exitácia 222 nm rezonancia na Trp, v subdoméne IIA 1358/1340 cm-1: zmena hydrofobicity okolia Trp 1464/1454 cm-1: pokles sily väzby N 1 -H v Trp 1555/1580 cm-1: zmena konfor. Trp bočného reťazca Záver: hydrofobna interakcia HY s HSA, v subdoméne IIA, vytvára vhodné priestorové predpoklady na vytvorenie vodíkovej väzby medzi C=O HY a N 1 -H Trp
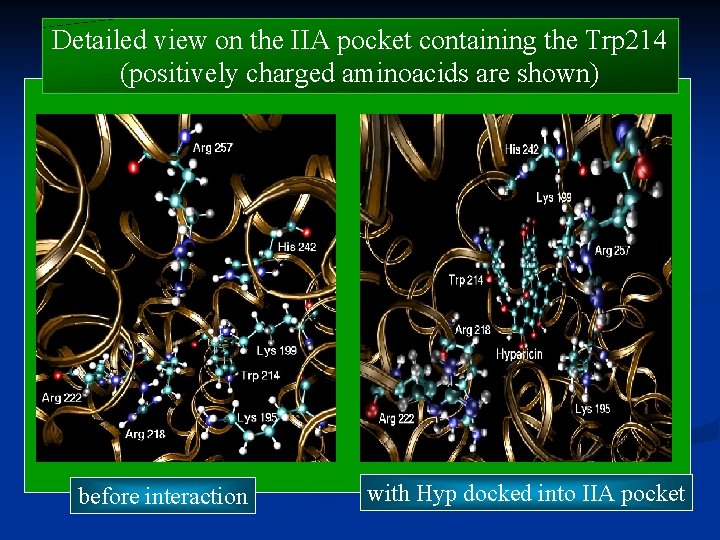
Detailed view on the IIA pocket containing the Trp 214 (positively charged aminoacids are shown) before interaction with Hyp docked into IIA pocket
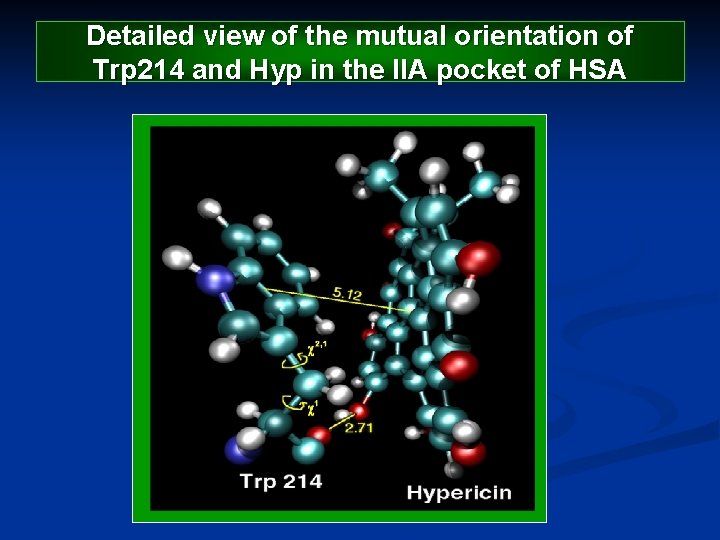
Detailed view of the mutual orientation of Trp 214 and Hyp in the IIA pocket of HSA
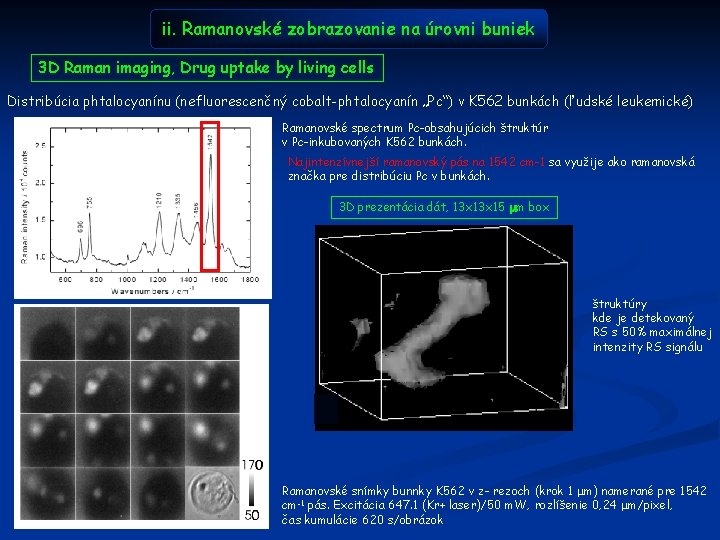
ii. Ramanovské zobrazovanie na úrovni buniek 3 D Raman imaging, Drug uptake by living cells Distribúcia phtalocyanínu (nefluorescenčný cobalt-phtalocyanín „Pc“) v K 562 bunkách (ľudské leukemické) Ramanovské spectrum Pc-obsahujúcich štruktúr v Pc-inkubovaných K 562 bunkách. Najintenzívnejší ramanovský pás na 1542 cm-1 sa využije ako ramanovská značka pre distribúciu Pc v bunkách. 3 D prezentácia dát, 13 x 15 mm box štruktúry kde je detekovaný RS s 50% maximálnej intenzity RS signálu Ramanovské snímky bunnky K 562 v z- rezoch (krok 1 mm) namerané pre 1542 cm-1 pás. Excitácia 647. 1 (Kr+ laser)/50 m. W, rozlíšenie 0, 24 mm/pixel, čas kumulácie 620 s/obrázok
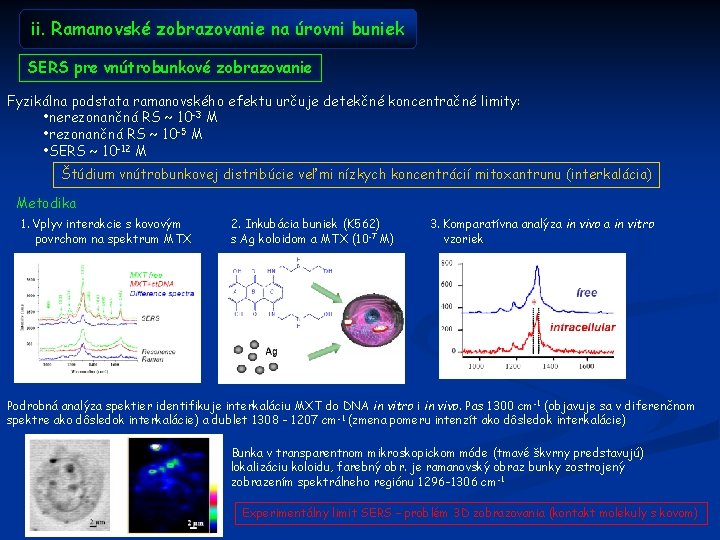
ii. Ramanovské zobrazovanie na úrovni buniek SERS pre vnútrobunkové zobrazovanie Fyzikálna podstata ramanovského efektu určuje detekčné koncentračné limity: • nerezonančná RS ~ 10 -3 M • rezonančná RS ~ 10 -5 M • SERS ~ 10 -12 M Štúdium vnútrobunkovej distribúcie veľmi nízkych koncentrácií mitoxantrunu (interkalácia) Metodika 1. Vplyv interakcie s kovovým povrchom na spektrum MTX 2. Inkubácia buniek (K 562) s Ag koloidom a MTX (10 -7 M) 3. Komparatívna analýza in vivo a in vitro vzoriek Podrobná analýza spektier identifikuje interkaláciu MXT do DNA in vitro i in vivo. Pas 1300 cm -1 (objavuje sa v diferenčnom spektre ako dôsledok interkalácie) a dublet 1308 - 1207 cm -1 (zmena pomeru intenzít ako dôsledok interkalácie) Bunka v transparentnom mikroskopickom móde (tmavé škvrny predstavujú) lokalizáciu koloidu, farebný obr. je ramanovský obraz bunky zostrojený zobrazením spektrálneho regiónu 1296 -1306 cm -1 Experimentálny limit SERS – problém 3 D zobrazovania (kontakt molekuly s kovom)

ii. Ramanovské zobrazovanie na úrovni buniek 3 D CARS zobrazovanie Najdôležitejšie požiadavky na optické zobrazovacie techniky pre vizualizáciu biologických objektov sú: i) neinvazívnosť, ii) chemická selektivita iii) vysoká citlivosť Klasická ramanovská mikroskopia môže spĺňať prvé dve požiadavky, ale nie poslednú (SERS – je invazívna technika). ü klasický RS detekuje jeden fotón z toku 10 10 fotónov prechádzajúcich vzorkou hrubou 1 mm ü 1/1016 z fluorescencie ü Vzhľadom na slabý signál potrebuje klasická ramanovská mikroskopia: ü Vysoký výkon lasera (> 10 m. W) ü Dlhý detekčný čas (cca minuty - hodiny na obrazok) CARS mikroskopia spĺňa všetky tri požiadavky. Jednoznačne predstavuje kvalitatívny prielom v zobrazovacích technikách Prvý CARS mikroskop bol zkonštruovaný v roku 1982: Duncan et al. Opt. Lett. 25, 387 (1982) Problémy: • slabé spektrálne rozlíšenie (fs lasery, 10 fs ~ 440 cm-1) • intenzívne nerezonančné pozadie Podstatné vylepšenie: 1999 A. Zumbusch et al. Phys. Rew. Lett. 82, 4142 (1999) • ps IR lasery (2 -5 ps, čo zodpovedá cca 10 – 20 cm -1) • objektív s veľou numerickou apertúrou (podstatné zlepšenie fázového synchronizmu) • IR lasery so stredným výkonom 1 -2 m. W (nedochádza k deštrukcii vzorky), hlbšia penetrácia, eliminácia nerezonančného pozadia • to umožňuje : - podstatne zvýšiť spektrálne a časové rozlíšenie (sledovanie in situ dynamiky dejov)
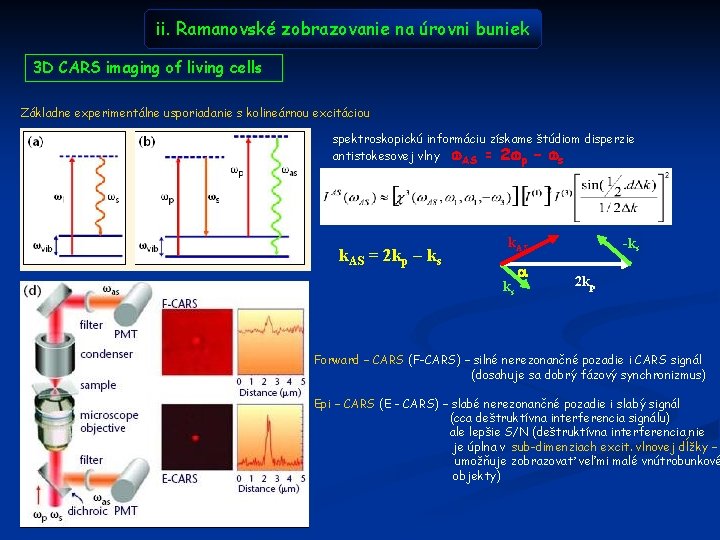
ii. Ramanovské zobrazovanie na úrovni buniek 3 D CARS imaging of living cells Základne experimentálne usporiadanie s kolineárnou excitáciou spektroskopickú informáciu získame štúdiom disperzie antistokesovej vlny w. AS = 2 wp – ws k. AS = 2 kp – ks k. AS ks a -ks 2 kp Forward – CARS (F-CARS) – silné nerezonančné pozadie i CARS signál (dosahuje sa dobrý fázový synchronizmus) Epi – CARS (E - CARS) – slabé nerezonančné pozadie i slabý signál (cca deštruktívna interferencia signálu) ale lepšie S/N (deštruktívna interferencia nie je úplna v sub-dimenziach excit. vlnovej dĺžky – umožňuje zobrazovať veľmi malé vnútrobunkové objekty)
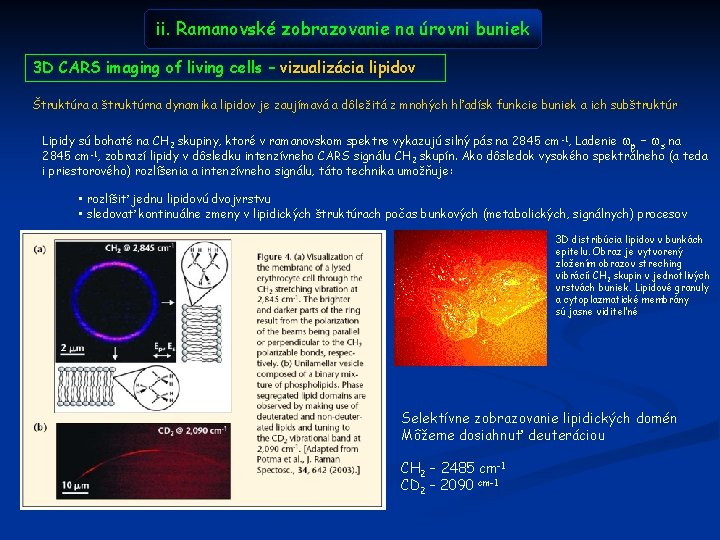
ii. Ramanovské zobrazovanie na úrovni buniek 3 D CARS imaging of living cells – vizualizácia lipidov Štruktúra a štruktúrna dynamika lipidov je zaujímavá a dôležitá z mnohých hľadísk funkcie buniek a ich subštruktúr Lipidy sú bohaté na CH 2 skupiny, ktoré v ramanovskom spektre vykazujú silný pás na 2845 cm -1, Ladenie wp – ws na 2845 cm-1, zobrazí lipidy v dôsledku intenzívneho CARS signálu CH 2 skupín. Ako dôsledok vysokého spektrálneho (a teda i priestorového) rozlíšenia a intenzívneho signálu, táto technika umožňuje: • rozlíšiť jednu lipidovú dvojvrstvu • sledovať kontinuálne zmeny v lipidických štruktúrach počas bunkových (metabolických, signálnych) procesov 3 D distribúcia lipidov v bunkách epitelu. Obraz je vytvorený zložením obrazov streching vibrácií CH 2 skupin v jednotlivých vrstvách buniek. Lipidové granuly a cytoplazmatické membrány sú jasne viditeľné Selektívne zobrazovanie lipidických domén Môžeme dosiahnuť deuteráciou CH 2 – 2485 cm-1 CD 2 – 2090 cm-1

iii. Ramanovské zobrazovanie na úrovni tkanív Motivácia: Zopakujme PREČO môže byť ramanovské zobrazovanie užitočné i na úrovni tkanív? Dôvodom je vyššie priestorové rozlíšenie (Rayleighovo rozlišovacie kritérium) ako napr. (NMR, OCT), resp. obsahovo bahatšie ako fluo-zobrazovanie • fluorescencia – je extrémne citlivá (s vysokým rozlíšením), ale obmedzená na pár fluorofórov (NAD+, elastín, flavín) tkanivách - fluorescenčné značky môžu ovplyvniť biologické deje prebiehajúce v Ramanovské zobrazovanie umožňuje získať informáciu odrážajúcu MOLEKULOVÉ ZLOŽENIE tkaniva až do hĺbky niekoľných milimetrov (v závislosti od vlnovej dĺžky excitácie) bez použitia ramanovských značiek Umožňuje hĺbkove merania relatívnych koncentrácií základných zložiek epidermu (voda, proteíny. . ) RAMANOVSKÉ ZOBRAZOVANIE = CHEMICKÉ ZOBRAZOVANIE Používané excitácie – NIR = eliminácia autofluorescencie pigmentov pokožky
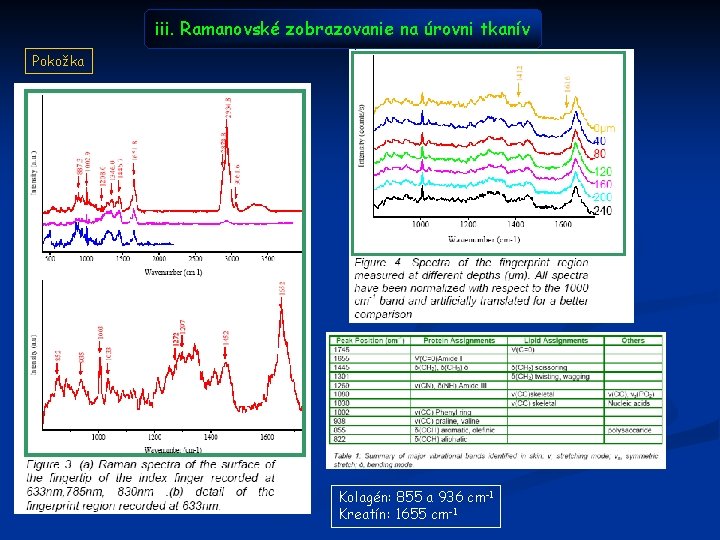
iii. Ramanovské zobrazovanie na úrovni tkanív Pokožka Kolagén: 855 a 936 cm-1 Kreatín: 1655 cm-1
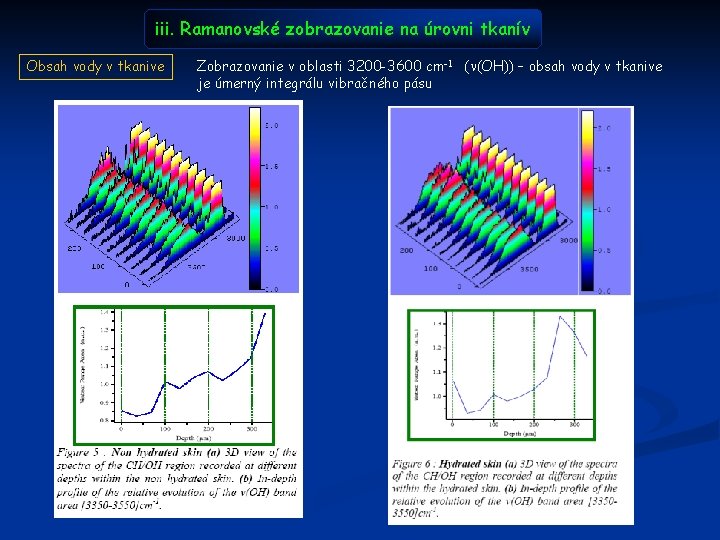
iii. Ramanovské zobrazovanie na úrovni tkanív Obsah vody v tkanive Zobrazovanie v oblasti 3200 -3600 cm-1 ( (OH)) – obsah vody v tkanive je úmerný integrálu vibračného pásu
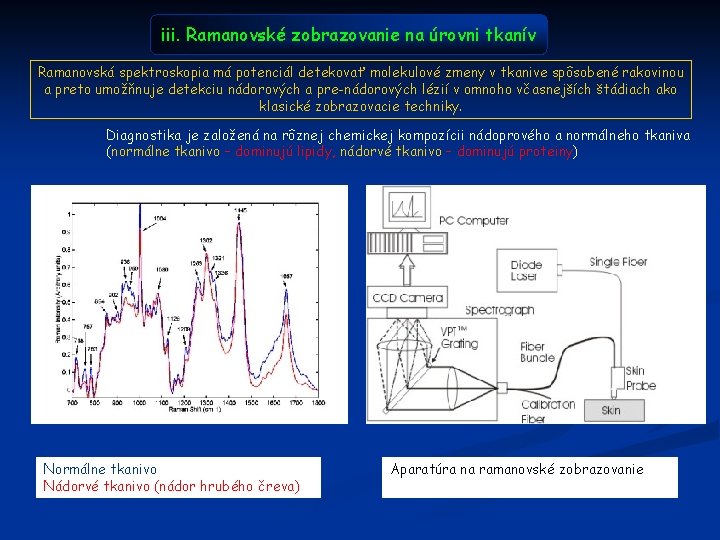
iii. Ramanovské zobrazovanie na úrovni tkanív Ramanovská spektroskopia má potenciál detekovať molekulové zmeny v tkanive spôsobené rakovinou a preto umožňnuje detekciu nádorových a pre-nádorových lézií v omnoho včasnejších štádiach ako klasické zobrazovacie techniky. Diagnostika je založená na rôznej chemickej kompozícii nádoprového a normálneho tkaniva (normálne tkanivo – dominujú lipidy, nádorvé tkanivo – dominujú proteiny) Normálne tkanivo Nádorvé tkanivo (nádor hrubého čreva) Aparatúra na ramanovské zobrazovanie
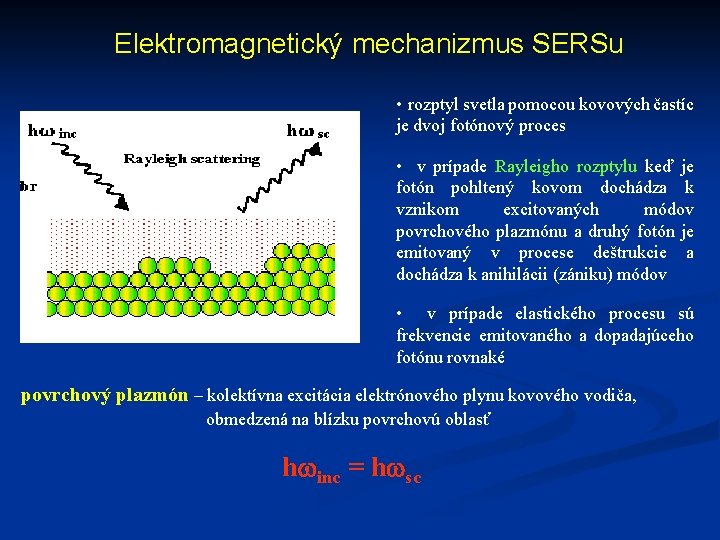
Elektromagnetický mechanizmus SERSu • rozptyl svetla pomocou kovových častíc je dvoj fotónový proces • v prípade Rayleigho rozptylu keď je fotón pohltený kovom dochádza k vznikom excitovaných módov povrchového plazmónu a druhý fotón je emitovaný v procese deštrukcie a dochádza k anihilácii (zániku) módov • v prípade elastického procesu sú frekvencie emitovaného a dopadajúceho fotónu rovnaké povrchový plazmón – kolektívna excitácia elektrónového plynu kovového vodiča, obmedzená na blízku povrchovú oblasť hwinc = hwsc

Chemický mechanizmus SERSu • krátkodosahový mechanizmus, ktorý si vyžaduje bezprostredný kontakt medzi skúmanou látkou a povrchom kovu Ø prvý krok je excitácia elektrónu vodivostného pásu kovu do prázdneho stavu Ø dochádza k prenosu náboja medzi kovom a molekulou Ø príslušný elektrónový stav, ECT, je označovaný ako virtuálny stav daný zmiešavaním neväzobného stavu molekuly a ľubovoľného stavu kovu Ø to znamená, že molekula sa počas vibračného prechodu nachádza v inom vibračnom stave, takže fotón ktorý opúšťa daný systém má trošku pozmenenú energiu Ø posledným krokom je dohasínanie elektrónu späť do jamy vo vodivostnom páse kovu
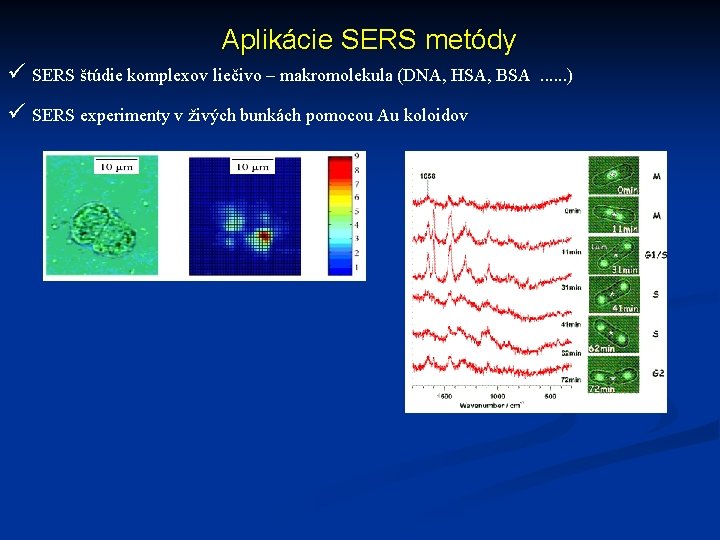
Aplikácie SERS metódy ü SERS štúdie komplexov liečivo – makromolekula (DNA, HSA, BSA ü SERS experimenty v živých bunkách pomocou Au koloidov . . . )

Aplikácie SERS metódy ü SERS štúdie komplexov liečivo – makromolekula (DNA, HSA, BSA . . . ) ü SERS experimenty v živých bunkách pomocou Au koloidov ü detekcia pozemných mín pomocou Ramanovho optického vlákna ü sledovanie hydrotermálnych oxidačných procesov Ramanovým optickým vláknom
- Slides: 58