Radian chemie Katalyztory Klra Opatrn Jakub Hofrichter Cle

Radiační chemie – Katalyzátory Klára Opatrná Jakub Hofrichter

Cíle • Cíl I: připravit řadu směsných oxidových katalyzátorů Ni. O-Ti. O 2 s proměnlivým zastoupením obou složek • Cíl II: chemická analýza připravených katalyzátorů • Cíl III: Studium katalytických vlastností připravené řady a ovlivnění těchto vlastností fyzikálně chemickými metodami

Příprava katalyzátorů Cíl I: připravit řadu směsných oxidových katalyzátorů Ni. O-Ti. O 2 s proměnlivým zastoupením obou složek Ø Výchozí látky: • tetra-n-butyl-orthotitanát • dusičnan nikelnatý • Kyselina dusičná • Hydroxid draselný

Příprava katalyzátorů Ø Postup přípravy: 1. Převedeme tetra-n-butyl-orthotitanát na dusičnan 2. V určitém poměru smícháme Ti(NO 3)4 a Ni(NO 3)2 3. Rozpustíme je v HNO 3 4. Vznikne Ti 4+ + Ni 2+ + NO 3 - + H 2 O v kyselém roztoku

Příprava katalyzátorů Ø Postup přípravy: 5. Srážíme pomocí KOH 6. Vytvoří se smíšené krystalky Ti(OH)4 + Ni(OH)2 7. Přefiltrujeme – zbavíme se části H 2 O 8. Kalcinace v peci (teplota v peci 450°C) → vznikne Ni. O + Ti. O 2 9. Vzniklou hmotu rozemeleme v mlýnku
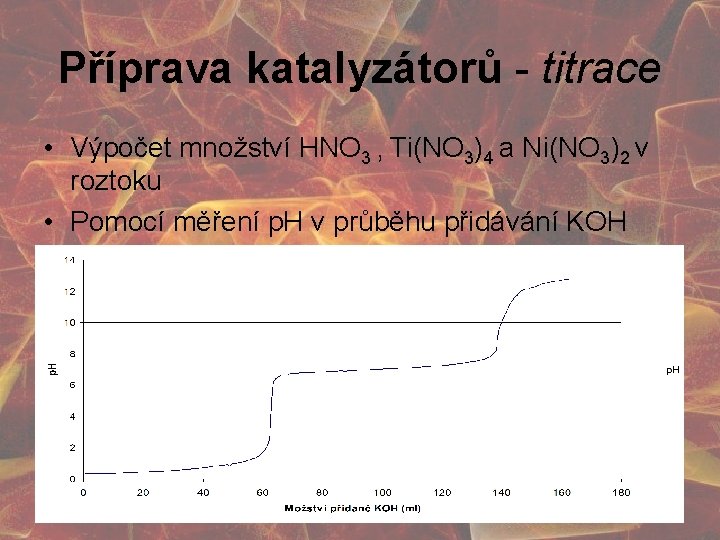
Příprava katalyzátorů - titrace • Výpočet množství HNO 3 , Ti(NO 3)4 a Ni(NO 3)2 v roztoku • Pomocí měření p. H v průběhu přidávání KOH

Analýza katalyzátorů • • Cíl II: chemická analýza připravených katalyzátorů Přesné stanovení složení vzorků Stanovení nadstechiometrického kyslíku Stanovení velikosti měrných povrchů RTG strukturální analýza

Nadstechiometrický kyslík Stanovení jodometrickou titrací Ø Potřebné chemikálie: • 0, 4% vodný roztok škrobu • 0, 01 M thiosiřičitan sodný • 0, 01 M kyselina chlorovodíková • 2 M kyselina sírová • Pevný jodid draselný

RTG strukturální analýza • Využití interference odražených paprsků rentgenového záření od krystalických rovin • Umožňuje určit mřížkovou konstantu • Braggova podmínka: 2 dsinν = nλ • Poznáme složení polykrystalických látek

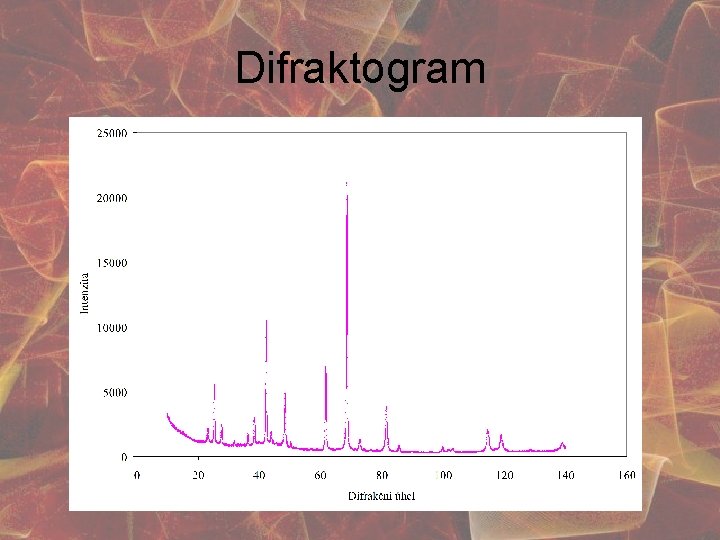
Difraktogram

Katalytická aktivita Cíl III: Studium katalytických vlastností připravené řady a ovlivnění těchto vlastností fyzikálně chemickými metodami • Měření rychlosti katalytického rozkladu peroxidu vodíku • Výpočty rychlostních konstant, zdánlivé aktivační energie • Vliv ionizujícího záření, tepelného opracování, chemické impregnace a termického rozkladu na katalytickou aktivitu

Rozklad peroxidu vodíku • Rozklad: 2 H 2 O 2 → 2 H 2 O + O 2
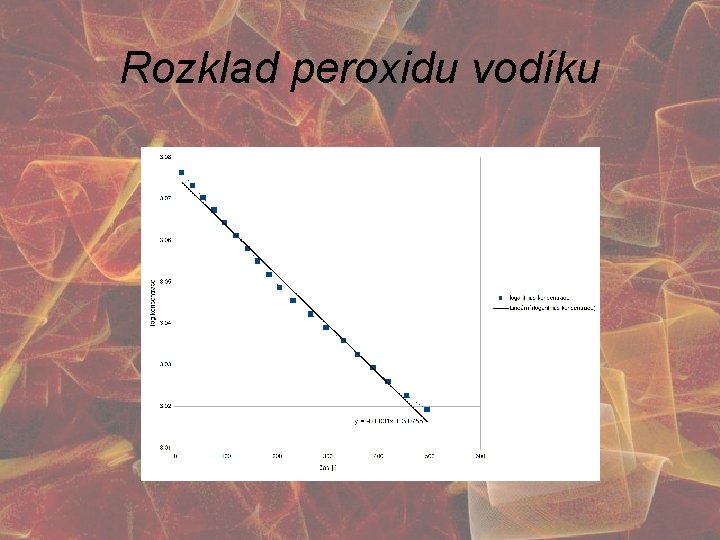
Rozklad peroxidu vodíku
- Slides: 14