RACTIONS DE LA PHASE I Ractions de dgradations







- Slides: 11

• RÉACTIONS DE LA PHASE I : Réactions de dégradations Siège principal: Hépatocyte (Réticulum endoplasmique - Mitochondries) Les principales réactions : Réactions d’oxydation Réactions de réduction Réactions d’hydrolyse 1

I. 1. OXYDATIONS Les plus importantes, essentiellement dans le foie au niveau des microsomes d’où le nom d’oxydations microsomales hépatiques I. 1. 1. Hydroxylations Elles correspondent à des réactions de fixation d’un groupement hydroxyle (–OH) sur des chaines linéaires ou des cycles aromatiques grâce à des hydroxylases microsomales Les chaines linéaires sont transformées en alcools secondaires, l’hydroxylation se faisant sur l’avant dernier carbone. C’est la principale réaction subie par les barbituriques Ex: Hydroxylation du Pentobarbital (Anesthésique général) - Enzyme : Hydroxylase - Métabolite : Propranolol Conséquence: accélération de l’élimination rénale 2

• I. 1. 2. N et S oxydations Elles aboutissent à la fixation d’une fonction oxygène sur des atomes d’azote ou de soufre. Les amines primaires et secondaires donnent des hydroxylamines, alors que les amines tertiaires donnent des dérivés N-oxydés. Les S oxydations conduisent à des sulfoxydes puis à des sulfones. Ex: N oxydation des sulfamides - Enzyme : N oxydase - Métabolite : N hydroxylés Conséquence: dérivés à potentialité méthémoglobinisante (anoxie) ce qui augmente la toxicité 3

I. 1. 3. Désalkylations oxydatives Ce sont des réactions qui détachent des radicaux alkyles (le plus souvent –CH 3)des atomes d’oxygène ou d’azote, on parle de O-désalkylation et de N-désalkylation, cette dernière conduit à des dérivés N. O. R (Nitrogen Ohne Radical) I. 1. 4. Désaminations oxydatives Elles correspondent au détachement de groupements amine (–NH 2) avec fixation d’une fonction oxygénée Ces réactions s’effectuent en dehors des microsomes hépatiques grâce aux monoamine-oxydases (MAO) et diamine-oxydases (DAO) localisés dans les mitochondries du foie, du rein et du système nerveux 4

I. 1. 5. Désulfurations oxydatives Elles substituent des atomes de soufre par des atomes d’oxygène I. 1. 6. Oxydations des alcools et des aldéhydes Elles se font en dehors des microsomes hépatiques grâce à des alcool-Déshydrogénases et des aldéhyde-déshydrogénases situées dans le cytochrome de l’hépatocyte 5

I. 2. RÉDUCTION • Ce sont des réactions moins fréquentes que les oxydations Elles se font en anaérobiose surtout dans les microsomes hépatiques. Elles sont importantes chez les ruminants, dans le tube digestif sous l’action de la flore réductrice • Ce sont des nitro- réductions et des azo-réductions. Ces réactions sont moins importantes que les oxydations Ex: Réduction de la Cortisone (Hormone cortico-surrénalienne et Corticoide) - Enzyme : Réductase - Métabolite : Hydrocortisol (Cortisol) Conséquence : un médicament en sa forme active (bioactivation) 6

I. 3. HYDROLYSE • Ce sont des réactions très importantes dans l’organisme, elles peuvent avoir lieu dans tous les organes et tissus compte tenu de leur richesse en eau • Elles intéressent les esters et les amides et sont souvent catalysées par des estérases et des amidases 7

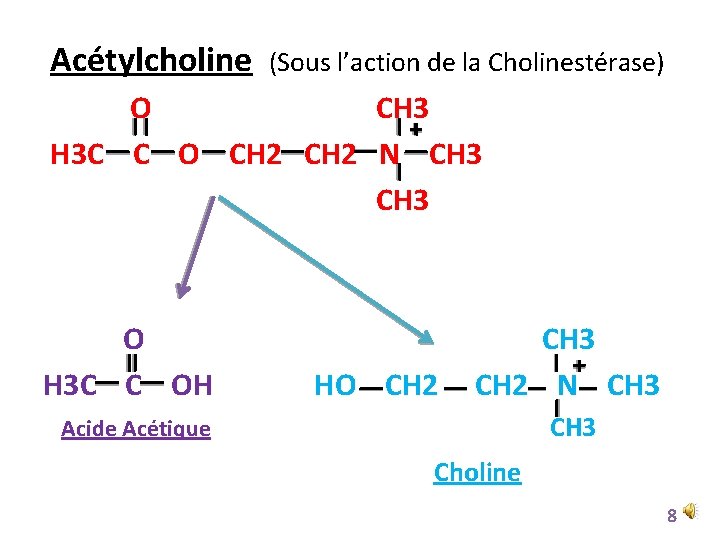
Acétylcholine (Sous l’action de la Cholinestérase) O CH 3 H 3 C C O CH 2 N CH 3 O H 3 C C OH HO CH 2 CH 3 CH 2 N CH 3 Acide Acétique Choline 8

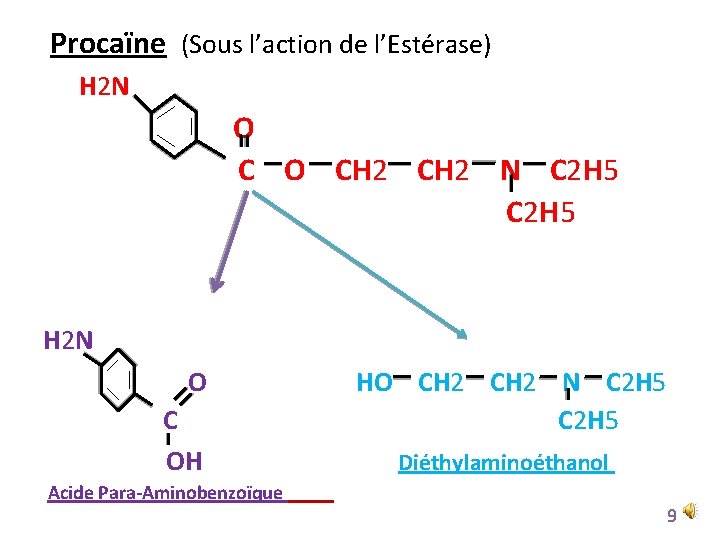
Procaïne (Sous l’action de l’Estérase) H 2 N O CH 2 N C 2 H 5 H 2 N O C OH Acide Para-Aminobenzoïque HO CH 2 N C 2 H 5 Diéthylaminoéthanol 9

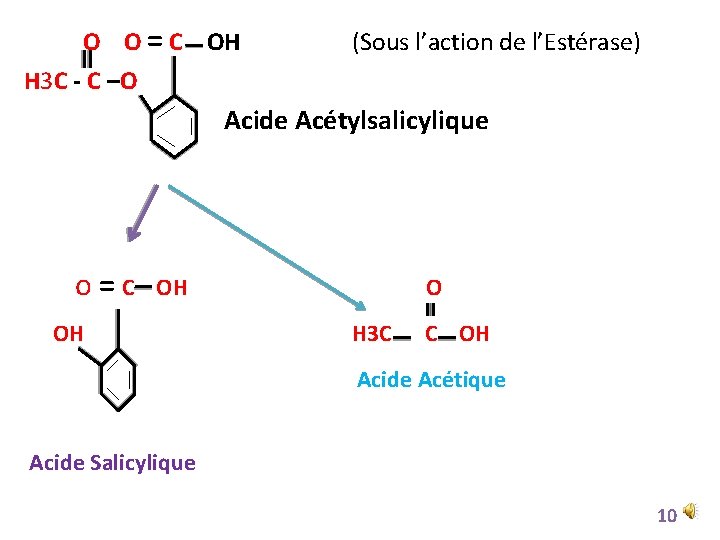
O O = C OH (Sous l’action de l’Estérase) H 3 C - C –O Acide Acétylsalicylique o=C OH OH O H 3 C C OH Acide Acétique Acide Salicylique 10

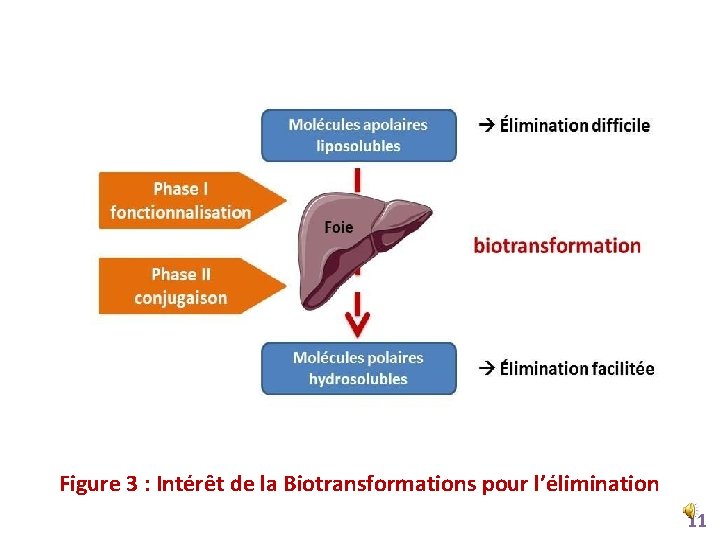
Figure 3 : Intérêt de la Biotransformations pour l’élimination 11