QUMICA QUMICA Joo Usberco Philipe Spitaleri Kaufmann 2

QUÍMICA

QUÍMICA João Usberco; Philipe Spitaleri Kaufmann 2º ano ensino médio

UNIDADE 4 – CINÉTICA QUÍMICA CAPÍTULO 9 – A RAPIDEZ DAS REAÇÕES QUÍMICAS Rapidez de uma reação • É comum encontrar o termo velocidade de reação ou velocidade média de reação como sinônimo de rapidez de reação ou reação média de alguns exames de seleção. Rapidez média: • é o quociente entre a variação das quantidades, dos reagentes ou dos produtos, e o intervalo de tempo no qual essa variação ocorreu. QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 4 – CINÉTICA QUÍMICA CAPÍTULO 9 – A RAPIDEZ DAS REAÇÕES QUÍMICAS Condições para a ocorrência de reação • A condição mais evidente para que uma reação ocorra é que os reagentes estejam em contato. O contato entre os reagentes permite que ocorra interações entre eles, originando os produtos. QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 4 – CINÉTICA QUÍMICA CAPÍTULO 9 – A RAPIDEZ DAS REAÇÕES QUÍMICAS Teoria da colisão • Reações diferentes apresentam energias de ativação diferentes, e as reações que exigem menor energia de ativação ocorrem mais rapidamente, ou seja, com maior rapidez. A energia de ativação • A quantidade, assim como a forma da Ea, varia de uma reação para a outra. Em um grande número de reações ela é fornecida aos reagentes através de um aquecimento, porém pode ser fornecida por outros meios. QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 4 – CINÉTICA QUÍMICA CAPÍTULO 9 – A RAPIDEZ DAS REAÇÕES QUÍMICAS Fatores que influem na rapidez das reações • Superfície de contato: quanto maior fragmentado está o sólido, maior a quantidade de reagentes em contato e maior o número de colisões, aumentando a rapidez com que a reação ocorre. Quanto maior a superfície de contato dos reagentes, maior a rapidez da reação. • Temperatura: como as moléculas se movimentam mais rapidamente, elas colidem com maior frequência e com maior energia, o que provoca um aumento na rapidez da reação química. QUÍMICA | Volume 2 – 3º Bimestre
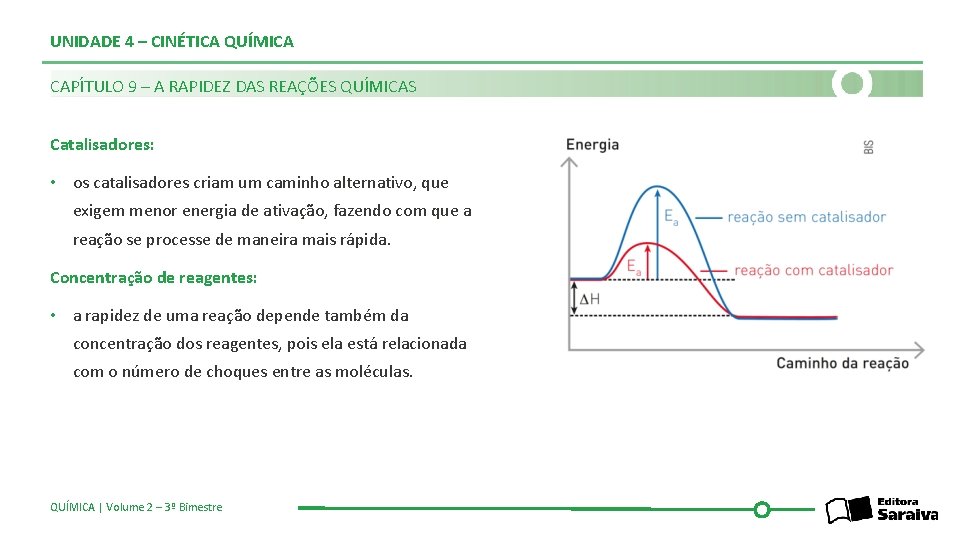
UNIDADE 4 – CINÉTICA QUÍMICA CAPÍTULO 9 – A RAPIDEZ DAS REAÇÕES QUÍMICAS Catalisadores: • os catalisadores criam um caminho alternativo, que exigem menor energia de ativação, fazendo com que a reação se processe de maneira mais rápida. Concentração de reagentes: • a rapidez de uma reação depende também da concentração dos reagentes, pois ela está relacionada com o número de choques entre as moléculas. QUÍMICA | Volume 2 – 3º Bimestre
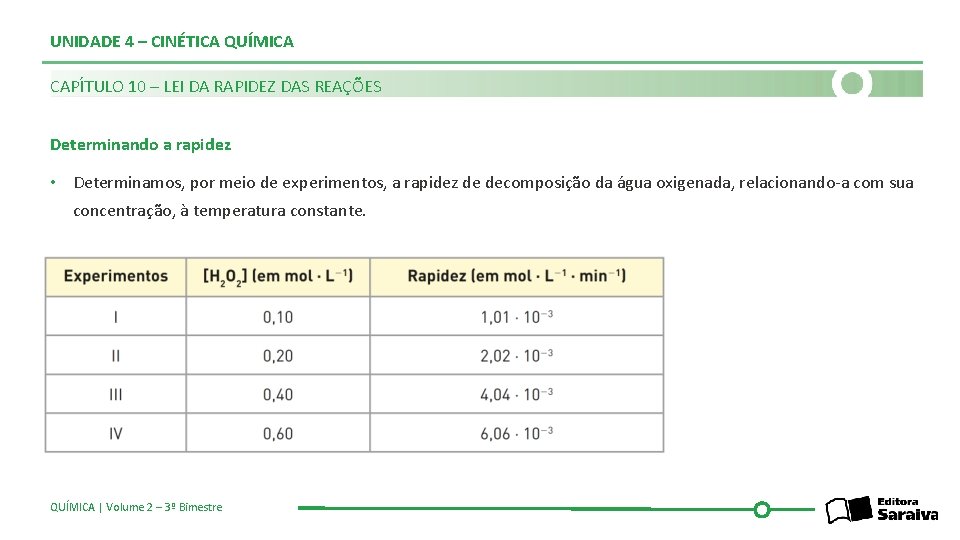
UNIDADE 4 – CINÉTICA QUÍMICA CAPÍTULO 10 – LEI DA RAPIDEZ DAS REAÇÕES Determinando a rapidez • Determinamos, por meio de experimentos, a rapidez de decomposição da água oxigenada, relacionando-a com sua concentração, à temperatura constante. QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 4 – CINÉTICA QUÍMICA CAPÍTULO 10 – LEI DA RAPIDEZ DAS REAÇÕES Ordem da reação • A ordem da reação, em relação à determinada espécie que reage, corresponde ao expoente da concentração em mol/L dessa espécie, representada na Lei da Rapidez. Meia-vida de uma reação de 1 a ordem • A meia-vida de uma reação de 1 a ordem indica o tempo necessário para que a concentração do reagente diminua para a metade do seu valor inicial. QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 11 – EQUILÍBRIOS • Várias reações ocorrem mediante o consumo total dos reagentes ou, pelo menos, de um deles. Essas são chamadas reações irreversíveis. • No entanto existem processos reversíveis. Um exemplo de processo físico reversível é o que ocorre com a água líquida em frasco fechado. • Quando montamos um sistema isolado com água líquida nas condições ambientais, notamos que o nível da água líquida no frasco vai diminuindo com o passar do tempo, até ficar constante. QUÍMICA | Volume 2 – 3º Bimestre
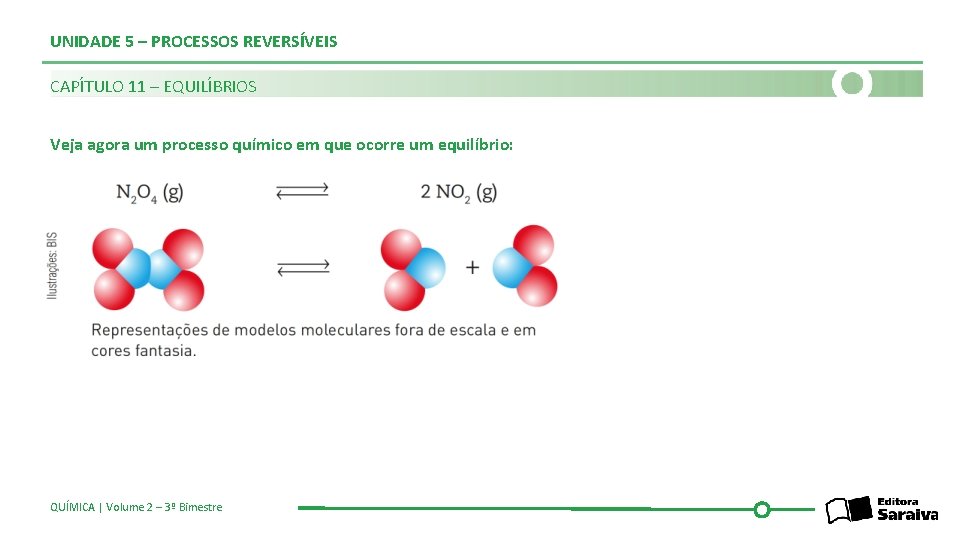
UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 11 – EQUILÍBRIOS Veja agora um processo químico em que ocorre um equilíbrio: QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 11 – EQUILÍBRIOS Constante de equilíbrio • A expressão constante de equilíbrio foi formulada pela primeira vez pelos noruegueses Cato Maximilian Guldberg (1836 – 1902) e Peter Waage (1833 – 1900), em 1863, e enunciada como a Lei da ação das massas. • Para um equilíbrio em que todos os participantes formam um sistema homogêneo, isto é, um equilíbrio homogêneo, genericamente representado por: QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 11 – EQUILÍBRIOS Deslocamento de equilíbrio Princípio de Le Chatelier • Quando um sistema está em equilíbrio, a rapidez da reação direta é igual à rapidez de reação inversa, e as concentrações molares de todos os participantes permanecem constantes. Se, sobre esse equilíbrio, não ocorrer a ação de nenhum agente externo, ele tende a permanecer nessa situação indefinidamente. Porém, se for exercida uma ação externa sobre esse equilíbrio, ele tende a reagir de maneira a minimizar os efeitos dessa ação. QUÍMICA | Volume 2 – 3º Bimestre
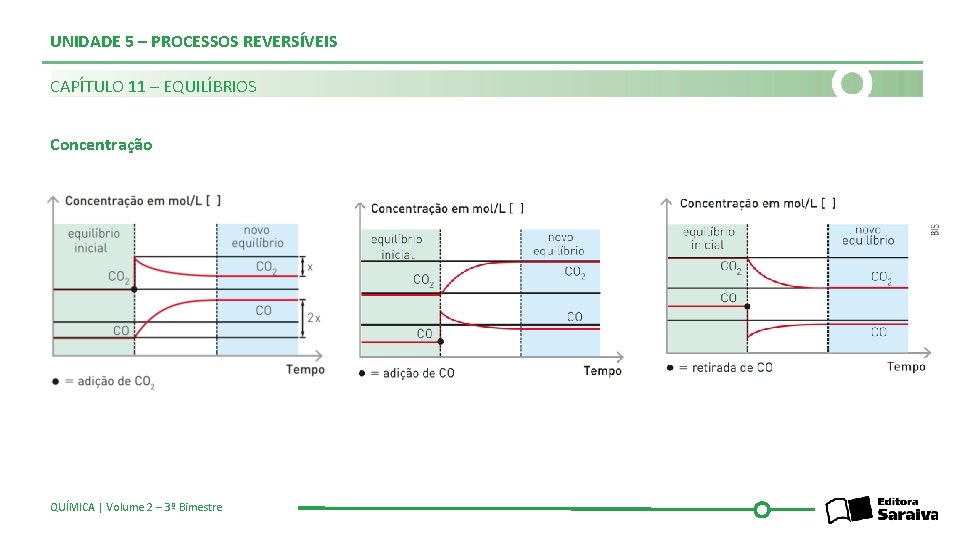
UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 11 – EQUILÍBRIOS Concentração QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 11 – EQUILÍBRIOS Pressão • De acordo com o princípio de Le Chatelier, um sistema em equilíbrio, quando submetido a uma ação externa, reage no sentido de minimizar os efeitos dessa ação. Quando, a uma temperatura constante, aumentamos a pressão sobre o equilíbrio gasoso, ele se desloca no sentido da reação capaz de minimizar essa pressão e vice-versa. Temperatura • Em um sistema em equilíbrio, sempre temos duas reações: a endotérmica, que absorve calor; e a exotérmica, que libera calor. Catalisadores • Em um equilíbrio, a diminuição de energia de ativação produzida pelo catalisador tem o mesmo valor para a reação direta e para a inversa. QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 12 – EQUILÍBRIOS IÔNICOS • Os compostos iônicos, orgânicos ou inorgânicos, liberados no esgoto pelas atividades humanas domésticas, industriais ou agrícolas podem prejudicar a qualidade da água dos mananciais. Há, no entanto, maneiras de identificá-los e removê-los, combinando-os com outros íons. Propriedades como potabilidade e dureza da água dependem da presença e da quantidade de certas espécies, como íons. QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 12 – EQUILÍBRIOS IÔNICOS Constantes de ionização de ácidos e bases QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 12 – EQUILÍBRIOS IÔNICOS Lei de diluição de Ostwald • No final do século Xl. X, Friedrich Wilhelm Ostwald (1853 – 1932), químico de origem russo-germânica, deduziu pela primeira vez uma expressão matemática relacionando a constante de ionização, a concentração em mol/L e o grau de ionização para monoácidos e monobases. QUÍMICA | Volume 2 – 3º Bimestre
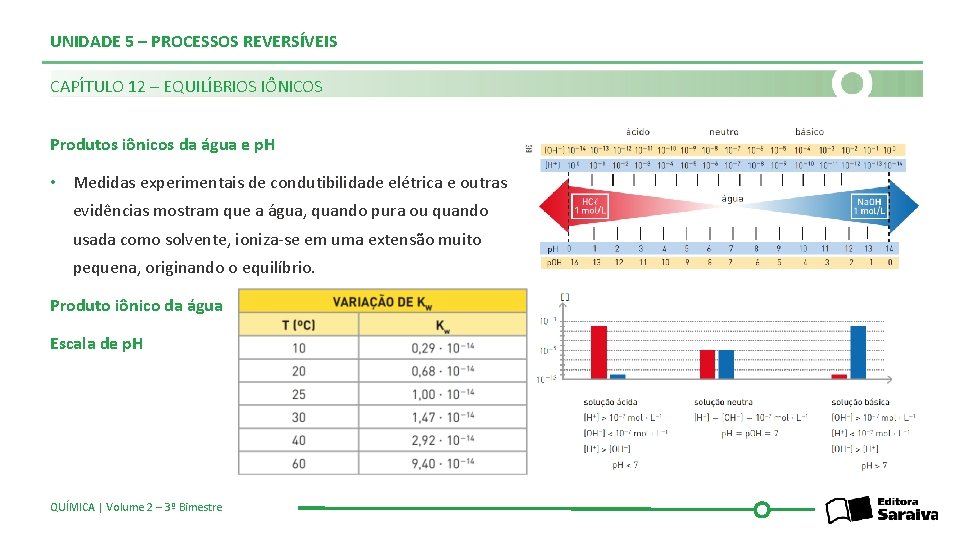
UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 12 – EQUILÍBRIOS IÔNICOS Produtos iônicos da água e p. H • Medidas experimentais de condutibilidade elétrica e outras evidências mostram que a água, quando pura ou quando usada como solvente, ioniza-se em uma extensão muito pequena, originando o equilíbrio. Produto iônico da água Escala de p. H QUÍMICA | Volume 2 – 3º Bimestre
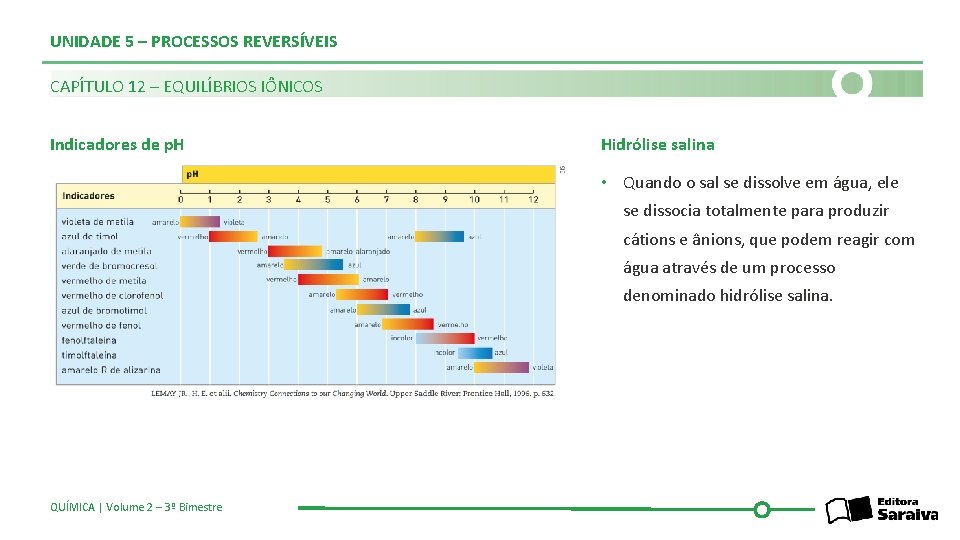
UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 12 – EQUILÍBRIOS IÔNICOS Indicadores de p. H Hidrólise salina • Quando o sal se dissolve em água, ele se dissocia totalmente para produzir cátions e ânions, que podem reagir com água através de um processo denominado hidrólise salina. QUÍMICA | Volume 2 – 3º Bimestre

UNIDADE 5 – PROCESSOS REVERSÍVEIS CAPÍTULO 12 – EQUILÍBRIOS IÔNICOS Constante do produto de solubilidade (Ks) • Muitos processos naturais dependem da precipitação e da dissolução de sais pouco solúveis. Os rins, por exemplo, excretam continuamente substâncias pouco solúveis, tais como fosfato de cálcio e o oxalato de cálcio. Quando a urina se torna saturada por essas substâncias, elas se cristalizam, originando os cálculos renais. Produto de solubilidade QUÍMICA | Volume 2 – 3º Bimestre
- Slides: 21