Qumica Professora Graa Porto WWW Quibio COM Profa

Química Professora: Graça Porto WWW. Quibio . COM Profa. Graça Porto

O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. Profa. Graça Porto
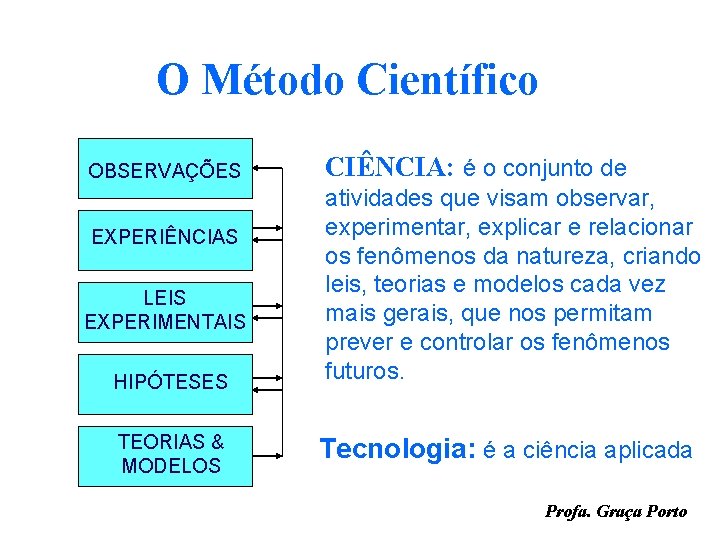
O Método Científico OBSERVAÇÕES EXPERIÊNCIAS LEIS EXPERIMENTAIS HIPÓTESES TEORIAS & MODELOS CIÊNCIA: é o conjunto de atividades que visam observar, experimentar, explicar e relacionar os fenômenos da natureza, criando leis, teorias e modelos cada vez mais gerais, que nos permitam prever e controlar os fenômenos futuros. Tecnologia: é a ciência aplicada Profa. Graça Porto
ESTRUTURA DA MATÉRIA A matéria é formada por moléculas, que por sua vez são formadas por partículas minúsculas chamadas de átomos. Profa. Graça Porto
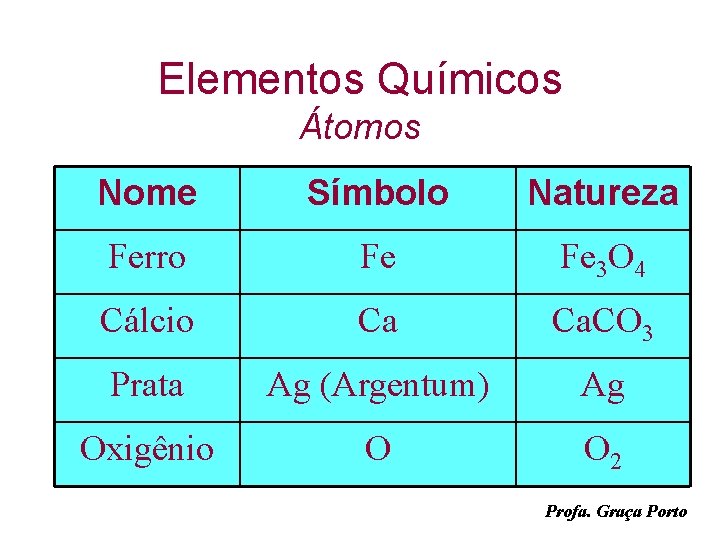
Elementos Químicos Átomos Nome Símbolo Natureza Ferro Fe Fe 3 O 4 Cálcio Ca Ca. CO 3 Prata Ag (Argentum) Ag Oxigênio O O 2 Profa. Graça Porto
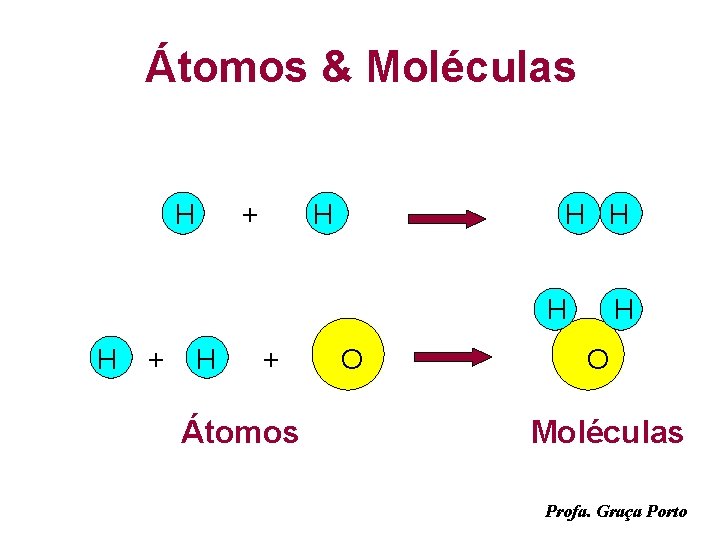
Átomos & Moléculas H + H H H + Átomos O H O Moléculas Profa. Graça Porto
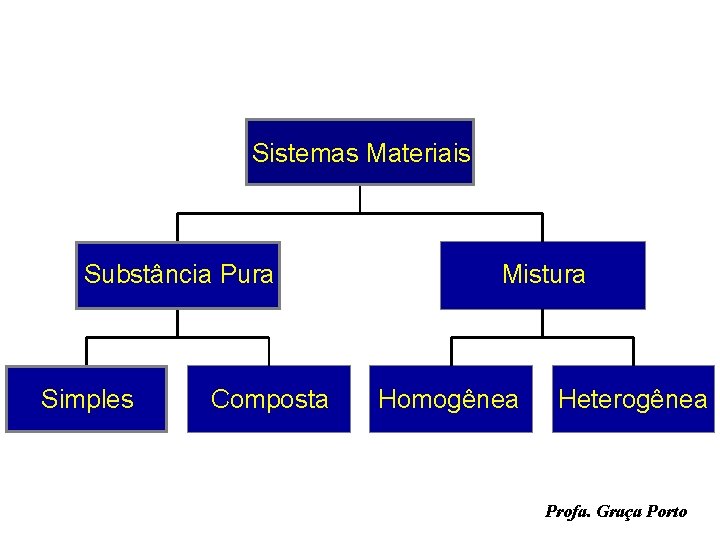
Sistemas Materiais Substância Pura Simples Composta Mistura Homogênea Heterogênea Profa. Graça Porto
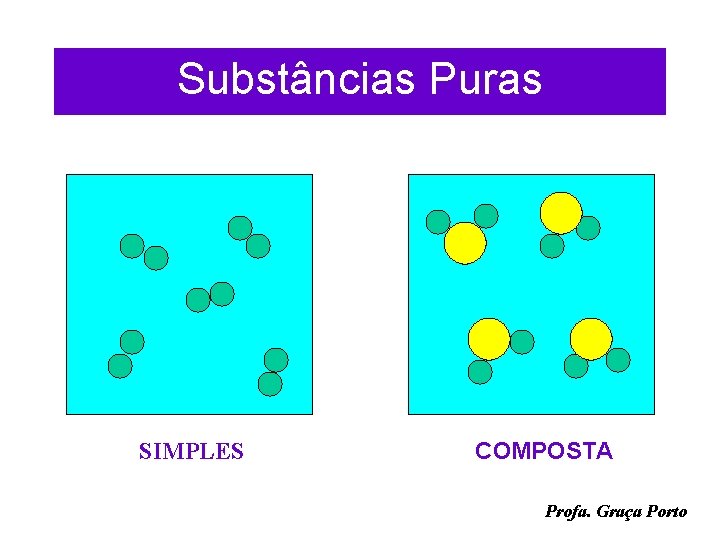
Substâncias Puras SIMPLES COMPOSTA Profa. Graça Porto
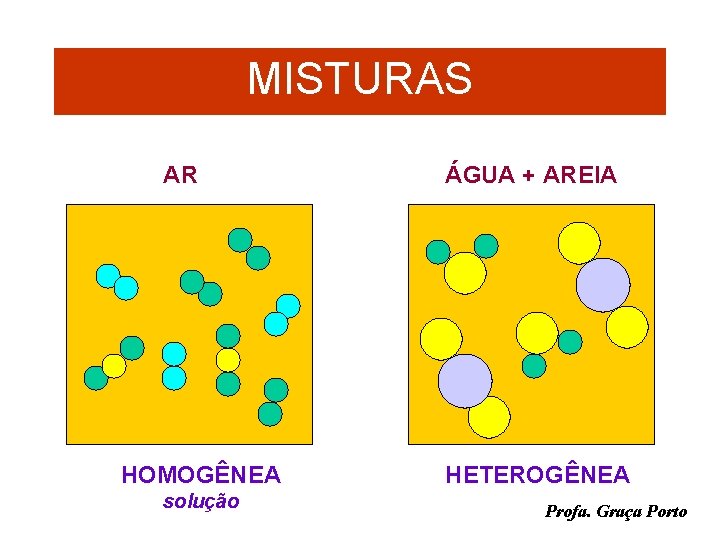
MISTURAS AR HOMOGÊNEA solução ÁGUA + AREIA HETEROGÊNEA Profa. Graça Porto
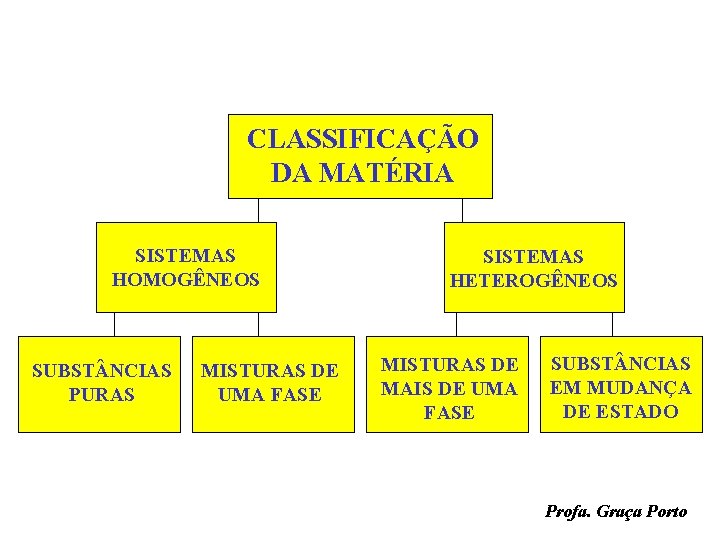
CLASSIFICAÇÃO DA MATÉRIA SISTEMAS HOMOGÊNEOS SUBST NCIAS PURAS MISTURAS DE UMA FASE SISTEMAS HETEROGÊNEOS MISTURAS DE MAIS DE UMA FASE SUBST NCIAS EM MUDANÇA DE ESTADO Profa. Graça Porto

OUTROS CONCEITOS v ATOMICIDADE v VARIEDADE ALOTRÓPICA v FENÔMENOS (Transformações): QUÍMICOS E FÍSICOS Profa. Graça Porto

ATOMICIDADE Atomicidade Substâncias Monoatômica He, Ne, Ar, Kr Diatômica H 2, N 2, HCl, CO Tetratômica P 4 (fósforo branco) Indeterminada P(verm), C(graf), metais v Atomicidade se refere ao número de átomos que compõem uma substância Profa. Graça Porto
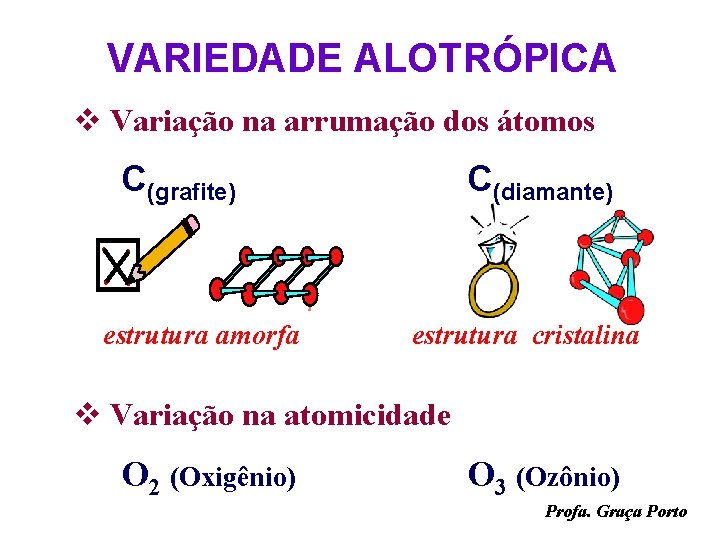
VARIEDADE ALOTRÓPICA v Variação na arrumação dos átomos C(grafite) estrutura amorfa C(diamante) estrutura cristalina v Variação na atomicidade O 2 (Oxigênio) O 3 (Ozônio) Profa. Graça Porto

FENÔMENO QUÍMICO Combustão do álcool etílico H 3 C- CH 2 - OH + 3 O 2 2 CO 2 + 3 H 2 O Reagentes Produtos v O fenômeno químico transforma a natureza íntima da matéria. Profa. Graça Porto
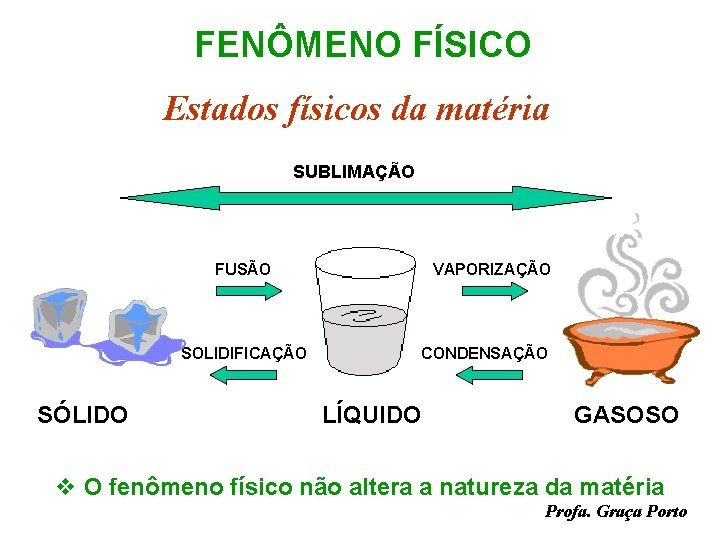
FENÔMENO FÍSICO Estados físicos da matéria SUBLIMAÇÃO FUSÃO SOLIDIFICAÇÃO SÓLIDO VAPORIZAÇÃO CONDENSAÇÃO LÍQUIDO GASOSO v O fenômeno físico não altera a natureza da matéria Profa. Graça Porto
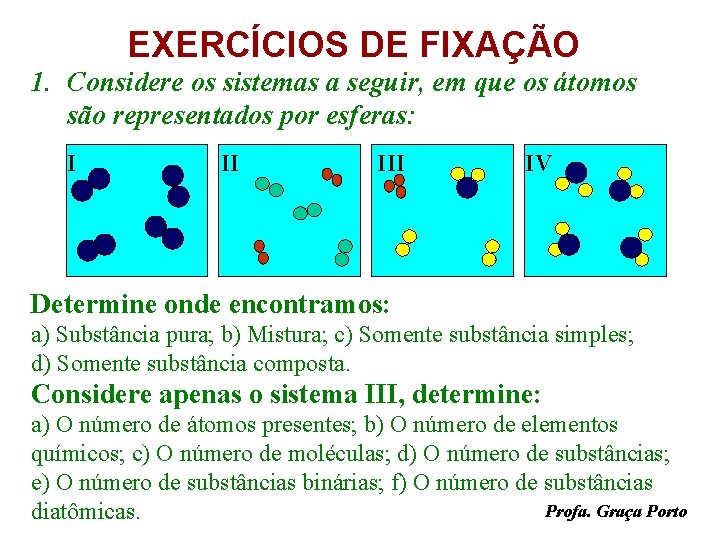
EXERCÍCIOS DE FIXAÇÃO 1. Considere os sistemas a seguir, em que os átomos são representados por esferas: I II IV Determine onde encontramos: a) Substância pura; b) Mistura; c) Somente substância simples; d) Somente substância composta. Considere apenas o sistema III, determine: a) O número de átomos presentes; b) O número de elementos químicos; c) O número de moléculas; d) O número de substâncias; e) O número de substâncias binárias; f) O número de substâncias Profa. Graça Porto diatômicas.

2. Considere o sistema representado abaixo. Pode-se descrever o sistema em questão como constituido por: a) Três fases e um componente. b) Duas fases e dois componentes. c) Três fases e dois componentes. d) Três fases e três componentes. Profa. Graça Porto

3. Os diferentes tipos de matéria podem ser classificados em dois grupos: Substâncias puras e misturas. As substâncias puras podem ser simples e compostas. Considerando esse modo de classificação, pode-se afirmar: (01) O ar atmosférico é uma substância pura. (02) A água é uma substância simples. (04) O sangue é uma mistura. (08) Uma solução de açúcar é uma mistura (16) O oxigênio e o ozônio são substâncias distintas, embora constituídas por átomos de um mesmo elemento. (32) A matéria que contém três tipos de moléculas é uma substância composta. (64) A matéria que contém apenas um tipo de molécula é uma substância simples, mesmo que cada molécula seja formada por dois átomos diferentes. Profa. Graça Porto

4. Observe os seguintes fatos: I – Uma pedra de naftalina deixada no armário. II – Uma vasilha com água deixada no freezer. III – Uma vasilha com água deixada no fogo. IV – O derretimento de um pedaço de chumbo quando aquecido. Nestes fatos estão relacionados corretamente os seguintes fenômenos: a) I – sublimação, II – solidificação, III – vaporização, IV – fusão. b) I – sublimação, II – solidificação, III – fusão, IV –vaporização. c) I – fusão, II – sublimação, III –vaporização, IV – solidificação. d) I – vaporização, II- solidificação, III – fusão, IV – sublimação. e) I – vaporização, II – sublimação, II –fusão, IV – solidificação. Profa. Graça Porto

5. Qual dos fenômenos a seguir não envolve reações químicas? a) Fusão de gelo. b) Digestão de alimentos. c) Combustão. d) Queima de vela. e) Explosão de dinamite. Profa. Graça Porto

PROPRIEDADES DA MATÉRIA v PROPRIEDADES GERAIS v PROPRIEDADES FUNCIONAIS v PROPRIEDADES ESPECÍFICAS: Profa. Graça Porto

PROPRIEDADES GERAIS v Massa v Volume v Inércia v impenetrabilidade v Dureza As propriedades gerais são comuns a todos os materiais. Profa. Graça Porto

PROPRIEDADES FUNCIONAIS v Hidrocarbonetos são inflamáveis. v Os ácidos têm sabor azedo. v Os sais fundidos conduzem corrente elétrica. As propriedades funcionais são aquelas apresentadas por um grupo de substâncias, chamado função química. Profa. Graça Porto

PROPRIEDADES ESPECÍFICAS v Ponto de Fusão / Solidificação v Ponto de Ebulição / Liquefação v Densidade ou Massa Específica v Coeficiente de Solubilidade As propriedades específicas caracterizam cada tipo de substância. Profa. Graça Porto

Ponto de Fusão / Solidificação v Ponto de Fusão é a temperatura em que uma substância muda do estado sólido para o estado líquido. v. Ponto de Solidificação corresponde ao processo inverso, embora as temperaturas sejam equivalentes. Obs. O PF e o PS são obtidos em uma dada pressão, quando esta não é citada, considera-se a pressão atmosférica Profa. Graça Porto

Ponto de Ebulição / Liquefação v Ponto de Ebulição é a temperatura em que uma substância muda do estado líquido para o estado gasoso. v. Ponto de liquefação corresponde ao processo inverso, embora as temperaturas sejam equivalentes. Obs. O PE e o PL são obtidos em uma dada pressão, quando esta não é citada, considera-se a pressão atmosférica Profa. Graça Porto
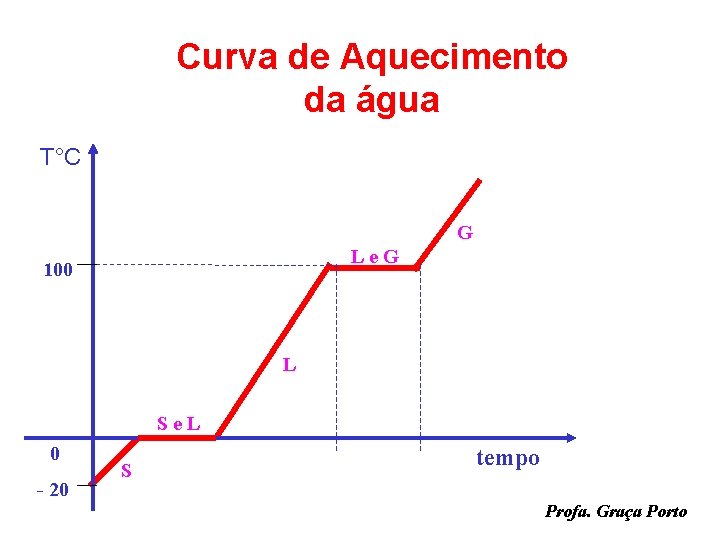
Curva de Aquecimento da água T°C G Le. G 100 L Se. L 0 - 20 S tempo Profa. Graça Porto
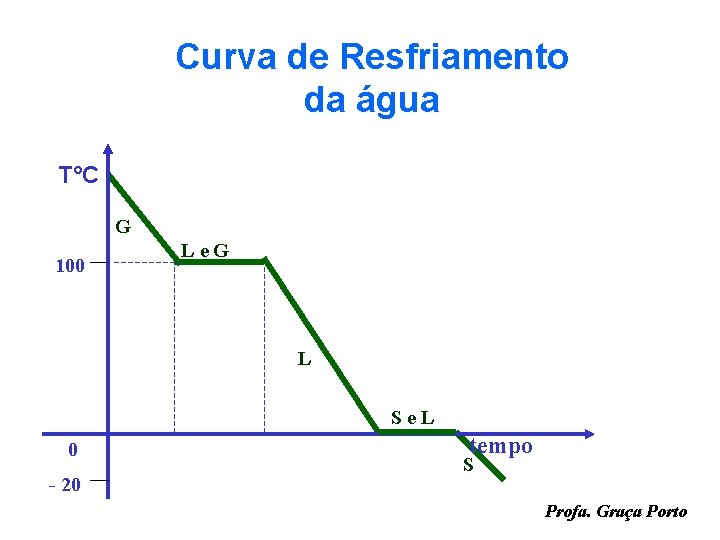
Curva de Resfriamento da água T°C G 100 Le. G L Se. L 0 - 20 tempo S Profa. Graça Porto
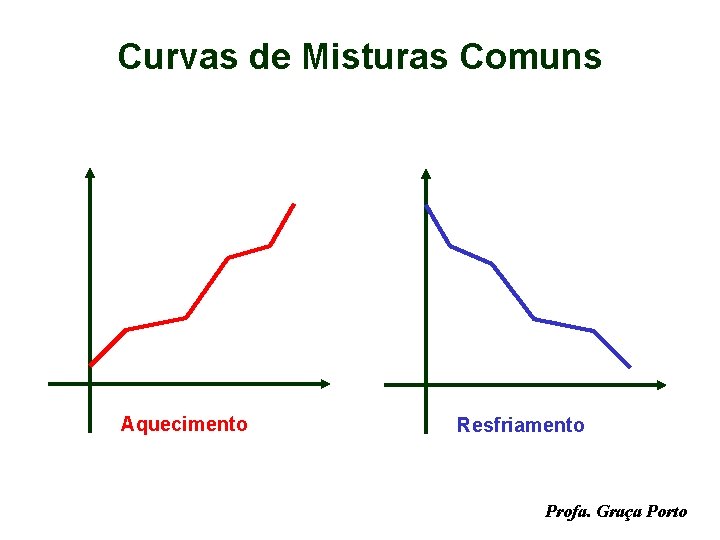
Curvas de Misturas Comuns Aquecimento Resfriamento Profa. Graça Porto
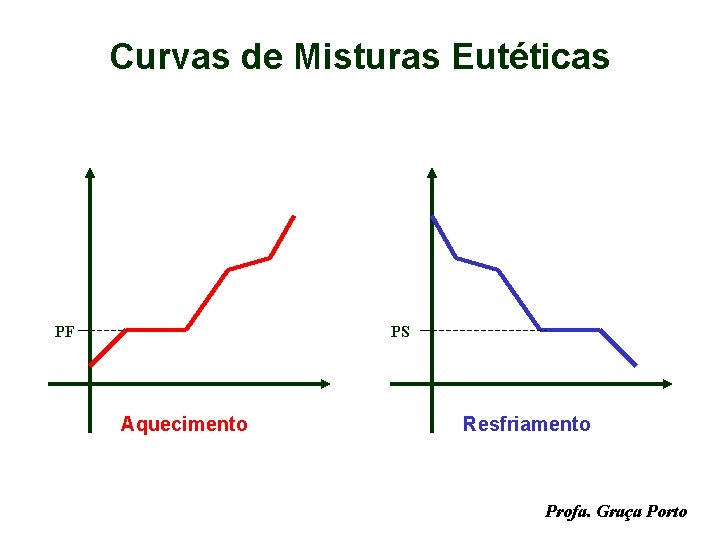
Curvas de Misturas Eutéticas PF PS Aquecimento Resfriamento Profa. Graça Porto
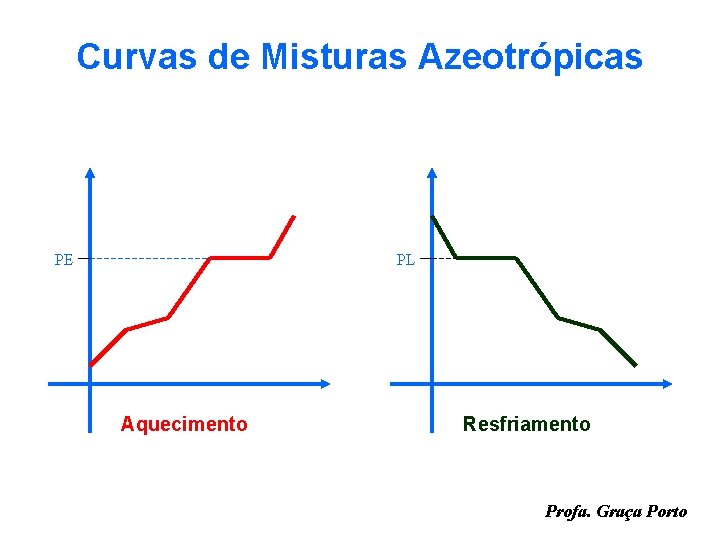
Curvas de Misturas Azeotrópicas PE PL Aquecimento Resfriamento Profa. Graça Porto
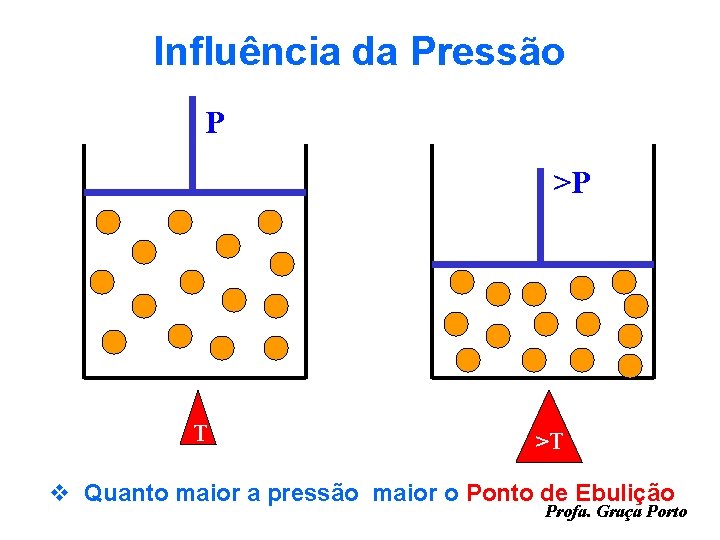
Influência da Pressão P >P T >T v Quanto maior a pressão maior o Ponto de Ebulição Profa. Graça Porto
Influência da Altitude >A <P <T A P T v Quanto maior a Altitude menor o Ponto de Ebulição Profa. Graça Porto

Densidade v Densidade é a relação da massa pelo volume de uma substância a uma dada Temperatura e Pressão: d=m/V Profa. Graça Porto
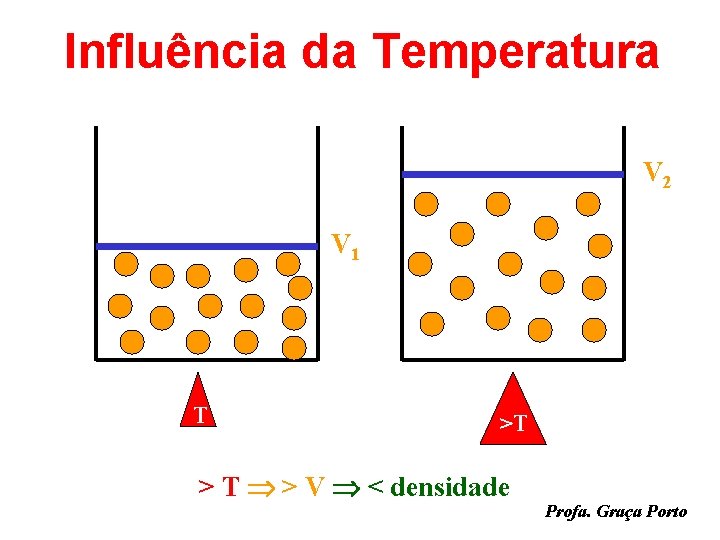
Influência da Temperatura V 2 V 1 T >T > T > V < densidade Profa. Graça Porto

Influência da Pressão P >P > P < V > densidade Profa. Graça Porto
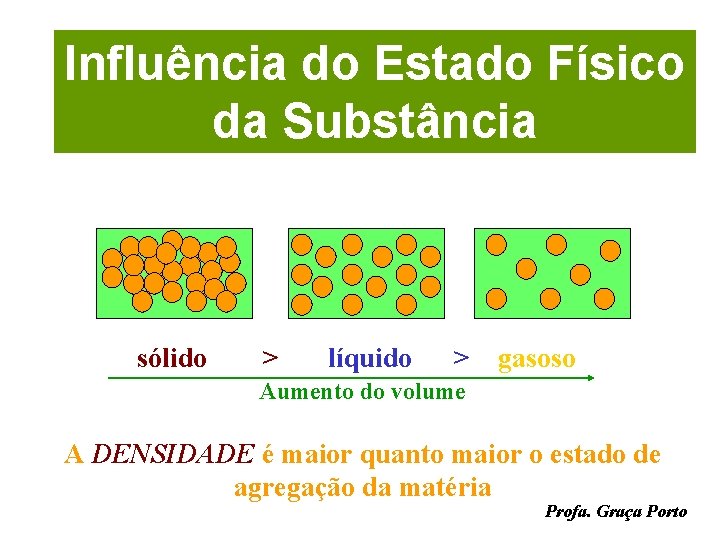
Influência do Estado Físico da Substância sólido > líquido > gasoso Aumento do volume A DENSIDADE é maior quanto maior o estado de agregação da matéria Profa. Graça Porto

Exceções a Regra • Água líquida é mais densa que o gelo. • Prata, Ferro e Bismuto, todos diminuem de volume quando fundidos, portanto fase líquida mais densa. Profa. Graça Porto
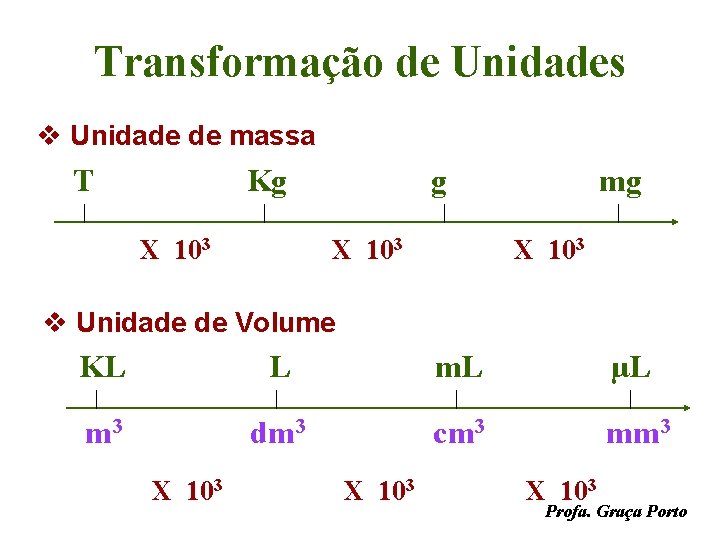
Transformação de Unidades v Unidade de massa T Kg X 103 mg X 103 v Unidade de Volume KL L m. L µL m 3 dm 3 cm 3 mm 3 X 103 Profa. Graça Porto

Exercícios de fixação: 1) Dada a tabela: PF PE – 63°C 61°C Fenol 43°C 182°C Cloro – 101°C Clorofórmio – 34, 5°C Determine o estado físico de cada substância nas condições ambientes ( 25°C e 1 atm). Clorofórmio Fenol Cloro Profa. Graça Porto
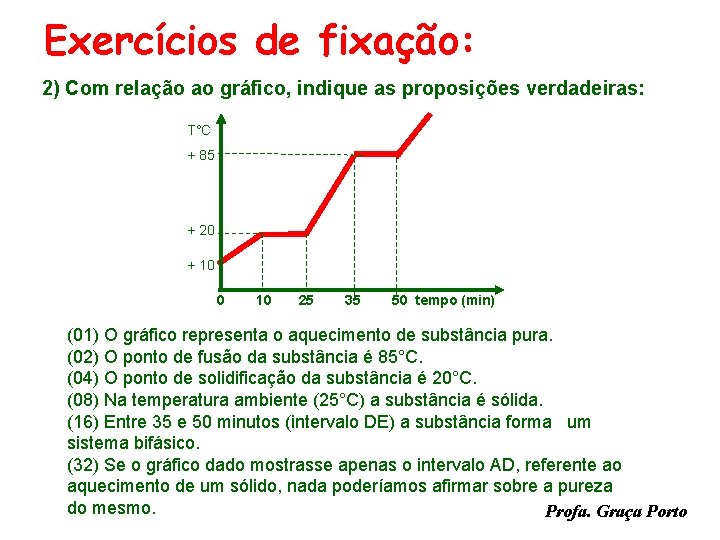
Exercícios de fixação: 2) Com relação ao gráfico, indique as proposições verdadeiras: T°C + 85 + 20 + 10 0 10 25 35 50 tempo (min) (01) O gráfico representa o aquecimento de substância pura. (02) O ponto de fusão da substância é 85°C. (04) O ponto de solidificação da substância é 20°C. (08) Na temperatura ambiente (25°C) a substância é sólida. (16) Entre 35 e 50 minutos (intervalo DE) a substância forma um sistema bifásico. (32) Se o gráfico dado mostrasse apenas o intervalo AD, referente ao aquecimento de um sólido, nada poderíamos afirmar sobre a pureza do mesmo. Profa. Graça Porto

Exercícios de fixação: 3) O gráfico está representando a ebulição de duas amostras, iguais ou diferentes, em experiências distintas realizadas cada uma a pressão constante. As quais foram realizadas em sistemas abertos. T°C T 1 B A T 2 tempo (min) (01) Se a amostra A e B forem idênticas, então a pressão é diferente para cada experiência. (02) Se a pressão é a mesma, então A e B poderão ser amostras idênticas em quantidades diferentes. (04) A e B são substâncias puras. (08) A e B podem ser misturas. (16) Se A e B são amostras idênticas, A foi realizada numa pressão maior que B. (32) Se A e B são amostras idênticas, A foi realizada numa altitude menor que B. Profa. Graça Porto (64) B pode ser uma substância pura e A, ser uma mistura azeotrópica.

Exercícios de fixação: 4) Responda a essa questão considerando três frascos contendo massas iguais de líquidos diferentes, A, B e C, cujos valores de densidade em g/m. L são respectivamente: 0, 8; 1, 0; 1, 2. I A alternativa que indica cada frasco com seu respectivo líquido é: a) I – A, II – B, III – C. II b) I – A, II – C, III – B. c) I – B, II – C, III – A. III d) I – B, II – A, III – C. e) I – C, II – B, III – A. Profa. Graça Porto

Exercícios de fixação: 5) (UFMG) As figuras abaixo representam densímetros como os usados em postos de gasolina. O primeiro contém etanol puro (d = 0, 8 g/cm 3). Dos dois restantes, um está cheio de etanol e água e o outro gasolina (d = 0, 7 g/cm 3), não estão necessariamente nessa ordem. Com base nessas informações, pode-se afirmar corretamente que: I II a) A densidade da bola preta é maior que 1 g/cm 3 b) A densidade da bola branca é menor que 0, 8 g/cm 3. c) A mistura no densímetro II, tem densidade menor que 0, 8 g/cm 3. d) A mistura no densímetro III, contém água. III e) As duas bolas apresentam densidade menores que 0, 7 g/cm 3. Profa. Graça Porto
Exercícios de fixação: 6) Uma torneira defeituosa goteja a cada 36 segundos. Sabendo-se que cada gota de água pesa 0, 25 g, quanto tempo levará para encher uma lata de 0, 01 m 3 ? Profa. Graça Porto

Coeficiente de Solubilidade - CS v Em geral é considerada como sendo a massa em gramas possível de ser solubilizada em 100 g de água, em uma dada Temperatura e pressão. Obs. Quando a temperatura / pressão não são indicadas, considera-se a temperatura de 25°C e pressão de 1 atm. Profa. Graça Porto
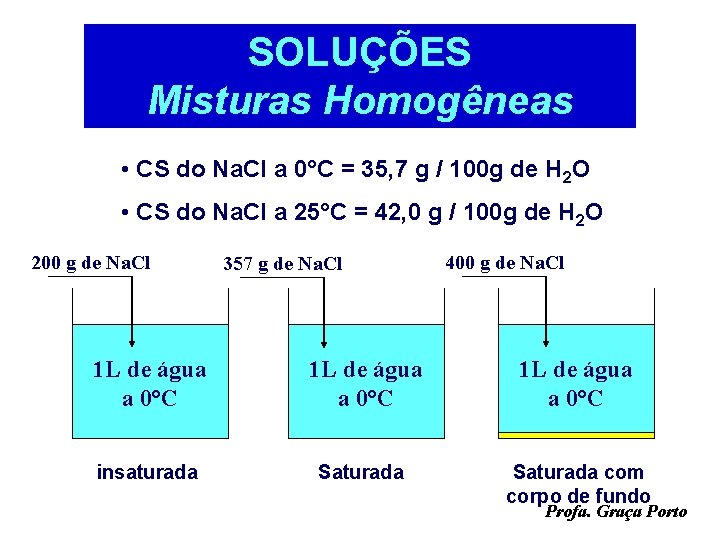
SOLUÇÕES Misturas Homogêneas • CS do Na. Cl a 0°C = 35, 7 g / 100 g de H 2 O • CS do Na. Cl a 25°C = 42, 0 g / 100 g de H 2 O 200 g de Na. Cl 357 g de Na. Cl 400 g de Na. Cl 1 L de água a 0°C insaturada Saturada com corpo de fundo Profa. Graça Porto

SOLUÇÃO SUPERSATURADA 400 g de Na. Cl 1 L de água a 0°C 1 L de água a 25°C 1 L de água a 0°C Supersaturada • A concentração na solução final está acima do CS do Na. Cl a 0°C. Profa. Graça Porto
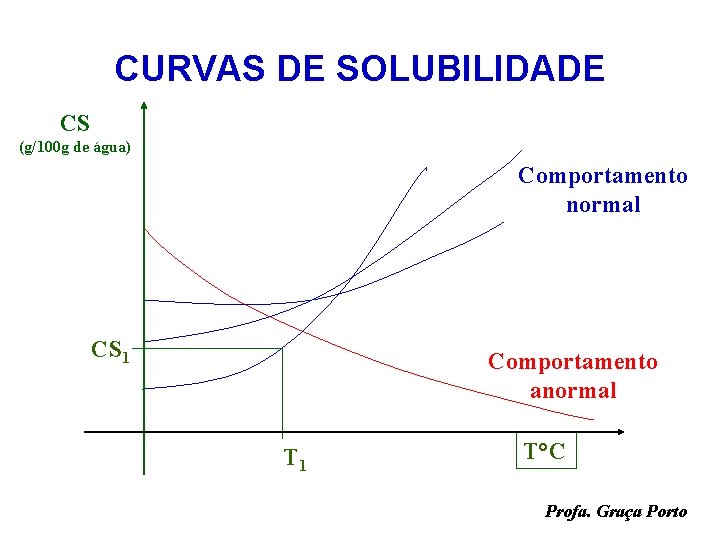
CURVAS DE SOLUBILIDADE CS (g/100 g de água) Comportamento normal CS 1 Comportamento anormal T 1 T°C Profa. Graça Porto

Exercícios de fixação: 1) A 18°C a solubilidade de uma substância X é de 60 g/100 m. L de água. Nessa temperatura 150 g de X foram misturados em 200 m. L de água. O sistema obtido é: a) Heterogêneo com uma fase. b) Homogêneo com duas fases. c) Uma solução aquosa com corpo de fundo. d) Heterogêneo com três substâncias. e) Apenas uma solução aquosa. Profa. Graça Porto

Exercícios de fixação: 2) 160 g de uma solução saturada de sacarose (C 12 H 22 O 11) a 30°C é resfriada a 0°C. Qual a massa de açúcar cristalizada? Dados: Temperatura °C CS da sacarose (g/ 100 g de água) 0° 30° 180 220 Profa. Graça Porto
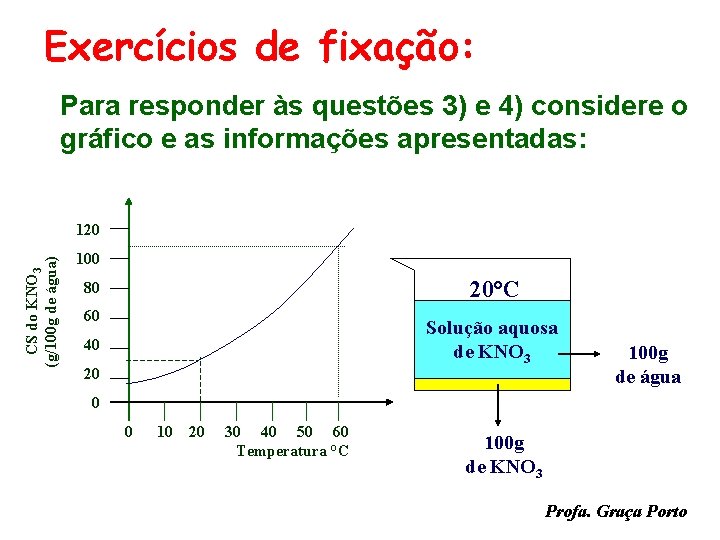
Exercícios de fixação: Para responder às questões 3) e 4) considere o gráfico e as informações apresentadas: CS do KNO 3 (g/100 g de água) 120 100 20°C 80 60 Solução aquosa de KNO 3 40 20 100 g de água 0 0 10 20 30 40 50 60 Temperatura °C 100 g de KNO 3 Profa. Graça Porto

Exercícios de fixação: 3) Essa mistura heterogênea, inicialmente a 20°C, é aquecida até 60°C. Dessa forma: a) A solução aquosa torna-se insaturada. b) A solução aquosa torna-se saturada e restam 5 g de corpo de fundo. c) A solução aquosa continua saturada, sem corpo de fundo. d) A solução aquosa continua saturada e restam 20 g de corpo de fundo. e) A massa de KNO 3 dissolvida triplica. Profa. Graça Porto

Exercícios de fixação: 4) Uma maneira conveniente para se recuperar todo o KNO 3 do sistema e obter o sal sólido e puro é: a) Evaporar toda água, por aquecimento. b) Agitar a mistura e depois filtrá-la. c) Decantar a solução sobrenadante. d) Resfriar a mistura a 0°C. e) Aquecer a mistura a 40°C Profa. Graça Porto

ANÁLISE IMEDIATA v Definição: processos de separação de uma mistura nos seus constituintes. v Classificação dos processos: Mecânicos: separações que não envolvem transformações físicas ou químicas. Físicos: processos que envolvem mudanças de estados físicos das substâncias. Normalmente indicados nas separações de misturas homogêneas. Profa. Graça Porto

ANÁLISE IMEDIATA v Misturas Heterogêneas: Sólido/sólido Sólido/líquido Sólido/gás Líquido/líquido v Misturas Homogêneas: sólido/sólido/líquido/gás gás/gás Profa. Graça Porto

Separação de Misturas Heterogêneas Sistemas Sólido/sólido: v Catação v Peneiração ou Tamisação v Ventilação v Levigação v Separação Magnética v Dissolução Fracionada v Flotação v Fusão Fracionada Profa. Graça Porto

Separação de Misturas Heterogêneas Sistemas Sólido/líquido: Sistemas Líquido/líquido: v Filtração v Decantação v Centrifugação v Cristalização Fracionada Sistemas Sólido/gás: v Filtração v Decantação v Câmara de Poeira Profa. Graça Porto
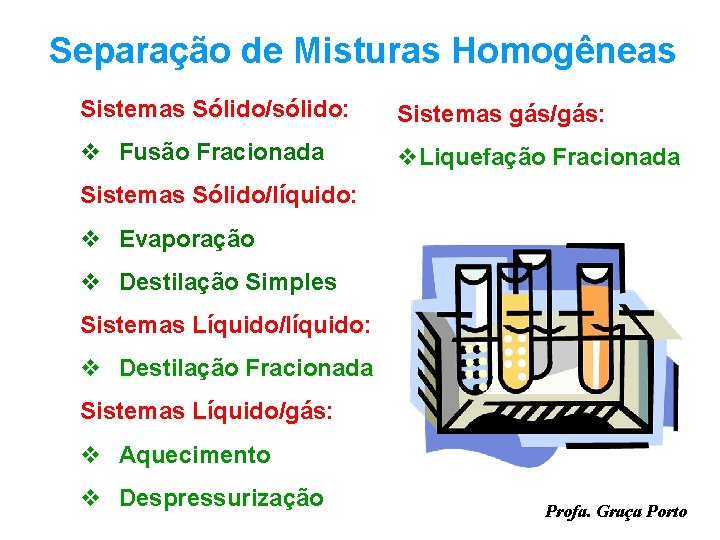
Separação de Misturas Homogêneas Sistemas Sólido/sólido: Sistemas gás/gás: v Fusão Fracionada v. Liquefação Fracionada Sistemas Sólido/líquido: v Evaporação v Destilação Simples Sistemas Líquido/líquido: v Destilação Fracionada Sistemas Líquido/gás: v Aquecimento v Despressurização Profa. Graça Porto

Materiais comuns de Laboratório v Tubo de Ensaio v Funil de Büchner v Béquer v Kitassato v Erlenmeyer v Proveta v Balão de Fundo Chato v Pipeta Volumétrica v Balão Volumétrico v Pipeta Graduada v Balão de Destilação v Condensador v Funil de Decantação v Funil de Filtração v Funil Liso Profa. Graça Porto

Materiais comuns de Laboratório v Bureta v Garras v Dessecador v Tripé de Ferro v Vidro de Relógio v Tela de Amianto v Almofariz e Pistilo v Bastão de Vidro v Cápsula de Evaporação v Frasco de Reagente v Cadinho de Porcelana v Cadinho de Platina v Piscete v Espátula v Suporte de Ferro Profa. Graça Porto
- Slides: 61