QUMICA ORGNICA I REACCIONES ORGNICAS E HIDROCARBUROS VERONICA

QUÍMICA ORGÁNICA I: REACCIONES ORGÁNICAS E HIDROCARBUROS VERONICA ISABEL PINZÓN MDCN - DOCENTE LFMN

TIPOS DE RUPTURAS DE ENLACES. Homolítica: El enlace covalente se rompe de manera simétrica (1 electrón para cada átomo). A: B A· + ·B (radicales libres) � Suele producirse en presencia de luz UV pues se necesita un aporte de energía elevado. Heterolítica: El enlace se rompe de manera asimétrica (uno de los átomos se queda con los dos electrones que compartían) A: B � Carbocationes: A: – + B+ R 3 C+ Ejemplo: (CH 3)2 CH+ � Carbanión: R 3 C: – Ejemplo: Cl 3 C: –
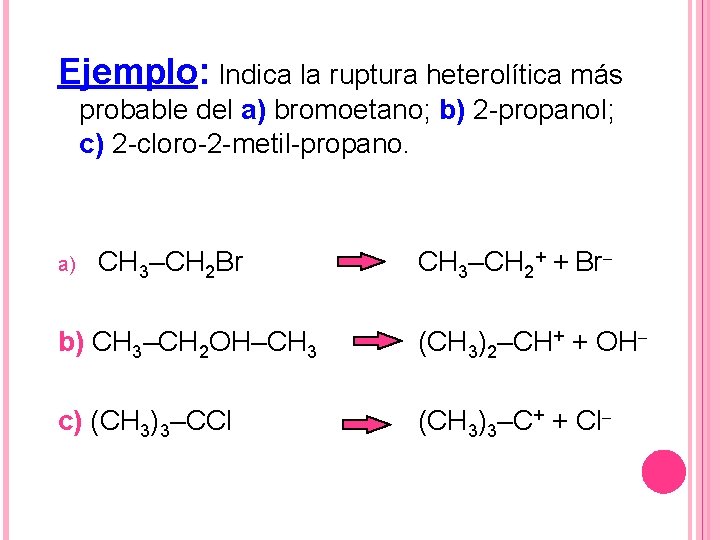
Ejemplo: Indica la ruptura heterolítica más probable del a) bromoetano; b) 2 -propanol; c) 2 -cloro-2 -metil-propano. a) CH 3–CH 2 Br CH 3–CH 2+ + Br– b) CH 3–CH 2 OH–CH 3 (CH 3)2–CH+ + OH– c) (CH 3)3–CCl (CH 3)3–C+ + Cl–
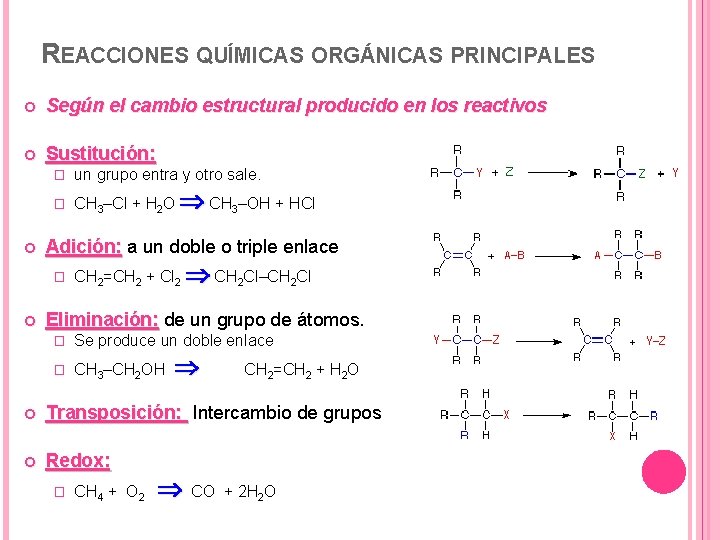
REACCIONES QUÍMICAS ORGÁNICAS PRINCIPALES Según el cambio estructural producido en los reactivos Sustitución: � un grupo entra y otro sale. � CH 3–Cl + H 2 O CH 3–OH + HCl Adición: a un doble o triple enlace � CH 2=CH 2 + Cl 2 CH 2 Cl–CH 2 Cl Eliminación: de un grupo de átomos. � Se produce un doble enlace � CH 3–CH 2 OH CH 2=CH 2 + H 2 O Transposición: Intercambio de grupos Redox: � CH 4 + O 2 CO + 2 H 2 O

Reaccciones de sustitución Son aquéllas en las que un átomo o grupo de átomos del sustrato son sustituidos por un átomo o grupo de átomos del reactivo.
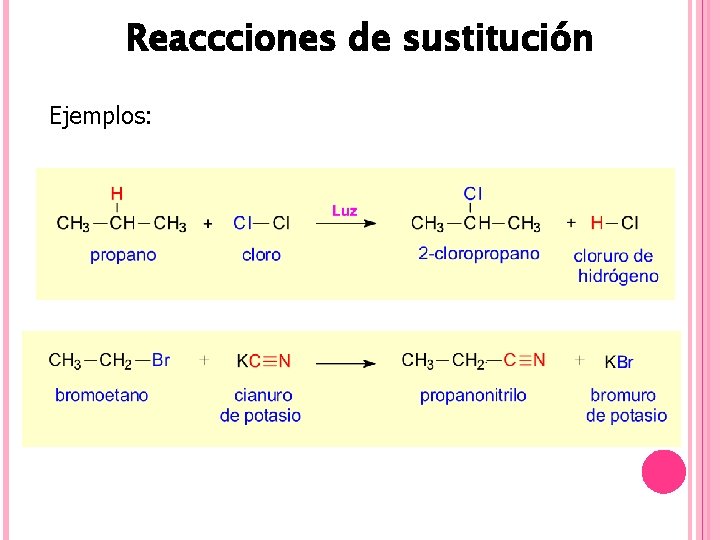
Reaccciones de sustitución Ejemplos:
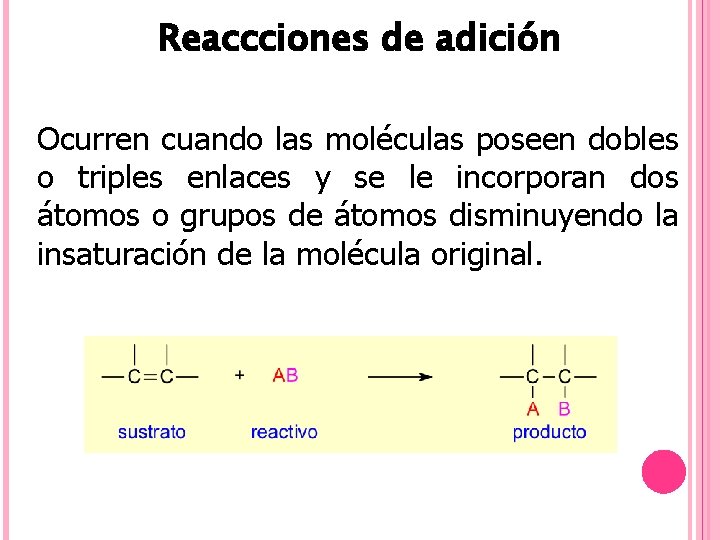
Reaccciones de adición Ocurren cuando las moléculas poseen dobles o triples enlaces y se le incorporan dos átomos o grupos de átomos disminuyendo la insaturación de la molécula original.
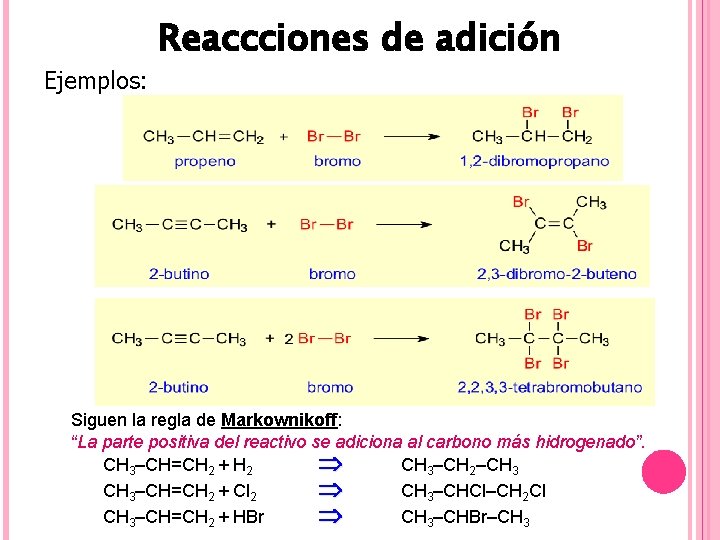
Ejemplos: Reaccciones de adición Siguen la regla de Markownikoff: “La parte positiva del reactivo se adiciona al carbono más hidrogenado”. CH 3–CH=CH 2 + H 2 CH 3–CH 2–CH 3–CH=CH 2 + Cl 2 CH 3–CHCl–CH 2 Cl CH 3–CH=CH 2 + HBr CH 3–CHBr–CH 3
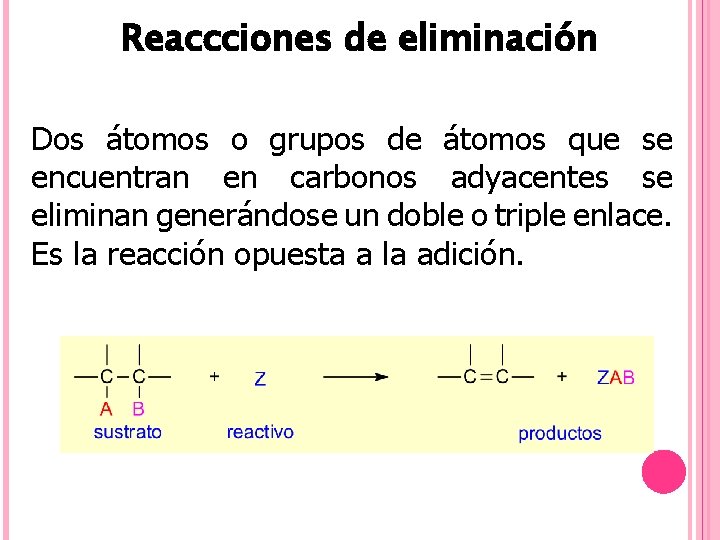
Reaccciones de eliminación Dos átomos o grupos de átomos que se encuentran en carbonos adyacentes se eliminan generándose un doble o triple enlace. Es la reacción opuesta a la adición.
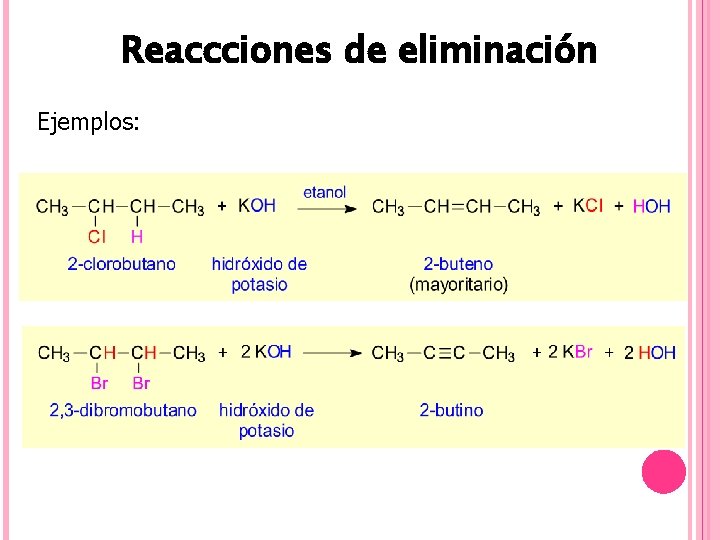
Reaccciones de eliminación Ejemplos:
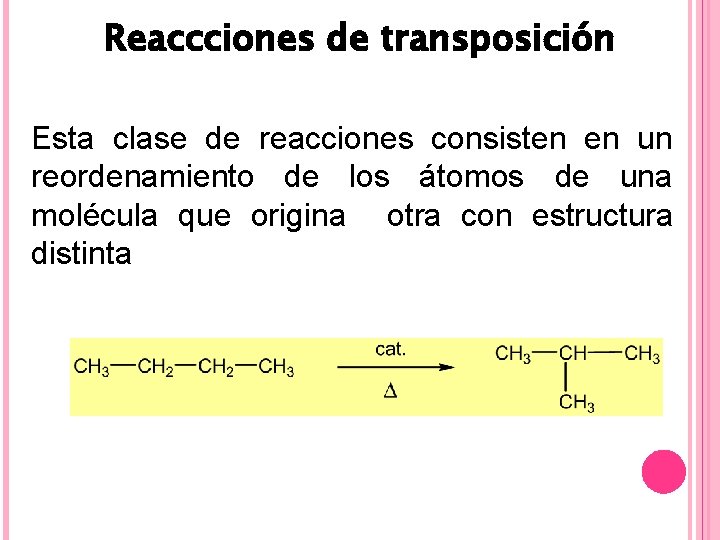
Reaccciones de transposición Esta clase de reacciones consisten en un reordenamiento de los átomos de una molécula que origina otra con estructura distinta

HIDROCARBUROS Y PETRÓLEO
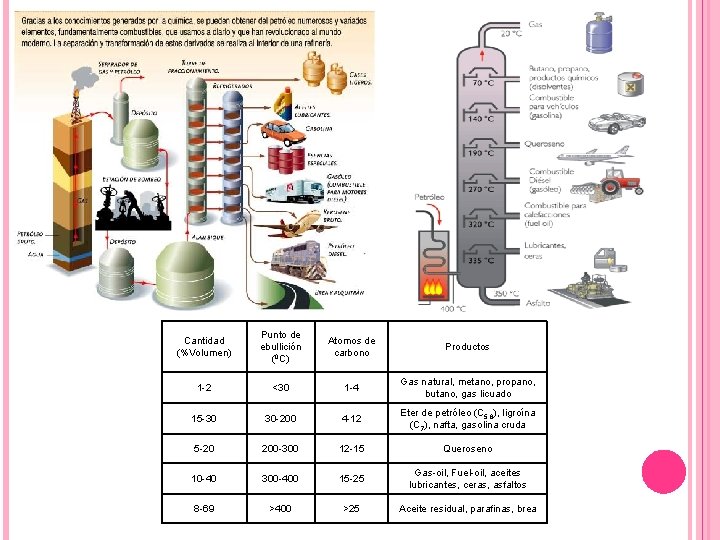
Cantidad (%Volumen) Punto de ebullición (0 C) Atomos de carbono Productos 1 -2 <30 1 -4 Gas natural, metano, propano, butano, gas licuado 15 -30 30 -200 4 -12 Eter de petróleo (C 5, 6), ligroína (C 7), nafta, gasolina cruda 5 -20 200 -300 12 -15 Queroseno 10 -40 300 -400 15 -25 Gas-oil, Fuel-oil, aceites lubricantes, ceras, asfaltos 8 -69 >400 >25 Aceite residual, parafinas, brea
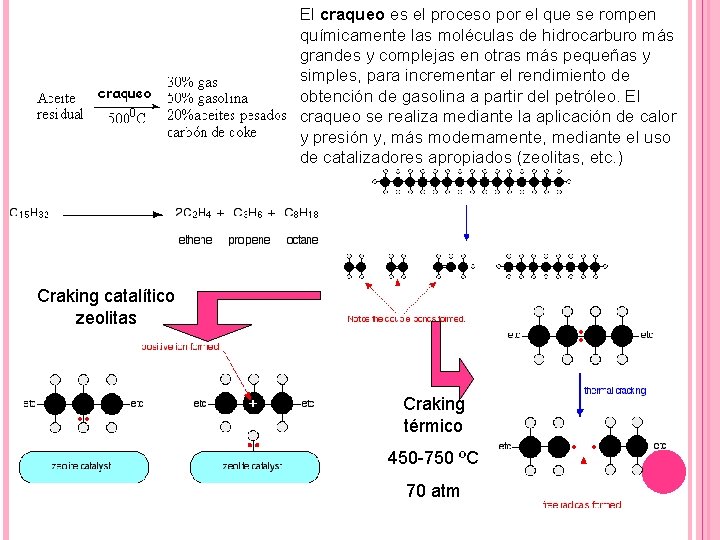
El craqueo es el proceso por el que se rompen químicamente las moléculas de hidrocarburo más grandes y complejas en otras más pequeñas y simples, para incrementar el rendimiento de obtención de gasolina a partir del petróleo. El craqueo se realiza mediante la aplicación de calor y presión y, más modernamente, mediante el uso de catalizadores apropiados (zeolitas, etc. ) Craking catalítico zeolitas Craking térmico 450 -750 ºC 70 atm
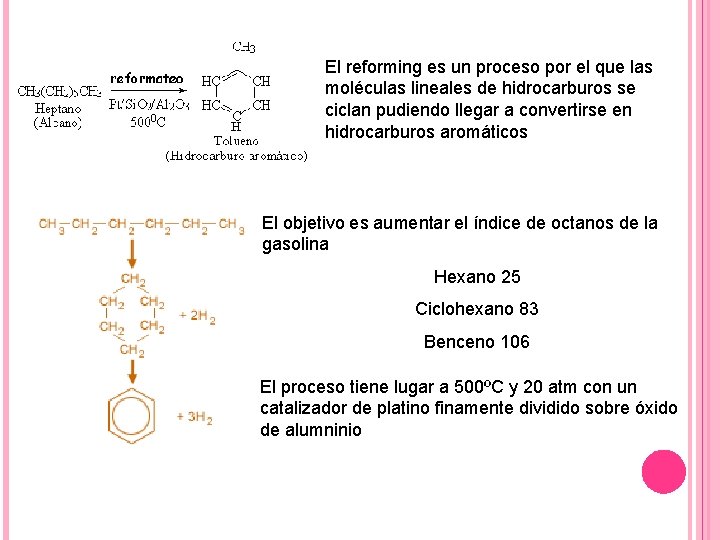
El reforming es un proceso por el que las moléculas lineales de hidrocarburos se ciclan pudiendo llegar a convertirse en hidrocarburos aromáticos El objetivo es aumentar el índice de octanos de la gasolina Hexano 25 Ciclohexano 83 Benceno 106 El proceso tiene lugar a 500ºC y 20 atm con un catalizador de platino finamente dividido sobre óxido de alumninio
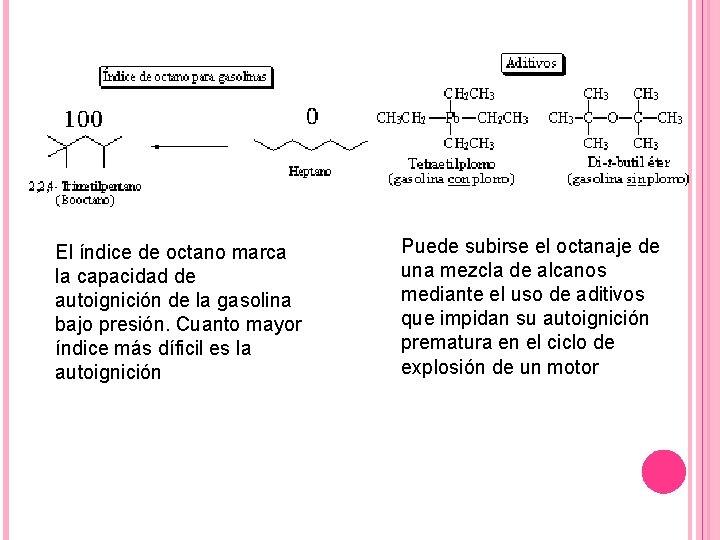
El índice de octano marca la capacidad de autoignición de la gasolina bajo presión. Cuanto mayor índice más díficil es la autoignición Puede subirse el octanaje de una mezcla de alcanos mediante el uso de aditivos que impidan su autoignición prematura en el ciclo de explosión de un motor
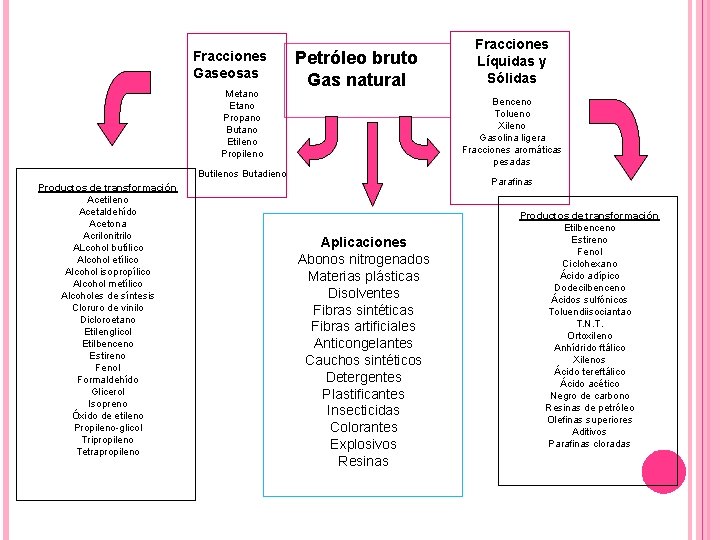
Fracciones Gaseosas Metano Etano Propano Butano Etileno Propileno Petróleo bruto Gas natural Benceno Tolueno Xileno Gasolina ligera Fracciones aromáticas pesadas Butilenos Butadieno Productos de transformación Acetileno Acetaldehído Acetona Acrilonitrilo ALcohol butílico Alcohol etílico Alcohol isopropílico Alcohol metílico Alcoholes de síntesis Cloruro de vinilo Dicloroetano Etilenglicol Etilbenceno Estireno Fenol Formaldehído Glicerol Isopreno Óxido de etileno Propileno-glicol Tripropileno Tetrapropileno Fracciones Líquidas y Sólidas Parafinas Aplicaciones Abonos nitrogenados Materias plásticas Disolventes Fibras sintéticas Fibras artificiales Anticongelantes Cauchos sintéticos Detergentes Plastificantes Insecticidas Colorantes Explosivos Resinas Productos de transformación Etilbenceno Estireno Fenol Ciclohexano Ácido adípico Dodecilbenceno Ácidos sulfónicos Toluendiisociantao T. N. T. Ortoxileno Anhídrido ftálico Xilenos Ácido tereftálico Ácido acético Negro de carbono Resinas de petróleo Olefinas superiores Aditivos Parafinas cloradas
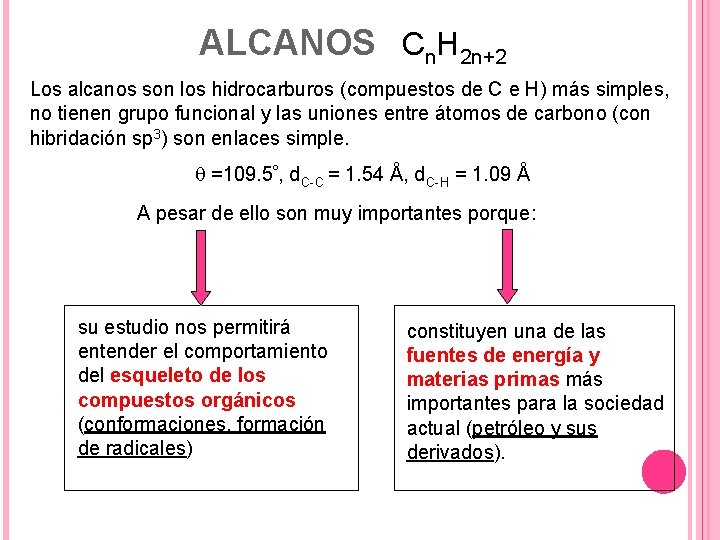
ALCANOS Cn. H 2 n+2 Los alcanos son los hidrocarburos (compuestos de C e H) más simples, no tienen grupo funcional y las uniones entre átomos de carbono (con hibridación sp 3) son enlaces simple. q =109. 5º, d. C-C = 1. 54 Å, d. C-H = 1. 09 Å A pesar de ello son muy importantes porque: su estudio nos permitirá entender el comportamiento del esqueleto de los compuestos orgánicos (conformaciones, formación de radicales) constituyen una de las fuentes de energía y materias primas más importantes para la sociedad actual (petróleo y sus derivados).
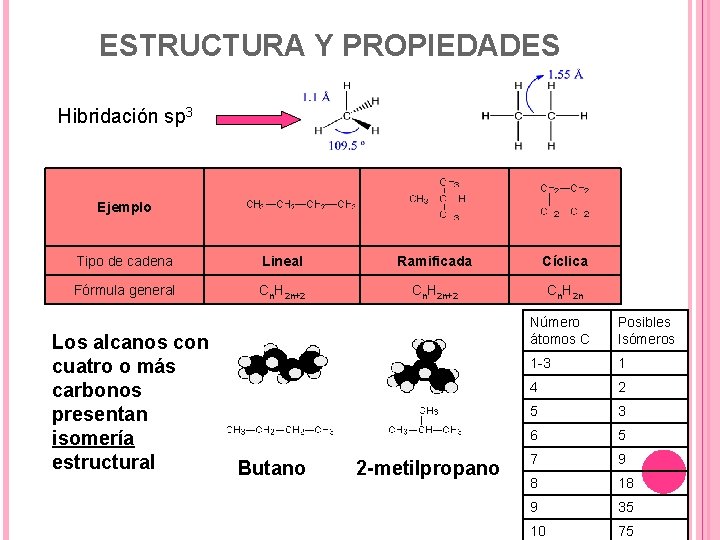
ESTRUCTURA Y PROPIEDADES Hibridación sp 3 Ejemplo Tipo de cadena Lineal Ramificada Cíclica Fórmula general Cn. H 2 n+2 Cn. H 2 n Los alcanos con cuatro o más carbonos presentan isomería estructural Butano 2 -metilpropano Número átomos C Posibles Isómeros 1 -3 1 4 2 5 3 6 5 7 9 8 18 9 35 10 75
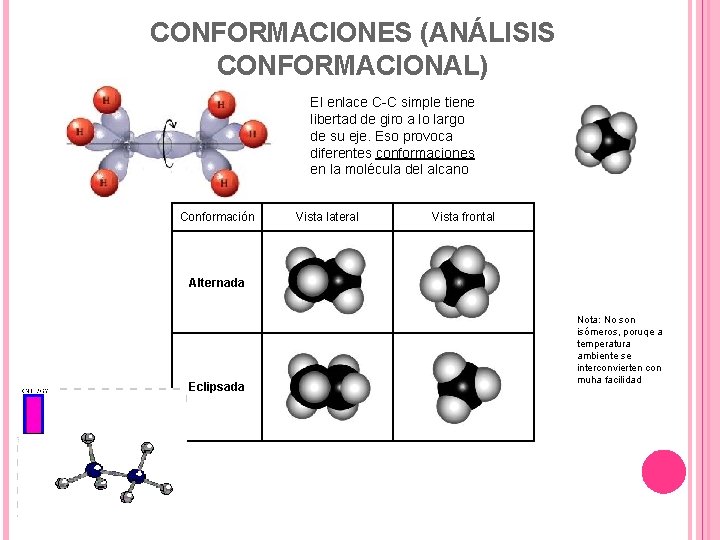
CONFORMACIONES (ANÁLISIS CONFORMACIONAL) El enlace C-C simple tiene libertad de giro a lo largo de su eje. Eso provoca diferentes conformaciones en la molécula del alcano Conformación Vista lateral Vista frontal Alternada Eclipsada Nota: No son isómeros, poruqe a temperatura ambiente se interconvierten con muha facilidad
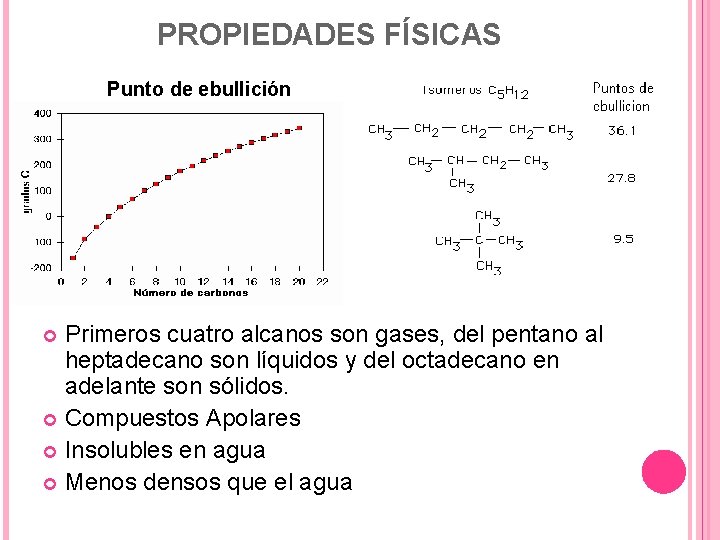
PROPIEDADES FÍSICAS Punto de ebullición Primeros cuatro alcanos son gases, del pentano al heptadecano son líquidos y del octadecano en adelante son sólidos. Compuestos Apolares Insolubles en agua Menos densos que el agua
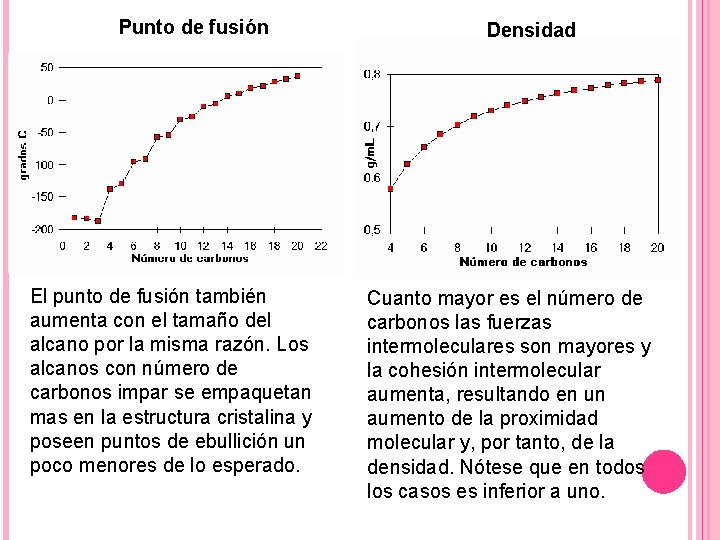
Punto de fusión El punto de fusión también aumenta con el tamaño del alcano por la misma razón. Los alcanos con número de carbonos impar se empaquetan mas en la estructura cristalina y poseen puntos de ebullición un poco menores de lo esperado. Densidad Cuanto mayor es el número de carbonos las fuerzas intermoleculares son mayores y la cohesión intermolecular aumenta, resultando en un aumento de la proximidad molecular y, por tanto, de la densidad. Nótese que en todos los casos es inferior a uno.
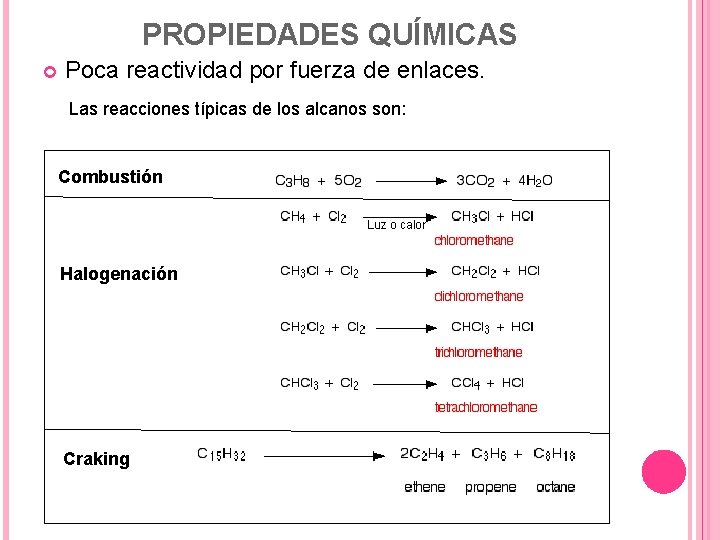
PROPIEDADES QUÍMICAS Poca reactividad por fuerza de enlaces. Las reacciones típicas de los alcanos son: Combustión Luz o calor Halogenación Craking
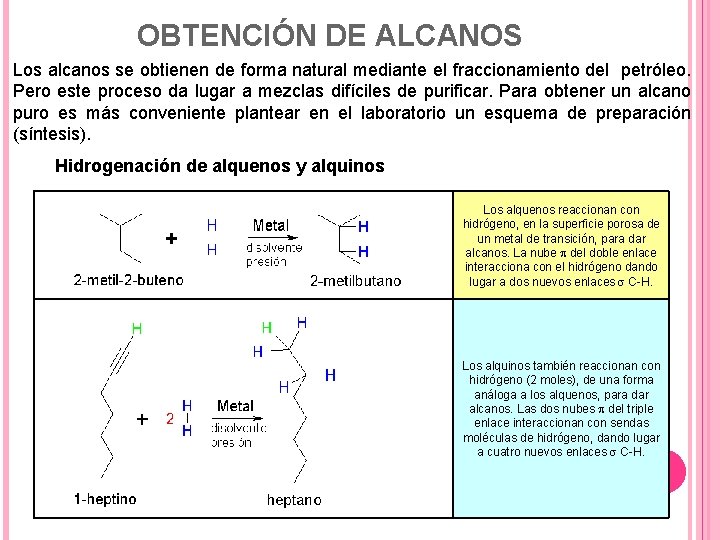
OBTENCIÓN DE ALCANOS Los alcanos se obtienen de forma natural mediante el fraccionamiento del petróleo. Pero este proceso da lugar a mezclas difíciles de purificar. Para obtener un alcano puro es más conveniente plantear en el laboratorio un esquema de preparación (síntesis). Hidrogenación de alquenos y alquinos Los alquenos reaccionan con hidrógeno, en la superficie porosa de un metal de transición, para dar alcanos. La nube p del doble enlace interacciona con el hidrógeno dando lugar a dos nuevos enlaces s C-H. Los alquinos también reaccionan con hidrógeno (2 moles), de una forma análoga a los alquenos, para dar alcanos. Las dos nubes p del triple enlace interaccionan con sendas moléculas de hidrógeno, dando lugar a cuatro nuevos enlaces s C-H.
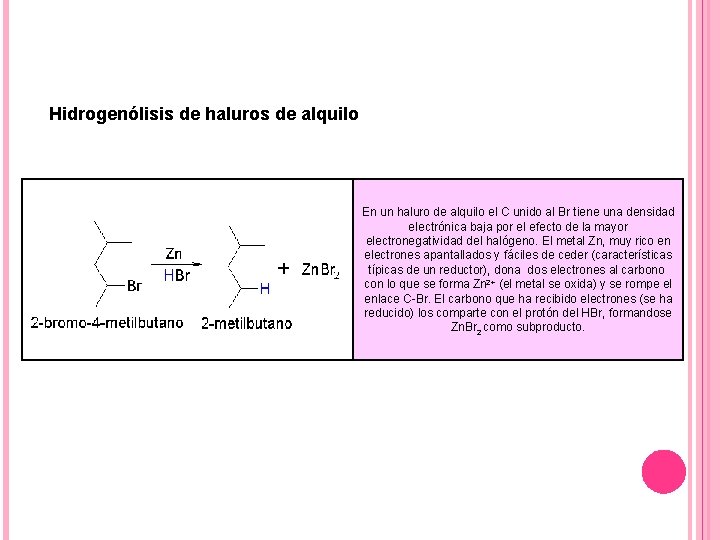
Hidrogenólisis de haluros de alquilo En un haluro de alquilo el C unido al Br tiene una densidad electrónica baja por el efecto de la mayor electronegatividad del halógeno. El metal Zn, muy rico en electrones apantallados y fáciles de ceder (características típicas de un reductor), dona dos electrones al carbono con lo que se forma Zn 2+ (el metal se oxida) y se rompe el enlace C-Br. El carbono que ha recibido electrones (se ha reducido) los comparte con el protón del HBr, formandose Zn. Br 2 como subproducto.
IMPORTANCIA, USOS Y APLICACIONES
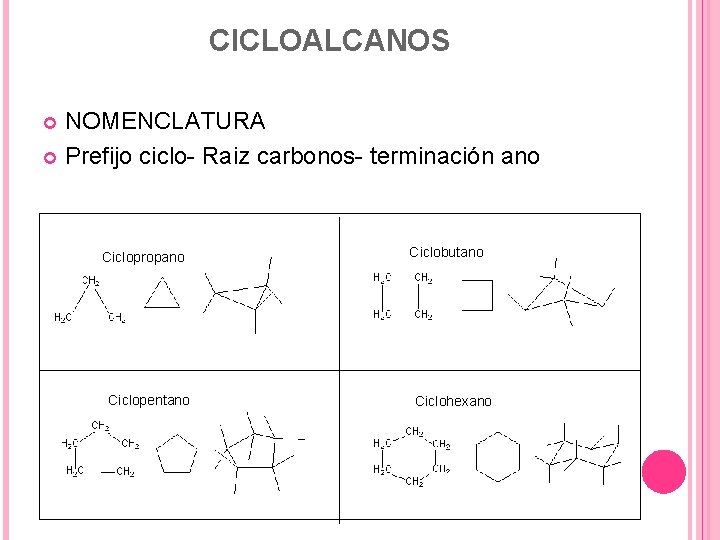
CICLOALCANOS NOMENCLATURA Prefijo ciclo- Raiz carbonos- terminación ano Ciclopropano Ciclopentano Ciclobutano Ciclohexano
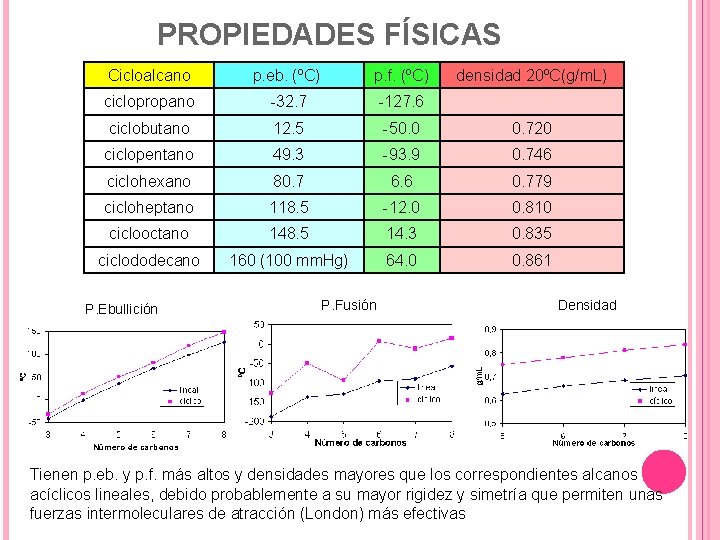
PROPIEDADES FÍSICAS Cicloalcano p. eb. (ºC) p. f. (ºC) ciclopropano -32. 7 -127. 6 ciclobutano 12. 5 -50. 0 0. 720 ciclopentano 49. 3 -93. 9 0. 746 ciclohexano 80. 7 6. 6 0. 779 cicloheptano 118. 5 -12. 0 0. 810 ciclooctano 148. 5 14. 3 0. 835 ciclododecano 160 (100 mm. Hg) 64. 0 0. 861 P. Ebullición P. Fusión densidad 20ºC(g/m. L) Densidad Tienen p. eb. y p. f. más altos y densidades mayores que los correspondientes alcanos acíclicos lineales, debido probablemente a su mayor rigidez y simetría que permiten unas fuerzas intermoleculares de atracción (London) más efectivas
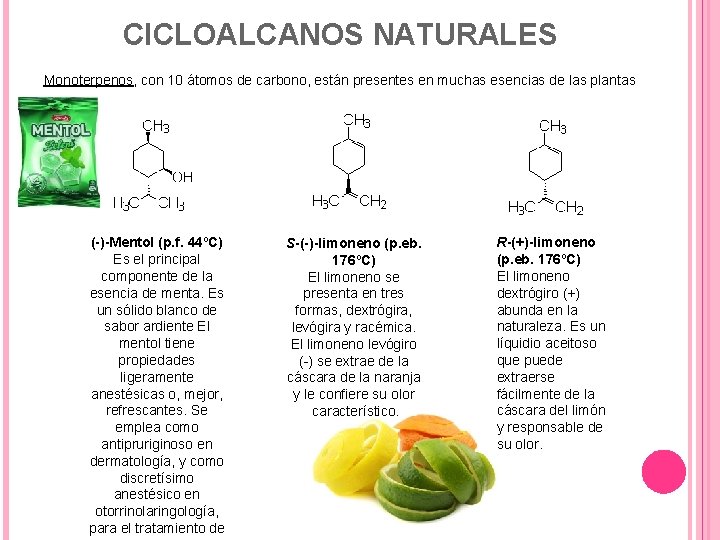
CICLOALCANOS NATURALES Monoterpenos, con 10 átomos de carbono, están presentes en muchas esencias de las plantas (-)-Mentol (p. f. 44ºC) Es el principal componente de la esencia de menta. Es un sólido blanco de sabor ardiente El mentol tiene propiedades ligeramente anestésicas o, mejor, refrescantes. Se emplea como antipruriginoso en dermatología, y como discretísimo anestésico en otorrinolaringología, para el tratamiento de S-(-)-limoneno (p. eb. 176ºC) El limoneno se presenta en tres formas, dextrógira, levógira y racémica. El limoneno levógiro (-) se extrae de la cáscara de la naranja y le confiere su olor característico. R-(+)-limoneno (p. eb. 176ºC) El limoneno dextrógiro (+) abunda en la naturaleza. Es un líquidio aceitoso que puede extraerse fácilmente de la cáscara del limón y responsable de su olor.
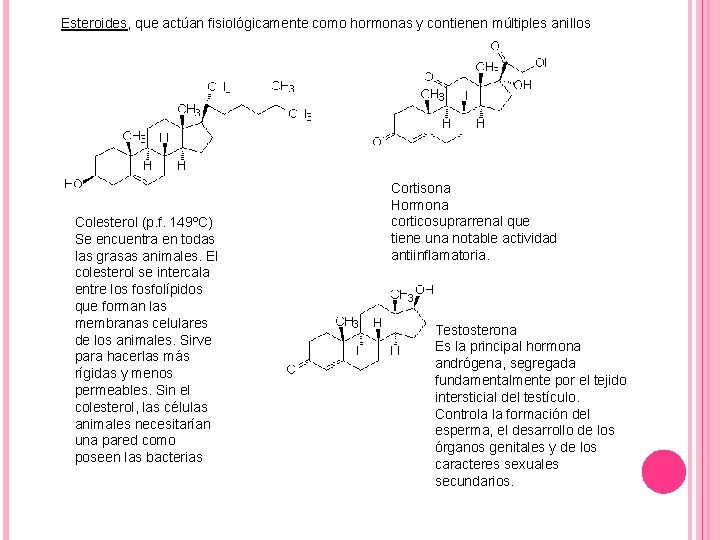
Esteroides, que actúan fisiológicamente como hormonas y contienen múltiples anillos Colesterol (p. f. 149ºC) Se encuentra en todas las grasas animales. El colesterol se intercala entre los fosfolípidos que forman las membranas celulares de los animales. Sirve para hacerlas más rígidas y menos permeables. Sin el colesterol, las células animales necesitarían una pared como poseen las bacterias Cortisona Hormona corticosuprarrenal que tiene una notable actividad antiinflamatoria. Testosterona Es la principal hormona andrógena, segregada fundamentalmente por el tejido intersticial del testículo. Controla la formación del esperma, el desarrollo de los órganos genitales y de los caracteres sexuales secundarios.

ALQUENOS Cn. H 2 n También conocidos como Olefinas Enlace doble (∏ y �) Hibridación sp 2 Geometría trigonal Isomería de cadena, de posición y geométrica Propiedades físicas: alquenos de 2 a 4 carbonos son gases, son líquidos alquenos de 5 a 15 carbonos y sólidos del 16 en adelante. Apolares Insolubles en agua Menos densos que el agua
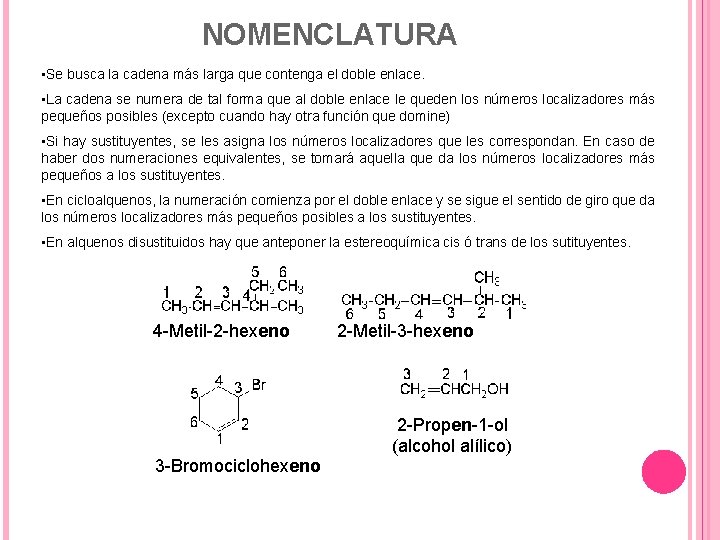
NOMENCLATURA • Se busca la cadena más larga que contenga el doble enlace. • La cadena se numera de tal forma que al doble enlace le queden los números localizadores más pequeños posibles (excepto cuando hay otra función que domine) • Si hay sustituyentes, se les asigna los números localizadores que les correspondan. En caso de haber dos numeraciones equivalentes, se tomará aquella que da los números localizadores más pequeños a los sustituyentes. • En cicloalquenos, la numeración comienza por el doble enlace y se sigue el sentido de giro que da los números localizadores más pequeños posibles a los sustituyentes. • En alquenos disustituidos hay que anteponer la estereoquímica cis ó trans de los sutituyentes. 4 -Metil-2 -hexeno 3 -Bromociclohexeno 2 -Metil-3 -hexeno 2 -Propen-1 -ol (alcohol alílico)
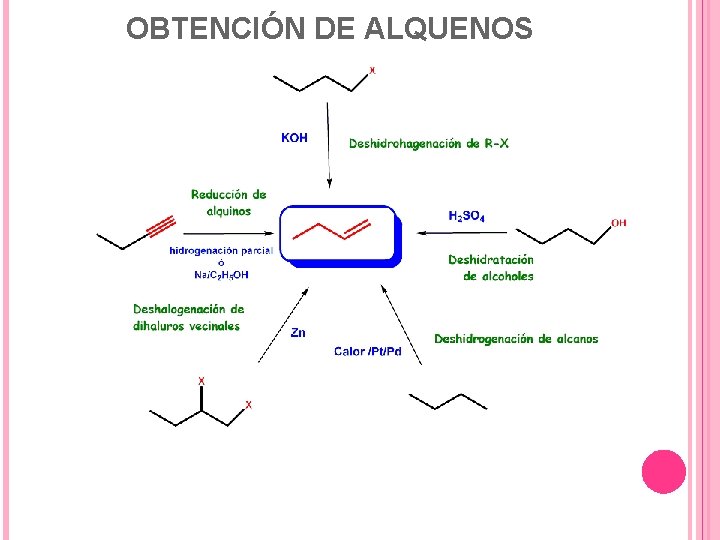
OBTENCIÓN DE ALQUENOS
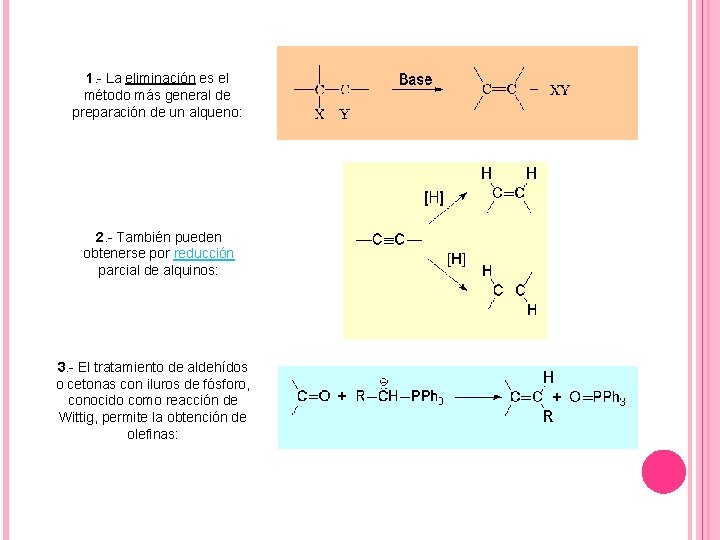
1. - La eliminación es el método más general de preparación de un alqueno: 2. - También pueden obtenerse por reducción parcial de alquinos: 3. - El tratamiento de aldehídos o cetonas con iluros de fósforo, conocido como reacción de Wittig, permite la obtención de olefinas:
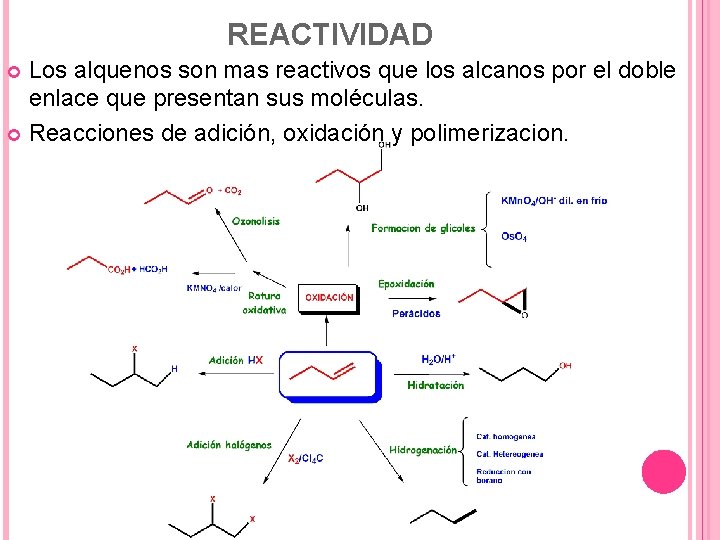
REACTIVIDAD Los alquenos son mas reactivos que los alcanos por el doble enlace que presentan sus moléculas. Reacciones de adición, oxidación y polimerizacion.
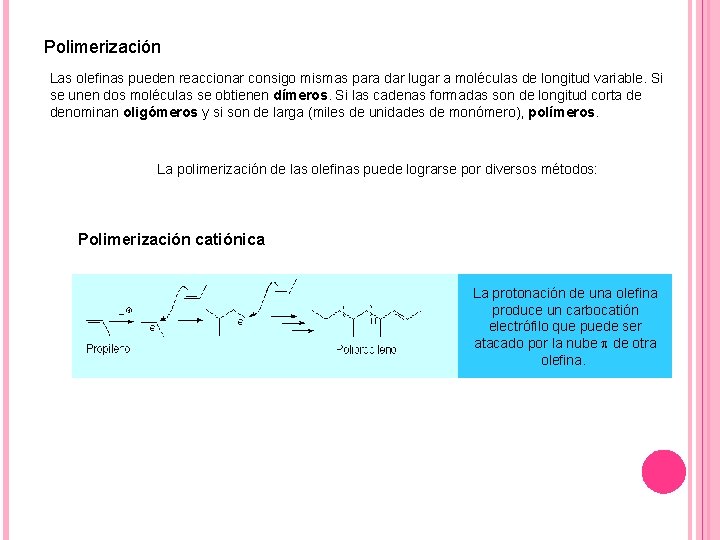
Polimerización Las olefinas pueden reaccionar consigo mismas para dar lugar a moléculas de longitud variable. Si se unen dos moléculas se obtienen dímeros. Si las cadenas formadas son de longitud corta de denominan oligómeros y si son de larga (miles de unidades de monómero), polímeros. La polimerización de las olefinas puede lograrse por diversos métodos: Polimerización catiónica La protonación de una olefina produce un carbocatión electrófilo que puede ser atacado por la nube p de otra olefina.
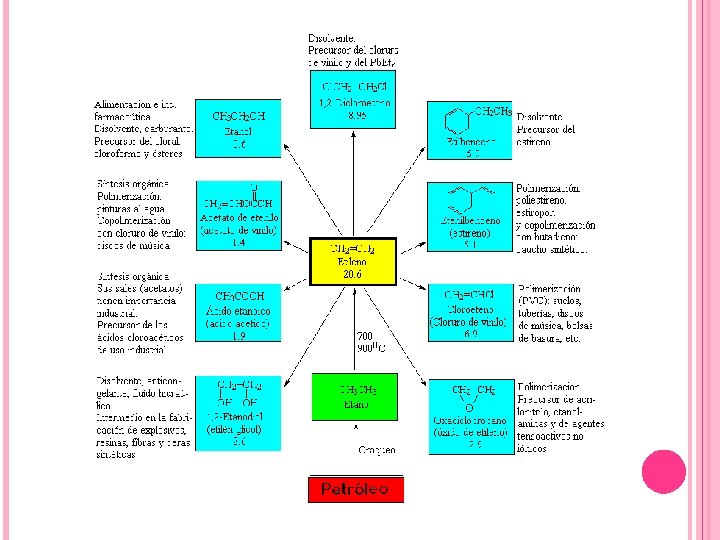

USOS Y APLICACIONES DE ALQUENOS

ALQUINOS Cn. H 2 n-2 Enlace triple Hibridación sp Etino, propino y 1 -butino son gases; 2 -butino y hasta 14 carbonos son líquidos y en adelannte sólidos. Menos densos que el agua e insolubles en ella.
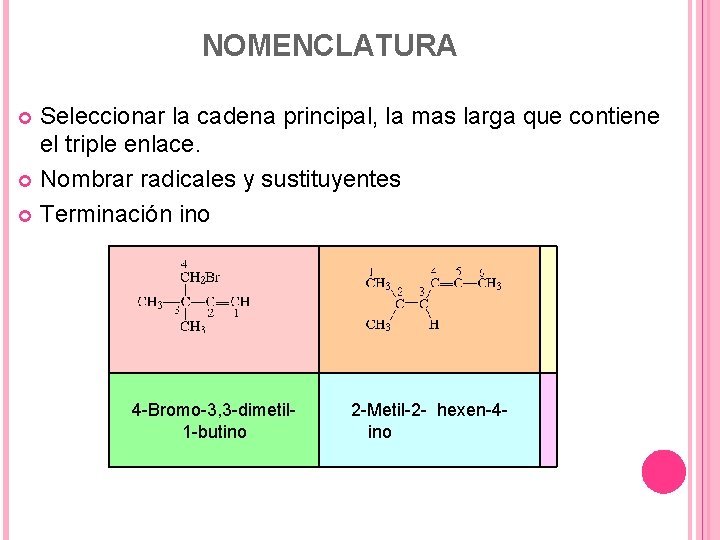
NOMENCLATURA Seleccionar la cadena principal, la mas larga que contiene el triple enlace. Nombrar radicales y sustituyentes Terminación ino 4 -Bromo-3, 3 -dimetil 1 -butino 2 -Metil-2 - hexen-4 ino
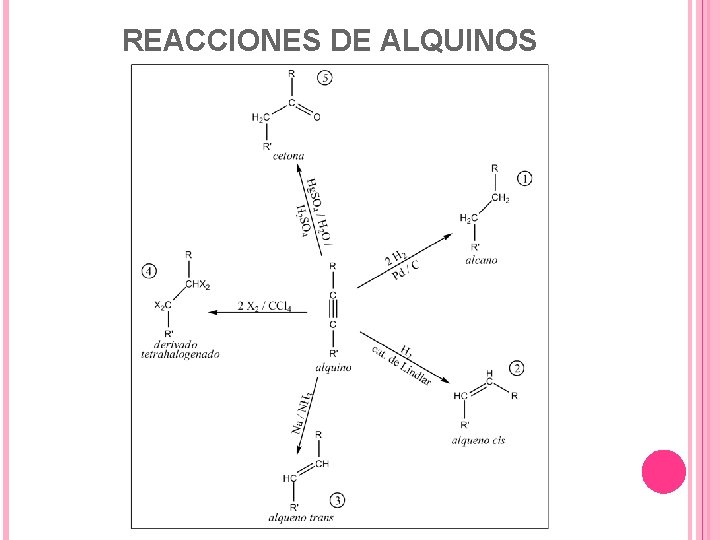
REACCIONES DE ALQUINOS
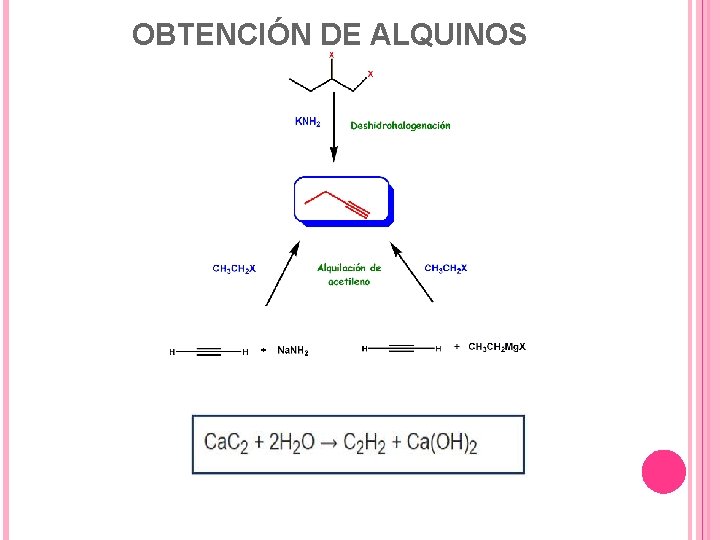
OBTENCIÓN DE ALQUINOS

USOS Y APLICACIONES DE ALQUINOS
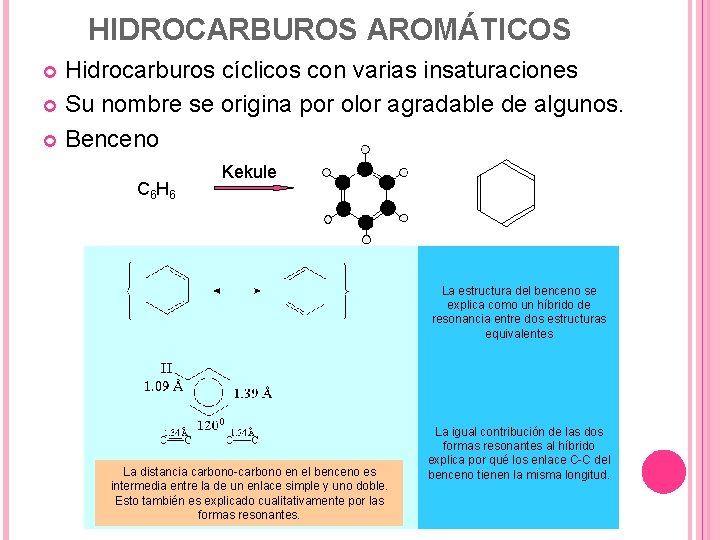
HIDROCARBUROS AROMÁTICOS Hidrocarburos cíclicos con varias insaturaciones Su nombre se origina por olor agradable de algunos. Benceno C 6 H 6 Kekule La estructura del benceno se explica como un híbrido de resonancia entre dos estructuras equivalentes La distancia carbono-carbono en el benceno es intermedia entre la de un enlace simple y uno doble. Esto también es explicado cualitativamente por las formas resonantes. La igual contribución de las dos formas resonantes al híbrido explica por qué los enlace C-C del benceno tienen la misma longitud.
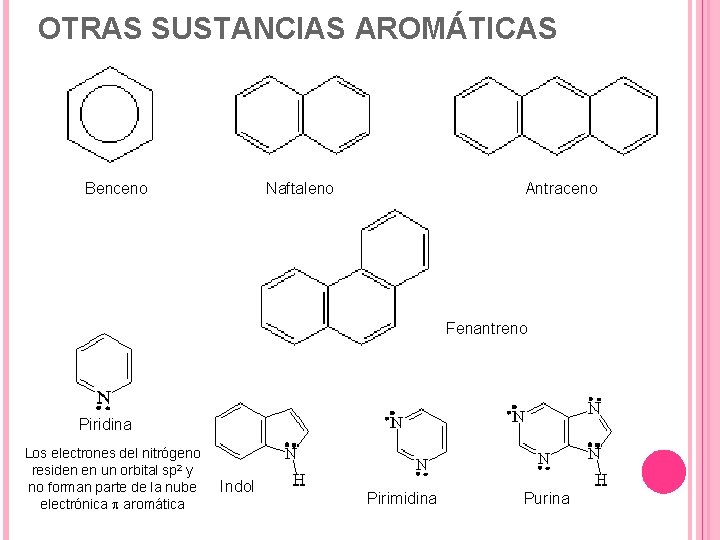
OTRAS SUSTANCIAS AROMÁTICAS Naftaleno Benceno Antraceno Fenantreno Piridina Los electrones del nitrógeno residen en un orbital sp 2 y no forman parte de la nube electrónica p aromática Indol Pirimidina Purina
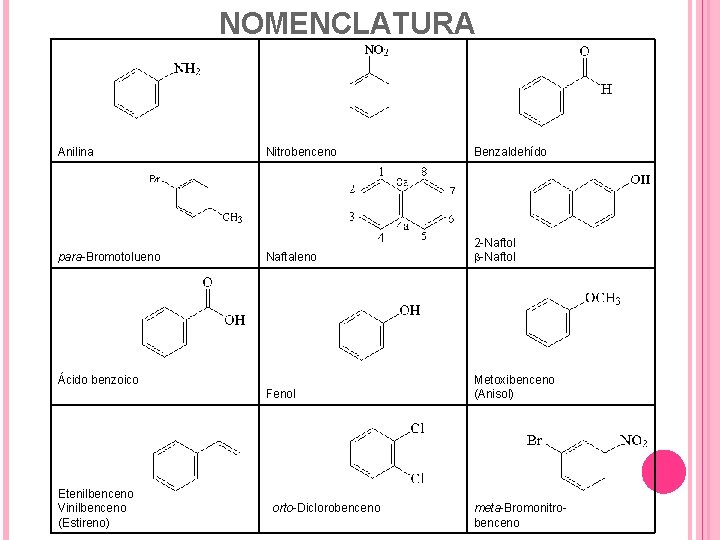
NOMENCLATURA Anilina para-Bromotolueno Nitrobenceno Benzaldehído Naftaleno 2 -Naftol b-Naftol Fenol Metoxibenceno (Anisol) Ácido benzoico Etenilbenceno Vinilbenceno (Estireno) orto-Diclorobenceno meta-Bromonitrobenceno
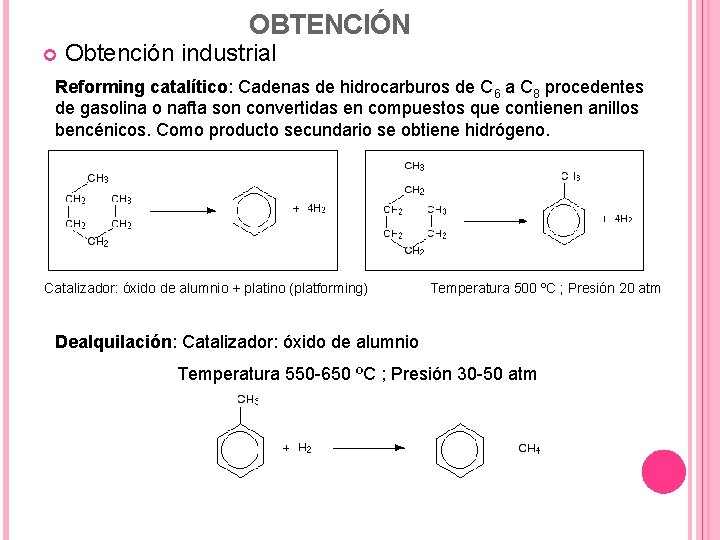
OBTENCIÓN Obtención industrial Reforming catalítico: Cadenas de hidrocarburos de C 6 a C 8 procedentes de gasolina o nafta son convertidas en compuestos que contienen anillos bencénicos. Como producto secundario se obtiene hidrógeno. Catalizador: óxido de alumnio + platino (platforming) Temperatura 500 ºC ; Presión 20 atm Dealquilación: Catalizador: óxido de alumnio Temperatura 550 -650 ºC ; Presión 30 -50 atm
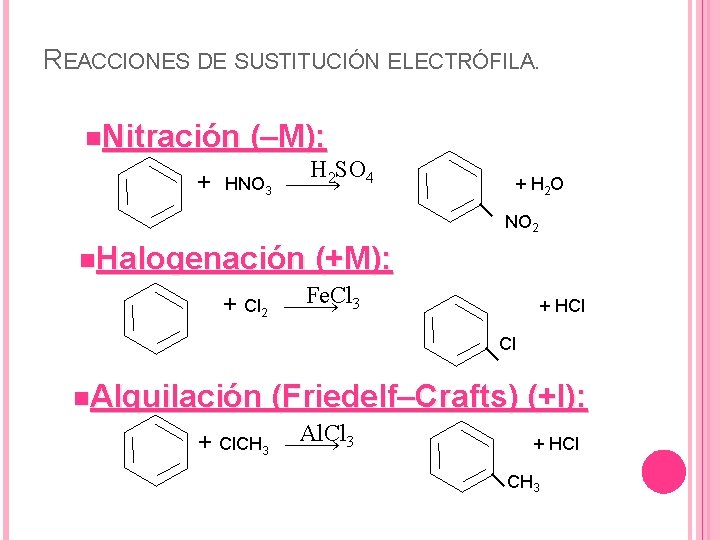
REACCIONES DE SUSTITUCIÓN ELECTRÓFILA. n. Nitración + (–M): H SO 4 2 HNO 3 + H 2 O NO 2 n. Halogenación (+M): Fe. Cl 3 + Cl + HCl 2 Cl n. Alquilación + Cl. CH 3 (Friedelf–Crafts) (+I): Al. Cl 3 + HCl CH 3
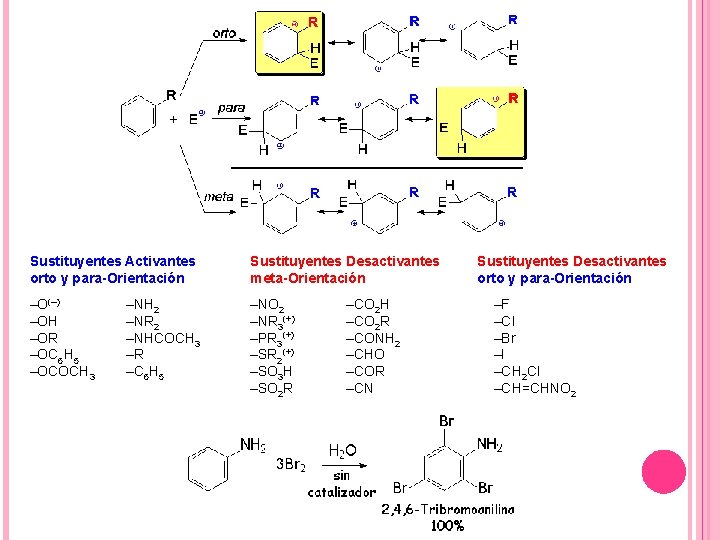
Sustituyentes Activantes orto y para-Orientación Sustituyentes Desactivantes meta-Orientación –O(–) –OH –OR –OC 6 H 5 –OCOCH 3 –NO 2 –NR 3(+) –PR 3(+) –SR 2(+) –SO 3 H –SO 2 R –NH 2 –NR 2 –NHCOCH 3 –R –C 6 H 5 –CO 2 H –CO 2 R –CONH 2 –CHO –COR –CN Sustituyentes Desactivantes orto y para-Orientación –F –Cl –Br –I –CH 2 Cl –CH=CHNO 2
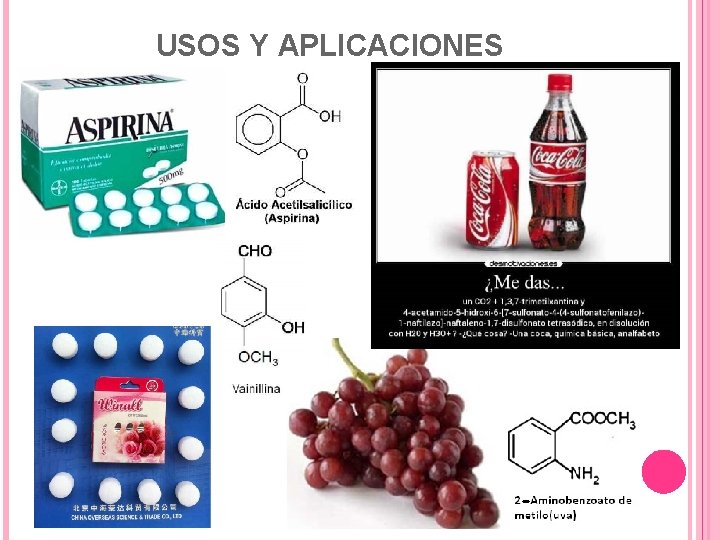
USOS Y APLICACIONES

REFERENCIAS Mc. Murry, J. 2008. Química Orgánica. 7° edición. Learning Editores. Mexico. UNAD. 2014. Módulo de química orgánica. ¡GRACIAS!
- Slides: 51