Qumica General 10112020 Ing Karla Dvila Reflexin del






















- Slides: 28

Química General 10/11/2020 Ing. Karla Dávila

Reflexión del día 10/11/2020 Ing. Karla Dávila

Objetivo • Analizar los tipos de reacciones químicas estableciendo sus diferencias para determinar cálculos químicos con ecuaciones químicas. • Fomentado el respeto, espirito crítico mediante la integración en la construcción del conocimiento. 10/11/2020 Ing. Karla Dávila

Contenidos • Tipos de Reacciones Química • Cálculos con Ecuaciones Químicas. 10/11/2020 Ing. Karla Dávila

Reacción química cambio químico en la cual una o mas sustancias se trasforman en nuevas sustancias con propiedades físicas y químicas diferentes a las que le dieron origen. 10/11/2020 Ing. Karla Dávila

q Reactivos: Son las sustancias iniciales, que van a reaccionar, responden a aquellas fórmulas (tanto simples como compuestas) q Productos: Son las sustancias formadas como resultado de la reacción química, responden a aquellas fórmulas (tanto simples, como compuesta) 10/11/2020 Ing. Karla Dávila

Condiciones y formas de manifestación de una ecuación química • • Formación de un precipitado. Formación de gases. Cambio de color. Desprendimiento o absorción de energía. 10/11/2020 Ing. Karla Dávila

Ecuación química • 10/11/2020 Ing. Karla Dávila

Tipos de Reacciones Químicas • • Descomposición Combinación Desplazamiento Doble Desplazamiento. • Reacciones REDOX. 10/11/2020 Ing. Karla Dávila

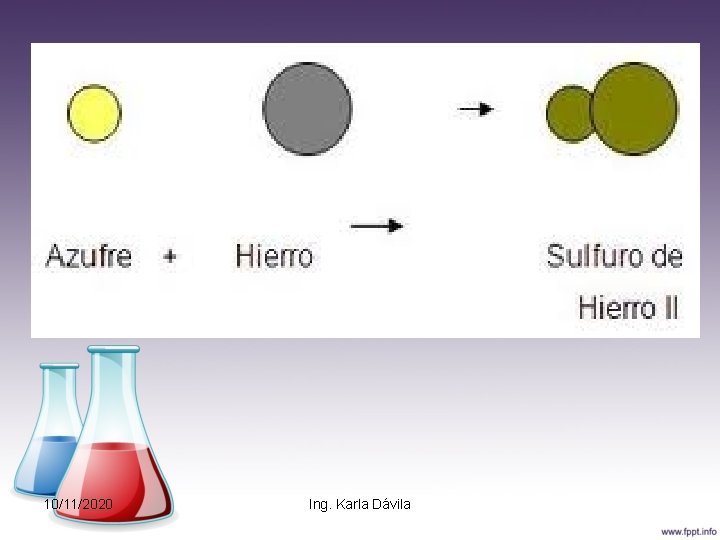
Combinación Proceso en el cual dos o más sustancias (simples o compuestas), dan lugar a una sustancia producto de naturaleza más compleja que las que le dieron origen. A este tipo de reacción también se les llaman reacciones de síntesi. 10/11/2020 Ing. Karla Dávila

10/11/2020 Ing. Karla Dávila

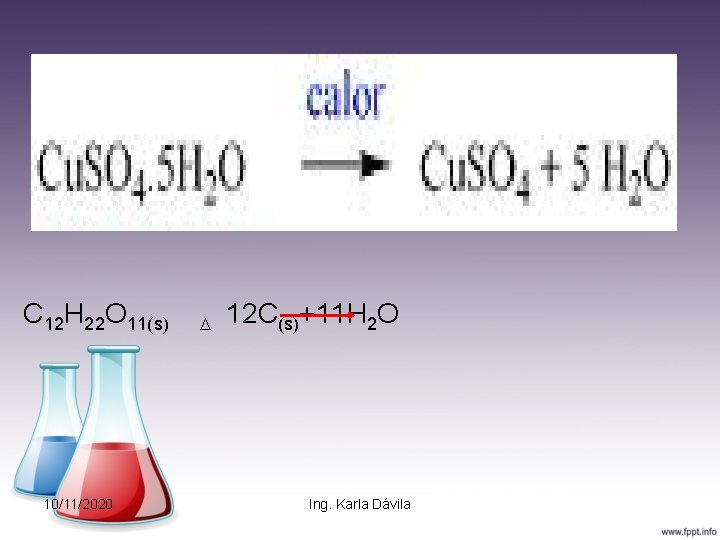
Descomposición Proceso en el cual a partir de una sustancia (Compuesto) reaccionante, se obtienen una o más sustancias productos(elementos o compuestos), de naturaleza menos compleja que las que le dio origen. Generalmente este tipo de reacción requiere calor para ocurrir. 10/11/2020 Ing. Karla Dávila

C 12 H 22 O 11(s) 12 C(s)+11 H 2 O 10/11/2020 Ing. Karla Dávila

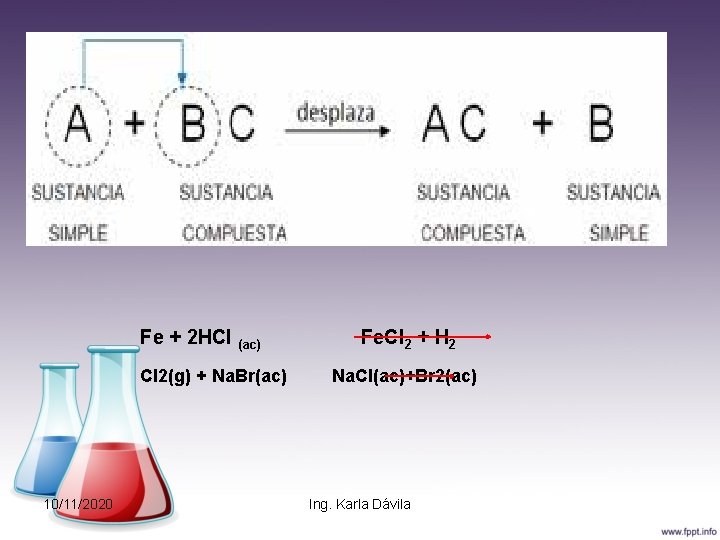
Sustitución o desplazamientosencilla Reacciona un elemento reemplazando a otro en un compuesto. Este tipo de reacción por lo regular ocurren en sln acuosa. 10/11/2020 Ing. Karla Dávila

Fe + 2 HCl (ac) Cl 2(g) + Na. Br(ac) 10/11/2020 Fe. Cl 2 + H 2 Na. Cl(ac)+Br 2(ac) Ing. Karla Dávila

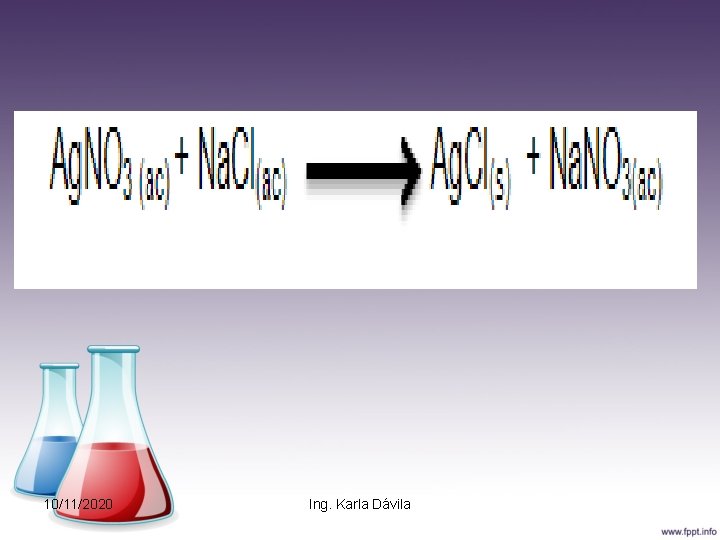
Reacciones de doble sustitución Llamadas también de metátesis, ocurren el sln acuosa. En dichas reacciones los cationes y aniones intercambian sus fracciones asociadas. 10/11/2020 Ing. Karla Dávila

10/11/2020 Ing. Karla Dávila

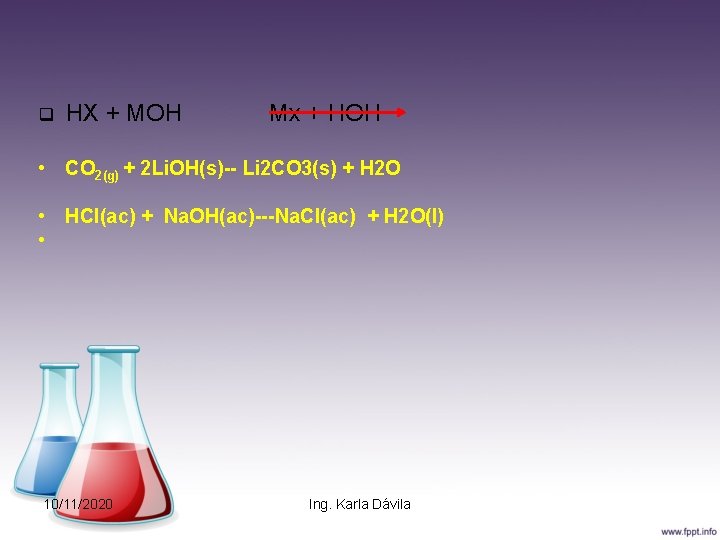
Neutralización Aquella en la cual reacciona un ácido (o un óxido ácido) con una base (óxido básico). En la mayoría de estas reacciones, uno de los productos es el agua. La formación del agua actúa como la fuerza motriz de la neutralización, debido a que el agua solo esta ligeramente ionizada y en esta formación también se libera calor. 10/11/2020 Ing. Karla Dávila

q HX + MOH Mx + HOH • CO 2(g) + 2 Li. OH(s)-- Li 2 CO 3(s) + H 2 O • HCl(ac) + Na. OH(ac)---Na. Cl(ac) + H 2 O(l) • 10/11/2020 Ing. Karla Dávila

• Redox: Calcular el número de oxidación Balanceo de ecuaciones químicas Se identifica la sustancia que se reduce y la sustancia que se oxida. Se calcula en cuanto varia el número de oxidación de la sustancia que se reduce donde el número resultante será el coeficiente de la sustancia que • Tanteo: se oxida KNO - Se calcula en cuanto varia el número de oxidación de la sustancia que se 3 --KNO 2+O 2 oxida donde el número resultante será el coeficiente de la sustancia que se reduce. - 10/11/2020 Ing. Karla Dávila

Cálculos químicos 10/11/2020 Ing. Karla Dávila

Ley de conservación de la masa • Ley de Lomonosov: «La masa de todas las sustancias que entran en una reacción es igual a la masa de las sustancias obtenidas como producto de dicha reacción»

Ley de las proporciones ctes o definidas • Ley de Prous: «Siempre que dos o más sustancias simples o compuestas, se combinen para dar lugar a un mismo compuesto, lo harán, según una relación cte y definida» - Cada compuesto posee una composición definida. - La composición de una sustancia dada no depende del procedimiento empleado para su obtención

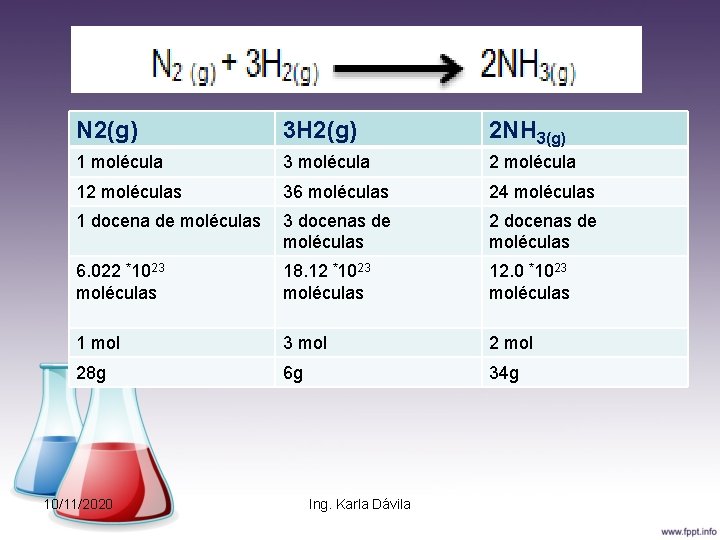
Ley de las masas de combinación • Ley de Richter: «Las masas de diferentes elementos que se combinan con la misma masa de otro , expresan por si mismas o multiplicadas por un factor sencillo, las relaciones según las cuales se combinan ellas entre sí»

N 2(g) 3 H 2(g) 2 NH 3(g) 1 molécula 3 molécula 2 molécula 12 moléculas 36 moléculas 24 moléculas 1 docena de moléculas 3 docenas de moléculas 2 docenas de moléculas 6. 022 *1023 moléculas 18. 12 *1023 moléculas 12. 0 *1023 moléculas 1 mol 3 mol 28 g 6 g 34 g 10/11/2020 Ing. Karla Dávila

1. ¿Cuántos moles de NH 3 se pueden producir a partir de 8 moles de. N 2? 10/11/2020 Ing. Karla Dávila

Bibliografía - Chang, R. (2006). Principios Esenciales de Química General. Madrid, España: Mc. Graw - Hill. - Malone, L. J. (2000). Introducción a la Química. México: LIMUSA, S. A - León. Ramírez, Rebeca. Química General, La Habana: Pueblo y Educación 11/10/2020 Ing. Karla Dávila

10/11/2020 Ing. Karla Dávila