Qumica do Hidrognio Hidrognio e Hidretos Abundncia Mais

Química do Hidrogênio

Hidrogênio e Hidretos Abundância • Mais abundante no universo (92%) • 10º elemento na crosta terrestre (minerais; oceanos, vulcões e toda forma de vida). Configuração Eletrônica - 1 s 1 - Forma ligação covalente, preferencialmente com não-metais CH 4 H 2 O H 2 O Aula 3: Química de Elementos 2
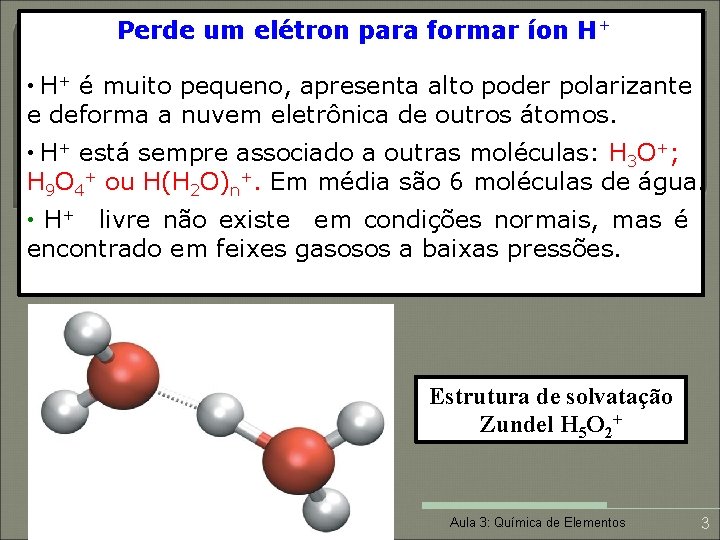
Perde um elétron para formar íon H+ • H+ é muito pequeno, apresenta alto poder polarizante e deforma a nuvem eletrônica de outros átomos. • H+ está sempre associado a outras moléculas: H 3 O+; H 9 O 4+ ou H(H 2 O)n+. Em média são 6 moléculas de água. • H+ livre não existe em condições normais, mas é encontrado em feixes gasosos a baixas pressões. Estrutura de solvatação Zundel H 5 O 2+ Aula 3: Química de Elementos 3

Adquire um elétron para formar Hidretos (H-) • Sólidos cristalinos: formados por metais altamente eletropositivos (grupo 1 e 2). Hidreto de Lítio (Li. H) • O Hidrogênio apresenta eletronegatividade igual a 2, 1, podendo doar ou receber elétrons. Aula 3: Química de Elementos 4
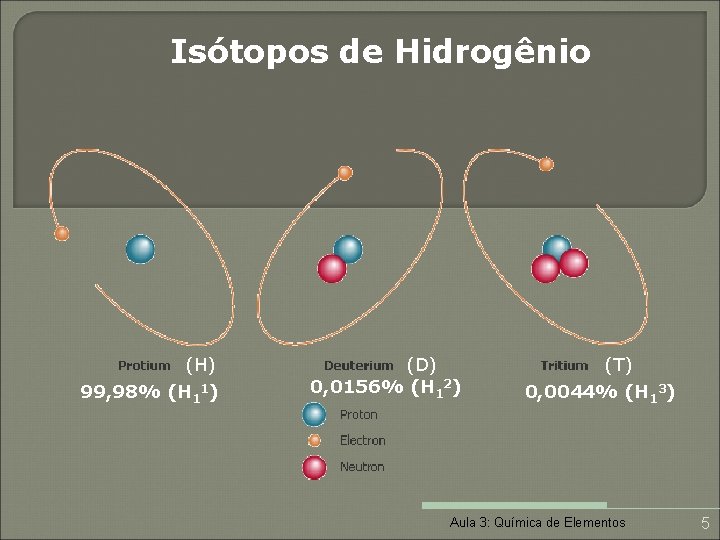
Isótopos de Hidrogênio (H) 99, 98% (H 11) (D) 0, 0156% (H 12) (T) 0, 0044% (H 13) Aula 3: Química de Elementos 5

Propriedades dos Isótopos • O trítio (H 3) é radioativo e sofre decaimento com emissão β 3 3 1 H /2 He + 1 e • H 2 reage mais rápido do que o D 2 Ea do H 2 é menor • H 2 O dissocia (Kd = 1, 0 x 10 -14 mol/L) três vezes mais do que a água pesada D 2 O (Kd = 3, 0 x 10 -15 mol/L); Aula 3: Química de Elementos 6

Propriedades dos Isótopos • Ligações com o prótio são rompidas mais facilmente (18 vezes) do que com o deutério Ex: eletrólise da água libera H 2 mais facilmente que D 2 e a água remanescente após a eletrólise torna-se enriquecida com D 2 O. A hidrólise de 29. 000 L de H 2 O fornece 1 L de D 2 O • D 2 O sofre todas as reações da H 2 O Ex. : D 2 O possui menor constante dielétrica menor solubilidade de íons Aula 3: Química de Elementos 7

Posição na Tabela Periódica • 1º elemento da TP (propriedades semelhantes ao G 18) • 1º período H e He (propriedades diferentes dos principais grupos da TP) Aula 3: Química de Elementos 8

Obtenção de Hidrogênio 1. Reforma a vapor: principal método comercial • Reação catalisada da água com hidrocarbonetos a altas temperaturas CH 4(g) + H 2 O(g) 1000°C CO(g) + 3 H 2(g) • Reação similar com coque como redutor: reação do gás de água 1000°C C(g) + H 2 O(g) CO(g) + H 2(g) • Ambas reações são seguidas por outra etapa Fe/Cr CO(g) + H 2 O(g) CO 2(g) + H 2(g) 2. Craqueamento de nafta e óleo combustível nas refinarias de petróleo : H 2 é subproduto da reação Aula 3: Química de Elementos 9

3. Eletrólise de Na. OH ou KOH: 99, 9% pureza Método caro, viável economicamente quando integrado com as indústrias de cloro-alcali. Anodo (Ni) 2 OH- H 2 O + ½ O 2 + 2 e. Catodo (Fe) 2 H 2 O + 2 e- 2 OH- + H 2 Reação global H 2 O H 2 + ½ O 2 4. Subproduto na indústria de cloro e álcalis Soluções aquosa de Na. Cl sofrem eletrólise para formar Na. OH, Cl 2 e H 2 5 - Reações de ácidos diluídos com metais do grupo 1, 2, 3, 4 e lantanídeos ou de álcalis com alumínio Zn + H 2 SO 4 Zn. SO 4 + H 2 2 Al + 2 Na. OH + 6 H 2 O 2 Na[Al(OH)4] + 3 H 2 6 - Reações de hidretos iônicos com água Li. H + H 2 O Li. OH + H 2 Aula 3: Química de Elementos 10
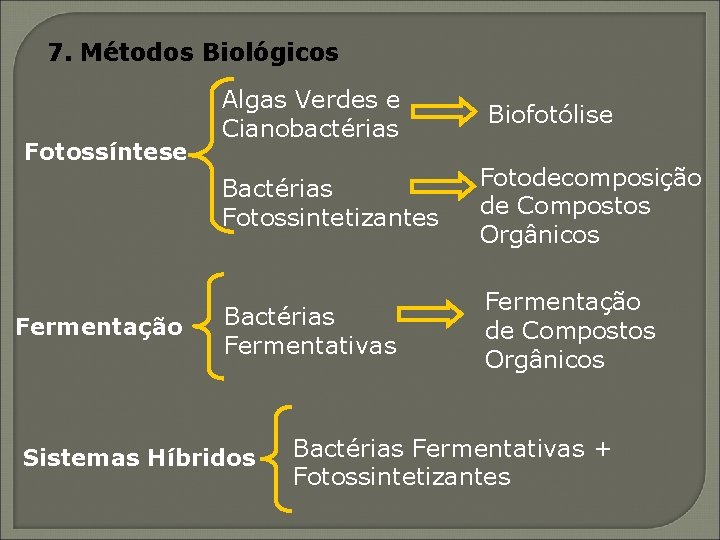
7. Métodos Biológicos Fotossíntese Fermentação Algas Verdes e Cianobactérias Biofotólise Bactérias Fotossintetizantes Fotodecomposição de Compostos Orgânicos Bactérias Fermentativas Fermentação de Compostos Orgânicos Sistemas Híbridos Bactérias Fermentativas + Fotossintetizantes

Obtenção de Hidrogênio Eletrólise da Água Reforma a vapor

Obtenção de Hidrogênio Metal + Acido Al + Na. OH

Usos do Hidrogênio (H 2) 1 - Síntese de amônia 2 H 2 + (O 2 + 4 N 2 (ar)) N 2 + 3 H 2 1100°C Fe/400°C/200 atm 2 H 2 O + 4 N 2 2 NH 3 2 - Hidrogenação catalítica de óleos - fabricação de margarina 3 - Manufatura de reagentes orgânicos – síntese do metanol pelo processo de hidroformilação CO + 2 H 2 Co Me. OH 4 - Produção de HCl, hidretos metálicos, combustível e na metalurgia (redução de óxidos a metais) Aula 3: Química de Elementos 14
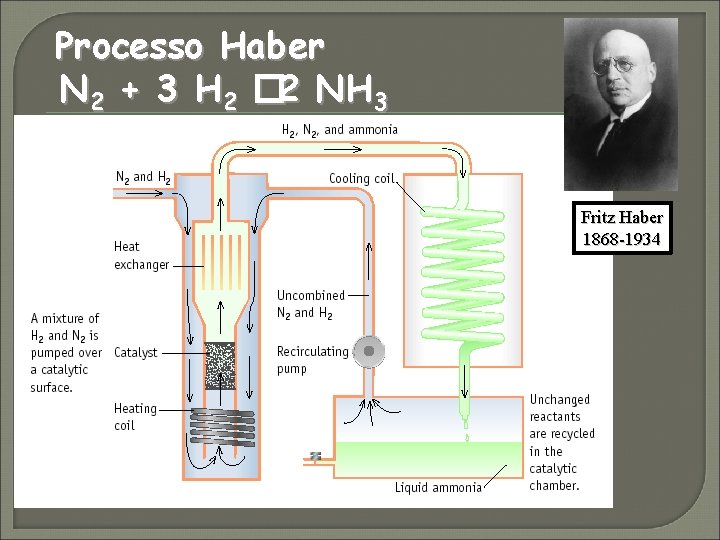
Processo Haber N 2 + 3 H 2 � 2 NH 3 Fritz Haber 1868 -1934

Propriedades Gerais e Químicas q H 2 - gás natural, inodoro, baixa solubilidade em solventes de baixa densidade. q Substitui o He em balões metereológicos q Possui ligação covalente muito forte (435, 9 k. Jmol-1) q Pouco reativo em condições naturais (predomina aspectos cinéticos em relação aos termodinâmicos). q Deve haver quebra da ligação H-H --> Ea alta ==> reações lentas ou requerem altas temperaturas ou catalisadores. Aula 3: Química de Elementos 16

Propriedades Gerais e Químicas q H 2 - queima no ar ou oxigênio, liberando muita energia: 2 H 2 + O 2 2 H 2 O ΔH = -485 k. Jmol-1 q H 2 reage com os halogênios: H 2 + F 2 2 HF ( violenta mesmo a baixa T) H 2 + Cl 2 2 HCl (catalisada pela luz, explosiva à luz solar direta Aula 3: Química de Elementos 17

q Formação de Hidretos: reações do H 2 com metais para formar Hidretos. As reações são violentas e requerem altas temperaturas. q Produção industrial de NH 3 (Processo Haber) N 2 + 3 H 2 2 NH 3 ΔG 298 K= -33, 4 k. Jmol-1 Favorecida por altas pressões, baixas T (380 a 450°C e 200 atm) e catalisadores (Fe) q Reações de hidrogenação - adição de H 2 a C=C Ex: saturação de ácidos graxos (Pd como catalisador) CH 3(CH 2)n. CH=CHCOOH + H 2 CH 3(CH 2)n. CH 2 COOH q Redução de nitrobenzeno a anilina em indústria de corantes q Produção de metanol CO + 2 H 2 CH 3 OH (necessita catalisador) Aula 3: Química de Elementos 18

q H 2 é muito estável: condições normais apresenta baixa tendência em dissociar. q H 2 2 H ΔH = 435, 9 k. Jmol-1 (muito endotérmica) Possível a altas T, campo elétrico ou radiação UV mas o átomo de H tem vida de menos de 1/2 segundo. q H 2 como combustível: substituir carvão e petróleo; não libera poluentes como SO 2, NOx, CO 2. Hidrocarbonetos Aula 3: Química de Elementos 19

Hidretos Os hidretos são compostos inorgânicos hidrogenados, que apresentam o hidrogênio como o elemento mais eletronegativo, ou seja, como ânion Hidretos de estado de oxidação -1 iônicos ( H-1 ). ou salinos Hidretos Iônicos q Reação do H com metais do grupo 1 e 2(Ca, Sr, Ba), a altas temperaturas Ex: Na. H, Ca. H 2 q Sólidos de ponto de fusão elevados q Quando fundidos conduzem eletricidade q Eletrólise da solução fundida libera H 2 q Possuem estrutura cristalina conhecida Aula 3: Química de Elementos 20

Hidretos Iônicos q Só é possível com elementos de eletronegatividade menor que 2, 1 q Hidretos com elementos do grupo 1 são mais reativos do que os do grupo 2. (Reatividade aumenta de cima para baixo no grupo – por quê? ) q H- é instável em água q Todos hidretos iônicos reagem com água Li. H + H 2 O Li. OH + H 2 q São poderosos agentes redutores 2 CO + Na. H H-COONa + C Aula 3: Química de Elementos 21

Hidretos Covalentes q Hidretos dos elementos do grupo p: pequena diferença de eletronegatividade entre estes átomos e o hidrogênio q São voláteis, baixo p. f e p. e q Constituídos por moléculas covalentes, mantidas por forças de Van der Walls q Hidretos do grupo 13 são polímeros mononucleares q Ex: B 2 H 6; B 4 H 10, B 10 H 14; (Al. H 3)n q Nos outros grupos, exceto halogênios, forma hidretos polinucleares. Principalmente C, N e O q Ex: CH 4; C 2 H 6; C 2 H 4; C 2 H 2; C 6 H 6; Si 10 H 22; Sn 2 H 6; N 2 H 4; NH 3; H 2 O 2 Aula 3: Química de Elementos 22

Hidretos metálicos ou intersticiais q Elementos do grupo d ou f reagem com hidrogênio; q Elementos situados no centro do bloco d não formam hidretos; q Propriedades semelhantes aos dos metais correspondentes: q Duros, brilho metálico, condutores de eletricidade, propriedades Magnéticas; q Formam hidretos com diferentes estequiometrias: Ex: Eu. H 2; Ce. H 2, 69; UH 3; Nb. H 0, 7; Pd. H 0, 6 Aula 3: Química de Elementos 23
- Slides: 23